DFT计算结合固体NMR研究富铝SSZ-13的铝分布和Brønsted 酸性
2020-04-24李诗涵赵侦超李世坤邢友东张维萍
李诗涵,赵侦超,李世坤,邢友东,张维萍
大连理工大学化工学院,精细化工国家重点实验室,辽宁 大连 116024
1 引言
具有CHA结构的SSZ-13分子筛由于其独特的孔道结构和水热稳定性而被广泛用于甲醇制烯烃(MTO)和NOx的选择性催化还原反应(SCR)1–3。Cu离子交换的小孔SSZ-13分子筛因在催化NH3-SCR反应中具有更宽的活性温窗、更高的N2选择性及优异的水热稳定性,已在柴油机车尾气处理上实现了商业化应用4,5。SSZ-13分子筛中的Al分布及相应的酸落位会显著影响Cu-SSZ-13的催化活性及水热稳定性。CHA笼中Cu离子位于六元环Al对中心位置是Cu-SSZ-13分子筛具有较高水热稳定性的原因之一,而B酸位于八元环有利于NH3的吸附活化6,7。富铝的SSZ-13 (Na型SSZ-13分子筛样品的Si/Al比为4–6)能够提供更多的离子交换位,可显著提高新鲜Cu-SSZ-13催化剂的低温活性,而含有B酸位的Al则十分容易脱除,导致老化后催化剂的性能显著降低8,9。最近人们研究不同Si/Al比的H-SSZ-13在MTO反应中的性能发现,高硅H-SSZ-13分子筛中孤立Al产生的孤立B酸有利于提高烯烃选择性,而富铝H-SSZ-13中的B酸对的存在则易于产生烷烃或积碳10。在甲醇制二甲醚反应中,富铝H-SSZ-13中B酸对的催化活性则远远大于孤立B酸的活性11。因此,研究富铝 SSZ-13分子筛中的Al分布及对应的酸性,对于深入理解其催化反应中的构效关系具有重要意义。
由于SSZ-13分子筛具有CHA结构,其骨架只有一个不等价T位,因此SSZ-13分子筛的27Al MAS NMR总是显现出一种高度对称的骨架四配位铝信号。我们通过Na+作为探针可很好地区分孤立Al及不同Al对的分布位置12。然而,当Al含量进一步增加时,随着CHA笼中Al含量的增加,对应笼中的Na+信号出现严重重叠,给富铝SSZ-13分子筛中的铝分布归属带来困难,且富铝SSZ-13分子筛客体离子的落位会随离子半径的变化而发生显著变化,因此H+的落位也必然不同于Na+13。密度泛函理论(DFT)计算结合固体核磁共振实验是研究分子筛的结构和性质特别是Al分布及酸性的有效手段14–18。Shah等人19通过计算去质子能认为H-SSZ-13分子筛中质子位于Al周围的O1位置最稳定。Lo等人20采用DFT研究了分子筛中八元环单Al及两Al取代情况,发现质子在Al原子周围四个不同氧位点上都具有几乎相同的酸性。Solans-Monfort等人21通过B3LYP泛函研究了NH3和H2O在H型SSZ-13分子筛中的吸附状态,证实了ONIOM方法在该体系中应用的可行性,该方法能在保证结果准确性的前提下大大降低计算成本。然而,以上研究主要集中在富Si仅存在Si(1Al)的SSZ-13分子筛上,富铝SSZ-13分子筛中存在大量Al-Si-Al分布时,其Brønsted酸分布仍未有系统研究。利用氘代乙腈作为探针分子吸附的固体核磁共振技术是表征分子筛中酸强度的有效方法22,23,尤其适用于小孔分子筛。本文采用DFT计算结合多核固体核磁共振技术来研究不同Si/Al比的H-SSZ-13分子筛的Al分布和Brønsted酸性,进一步揭示Brønsted酸强度与对应的骨架铝位置之间的内在关系。为SSZ-13分子筛酸性质调控和理解其在催化反应中的独特性能提供重要参考。
2 实验部分和理论计算方法
2.1 样品制备与固体NMR表征
不同Si/Al摩尔比的H-SSZ-13分子筛(Si/Al =5.8,25)由德国巴斯夫公司(BASF)提供,XRD显示其具有高结晶度的CHA结构12。在氘代乙腈(99.5%)吸附之前,将样品在400 °C真空条件(~10−4Pa)脱水12 h,冷却至室温,在平衡压力(10 kPa,297 K)下进行吸附。最后在N2手套箱中将样品转移到4 mm的ZrO2转子中。所有固体核磁共振实验均在Agilent DD2-500 MHz谱仪上进行,对应1H、27Al、29Si共振频率分别为499.8、130.2和99.3 MHz。29Si MAS NMR谱图在6 mm HX双共振探头上采集,采用高功率质子去偶,π/4脉宽2.8 µs,弛豫延迟为120 s,100次累加,转速为4 kHz,化学位移参考为四甲基硅烷(TMS)。27Al MAS NMR采用4 mm HX双共振探头,样品转速为14 kHz。27Al MAS NMR谱的π/12脉冲宽度为0.3 µs,弛豫延迟为2 s,200次累加,化学位移参考为1.0 mol·L−1Al(NO3)3水溶液。1H MAS NMR谱图在4 mm HX双共振探头上采集,采样π/4脉冲宽度为1.25 μs,转速为10 kHz,弛豫延迟为4 s,扫描64次,化学位移参考物为TMS。采用DMFIT软件及合适的线型对谱图进行分峰拟合。
2.2 计算方法
SSZ-13分子筛的模型取自Calligaris等人24的实验数据,为了确定SSZ-13分子筛中Al原子和B酸中心的落位,计算采用B3LYP和wB97XD两种不同的泛函对簇模型(1Al模型为25T,2Al模型为36T)进行几何优化和取代能计算。几何优化选择6-31G(d,p)基组,单点能计算采用6-311+G(2d,p)基组。所有簇模型中的悬断键用氢原子饱和,Si―H键的朝向和原结构中的Si―O键方向保持一致,其键长设定为1.47 Å25(1 Å = 0.1 nm)。在能量计算中考虑了零点能量校正。为了减少基组叠加误差(BSSE)对吸附模型能量计算结果的影响,采用包含了较大弥散函数的6-311++G(2d,p)基组26。所有计算均在Gaussian 09,Revision D01程序包上进行27。
取代能由公式(1)算得,其中E(nAlH)表示n个Al进入分子筛骨架后的H-SSZ-13模型的能量,E(Si)表示全硅的SSZ-13分子筛的能量。
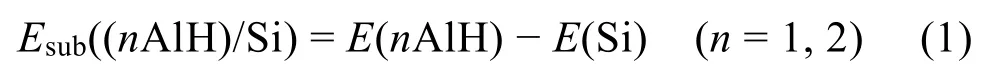
对于Brønsted酸强度的定量测量,选择最可能的Al分布模型进一步进行质子亲和势(PA),NH3脱附能和吸附氘代乙腈后的1H NMR化学位移计算。质子亲和势(PA)是分子筛酸性表征的本征方法,它代表分子筛给出一个质子所需要的能量,Brønsted酸的酸度越强,质子H越容易失去,质子亲和势越小。计算公式如公式(2)所示,其中E(nAln−)表示失去质子H后分子筛骨架的能量。

NH3脱附能计算公式由公式(3)所示,其中E(nAlH-nNH3)、E(nAlH)和E(NH3)分别对应于限制优化后的NH3吸附模型、吸附前H型SSZ-13模型以及完全优化后NH3分子的能量。
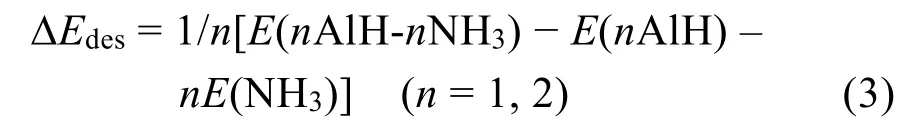
研究表明28–30,簇模型的大小对计算探针分子在分子筛中的吸附结果影响较大。因此我们采用较大的簇模型研究NH3和乙腈在SSZ-13分子筛中的吸附,并采用ONIOM方法,即用高精度的方法计算内层结构,低精度的方法计算外层结构,该方法既能保证计算的准确性也兼顾经济性31–32。只有最外层的Si和H原子被设置为低层,所有其他原子被视为高层。对于低层,3-21G**和3-21G基组分别应用于单点能计算和几何优化,高层的几何优化用6-31G(d,p)基组。计算质子亲和势时高层用6-311+G(2d,p)基组,为了比较不同泛函对计算结果的影响,采用了B3LYP和wB97XD两种泛函对比。我们发现不同泛函对计算结果影响不大,故后续计算只采用一种泛函。6-311++G(2d,p)基组被用于有吸附分子存在的单点能计算,并采用考虑了色散校正的杂化泛函(wB97XD)。计算乙腈吸附后的1H NMR化学位移采用GIAO和B3LYP/pcS-1方法32,33,选择相同方法计算完全优化后的四甲基硅烷(TMS)的1H NMR化学位移作为参考值。
3 结果与讨论
3.1 27Al MAS NMR和29Si MAS NMR
27Al MAS NMR (图1a)显示富铝和富硅HSSZ-13分子筛中主要铝物种是δ 58处的骨架Al而δ−1处的非骨架Al含量较少,并且富铝样品中的骨架铝含量远高于富硅样品。通过定量拟合29Si MAS NMR谱,可以计算出两个样品的骨架硅铝比分别为5.8和25 (图1b)。此外,富铝H-SSZ-13(5.8)的29Si MAS NMR谱显示样品中的Si主要以Q4,Si(1Al)和Si(2Al)形式存在,仅存在由于脱铝导致的少量一元硅羟基(Q3)和二元硅羟基(Q2)信号。富硅H-SSZ-13(25)的29Si信号主要为Q4,仅有少量的Si(1Al)和Q3。根据29Si MAS NMR谱中Si(1Al)和Si(2Al)的强度I1、I2,可以得到Si(2Al)中的Al在所有Al分布中的比例最小和最大值17。(1)假设所有的Si(2Al)均以Al为中心以4个Al-Si-Al形式连接,则没有Al-Si-Al产生的Si(1Al),因而所有Al中Si(2Al)占的比例最少,每个Si(2Al)单元中含有2 × 1/4 = 1/2个Al;(2)假设Si(2Al)均以孤立分布存在,则Si(2Al)中的Al占据了大部分Si(1Al)而导致以Si(1Al)形式存在的Al含量最小,Si(2Al)形式的Al含量最大,每个Si(2Al)分别对应6个Si(1Al),因此所有Al分布中Si(2Al)含量最小和最大值可由如下公式(4)和(5)计算得出。
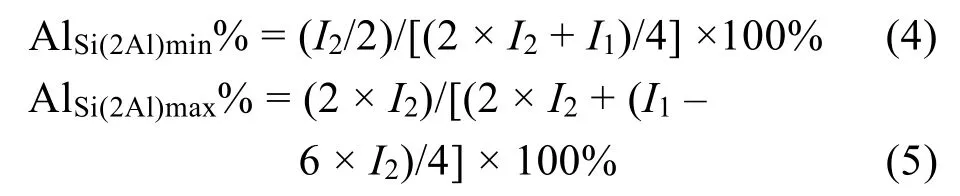
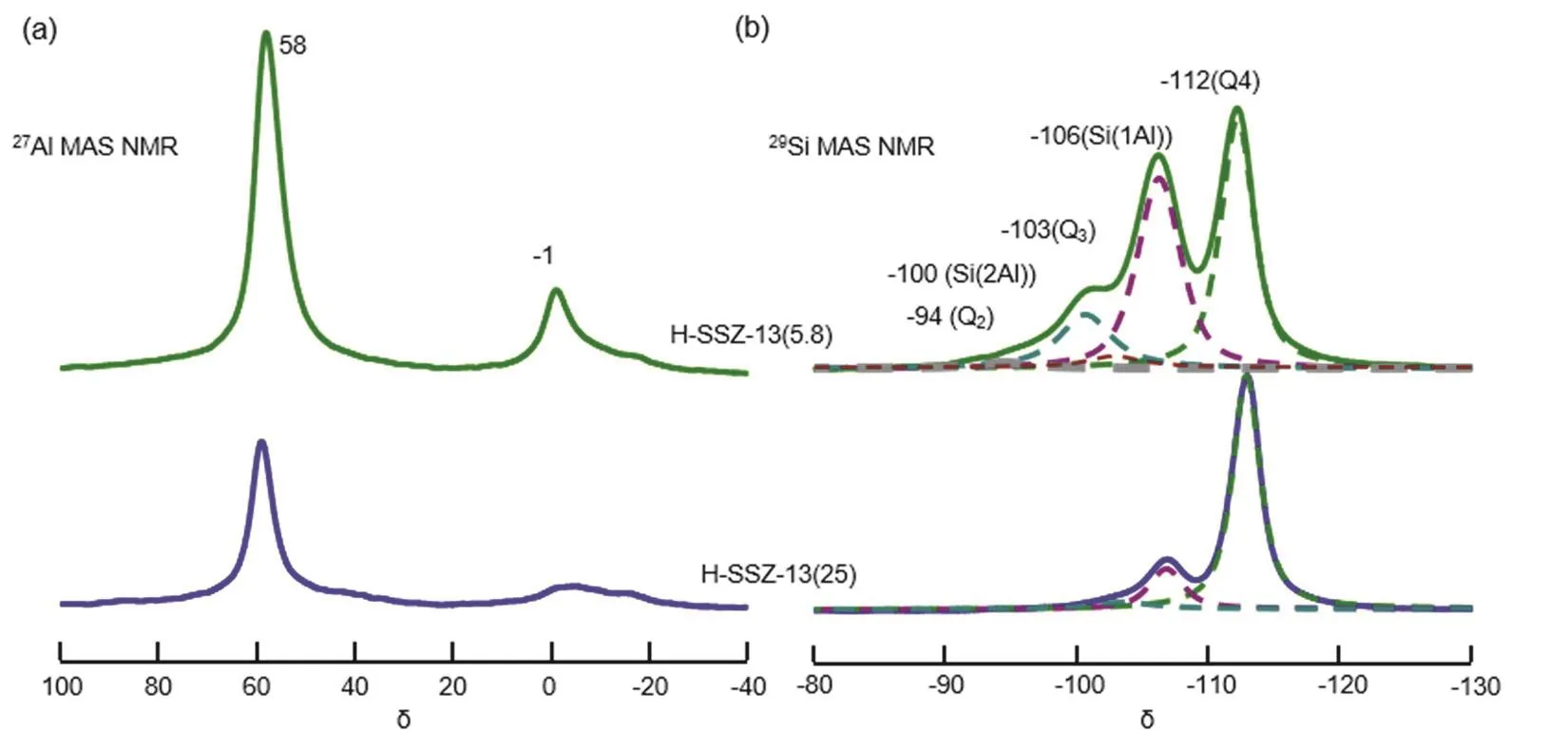
图 1 富铝 H-SSZ-13(5.8)和富硅H-SSZ-13(25)的 27Al MAS NMR (a)和 29Si MAS NMR (b)谱Fig. 1 29Si MAS NMR (a) and 27Al MAS NMR (b) spectra of Al-rich H-SSZ-13(5.8) and Si-rich H-SSZ-13(25).
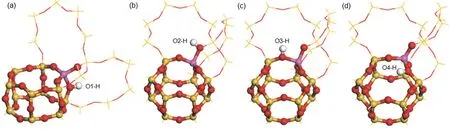
图2 孤立Al位周围四个可能的B酸位Fig. 2 Four possible B acid sites around solo Al atom.Color code: aluminum (pink), silicon (yellow), oxygen (red), hydrogen (white).
通过分峰拟合并积分可以得到富铝H-SSZ-13(5.8)中I1和I2,由上式计算得出Si(2Al)在所有Al分布中所占比例最小为43%,而最高可达100%。
3.2 SSZ-13分子筛中Al分布和B酸位置
29Si MAS NMR只能给出H-SSZ-13分子筛中AlSiAl在所有Al中极端情况下含量的最小和最大值,并不能给出其在CHA笼中的分布。因此,需要通过理论计算来进一步预测富铝H-SSZ-13分子筛中Al的具体位置。SSZ-13分子筛是由相互连接的双六元环(D6R)单元组成的具有四元环、六元环和八元环的多孔沸石,该分子筛所有的T位都位于相同的化学环境中,但和每个T位相连的四个O原子所处的化学环境不完全相同。如图2所示,当Al原子取代Si原子进入分子筛骨架中,根据CHA型分子筛的拓扑结构34将四个O分别标记为O1–O4。O1–O3位点是八元环的一部分,而O4位点是六元环的一部分。结构优化后,我们计算取代能以比较质子位于四个可能的酸位点的稳定性。
从表1中可以看出,质子位于不同的O位上取代能的差异在9 kJ∙mol−1内,当质子与O1位点结合时孤立Al模型的取代能最低,质子落于O3位的取代能次之,表明O1位可能是质子相对易落位的位置,这与大多数研究的观点一致19,35,36。
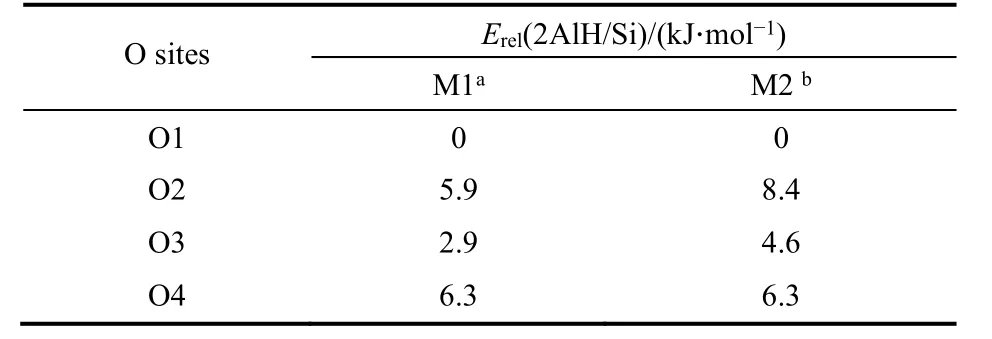
表1 1Al-H模型中的相对替代能Table 1 Relative substitution energies obtained for the 1Al-H types.
对于富铝的SSZ-13分子筛,增加Al原子数量导致两个Al原子之间的距离更近,由图1中29Si MAS NMR结果可知骨架中NNNN序列和NNN序列的数量增加。因此,我们分别比较了NNNN序列和NNN序列中不同落位的2Al模型的替代能,以找出2Al模型中最可能的落位。双六元环单元(D6R)为CHA型分子筛结构中最小的重复单元,对于NNNN序列,两个Al有可能落在同一六元环的对位或分别落在上下两个六元环中(图3a),对于NNN序列也是如此,两个Al有可能落在同一六元环上或分别落在上下两个六元环中即六棱柱侧棱的四元环对位上(图3b)。在孤立的1A1模型中的计算结果显示质子位于O1、O3位更加稳定,且Smith等人37通过中子衍射只观察到这两个位点有质子的存在,因此2Al模型计算中H的位置选取Al原子周围的O1或O3位。如图3,每种Al分布对应于三种不同的酸分布:(1)两个质子都与O1原子连接;(2)两质子都与O3原子连接;(3)一个质子与O1连接,另一个质子与O3连接。
从表2可以看出,当两个Al在同一个六元环的对位,两个质子与O1原子相连时,是Al-Si-Si-Al序列中最易取代的结构。当Si/Al比进一步降低时,有更多的Al-Si-Al序列出现在分子筛骨架中。最易取代的NNN序列是当两个Al原子位于同一四元环的对角位置,两个质子都与O1原子相连,面向不同的八元环孔道。在Y型分子筛中也发现相似的结论38,当Y型分子筛中出现NNN序列时,两个Al原子易分布在同一四环的对角线位置,而Y型分子筛也具有与CHA型分子筛类似的双六元环结构。wB97XD泛函包含了色散相互作用39,从表2我们可以看到,两种不同方法得到的相对取代能差异在8 kJ∙mol−1内,说明色散相互作用对Al原子的相对取代能影响不大。值得注意的是,不同于孤立的Al位,对于2Al取代,质子H位于不同O位上的能量差别很大,质子更倾向于全部位于O1位点。另外,对于NNN序列位于同一六元环时,其取代能略高于Al分布于六棱柱不同六元环的情况(约25 kJ∙mol−1)。富铝SSZ-13分子筛在无有机模板剂条件下合成,Na+为平衡离子,交换成H+后,这两种Al分布(NNN-1和NNN-2)的B酸均可能存在,较大的取代能可能会导致H-SSZ-13分子筛中NNN-1铝相对容易脱除。
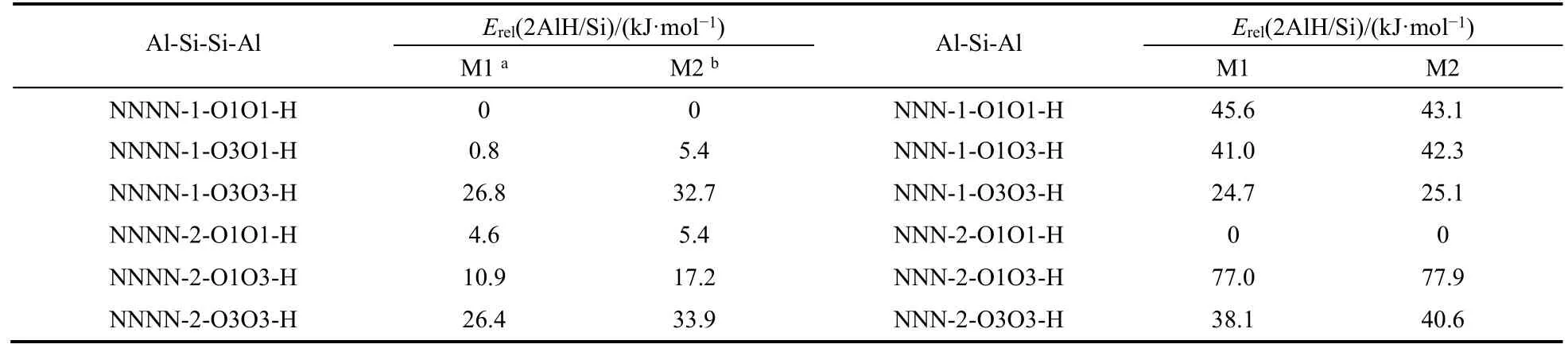
表2 2Al-H模型中的相对取代能Table 2 Relative substitution energies obtained for the 2Al-H types.
3.3 SSZ-13分子筛的B酸强度
分子筛催化剂的Brønsted酸强度与骨架中的Al分布密切相关。基于替代能的计算结果,我们选择1Al和2Al模型中易取代结构计算质子亲和势(PA),NH3脱附能和吸附氘代乙腈后1H NMR化学位移来考察SSZ-13分子筛的Brønsted酸性。由于在富Al分子筛的NNNN和的NNN序列中存在两个Brønsted酸位,因此在比较时将双B酸位的计算值经平均化处理后与孤立Al位的计算值对比。质子亲和势、NH3吸附后的结构参数及脱附能的计算结果如表3所示。
从表3可以看出,孤立Al位周围的B酸位失去质子的PA值为1179.0–1192.4 kJ∙mol−1,NNN序列中的PA值为1823.4–1854.8 kJ∙mol−1,明显高于NNNN序列的PA值(1269.4–1286.2 kJ∙mol−1)和孤立Al位的PA值,同时也可以看到NNNN序列的PA值也是略大于孤立Al位的。即富铝SSZ-13分子筛的平均PA值显著大于富硅SSZ-13的PA值。因此通过PA值的变化可以看出富铝SSZ-13分子筛较富硅的SSZ-13分子筛具有更弱的B酸强度。

表3 1Al和2Al易取代构型的质子亲和势(PA)、NH3吸附后的结构参数及脱附能Table 3 Proton affinities (PA), geometry parameters and NH3 desorption energies for the most possible models.

图3 Al-Si-Si-Al和Al-Si-Al序列可能的Al分布与B酸位置Fig. 3 Possible Al locations and acid sites in Al-Si-Si-Al and Al-Si-Al sequences.
NH3经常被用作探针分子来检测分子筛催化剂的酸性,根据NH3在分子筛表面的吸附量和脱附温度获得酸量和酸强度的信息。通过理论计算的方法,我们得到了NH3吸附在SSZ-13分子筛上的构型,如图4所示。可以看到,H型SSZ-13分子筛吸附氨气后分子筛骨架上H―OSSZ-13键长延长,在1Al模型中为1.62 Å,而H―NH3距离缩短,在1Al模型中为1.06 Å,因此氨气吸附后NH3分子以NH4+离子形式位于SSZ-13分子筛的八元环平面内,与分子筛骨架形成三个氢键。其中一个氢键是与Al旁边的O1成键,另外两个氢键是和八元环内上下两个Si原子相邻的O3成键(图4)。这与Solans-Monfort等人21采用周期性方法和簇模型计算孤立Al位的SSZ-13分子筛吸附NH3后的几何参数和吸附能的研究结果一致。而对于2Al模型,和1Al情况类似,两个NH3分子吸附后以NH4+离子形式分别位于不同的八元环平面内,与分子筛骨架形成三个氢键。但从表3中可以看出,NNNN序列和NNN序列中NH4+和O1之间的距离d(NH+4-O)相对于1Al模型持续减小,而NH4+离子内NH3和H+之间的键长d(NH3-H)持续增大。对于模型中有两个NH3分子的情况,Edes是两个NH3分子脱附能的平均值。对于孤立Al位,脱附能计算值为133.6 kJ∙mol−1,而NNNN序列的脱附能略有减小,为130.6 kJ∙mol−1。对于NNN序列,脱附能进一步减小,为124.3 kJ∙mol−1。说明吸附在富铝SSZ-13的B酸位上的NH3相对于富硅SSZ-13更容易脱附,尤其是在NNN这样的Al分布下,这和上面质子亲和势的结果一致。
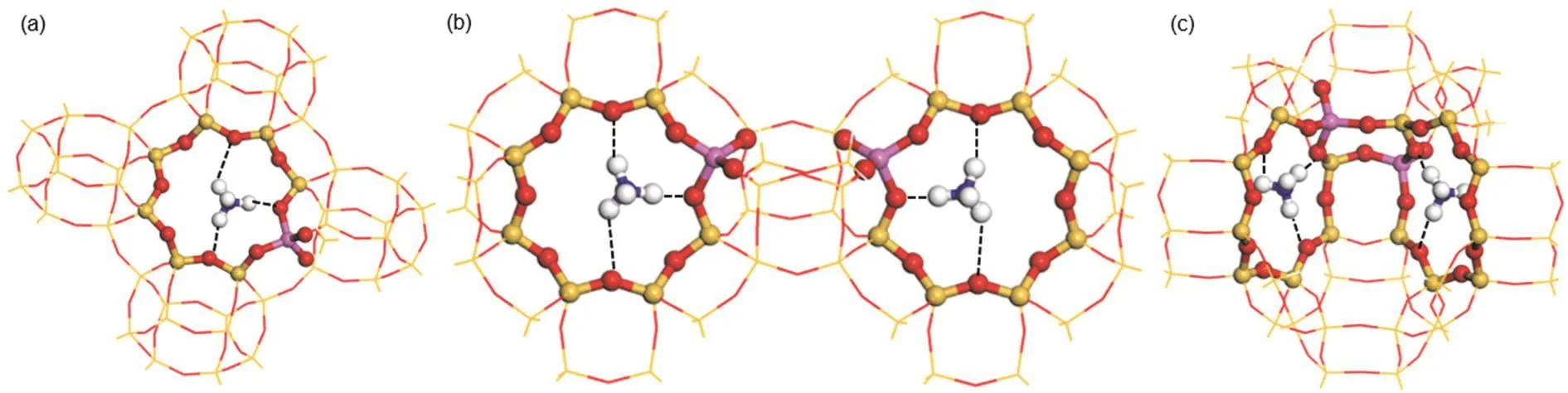
图4 在SSZ-13分子筛1Al和2Al优化模型上吸附氨分子后的平衡构型Fig. 4 Equilibrium geometries of ammonia molecules adsorbed on the optimized 1Al model and 2Al models of SSZ-13 zeolite.
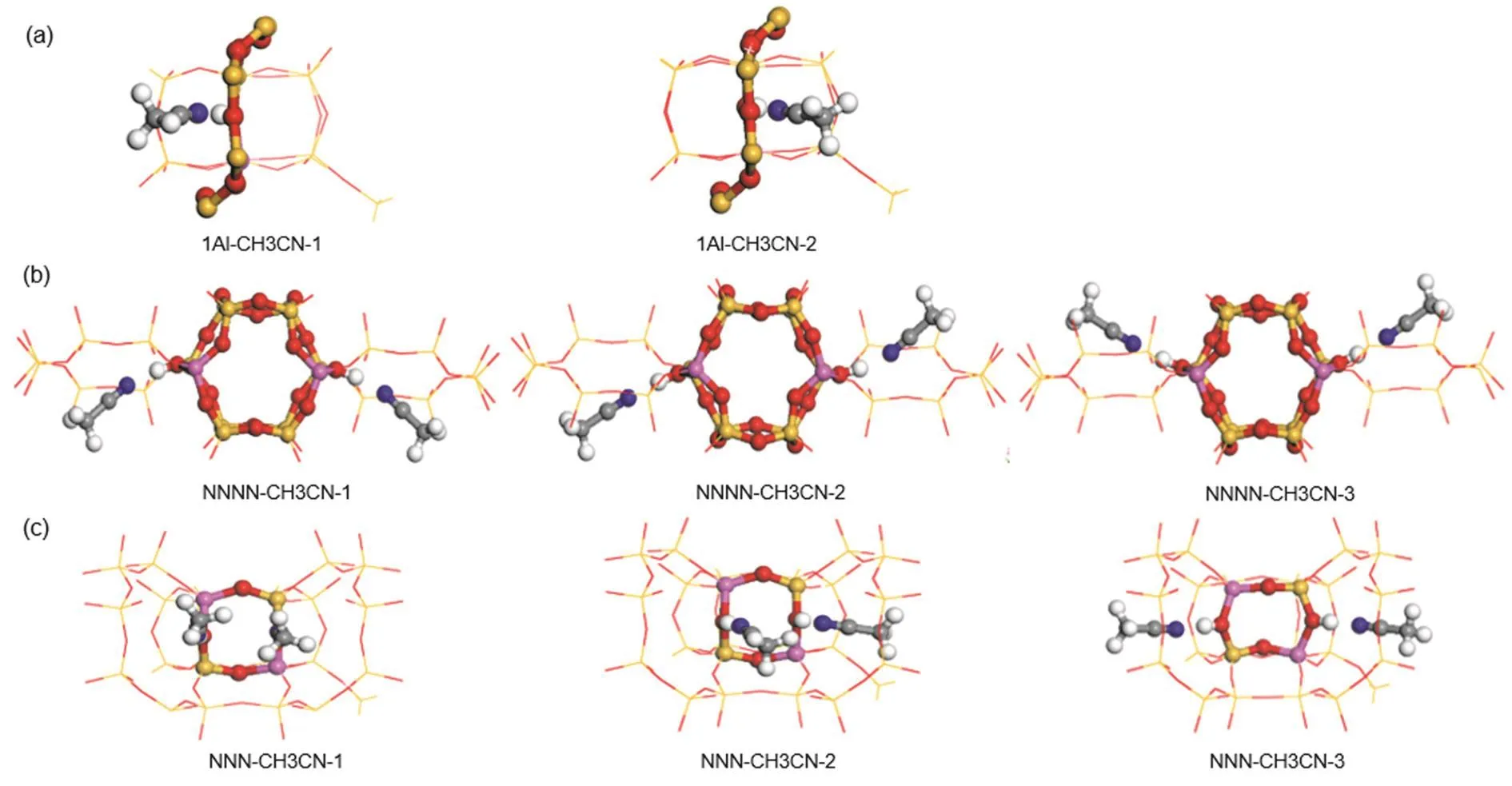
图5 在SSZ-13分子筛1Al和2Al优化模型上吸附氘代乙腈后的平衡构型Fig. 5 Equilibrium geometries of d3-acetonitrile molecules adsorbed on the optimized 1Al model and 2Al models of SSZ-13 zeolite.
为了进一步理解SSZ-13分子筛的B酸强度与Al分布的关系,我们将弱碱性的氘代乙腈作为探针分子吸附到分子筛孔道中,如图5所示。在1Al取代时(图5a),氘代乙腈分子的线性C-C-N轴位于分子筛八元环外,在B酸中心处有两个可能的吸附位置。这两个位置关于八元环呈镜像对称,两种不同结构所有的几何参数都相当,氘代乙腈还是以分子的形式存在于孔道中,未和骨架中的H质子形成离子。当骨架中增加一个Al原子取代Si原子时,会产生另一个B酸位点,因此当两个氘代乙腈分子吸附在富铝的SSZ-13分子筛上时,有三种可能的吸附结构(图5b,c),第一种情况为两个氘代乙腈分子分别朝向两个八元环平面的前侧;第二种情况为一个氘代乙腈分子朝向一个八元环平面的前侧,另一个氘代乙腈分子朝向另一个八元环平面的后侧;第三种情况为两个氘代乙腈分子分别朝向两个八元环平面的后侧。氘代乙腈吸附后的具体结构数据如表4所示,可以看出氘代乙腈分子偏向八元环不同侧时,对于1Al和2Al模型,各个吸附结构的吸附能差距在5 kJ∙mol−1内,从能量上无法分别哪种吸附结构更稳定,实际情况中这些结构可能有相同的出现概率。
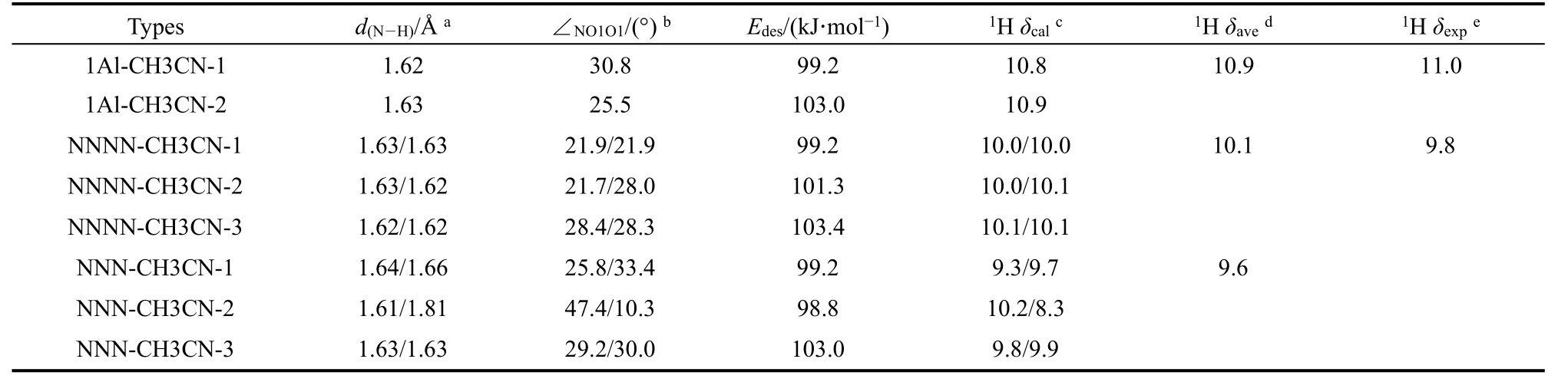
表4 SSZ-13分子筛上吸附氘代乙腈后的结构参数、吸附能和1H NMR化学位移Table 4 The geometry parameters, adsorption energies and 1H NMR chemical shifts of d3-acetonitrile adsorbed on SSZ-13 zeolite.
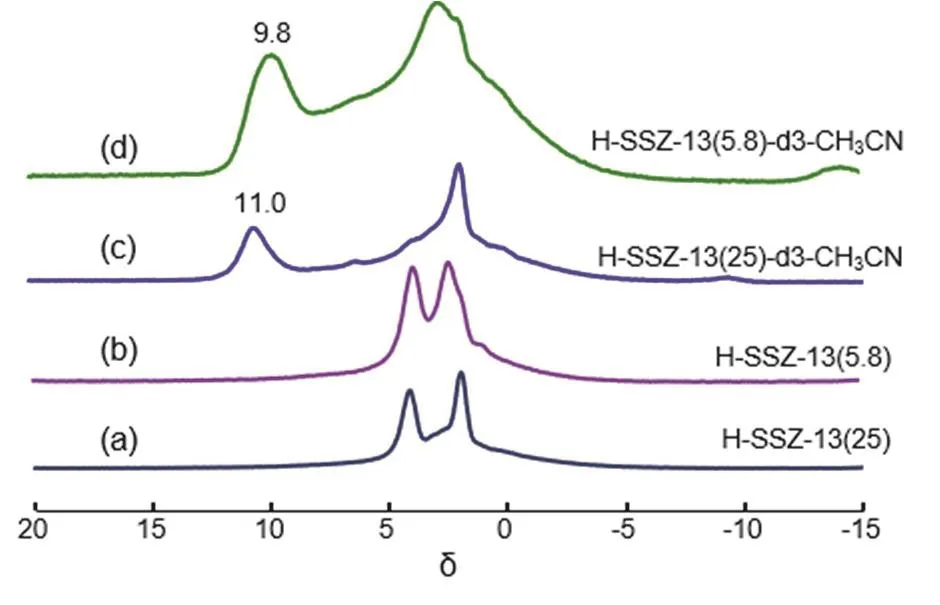
图6 吸附氘代乙腈前(a,b)后(c,d)不同硅铝比H-ZZS-13的1H MAS NMR谱Fig. 6 1H MAS NMR spectra of H-SSZ-13 with different Si/Al ratios before (a, b) and after d3-acetonitrile adsorption (c, d).
氘代乙腈吸附后的1H NMR化学位移是表征B酸强度的有效手段,吸附氘代乙腈后1H化学位移出现在低场表明该B酸中心的酸度更强40。从计算的1H NMR化学位移可以看到,孤立Al模型中氘代乙腈吸附的两个模型具有相同的1H NMR化学位移。在富Al的情况下,当在一个氘代乙腈在八元环一侧而另一氘代乙腈在八元环平面的另一侧时,两个酸性位点的1H NMR化学位移有细微的差别,该差异可能是由于模型尺寸限制导致的计算偏差。但实际的SSZ-13分子筛孔道中八元环平面两侧的化学环境是相同的,因此采用平均化学位移更可靠。图6显示了吸附氘代乙腈的H-SSZ-13分子筛的1H MAS NMR谱,吸附前高硅(图6a)和富铝(图6b)HSSZ-13分子筛中均存在1H NMR δ 1.9、2.4和4.1的三个信号,分别对应为Si―OH、Al―OH及B酸信号18,32。富Al的H-SSZ-13分子筛具有更多的B酸量。吸附氘代乙腈后,δ 4.1处B酸信号消失,且高硅(图6c)和富铝(图6d)的SSZ-13分子筛分别在δ 11.0和δ 9.8处出现新的信号,该信号归属为骨架中B酸位点的H和氘代乙腈之间形成的氢键41。富铝SSZ-13的NNNN序列和NNN序列吸附氘代乙腈后1H NMR化学位移计算值在9.6–10.1,与实验中H-SSZ-13(5.8)上吸附氘代乙腈后δ 9.8处谱峰一致,而富Si的H-SSZ-13(25)吸附后的1H NMR化学位移实验值为11.0,与孤立Al模型的计算值(δ 10.9)一致。这说明富Al分子筛中Al分布多以NNNN和NNN形式出现,而富硅分子筛中多存在孤立的Al原子。富Al的SSZ-13分子筛吸附氘代乙腈后的1H NMR化学位移和富Si的相比向高场移动,这进一步证明了富Al的SSZ-13分子筛具有较弱的Brønsted酸强度。
4 结论
本文采用DFT计算结合固体核磁共振研究了不同硅铝比的H-SSZ-13分子筛上Al分布和B酸酸性。发现对于高硅H-SSZ-13分子筛主要是孤立Al的分布形式,H位于不同的O位能量差比较小,Al周围的质子H位于O1时最稳定。富铝H-SSZ-13分子筛中,Al主要以NNNN和NNN分布形式存在,质子位于O1位点时,Al原子替代骨架Si原子的替代能比位于其他位点的显著降低。两个Al位于同一六元环对位和两个Al位于同一四元环对位分别是富铝H-SSZ-13中NNNN和NNN取代的最稳定的Al分布。通过计算质子亲和能,NH3吸附能和氘代乙腈吸附的1H NMR化学位移,发现随着Al含量的增加,Brønsted酸强度趋于减弱,主要由于Si(2Al)分布增加所致。这与29Si MAS NMR和氘代乙腈吸附后1H MAS NMR谱图的实验结果一致。
