《2019年美国肝病学会实践指引和指南:成人和儿童自身免疫性肝炎的诊断与治疗》摘译
2020-04-24崔娜娜王绮夏审校
崔娜娜, 王绮夏 译, 马 雄 审校
上海交通大学医学院附属仁济医院 消化内科, 上海市消化疾病研究所, 上海 200001
2019年美国肝病学会(AASLD)发布的实践指引和指南是对2010年版自身免疫性肝炎(AIH)指南的更新,从而在现有证据和专家意见的基础上为AIH的诊疗提供指引,并在系统回顾文献和证据质量的基础上为相关临床问题提供指导。该实践指引更新了成人和儿童AIH的流行病学、诊断、治疗和预后,包括两个部分:指导性建议和指引性声明。指导性建议均基于对医学文献的系统回顾所获得的证据,并在适当时通过Meta分析予以支持。指引性声明是指由专家小组在正式审查和分析已发表文献的基础上协商一致后达成的共识。
AIH是一种免疫介导的无明确病因的炎症性肝病,患病人群涉及所有年龄、性别和种族。女性在成人(71%~95%)和儿童(60%~76%)患者中均占比较大。临床表现可为无症状、慢性病程或出现急性肝衰竭。所有急、慢性肝炎患者,包括肝移植术后移植物功能障碍者,均应考虑本诊断。AIH无特异性诊断指标,诊断基于临床表现、生化检查、血清免疫学和组织学表现的综合诊断。AIH可进展至肝纤维化、肝硬化、肝衰竭死亡或肝移植。免疫抑制治疗可改善预后,但需长期维持。相关定义见表1。
1 AIH诊断
指引性声明:(1)AIH的诊断需要符合本病特点的肝组织学检查结果支持,并符合以下特征:①血清转氨酶水平升高;②血清IgG水平升高和(或)一种或多种自身抗体阳性;③排除其他可导致慢性肝炎的病因:病毒性、遗传性、代谢性、胆汁淤积性,以及药物可能诱发类似AIH的疾病(图1)。
指引性声明:(2)初始血清学检测应包括,①成人:ANA和SMA;②儿童:ANA、SMA和抗LKM1。如有必要,考虑额外的自身抗体检测以确保诊断。
注:1)肝硬化患者在生化缓解后IgG可能持续升高;INR,国际标准化比值。
AIH根据特异性自身抗体不同可分为2型:1型以ANA和(或)SMA/抗肌动蛋白抗体阳性为特征;2型以抗LKM1阳性为特征。此外,高达20%的AIH患者中上述自身抗体呈阴性(即血清阴性AIH)。对于那些常规自身抗体阴性且仍疑诊AIH的患者,可以考虑加测额外的自身抗体。抗可溶性肝抗原抗体存在于7%~22%的1型AIH患者中,对诊断具有高特异度(99%),且与疾病严重程度和停药后复发有关。非典型pANCA常见于1型AIH(50%~92%),但缺乏诊断特异性,也可见于PSC、AIH-PSC重叠综合征等。
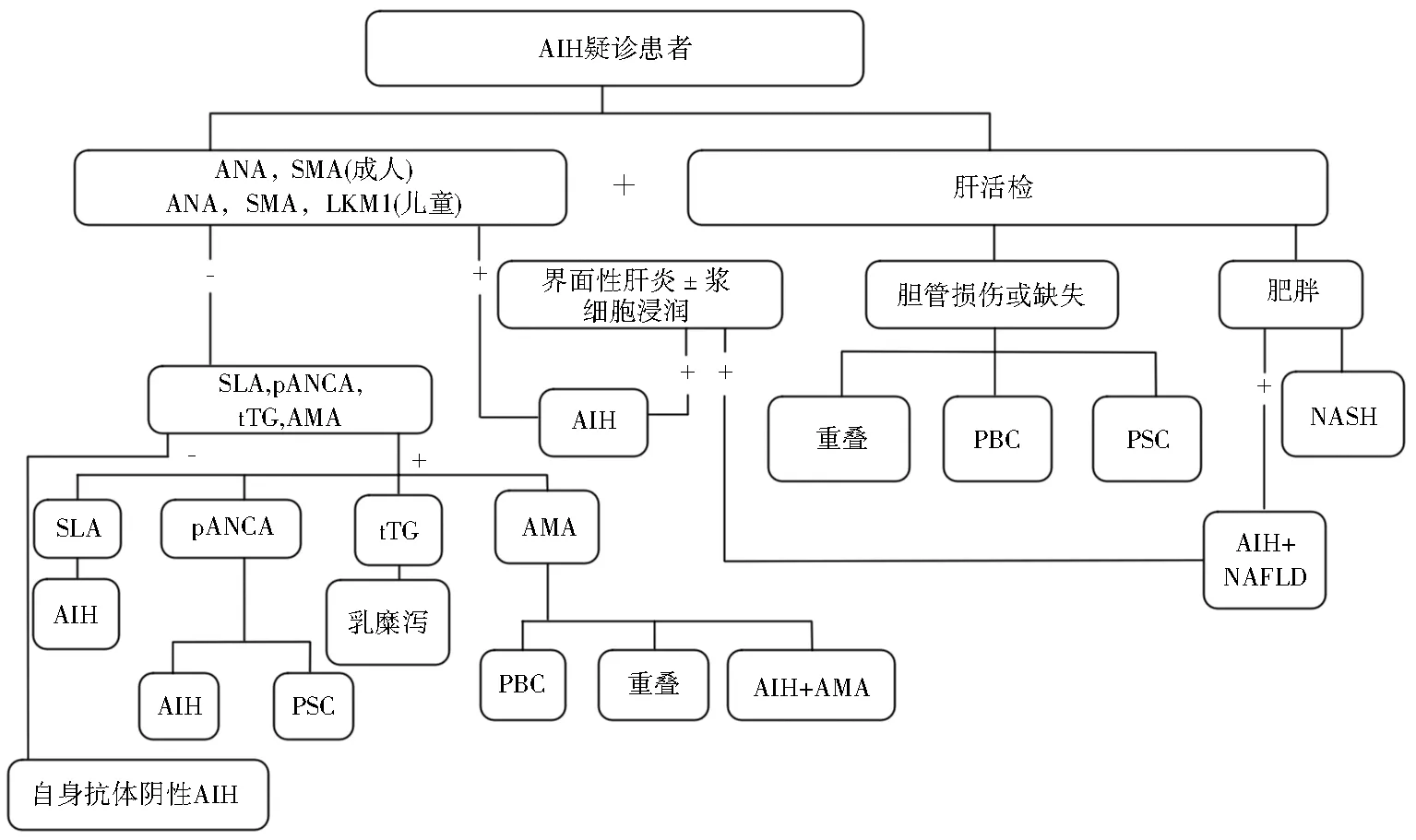
注:ANA,抗核抗体;SMA,平滑肌抗体;LKM1,肝肾微粒体抗体1型;SLA:抗可溶性肝抗原;pANCA:核周型抗中性粒细胞胞浆抗体;tTG:抗组织谷氨酰胺转移酶;AMA: 抗线粒体抗体;PBC:原发性胆汁性胆管炎;PSC:原发性硬化性胆管炎;NASH:非酒精性脂肪性肝炎;NAFLD:非酒精性脂肪性肝病。
图1AIH诊断流程图
指引性声明:(3)启动治疗前,不典型或疑难病例应请有经验的肝病中心审核或直接转诊。
2 临床表现
指引性声明:(1)所有急性或慢性肝病患者,包括无症状肝功能异常、急性肝衰竭和常规自身抗体阴性肝炎患者,都必须考虑AIH的诊断。
AIH患者起病时多以慢性非特异性症状(疲劳、不适、关节痛或闭经)为主。25%~34%的AIH患者不出现临床症状。无症状者很少有自发的实验室指标改善(12%),组织学检查可提示病情,且10年生存率较低。无症状患者应接受治疗。
25%~75%的AIH患者表现为急性起病(持续时间<30 d)。3%~ 6%的北美和欧洲患者发生与肝性脑病相关的急性肝衰竭(ALF)。急性重症AIH患者中29%~39%存在ANA弱阳性,血清IgG水平正常率为25%~39%。组织学检查是关键,小叶性肝炎、淋巴-浆细胞浸润和界面性肝炎支持急性AIH的诊断,肝硬化的相似症状提示慢性病情加重。AIH患者发生急性肝衰竭时可出现中心性静脉炎、淋巴-浆细胞浸润、淋巴滤泡和大面积肝细胞坏死。在65%的急性重症AIH患者中,平扫CT显示肝内不均匀低密度区域,可能存在疾病特异性。
在北美和德国最初被诊断为隐源性肝炎,后经修订的诊断评分系统重新被归类为AIH的患者中,19%~34%的患者ANA、SMA和抗LKM1检查缺失。ANA和SMA可能在病程后期表达,抗可溶性肝抗原抗体和非典型pANCA的出现提示AIH。
指引性声明:(2)AIH患者诊断时应进行乳糜泻和甲状腺疾病的筛查。
指引性声明:(3)AIH患者应根据症状来评估是否合并类风湿关节炎、炎症性肠病、自身免疫性溶血性贫血、糖尿病和其他肝外自身免疫性疾病。
14%~44%的AIH患者常与其他自身免疫性疾病并存。1型AIH患者中最常见的是自身免疫性甲状腺疾病(10%~18%),2型AIH患者中更为常见的是1型糖尿病、自身免疫性甲状腺疾病和自身免疫性皮肤病(白癜风、白细胞增生性血管炎、荨麻疹、斑秃)。
指引性声明:(4) AIH患者若实验室检查/组织学结果与PBC一致,且AMA呈阳性者应考虑为AIH-PBC重叠综合征。
指引性声明:(5) “巴黎标准”有助于诊断AIH-PBC重叠综合征,但该标准可能排除胆汁淤积程度较轻的AIH-PBC患者。
“巴黎标准”有助于识别AIH-PBC重叠患者。PBC应符合以下三项标准中的两项:(1) ALP≥2 倍正常值上限(ULN) 或 GGT≥5×ULN; (2) 抗线粒体抗体阳性; (3) 肝活检提示典型的胆管病变。AIH应符合下列至少两条可诊断: (1) ALT≥5×ULN; (2) 血清 IgG≥2×ULN 或 SMA 阳性; (3)肝活检显示门静脉周围或小叶间隔中重度碎屑样坏死伴淋巴细胞浸润。对“巴黎标准”和AIH评分系统的单中心比较发现,“巴黎标准”更可靠(敏感度92%,特异度97%)。然而,对于胆汁淤积程度较轻的AIH-PBC重叠综合征患者,“巴黎标准”可能漏诊。
指引性声明:(6)对于AIH患者,若实验室检查结果提示胆汁淤积,组织学显示胆管损伤或丢失以及并发慢性溃疡性结肠炎,建议进行胆管造影来评估是否存在AIH-PSC重叠综合征。
指引性声明:(7) 修订或简化版的IAIHG AIH诊断评分系统均不应用于评估重叠综合征。
AIH-PSC重叠综合征的诊断标准[在儿童中也称为自身免疫性硬化性胆管炎(autoimmune sclerosing cholangitis,ASC)]包括存在AIH典型特征、AMA的缺失、内镜或磁共振胆管造影证实的大胆管型PSC,或组织学上基于“洋葱皮样”的胆管周围纤维化的小胆管型PSC的诊断依据。
16%的AIH成人患者伴发慢性溃疡性结肠炎(ulcerative colitis,UC),42%的AIH伴发UC患者中出现PSC的胆管造影改变。20%AIH患儿伴发UC,且AIH-PSC重叠综合征的发病率高达45%。所有AIH和慢性UC患者、不明原因的胆汁淤积或对常规糖皮质激素治疗无效者应考虑AIH-PSC重叠综合征的诊断。
3 药物性自身免疫性肝损伤
指引性声明:(1)在AIH鉴别诊断中,必须考虑药物诱导的自身免疫性肝损伤。
指引性声明:(2)必须停用致病药物,并持续随访以确保实验室检测结果缓解。
药物性肝损伤可能与AIH相似,2%~17%具有AIH典型特征的患者存在未知的特异性或超敏反应。米诺环素、呋喃妥因和英夫利昔单抗为最常见引起AIH的药物。从接触药物到发病的潜伏期常为1~8周至3~12个月,呋喃妥因和米诺环素的潜伏期可超过12个月。临床病史应详细说明已接触过的所有药物和膳食补剂。药物诱发的AIH组织学表现与经典AIH相似,但多数情况下无进展期肝纤维化或肝硬化。
诊断由急性起病、超敏反应特征、所涉及药物的已发表文献、药物暴露于肝损伤潜伏期以及无纤维化进展或肝硬化出现进行综合判断。对于诊断不明确、实验室结果提示严重肝损伤,或考虑使用糖皮质激素治疗的患者,建议行肝活检来帮助诊断和指导治疗。
指引性声明:(3)对于药物诱导的AIH,当症状或疾病活动严重(如符合Hy’s定律)或症状和实验室检查结果在停药后未能改善甚至恶化时,应启动糖皮质激素治疗。
指引性声明:(4)停用糖皮质激素后实验室检测结果再次升高者,则提示AIH并需要免疫抑制剂治疗。
治疗需停用致病药物,且密切监测直到临床症状和实验室指标好转。病程常为1个月(少数为3个月)。根据“Hy’s定律”,9%~12%患者中血清转氨酶水平>3×ULN和血清总胆红素水平>2×UNL者死亡风险或肝移植需求增加。满足“Hy’s定律”标准或在观察期内,停药后症状和实验室检查结果恶化的患者,糖皮质激素应继续使用。药物性自身免疫性肝损伤的预后良好。
4 无创性肝纤维化评估
指引性声明:(1) 评估肝纤维化的血清学指标,不适用于AIH患者。
评估肝纤维化的血清学指标,如Fibro-Test、血清AST/PLT比值指数、纤维化-4指数和增强型肝纤维化测试在AIH中的作用及其在评估肝纤维化进展或逆转、预后、肝细胞癌风险和治疗结果等方面的相对价值尚不清楚。
指引性声明:(2)瞬时弹性成像可以准确评估AIH患者的进展期纤维化或肝硬化程度,但应在AIH有效治疗6个月后使用,以避免肝脏炎症的混杂效应。
超声振动控制瞬时弹性成像(VCTE)或FibroScan®与AIH的纤维化组织学分级密切相关,但治疗的前3个月内的测量数值准确性较低。VCTE测量的肝硬度受炎症和纤维化的双重影响,VCTE结果与炎症的组织学分级相关而非纤维化分期。在有效进行至少6个月的免疫抑制治疗以减轻肝脏炎症后,VCTE可以准确诊断肝硬化,并可将进展期纤维化(F3、F4)与早期阶段(F0~F2)区分开来。肝硬度改善与生化缓解、纤维化消退和良好预后相关。
5 治疗前评估
指引性声明:(1)在开始硫唑嘌呤治疗之前,建议在AIH患者中进行硫嘌呤甲基转移酶(TPMT)活性缺失或接近缺失个体的筛查。
治疗前检测TPMT活性可预测接受硫唑嘌呤或6-巯基嘌呤(6-MP)治疗时存在的严重骨髓抑制毒性。低TPMT活性仅发生在0.3%~0.5%的正常人群中。血液TPMT活性的基因型和表型筛查并不能减少常见硫唑嘌呤或6-MP其他副作用的发生率,如恶心、皮疹和关节痛,且TPMT活性正常不能排除AIH患者发生剂量依赖性毒性(细胞减少)。
指引性声明:(2) 根据疾病控制与预防中心的指南,建议所有考虑AIH诊断的患者均应接种与其年龄段相匹配的疫苗。
疫苗接种详情建议在免疫抑制治疗启动之前查阅并及时更新。不建议高剂量免疫抑制剂治疗者接种减毒活疫苗,重组疫苗和灭活疫苗相对而言比较安全。免疫抑制患者对疫苗的应答率较低,但仍可起到保护效果。
指引性声明:(3) AIH患者中未接受HAV和HBV疫苗预防接种者,应在免疫抑制治疗启动前接种。
大多数自身免疫性肝病患者对HAV(51%)和HBV(86%)易感,感染率分别为1.3/1000人年和1.4/1000人年。在所有接种甲型肝炎疫苗的患者和76%接种乙型肝炎疫苗的患者中可测得保护性抗体,接种失败主要为同期的免疫抑制治疗。
6 治疗前咨询
指引性声明:(1) 应在治疗开始时主动识别并解决长期服药依从性的潜在障碍,并在治疗开始后进行监测。
开始治疗前,应先行咨询以确保患者既了解到药物的积极益处和潜在副作用,也要获知治疗性缓解和治疗后未充分应答的相关风险。
指引性声明:(2) 在AIH的整个治疗过程中,应监测抑郁症的表现和生活质量的变化,并可通过结构化、有效的问卷对其进行客观评估。
相较于一般人群而言,抑郁和焦虑在AIH患者中更为常见,主要原因在于患者担忧疾病的进展。抑郁与身体疲劳密切相关,焦虑主要源于对疾病的性质、结局及治疗的误解,从而导致患者依从性低。
健康相关生活质量评估的低分值与使用糖皮质激素密切相关。在糖皮质激素治疗期间,患者治疗前的心理障碍,特别是抑郁可加剧。抑郁、焦虑和糖皮质激素相关情绪不稳定的综合效应可影响治疗效果。这些表现可通过结构化、有效的问卷来进行评估,如12项简表调查、患者健康问卷的抑郁模块和通用焦虑症筛查问卷(GAD-7)。
7 妊娠咨询
指引性声明:(1)有生育意向的患者应在受孕前1年内达到AIH生化缓解。
指引性声明:(2)有生育意向的妇女应接受产前咨询,了解活动期AIH对妊娠的显著不良影响以及妊娠期间和之后疾病复发的风险。
指引性声明:(3)整个妊娠期间应继续服用糖皮质激素和(或)硫唑嘌呤的维持剂量。
指引性声明:(4)妊娠期间禁止使用吗替麦考酚酯(MMF),在开始MMF治疗之前,育龄期女性应了解MMF对妊娠的不良影响。
孕期使用MMF与妊娠早期流产和出生缺陷相关,最常见的是耳朵、心脏和唇裂缺陷。因此,妊娠期应避免服用MMF。美国食品药品监督管理局建议在开始使用MMF的1周内进行妊娠测试,并在使用MMF前4周和后6周采用两种有效的节育方法。在哺乳期母亲的乳汁中亦可检测到少量的MMF。
指引性声明:(5)妊娠期或计划在次年怀孕的肝硬化女性患者应在妊娠前或妊娠中期通过内镜筛查静脉曲张,并进行套扎治疗。
妊娠期肝硬化患者,逐渐增加的血容量可导致静脉曲张出血的风险增加。由于β-受体阻滞剂和特利加压素在妊娠期有潜在的不良影响,因此必须通过曲张静脉套扎术进行早期识别和治疗干预。妊娠期间内镜检查的安全性已在其他指南中进行阐述。
指引性声明:(6) 应在产后前6个月密切监测女性AIH患者,从而早期发现疾病复发。
8 治疗
指导性建议:(1)对于未经治疗的AIH儿童和成人患者,若非肝硬化或急性重症者,AASLD建议将布地奈德联合硫唑嘌呤,或泼尼松(龙)联合硫唑嘌呤作为初始一线治疗方案(条件性推荐,确定性低)(图2)。
布地奈德(肝脏有90%的首过效应)联合硫唑嘌呤治疗AIH初治患者的疗效和安全性在一项随机试验中得到证实。服用布地奈德(3 mg/d,3 次/d,缓解后减至2 次/d)和基础体质量剂量的硫唑嘌呤(1~2 mg·kg-1·d-1)患者在治疗6个月后获得生化缓解,与泼尼松(40 mg/d逐渐减至10 mg/d)相比,前者获得缓解率更高(60% vs 39%),且类固醇特异性副作用更少(28% vs 53%)。骨密度的维持是布地奈德治疗的一个潜在长期获益点。
指导性建议:(2) 对于伴有肝硬化的儿童和成人AIH患者或急性重症AIH者,AASLD不建议使用布地奈德(条件性推荐,确定性非常低)(表2)
肝硬化患者不应使用布地奈德,因为门体分流可降低药物疗效并促进类固醇特异性副作用发生。布地奈德在急性重症AIH或急性肝衰竭中作为一线治疗药物的作用未知,因此不建议在此类情况下使用。
指导性建议:(3)对于一线药物治疗失败、不完全应答或不耐受的AIH儿童或成人患者,AASLD建议使用MMF或他克莫司达到并维持生化缓解(条件性推荐,确定性低)。
MMF用于对硫唑嘌呤不耐受或对糖皮质激素/硫唑嘌呤治疗不完全应答或治疗失败的AIH患者。MMF治疗耐受性良好,合并不良事件发生率为14%,仅8%的患者停止治疗。一项Meta分析提示MMF和泼尼松联合治疗是目前最广泛使用的二线疗法,MMF方案使血清AST和ALT水平降低79%,组织学缓解率为89%。在治疗失败的儿童患者中也有类似发现。
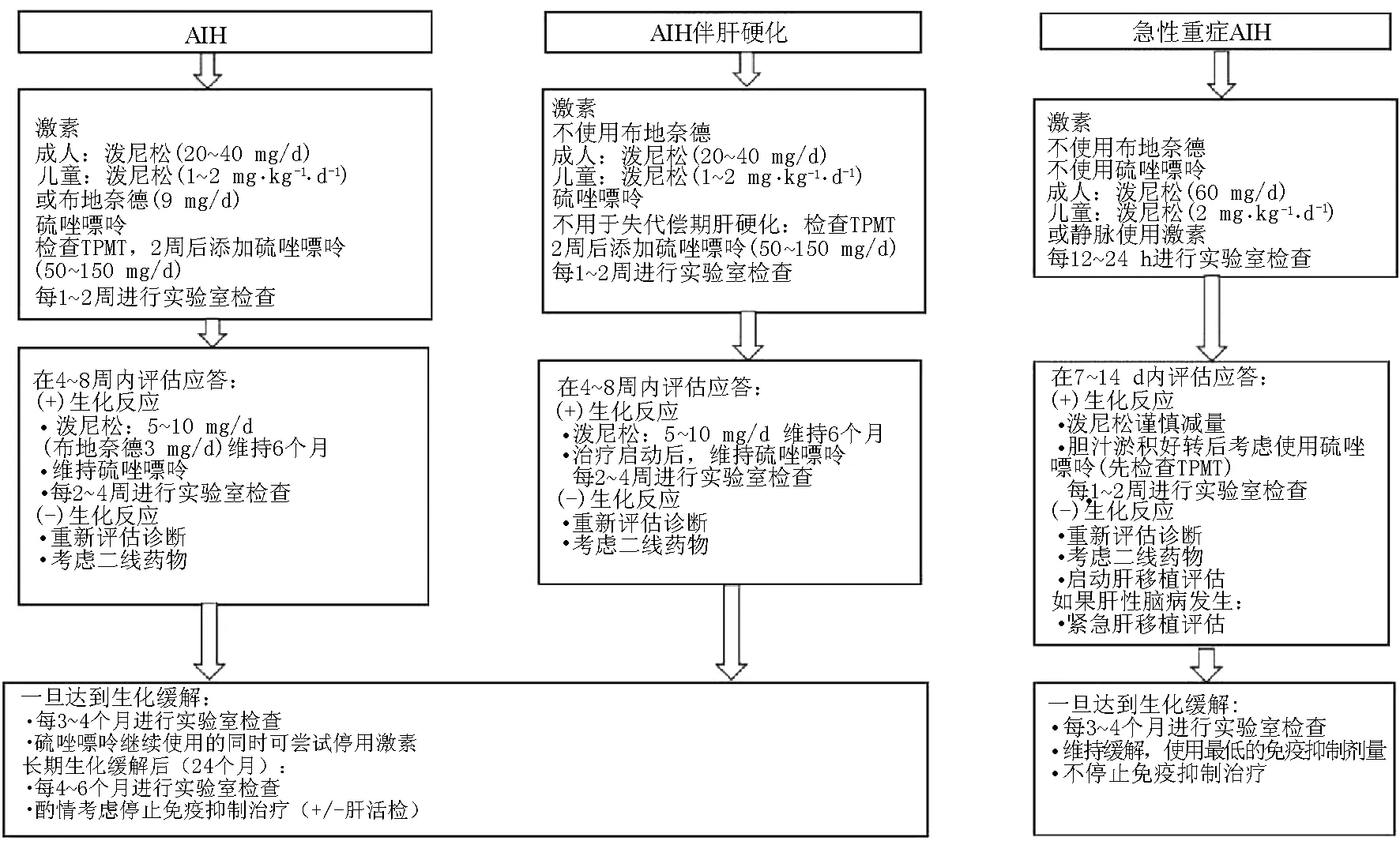
图2 AIH一线治疗

表2 AIH一线治疗药物相关副作用
在治疗失败、不完全应答和对硫唑嘌呤不耐受患者的多项研究证实了他克莫司的可观疗效。两项关于成人二线治疗的Meta分析显示,75%~94%的患者血清转氨酶得到改善或正常化。单中心的儿童研究中也报道了相似应答率,因副作用需减少剂量或停用他克莫司的发生率约为25%。最常见的副作用是神经系统症状(震颤、头痛)、肾脏并发症(高血压、肾功能不全)和脱发。与他克莫司相比,环孢素是AIH合并糖尿病患者的二线治疗选择。
指导性建议:(4)基于易用性和副作用,AASLD建议在AIH患者中使用MMF优先于他克莫司作为二线临床用药(条件性推荐,确定性非常低)。
指引性声明:(1)急性重症AIH患者应单独使用泼尼松(龙)进行试验性治疗,而AIH相关ALF患者应直接进行肝移植评估。
指引性声明:(2)急性重症AIH患者在糖皮质激素治疗1~2周内实验室检查无改善或临床症状恶化者,应进行肝移植评估。
当AIH患者表现为急性重症AIH或ALF时,治疗将面临极大挑战。糖皮质激素治疗的潜在优势须与其风险相权衡,即延迟肝移植和感染。糖皮质激素治疗[通常是泼尼松(龙)单药治疗,成人0.5~1 mg·kg-1·d-1,儿童高达2 mg·kg-1·d-1]对20%~100%的急性重症AIH患者有效,不增加败血症发生,但与总体生存率的提高无关,且MELD评分>40的患者生存率较低。急性重症AIH患者治疗成功的关键是迅速放弃无效治疗(根据临床状况和治疗反应,在1~2周内),并进行肝移植。
指引性声明:(3)少数患者可以停药并实现AIH长期缓解,血清转氨酶和IgG水平持续正常2年以上者可考虑停药。
指引性声明:(4)停药前的肝组织检查对排除可疑炎症和减少复发率很有价值,但在成年患者中并非强制性。
停药前需维持血清AST、ALT和IgG水平降至正常(生化缓解) 2年以上。肝硬化患者可能有血清IgG水平的持续性升高,如果在较长稳定期(≥2年)内其他检查均正常,可考虑停药治疗。停药前进行肝活检复查一直是首选策略,组织学缓解可将复发率降低到28%。但并非所有成年患者在停药前都必须进行肝活检。
指引性声明:(5) 患者在停止治疗后的最初12个月应进行密切监测,之后每年进行1次实验室检查。
指引性声明:(6)若患者出现复发,则需立即重新启动治疗,直至生化缓解。之后过渡到长期维持治疗。
复发患者对再次治疗反应迅速,即糖皮质激素和硫唑嘌呤诱导生化缓解。94%的患者在(4±1)个月内达到生化缓解,59%的患者在(8±2)个月内达到组织学消退。随后的停药尝试通常伴随着再次复发,多次复发的患者更易出现肝硬化,预后不佳。因此,已发生1次复发的患者建议长期维持治疗。
指引性声明:(7)对于重叠综合征患者,可考虑在泼尼松(龙)+硫唑嘌呤的方案中加用熊去氧胆酸(UDCA)进行联合治疗。
不符合巴黎标准的AIH-PBC患者经常规免疫抑制治疗后均有改善,而以PBC为主伴有AIH特征的患者仅接受UDCA治疗后病情即可得到改善。在满足巴黎标准的患者中,泼尼松(龙)(30 mg/d,4周后逐渐减少至10 mg/d)与UDCA(13~15 mg·kg-1·d-1)联合治疗优于单独使用糖皮质激素或UDCA患者。联合疗法可改善实验室指标,稳定肝纤维化进程和AIH-PBC患者的5年无移植率(100%)和10年总生存率(92%)。
与经典的PSC相比,泼尼松(龙)(0.5 mg·kg-1·d-1逐渐减少至10~15 mg/d)联合UDCA(13~15 mg·kg-1·d-1)治疗,可提高生存率并降低移植率,因此欧洲肝病研究学会和AASLD已推荐该方案用于治疗AIH-PSC重叠综合征。
9 新型治疗方式
指引性声明:(1)对于一线治疗无应答的儿童或成人AIH患者,应重新评估原始诊断的准确性和患者的服药依从性。
指引性声明:(2)在一线和二线治疗方案失败后,抗TNF和抗CD20或可成为替代疗法,但证据有限。
抗TNFα(英夫利昔单抗)的单克隆抗体可致肝损伤,甚至可引起药物诱导的AIH样损伤。抗TNF抗体也可在AIH中起治疗作用,但证据不足。利妥昔单抗是针对B淋巴细胞表面受体CD20的单克隆抗体,利妥昔单抗在对6例成人AIH患者(3例硫唑嘌呤不耐受、3例对糖皮质激素/硫唑嘌呤和MMF无效)的治疗中,所有患者血清转氨酶和IgG水平显著改善,67%的患者获得生化缓解。但其作为二线治疗的证据仍有限。
10 伴发疾病
指引性声明:(1)对于HBsAg阴性/抗HBc阳性的AIH患者,在使用泼尼松(龙)联合硫唑嘌呤进行常规治疗期间,应定期进行血清学检测(HBsAg、HBV DNA),以评估HBV是否再激活和是否需要启动抗病毒治疗。
指引性声明:(2)有血清学HBV感染证据的患者,经大剂量糖皮质激素或其他免疫调节剂(特别是B淋巴细胞剔除剂)治疗后,有中度HBV再激活的风险,应考虑采用预防性抗病毒治疗。
AIH患者使用免疫抑制剂后有HBV再激活的风险,建议治疗前对患者常规筛查HBsAg和抗HBc。AASLD建议每隔1~3个月检测1次血清HBV DNA和HBsAg。根据血清学特征(HBsAg阳性或阴性/抗HBc阳性)和免疫抑制治疗的类型、剂量和持续时间,可以评估治疗期间HBV再激活的风险程度:高(≥10%)、中(1%~10%)和低(<1%)。在免疫抑制治疗期间和治疗后至少6个月(或使用抗CD20药物治疗后至少12个月),建议对HBV再激活的中高危个体进行预防性抗病毒治疗,推荐使用恩替卡韦或替诺福韦。对低风险患者建议进行有目的按需治疗的观察性监测。
指引性声明:(3)所有具有骨质疏松危险因素的AIH成年患者应在基线时进行骨密度检测,并应在糖皮质激素治疗期间每2~3年复查1次。
对于有骨质疏松症的患者,应在基线时采用双能X线骨密度仪对腰椎和髋部进行骨密度评估。此后,应每隔2~3年复查1次。最常见危险因素为长期使用糖皮质激素、绝经后状态、低创伤骨折史和老龄(女性>65岁,男性>70岁)。
指引性声明:(4)诊断时应测定患者血清25-羟基维生素D水平,此后每年复查1次。
指引性声明:(5)在糖皮质激素治疗期间,应补充钙元素(1000~1200 mg/d)和维生素D(>400~800 IU/d),并根据临床实际情况对维生素D不足的患者给予剂量补充。
指引性声明:(6)AIH患者出现骨质疏松症时可使用二磷酸盐类药物。
68%~81%的AIH患者出现血清25-羟基维生素D缺乏(≤29 ng/ml),20%出现重度缺乏(<20 ng/ml)。建议对所有患者在诊断时以及补充维生素D时评估血清25-羟基维生素D水平。该剂量和监测方法同样适用于儿童患者。已有的临床经验支持在出现骨质疏松症时,使用二磷酸盐治疗。
指引性声明:(7)应在治疗前和治疗期间评估患者是否存在代谢综合征,此类患者的治疗方案需进行个体化调整和生活方式的干预。
代谢综合征是心血管疾病和2型糖尿病的危险因素,该危险因素可因长期糖皮质激素疗法加重或诱发,应在此类治疗实施前评估其是否存在。代谢综合征的5个主要组分是高血压、高甘油三酯血症、高密度脂蛋白胆固醇低水平、空腹高血糖和中心性肥胖(腰臀比或BMI> 30 kg/m2)。5项中的3项出现异常结果证实诊断。合并代谢综合征的患者可能需要修改糖皮质激素治疗方案、补充治疗和调整生活方式(运动、减肥)。
指引性声明:(8) 恶性肿瘤监测应包括肝硬化患者每6个月进行1次肝脏超声检查和血清甲胎蛋白水平测定,并遵循其他肝外恶性肿瘤排查的指南标准。
肝癌发生在1%~9%的AIH相关肝硬化患者中,年发病率为1.1%~1.9%,标准化发病率为23.3(95%CI:7.5~54.3),标准化病死率为42.3(95%CI:20.3~77.9)。肝癌的危险因素是肝硬化≥10年、门静脉高压、持续性炎症和免疫抑制治疗≥3年。接受治疗的AIH患者中有5%发展为不同细胞类型(宫颈、淋巴组织、乳腺、膀胱、软组织和皮肤)的肝外恶性肿瘤。非黑色素瘤性皮肤癌最常见,肝外恶性肿瘤的标准化发病率为2.7(95%CI:1.8~3.9)。
11 肝移植
指导性建议:由于长期应用糖皮质激素预防移植后排斥反应、移植物功能丧失或AIH复发,改善成人患者和移植物存活率的证据有限,AASLD建议肝移植术后应考虑逐渐停用糖皮质激素(条件性推荐,确定性非常低)。
成人AIH移植患者较酒精性肝硬化移植患者发生急性排斥反应(81% vs 47%)和激素抵抗(38% vs 13%)的频率高。此外,AIH移植患者的慢性排斥反应发生率(16%)高于PBC移植患者(8.2%)、PSC移植患者(5.2%)和酒精性肝硬化患者(2%)。近期经验(2000年-2010年)显示,AIH晚期急性排斥反应的发生率为9%。即与其他肝病相比,AIH的急慢性排斥反应率较高。
以往认为,肝移植后继续糖皮质激素治疗,可防止排斥反应和AIH复发。然而,肝移植后停用激素可降低感染风险和类固醇相关副作用。肝移植术后是否长期应用激素仍有争议,文献表明一些患者可安全停用类固醇。
指引性声明:(1)肝移植受者出现提示移植物功能受损的实验室指标变化时,必须怀疑AIH复发或肝移植术后新发AIH和浆细胞性肝炎/排斥反应的可能。
指引性声明:(2)建议复查肝活检、血清IgG水平和自身抗体来区分免疫介导性疾病和其他导致同种异体移植功能障碍的原因。
指引性声明:(3)AIH复发或移植术后新发AIH的肝移植患者建议在钙调蛋白抑制剂的方案上加用泼尼松(龙)和硫唑嘌呤来联合治疗。
