经鼻高流量正压通气联合头孢哌酮钠舒巴坦钠治疗对重症肺炎患儿免疫功能和肺功能的影响
2020-04-22康英李娟许亚红
康英,李娟,许亚红
(西部战区空军医院儿科,成都 610061)
重症肺炎是儿童常见危重症之一,以发热、咳嗽咳痰、呼吸困难为主要临床表现[1]。如果治疗不及时、不得当会诱发心力衰竭、呼吸衰竭、肾衰竭、全身炎症反应综合征等严重并发症[2],甚至导致多脏器衰竭,最终导致死亡,严重威胁儿童健康,特别是5岁以下儿童[3]。重症肺炎患儿多为多重复杂细菌感染,且由于儿童气道较为狭窄,纤毛功能尚不完善,气道分泌物不易排除,故加重感染;此外,抗生素和激素的过度使用使得患儿一旦发生重症感染,病情控制变得较为困难[4]。据统计,全球每年5岁以下发生重症肺炎的患儿约1 400万,发展中国家发病率较高,约为1.2%[5]。因此,如何尽快改善患儿气道阻塞、促进痰液、炎症分泌物等引流及控制感染是治疗儿童重症肺炎的关键。重症肺炎发生时,炎症反应和炎症因子大量消耗患儿肺泡表面活性物质,导致通气/血流比例失调、肺内分流,造成肺组织复张困难,肺泡萎缩塌陷,引起呼吸衰竭,形成高碳酸血症,从而增加治疗难度[6]。经鼻高流量正压通气是一种无创、安全、操作简单的呼吸支持技术,其可有效复张塌陷的肺泡,控制肺泡内液体过度渗出。另外,经鼻高流量正压通气可以根据患儿呼吸衰竭情况及气道情况调节氧浓度、流量及局部湿化的温度来改善肺部通气功能,对治疗儿童重症肺炎有重要意义[7-8]。本研究旨在探讨经鼻高流量正压通气联合头孢哌酮钠舒巴坦钠对重症肺炎患儿免疫功能和肺功能的影响。
1 资料与方法
1.1一般资料 选取2017年9月至2019年9月在西部战区空军医院住院的100例重症肺炎患儿作为研究对象。纳入标准:①所有患儿均>28 d;②均符合儿童重症肺炎诊断标准[9];③降钙素原>1.5 μg/L;④患儿家属均签署知情同意书。排除标准:①近1个月内使用过免疫抑制剂;②合并心、脑、肾等重要脏器严重疾病;③非细菌感染性疾病。上述患儿根据治疗方法不同分为对照组和观察组,各50例。两组患儿性别、年龄、病程比较差异无统计学意义(P>0.05),见表1。

表1 两组重症肺炎患儿的一般资料比较
对照组:给予经鼻高流量正压通气联合头孢唑肟治疗;观察组:给予经鼻高流量正压通气联合头孢哌酮钠舒巴坦钠治疗;a为χ2值,余为t值
1.2治疗方法 两组患儿均给予维持水电解质平衡、吸氧以及盐酸氨溴索(勃林格殷格翰制药公司生产,批号:727937)15 mg+吸入用布地奈德(阿斯利康制药有限公司生产,批号:324588)1 mg雾化吸入治疗。其中,对照组在基础治疗的基础上将头孢唑肟(重庆西南药业股份有限公司生产,批号:20180135)40~80 mg/kg加入0.9%氯化钠注射液100 mL中静脉滴注,每8小时1次,并联合经鼻高流量正压通气(调整呼吸机流量为30 L/min,吸氧浓度为2 L/min,气道湿化温度30 ℃)治疗,吸气压6~8 cmH2O(1 cmH2O=0.098 kPa),呼气压4~6 cmH2O,12 h<每日通气时间<18 h。观察组在基础治疗的基础上将注射用头孢哌酮钠舒巴坦钠(辉瑞制药有限公司生产,批号:20180924)30~60 mg/kg加入0.9%氯化钠注射液100 mL中静脉滴注,每8小时1次,并联合经鼻高流量正压通气治疗,方法同对照组。
1.3观察指标 ①治疗后,分别记录两组患儿的退热时间、体征消失时间、咳嗽咳痰好转时间及住院时间。②免疫功能指标:治疗前后清晨空腹抽取患儿肘静脉血液5 mL,使用美国BD公司的流式细胞测定仪(型号:Biosciences FACSCANTO Ⅱ)检测CD3+、CD4+、CD8+。③炎症免疫指标:采用酶联免疫吸附法测定单核细胞趋化蛋白1(monocyte chemoattractant protein-1,MCP-1)、可溶性髓样细胞触发受体-1(soluble triggering receptor expressed on myeloid cells-1,sTREM-1)、可溶性细胞间黏附分子-1(soluble intercelluar adhesion molecules-1,sICAM-1),所有试剂盒均购自美国Abcam公司,严格按照说明书进行操作,酶标仪下读取OD值。④肺功能指标:使用德国耶格儿童肺功能仪(型号:Master Screen Paed)检测两组患儿治疗前后潮气量(tidal volume,V-T)、第一秒用力呼气量(forced expiratory volume in first second,FEV1)。
1.4疗效判断标准 按照王蔚文[10]的临床疗效判断标准进行评定。治愈:患儿治疗后意识清楚,无需使用机械辅助通气,肺功能及实验室指标恢复正常;好转:主要临床症状体征基本消失,胸部X线片提示肺部实变阴影基本消失,每日使用无创通气时间<2 h;无效:治疗后患者症状体征无变化。

2 结 果
2.1两组患儿的临疗效比较 观察组临床疗效优于对照组(Z=2.347,P=0.019)。见表2。

表2 两组重症肺炎患儿的临床疗效比较 (例)
对照组:给予经鼻高流量正压通气联合头孢唑肟治疗;观察组:给予经鼻高流量正压通气联合头孢哌酮钠舒巴坦钠治疗
2.2两组患儿的临床症状好转时间比较 治疗后,观察组的退热时间、体征消失时间、咳嗽咳痰好转时间、住院时间均明显短于对照组(P<0.01)。见表3。


组别例数退热时间体征消失时间咳嗽咳痰好转时间住院时间对照组506.6±1.213.4±2.09.6±1.418.7±3.0观察组505.2±0.810.2±1.37.4±0.814.1±2.8t值6.8619.2399.7718.050P值<0.001<0.001<0.001<0.001
对照组:给予经鼻高流量正压通气联合头孢唑肟治疗;观察组:给予经鼻高流量正压通气联合头孢哌酮钠舒巴坦钠治疗
2.3两组患儿的免疫功能指标比较 治疗前,两组患儿的CD3+、CD4+、CD8+水平比较差异无统计学意义(P>0.05);治疗后,两组患儿的CD3+、CD4+水平均升高,且观察组高于对照组(P<0.05);CD8+水平降低,观察组低于对照组(P<0.05)。两组各指标组间、时点间、组间和时点间交互作用比较差异有统计学意义(P<0.05)。见表4。
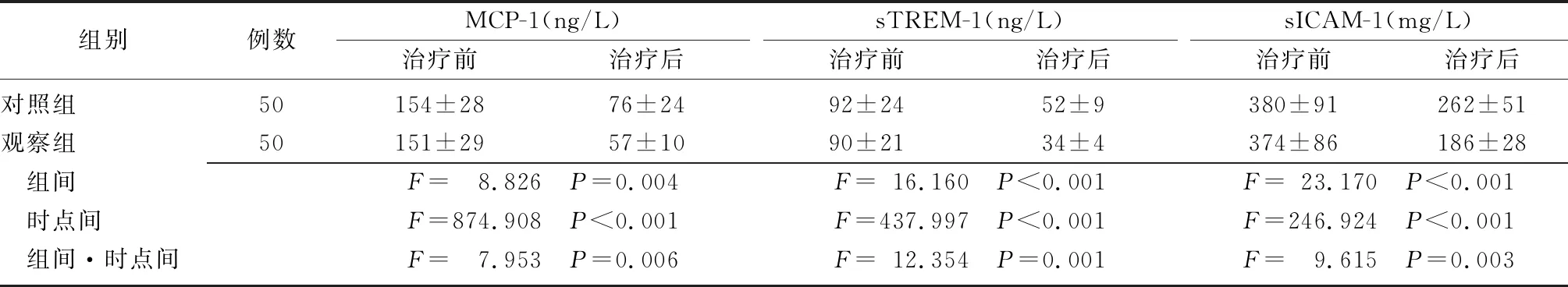
2.4两组患儿的炎症免疫指标比较 治疗前,两组患儿的MCP-1、sTREM-1、sICAM-1比较差异无统计学意义(P>0.05);治疗后,两组患儿的MCP-1、sTREM-1、sICAM-1水平均降低,且观察组低于对照组(P<0.05)。两组患儿各指标组间、时点间、组间和时点间交互作用比较差异有统计学意义(P<0.01)。见表5。


组别例数CD3+治疗前治疗后CD4+治疗前治疗后CD8+治疗前治疗后对照组5045.8±5.451.5±5.031.6±3.836.9±4.839.2±5.534.1±3.5观察组5044.8±4.756.0±4.532.2±3.041.6±5.639.2±4.229.0±4.5 组间F=29.031 P<0.001F=17.346 P<0.001 F=17.823 P<0.001 时点间F=140.005 P<0.001F=11.847 P=0.001 F=130.900 P<0.001 组间·时点间F=6.746 P=0.011F=144.282 P<0.001 F=14.854 P<0.001
对照组:给予经鼻高流量正压通气联合头孢唑肟治疗;观察组:给予经鼻高流量正压通气联合头孢哌酮钠舒巴坦钠治疗

组别例数MCP-1(ng/L)治疗前治疗后sTREM-1(ng/L)治疗前治疗后sICAM-1(mg/L)治疗前治疗后对照组50154±2876±2492±2452±9380±91262±51观察组50151±2957±1090±2134±4374±86186±28 组间F=8.826 P=0.004F=16.160 P<0.001F=23.170 P<0.001 时点间F=874.908 P<0.001F=437.997 P<0.001F=246.924 P<0.001 组间·时点间F=7.953 P=0.006F=12.354 P=0.001F=9.615 P=0.003
MCP-1:单核细胞趋化蛋白1;sTREM-1:可溶性髓样细胞触发受体-1;sICAM-1:可溶性细胞间黏附分子-1;对照组:给予经鼻高流量正压通气联合头孢唑肟治疗;观察组:给予经鼻高流量正压通气联合头孢哌酮钠舒巴坦钠治疗
2.5两组患儿的肺功能指标比较 治疗前,两组患儿的V-T、FEV1比较差异无统计学意义(P>0.05);治疗后,两组患儿的V-T、FEV1均升高,且观察组高于对照组(P<0.05)。两组各指标组间、时点间、组间和时点间交互作用比较差异有统计学意义(P<0.01)。见表6。


组别例数V-T(mL/kg)治疗前治疗后FEV1(L)治疗前治疗后对照组508.77±0.829.72±1.081.24±0.151.79±0.24观察组508.70±0.8812.05±2.031.21±0.122.80±0.45 组间F=35.470 P<0.001F=166.572 P<0.001 时点间F=147.431 P<0.001F=734.128 P<0.001 组间·时点间F=45.678 P=0.006F=172.731 P<0.001
V-T:潮气量;FEV1:第一秒用力呼气量;对照组:给予经鼻高流量正压通气联合头孢唑肟治疗;观察组:给予经鼻高流量正压通气联合头孢哌酮钠舒巴坦钠治疗
3 讨 论
儿童重症肺炎是病死率较高的儿科危急重症之一[11],多由细菌感染后释放大量内毒素所致[12]。这些内毒素激活患者机体内的巨噬细胞系统,促进炎症因子释放,并释放溶酶体、内毒素等致热物质,导致患儿发热咳嗽[13]。机体炎症反应不断刺激肺泡壁过度分泌炎症分泌物,致使患儿局部炎症反应加重,大量炎症分泌物产生,出现咳嗽咳痰症状及肺部啰音。本研究结果显示,治疗后,观察组患儿的退热时间、体征消失时间、咳嗽咳痰好转时间及住院时间均短于对照组,提示头孢哌酮钠舒巴坦钠较头孢唑肟具有更好的抗炎作用。
研究表明,T淋巴细胞亚群失衡在肺炎发病机制中发挥重要作用,当患者发病后,外周血CD3+、CD4+淋巴细胞亚群比例下降,CD8+T淋巴细胞比例上升,CD4+/CD8+下降,表明肺炎患者存在细胞免疫功能下降,免疫功能受损[14-15]。而免疫功能下降会导致机体对病原微生物防御功能下降,呼吸道反复感染,加重患者全身炎症反应及肺功能损伤[16]。本研究结果显示,治疗后,两组患儿的CD3+、CD4+表达水平均升高,且观察组高于对照组(P<0.05);CD8+表达水平降低,观察组低于对照组(P<0.05),提示使用经鼻高流量正压通气联合头孢哌酮钠舒巴坦钠治疗后患儿的免疫功能得到有效改善,效果优于头孢唑肟抗感染治疗。
MCP-1是一种单核-巨噬细胞趋化因子[17],当肺部感染时其会趋化大量的巨噬细胞聚集于感染灶周围,并释放大量的致炎因子(白细胞介素-6、白细胞介素-8)产生炎症级联效应[18]。sICAM-1是一种主要分布在白细胞及内皮细胞表面,是一种表面跨膜蛋白抗原,当机体发生炎症时,sICAM-1分泌增加。研究发现,sICAM-1与重症肺炎患儿的肺部感染评分呈正相关,提示其可以作为评价肺炎严重程度的可靠指标之一[19-21]。sTREM-1在健康状态下基本不表达,当肺部感染时,炎症刺激中性粒细胞释放大量的sTREM-1。左玉等[22]研究发现,MCP-1、sTREM-1、sICAM-1与重症肺炎患儿的病情严重程度呈正相关。本研究结果显示,治疗后观察组的MCP-1、sTREM-1、sICAM-1水平显著低于对照组(P<0.05),说明头孢哌酮钠舒巴坦钠治疗后患儿的炎症免疫改善较好。
肺功能检查是小儿呼吸系统疾病常见的无创检查指标之一,其不仅可以作为肺脏通气肝功能的评价金标准,还可以作为药物治疗儿童肺炎的疗效判定指标及预后指标。本研究结果显示,治疗后两组患儿的V-T、FEV1均升高,且观察组高于对照组(P<0.05),说明经过联合使用头孢哌酮钠舒巴坦钠治疗后,患儿的肺功能得到有效改善。
综上所述,经鼻高流量持续正压通气联合头孢哌酮钠舒巴坦钠治疗儿童重症肺炎可以提高临床疗效,缩短住院时间,提高患儿体液免疫,改善肺功能及炎症免疫状况,但本研究过程可能存在一定的偏倚,后期需进一步研究证实。
