山药不同炮制品丸剂物性参数及尿囊素体外溶出研究*
2020-04-20陈天朝耿梦丽常倩倩于兰兰马彦江
陈天朝,李 沁,姚 超,耿梦丽,常倩倩,于兰兰,马彦江
(1.河南中医药大学药学院,河南 郑州 450008; 2.河南中医药大学第一附属医院药学部,河南 郑州 450000; 3.河南医药技师学院制剂工程系,河南 开封 457000;4.河南省直第三人民医院药学部,河南 郑州 450000)
中药炮制是根据中医药理论,依照辨证论治用药的需要、药物自身性质和调剂、制剂的不同要求所采取的一项传统制药技术,是中药内部大分子和小分子受热发生变化,分子间化学键发生断裂后重新结合的过程[1]。中药饮片经过炮制后可加工制成丸剂,具有便于携带、服用方便、保质期长等优点。丸剂的制作,从饮片到打粉再到制丸,存在着物性的变化。物性即物质固有的物理和化学属性,对所选取中药饮片及炮制品,一般从“形”“色”“气”“味”“质”进行评价,而这些评价指标可以通过物料相关物性的相对密度、氧化值、吸水率、吸水膨胀度、pH值等测定进行数字化度量,再通过对炮制过程中小分子成分含量的变化,优选出符合中医药整体观的、过程可控的中药炮制方法。山药来自薯蓣科植物薯蓣DioscoreaoppositeThunb.的干燥根茎,载于《神农本草经》,位列上品,具有补脾胃、益肺肾的作用[2]。山药的炮制有麸制和清炒制,有关麸炒的研究比较多。本实验侧重于清炒炮制中的炒黄、炒焦研究[3-4]。清炒制的山药具有降血糖、调节免疫和抗衰老的作用[5]。山药中所含的尿囊素是小分子化合物,是山药的有效成分,可以促进上皮组织修复,生肌,被用于胃及十二指肠溃疡的治疗。本实验着重研究炮制后山药丸剂中尿囊素与丸剂物性间的相关性,通过对山药不同炮制品丸剂物性参数(吸水率、膨胀度、氧化值、pH值)与有效成分间的相关性研究并建立回归线性模型。
1 药品、试剂与仪器
山药(批号1710201)、山药炒黄(批号1710201)、山药炒焦(批号1710201),均为河南中一医药经营有限公司产品,经河南中医药大学第一附属医院药学部王宏贤副主任药师鉴定为薯蓣科植物薯蓣DioscoreaoppositeThunb.的干燥根茎。尿囊素,纯度≥98%,中国食品药品检定研究所提供,批号111501-200202;甲醇(批号20170903)、无水乙醇(批号20170529)、乙醚(批号20170415),均为分析纯,烟台市双双化工有限公司产品;甲醇,色谱纯,Sigma试剂公司产品。元素型18120纯水装置,上海摩勒科学仪器有限公司产品;UltiMate 3000高效液相色谱仪,美国赛默飞世尔科技公司产品;BSA224S-CW型电子天平,德国赛多利斯公司产品;KQ5200B型机械超声波清洗仪器,上海合金超声设备有限公司产品。
2 方法与结果
2.1 山药丸剂制备


表1 山药丸剂均匀设计表 n=3

表2 山药丸剂最佳泛制工艺

表3 山药丸剂质量检测 n=3
2.2 山药丸剂物性参数的测定
按照参考文献[8]方法。
2.2.1 吸水率测定
将漏斗放置于恒温恒湿、盛有纯化水的干燥器内。将滤纸折叠后放入漏斗内饱和3 min,取出后放置于干燥滤纸上并放置配重。静置30 s后,精密称取吸水饱和滤纸质量,再放回内漏斗内。精密称取1.00 g不同炮制品丸剂置于滤纸中(水完全浸没不同炮制品丸剂,但水面低于滤纸上层边缘)。静置1 h后,过滤3 min,同法处理带有丸剂的滤纸。每种不同炮制品丸剂平行测定3次,取平均值,计算吸水率。

2.2.2 膨胀度的测定
按照2015版《中国药典》四部通则2101膨胀度的测定方法[9]。
2.2.3 相对密度的测定
称取不同炮制品丸剂1.00 g并记录其质量m;取25 mL膨胀度测定管,量取一定体积轻质液态石蜡并记录其体积V1;将称量质量后的中药饮片投入膨胀度测定管中,使不同炮制品丸剂完全浸没于液态石蜡液面以下,静置至无气泡产生。记录投入不同炮制品丸剂后轻质液态石蜡体积V2。每种炮制品丸剂平行测定3次,取平均值作为其相对密度[10]。计算不同炮制品丸剂相对密度d。
2.2.4 pH值的测定
取纯水100 mL,准确称取不同炮制品丸剂1.00 g,加入100 mL纯化水中,室温下浸泡1 h,过滤,取滤液,测pH值。每种炮制品丸剂平行测定3次,取平均值。
2.2.5 氧化值的测定
称取山药炮制品丸剂7.50 g,置于装有300 mL纯水的圆底烧瓶中,混合均匀后接入蒸馏装置,精确收集前50 mL馏分。用移液管准确移取20 mL馏分于滴定瓶内,加入硫酸水溶液5 mL和0.002 mol/L KMnO4溶液10 mL,振荡均匀后室温下反应30 min;然后加入质量分数100 g/L的KI水溶液5 mL,滴加Na2S2O3标准溶液,当溶液由黄棕色或深黄色变成浅黄色时,加1 mL淀粉溶液为指示剂,继续用0.02 mol/L Na2S2O3标准溶液滴定至无色。记录消耗Na2S2O3标准溶液体积为V3(mL)[11]。另以丸剂等质量水代替样品重复上述操作进行空白试验,记录消耗Na2S2O3标准溶液体积为V4(mL)。氧化值OX公式:
式中:C为Na2S2O3标准溶液浓度(mol/L),m为丸剂质量。
2.2.6 物性参数测定结果
测得不同炮制品山药丸剂物性参数(吸水率、吸水膨胀度、相对密度、pH值、过氧化值)3次平均值,见表4。经过不同程度的炮制,相对密度、pH值、过氧化值增大。

表4 山药丸剂物性参数均值 n=3
2.3 尿囊素含量的测定
2.3.1 色谱条件
色谱柱Agilent ZORBAX SB-Aq( 4.6 mm×250 mm,5 μm ),流动相为甲醇-水(1∶99),流速 0.5 mL /min,进样量10 μL,检测波长224 nm,柱温30 ℃[8]。尿囊素色谱图如图1。

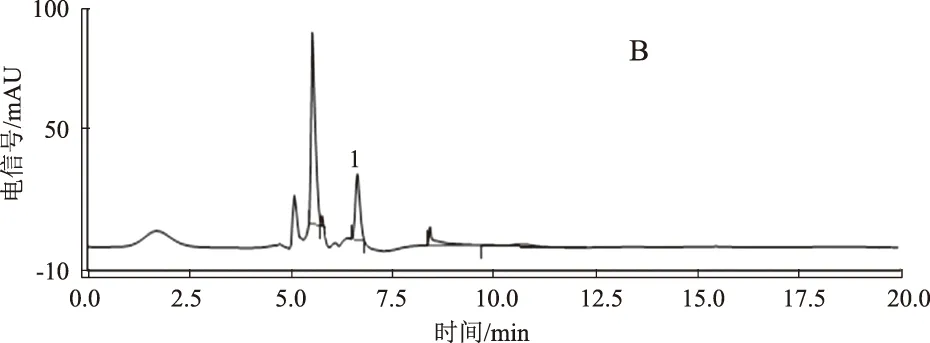
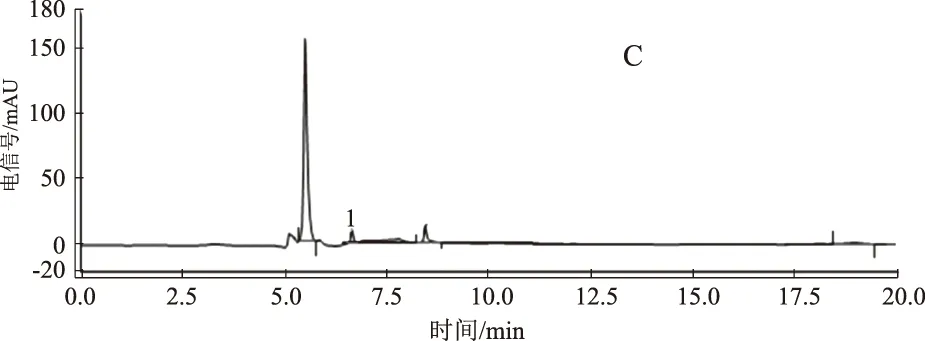

A.尿囊素对照品;B.山药生品丸剂;C.山药炒黄丸剂;D. 山药炒焦丸剂;1. 尿囊素
2.3.2 供试品溶液制备
取上述丸剂适量,粉碎,精密称量1.00g,加体积分数为200 mL/L的乙醇20 mL,超声(200 W,40 KHz)提取60 min,滤过,加体积分数为200 mL/L的乙醇定容于25 mL容量瓶中,震荡10 min,3 000 r/min 离心20 min,用0.45 μm微孔滤膜过滤,即得[8]。
2.3.3 对照品溶液制备
精密称取尿囊素对照品10.00 mg于25 mL量瓶中,加200 ml/L乙醇溶解定容至刻度,即得。
2.3.4 线性关系考察
精密吸取0.1,0.5,1,1.5,2,2.5,3,5,10 mL对照品溶液于10 mL量瓶,加200 mL/L的乙醇定容。依次进样10 μL,按2.3.1项下方法进样测定,记录色谱峰面积,以进样量为横坐标,色谱峰面积为纵坐标,绘制标准曲线Y= 9.874X+0.258,r2=0.998。结果表明,尿囊素在4~400 mg/L范围内线性关系良好。
2.3.5 精密度试验
取山药丸剂粉末,制备供试品溶液,按照2.3.1项下的方法进行精密度考察,结果峰面积平均值为9.08,RSD值为0.94%。结果表明,此方法精密度良好。
2.3.6 稳定性实验
取山药丸剂粉末,按照2.3.1项下方法,在时间点0,2,4,8,12,24 h进行稳定性考察,结果平均峰面积为9.09, RSD值为0.98%。结果表明,此方法稳定性良好。
2.3.7 重复性实验
取山药丸剂20.00 g,平行取6份,精密称定,按2.3.1项下方法进行重复性实验,结果得到的RSD值为1.41%。结果表明,此方法重复性良好。
2.3.8 加样回收率实验
取已知尿囊素含量的山药生品丸剂细粉0.5 g,精密称定,平行操作6份,分别加入200 mg/L尿囊素对照品溶液5 mL,按2.3.2项下方法制备供试品溶液,计算得出尿囊素的平均加样回收率、RSD值,见表5。结果表明,此方法准确性良好。

表5 尿囊素回收率考察 n=6
2.3.9 尿囊素含量测定结果
取丸剂粉末1.00 g,平行3份,精密称定,按2.3.2项下方法制备供试品溶液,进样测定。通过与尿囊素对照品对比,山药炒焦后丸剂中尿囊素所对应的峰消失,且山药炒黄、炒焦后共同出现了3号峰,炒焦后出现4号峰,清炒制后的山药丸剂出现了新峰。山药不同炮制品丸剂尿囊素含量测定结果见表6。

表6 丸剂中尿囊素含量测定结果 n=3
2.4 山药丸剂体外溶出含量测定及溶出模型构建
2.4.1 溶出液含量测定
选择桨法进行丸剂体外溶出实验[12],以脱气后的纯水900 mL作为溶出介质,设定溶出仪转速为100 r/min,调节温度为(37±0.5) ℃。在投药前先将溶出仪保温30 min,精密称量丸剂20.00 g投入溶出杯,投药时打开溶出仪转桨并开始计时;在投药后2,5,10,20,30,60,120,240,480 min取样25 mL,并补充同体积、同温度溶出介质。山药丸剂各时间点累积溶出百分率结果见表7。溶出液处理后经0.45 μm 滤头过滤后,置于HPLC中进样,进行含量测定。通过溶出百分率做出尿囊素溶出曲线图,见图2。结果表明,清炒炮制对山药丸剂尿囊素的溶出速率有减缓作用。
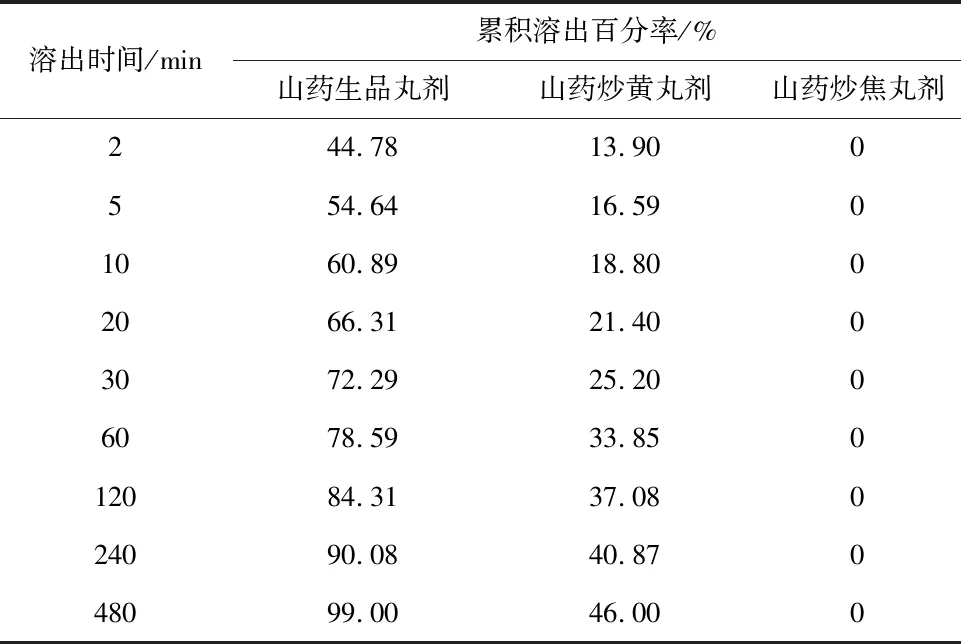
表7 山药丸剂尿囊素各时间点累积溶出百分率

图2 山药丸剂尿囊素溶出曲线图
2.4.2 山药丸剂尿囊素溶出模型拟合方程
利用威布尔分布(WeibuLL)建立模型F=1-exp(-(t-α)^γ/β),F表示尿囊素溶出率百分比,γ为形状参数即斜率。用Excel分析ln(ln(1/(1-F(t))))与ln(t-α)得到一元线性回归方程[13],通过对比R2得出威布尔模型优于对数模型,故以威布尔模型作为山药丸剂尿囊素溶出规律模型,结果见表8。

表8 山药丸剂尿囊素溶出模型拟合方程
注:e为自然对数的底数,t代表溶出时间。
2.5 相关性分析
2.5.1 清炒法对丸剂物性参数相关性检验
运用SPSS 24.0对山药丸剂指标成分与物性参数进行相关性分析[14],结果见表9。从表9中可知,山药丸剂尿囊素与相对密度、pH值及氧化值间存在极强相关性。
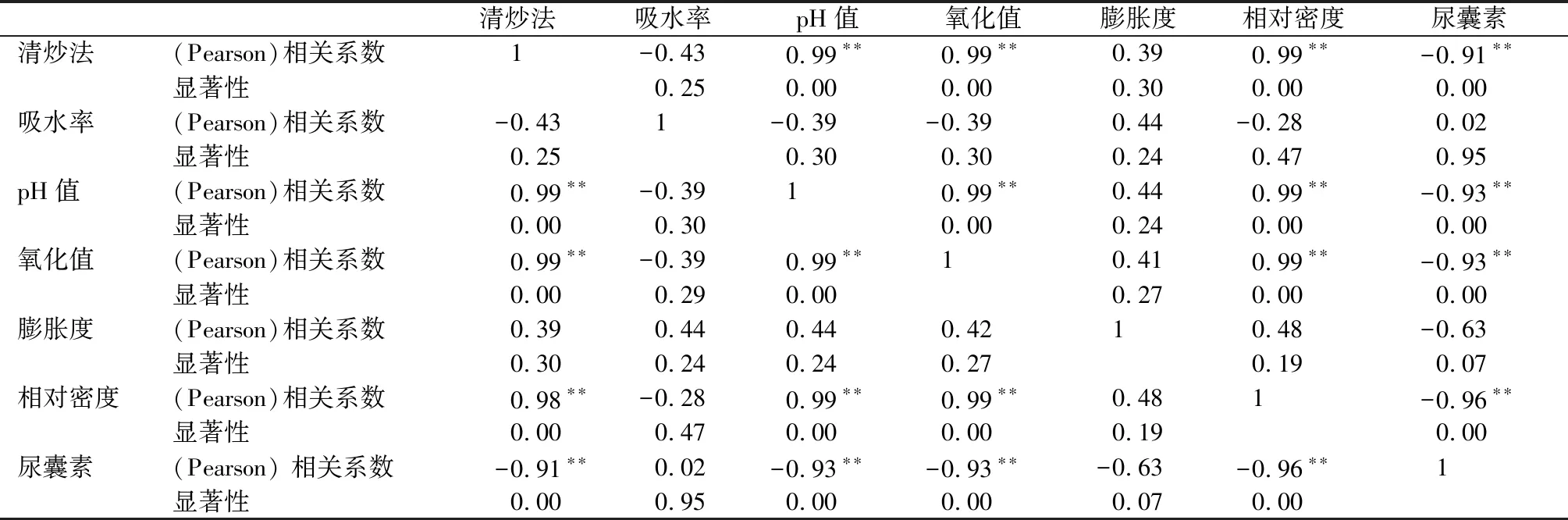
表9 山药丸剂尿囊素与物性参数之间相关性 n=9
注:*P<0.01。
2.5.2 尿囊素与氧化值及相对密度线性关系分析
运用SPSS 24.0软件,采用步进法进行线性回归分析[15],可知尿囊素与氧化值及相对密度呈线性回归关系(P<0.01),与pH值线性关系不明显。线性回归方程为Y=24.297 86+0.050 111X1-27.312 2X2(X1为氧化值,X2为相对密度)。因此,可以通过对氧化值与相对密度的测定来间接反映不同炮制品山药丸剂尿囊素的含量,山药丸剂尿囊素与氧化值及相对密度相关性分析见表10。
2.5.3 清炒制法与尿囊素含量间多重性分析
清炒制法与尿囊素含量间多重性分析得出,山药炒黄、炒焦丸剂与山药生品丸剂显著性相关,置信水平95%,见表11。
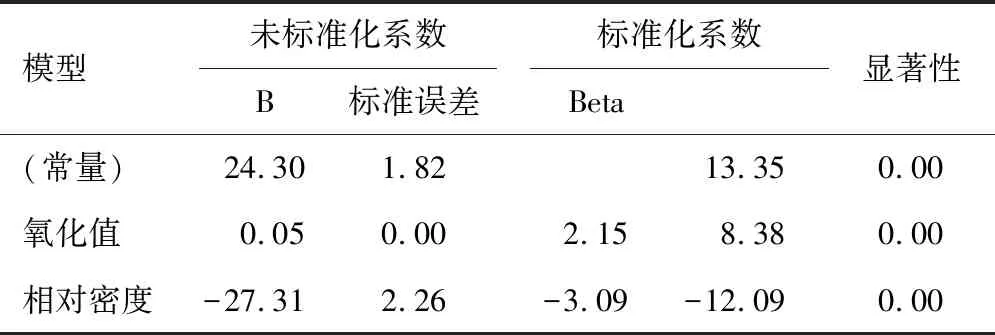
表10 山药丸剂尿囊素与氧化值及相对密度间的线性相关性分析
注:因变量为尿囊素。

表11 尿囊素含量与清炒法的多重性分析
注:因变量为尿囊素,*P<0.05。
3 讨 论
本实验通过对3种山药炮制品丸剂物性参数的测定发现:随着炮制程度的加大,丸剂的相对密度、pH值、氧化值增大,吸水率先减小后增大,吸水膨胀度先增大后减小。中药饮片在炮制过程中由于温度的持续上升快速地氧化。美拉德反应证明:中药饮片在高温下,其成分中的氨基和羰基发生反应,产生褐色成分同时伴随pH值和过氧化值的变化;随着炮制温度的升高、炮制时间的增加,药材的质地变硬,导致吸水率减小;随着炒制程度加深,药材粉性增加,从而吸水率增加。另外,炮制也会对山药饮片中的小分子成分产生影响。尿囊素作为山药丸剂的指标性成分,随着炮制程度加深其含量减少,HPLC色谱中出现新的色谱峰,提示可能在此过程中产生了新的化学成分。本实验可以看出,炮制后的山药丸剂物性参数与有效成分之间具有一定的相关性。从中医药的整体观来看,物性和炮制工艺间有着一定的传递性,炮制会引起中药丸剂物性参数及有效成分含量的变化,可以两者之间的相关性为基础,更加全面科学地对中药炮制理论进行研究。
本次实验得出山药丸剂中尿囊素的溶出可以构建一定的线性回归模型,结合尿囊素与物性参数间的相关性,可以为中药饮片制丸提供一定的数据参数指导, 可以克服一些传统经验鉴别的弊端,比如通过色泽、外形等对中药饮片进行鉴别。中药炮制需要现代化、智能化。探讨山药不同炮制品丸剂的有效成分和物性参数,以及物性参数之间存在的关联性为中药炮制的标准化和智能数字化奠定了一定的基础。
