肺动脉高压合并甲状腺功能异常临床特点分析
2020-04-18朱光发
孙 茜 高 杨 王 艳 朱光发
肺动脉高压(pulmonary arterial hypertension, PAH)是由已知或未知原因引起肺循环血流受限,肺血管阻力进行性增高而导致的疾病或病理生理综合征,最终导致不可逆性右心衰竭甚至死亡的严重疾病[1]。因此,发现影响肺动脉高压预后不良的危险因素,及时采取适当治疗,对改善患者预后有重要意义。肺动脉高压患者中,有10%~24%的病例在病程中曾出现甲状腺功能减退[2-4]。一项前瞻性的研究显示肺动脉高压的患者中自身免疫性甲状腺疾病的发病率高达49%[5],并且,30%的患者检测出抗甲状腺抗体[2]。国内关于肺动脉高压合并甲状腺功能异常与单纯肺动脉高压患者临床特点的文献报道较少。本文通过回顾性分析52例肺动脉高压患者的资料,探讨肺动脉高压合并甲状腺功能异常患者的临床特征,提高对该疾病的认识水平,为临床治疗提供参考。

表1 肺动脉高压患者一般临床资料比较
资料与方法
1.研究对象 选择首都医科大学附属北京安贞医院呼吸与危重症医学科,2018年1月至2018年12月,收治的52例肺动脉高压患者为研究对象。根据患者入院次日空腹抽取静脉血检测甲状腺功能,分为肺动脉高压合并甲状腺功能异常组(n=30),包括甲状腺功能亢进(n=8)、甲状腺功能减退(n=13)、低T3综合征(n=9)[6],和不合并甲状腺功能异常组(n=22)。所有患者均行详细的问诊、体格检查、超声心动图检查、实验室检查。所有患者静息状态由有经验的超声医师进行经胸超声心动图检查,测得肺动脉收缩压(systolic pulmonary artery pressure, SPAP)>40 mmHg(1mmHg=0.133 kPa)[7]。所有患者除外了甲状腺原发疾病病史、胺碘酮治疗史、慢性呼吸系统疾病。
2.研究方法 记录患者的年龄、性别、身高、体质量、既往史、吸烟史、入院24 h纽约心脏病协会(New York heart association, NYHA)分级。入院后首次超声心动图检查,根据三尖瓣反流速度估算SPAP值[8](SPAP>70 mmHg为重度肺动脉高压[9]),测量LVEF。于入院时即刻抽取动脉血气分析,次日空腹抽取静脉血,分离血清,检测甲状腺功能,包括总三碘甲腺原氨酸(total triiodothyronine, TT3)、游离三碘甲腺原氨酸(free triiodothyronine, FT3)、总甲状腺素(total thyroxine, TT4)、(游离甲状腺素(free thyroxine, FT4)、促甲状腺激素(thyroid stimulating hormone, TSH),BNP的实验室结果。
3.统计学方法 采用统计软件SPSS 22.0进行数据分析。计量资料以均数±标准差表示,组间比较采用t检验;非正态分布资料以中位数(P25,P75)表示,采用秩和检验;计数资料以频数(率)表示,比较采用χ2和Fishu’s精确法检验。以P<0.05为差异有统计学意义。
结 果
1.临床资料分析 入组的52例肺动脉高压患者,合并甲状腺功能异常的30例,不合并甲状腺功能异常的22例,根据2018年中国肺高血压诊断和治疗指南进行病因分类[10](表1~2)。两组患者的年龄、性别、BMI、吸烟比例、病因、NYHA分级(表3)在各组间,差异无统计学意义(P>0.05),但合并甲状腺功能异常组的吸烟指数高于不合并甲状腺功能异常组(P<0.05)。
2.超声心动图参数 肺动脉高压合并甲状腺功能异常组LVEF低于不合并甲状腺功能异常组(P<0.05),超声估测的肺动脉收缩压力高于不合并甲状腺功能异常组(P<0.05,表4)。

表3 肺动脉高压患者NYHA分级比较[n(%)]
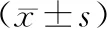
表4 肺动脉高压患者超声心动图参数比较
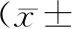
表5 肺动脉高压患者实验室检查结果s)
3.实验室检查 肺动脉高压合并甲状腺功能异常组入院血气分析的PO2低于不合并甲状腺功能异常组(P<0.05),而两组入院血气分析的pH值、PCO2差异无统计学意义(P>0.05,表5)。肺动脉高压合并甲状腺功能异常组的BNP的水平更高(P<0.05)。
讨 论
肺动脉高压是一种以肺血管阻力进行性升高为特征,最终导致患者右心衰竭的致死性疾病[11]。1998年第2次WHO肺动脉高压专家组会议指出甲状腺疾病是特发性肺动脉高压可能危险因素之一[12]。根据本研究回顾性分析,42.3%肺动脉高压患者合并甲状腺功能异常,提示肺动脉高压患者中合并甲状腺功能异常发生率可能较高,与Curnock等[3]和Chu等[2]的研究结果一致。且Ferris等[13]的研究回顾性地分析了134例肺动脉高压患者的资料,发现19%的患者合并有甲状腺疾病。因此肺动脉高压患者应早期检测甲状腺功能,积极采取干预措施,可能对于改善患者预后具有重要临床意义。
本研究回顾了肺动脉高压合并甲状腺功能异常患者的临床特点:与不合并甲状腺功能异常相比,肺动脉高压合并甲状腺功能异常患者的吸烟指数更高,血气分析中氧分压偏低,BNP水平更高。而超声心动图中LVEF偏低,超声估测肺动脉收缩压力更高。WANG等[14]认为合并甲状腺功能异常的心血管疾病患者全因死亡及心源性死亡风险增加,推荐心血管疾病患者监测甲状腺功能水平变化。
目前,肺动脉高压诊断的金标准和最终依据是右心导管检查[15-16, 10],超声心动图是临床上最常用的肺动脉高压筛查及病情评价方法[17]。本研究结果显示,肺动脉高压合并甲状腺功能异常组的估测肺动脉压力升高,随着肺循环阻力增大,动脉压力升高,右心室增大,可能出现右心失代偿及右心衰竭。本研究中肺动脉高压合并甲状腺功能异常的LVEF值降低,可能与此类患者的右心负荷更重相关。其病理生理机制可能为肺循环阻力增大,右心负荷增加[18],右心的充盈受损将影响到左心,右心功能障碍引发左心功能障碍[19]。本研究结果显示肺动脉高压合并甲状腺功能异常患者的动脉血氧分压较不合并甲状腺功能异常组低,可能与甲亢患者代谢加速、耗氧增多,甲减患者机体代谢率下降、细胞水肿引起缺血、缺氧相关。同时,缺氧所致的负性肌力作用也可能引起心脏收缩功能下降[20]。
甲状腺疾病合并肺动脉高压的发病机制目前尚未完全清楚,甲亢和甲减的发生公认为与自身免疫有关。肺动脉高压合并甲状腺疾病的发病机制可能与以下病理生理因素有关:①自身免疫反应导致肺血管内皮损伤,功能紊乱。Yanai等[5]研究发现,在40例特发性肺高压患者中,有30%的患者血清中检测出抗TGAb(anti-thyroglobulin antibodies, TGAb)阳性,推测抗甲状腺自身抗体可能是全身免疫激活的一个标志,是特发性肺高压的发病机制之一。②甲状腺激素导致高循环血流动力学改变,引起心脏形态和功能异常,最终导致心力衰竭,肺动脉压力升高。Siu[21]的研究结果显示在各种病因引起的甲亢分类中,肺动脉高压的发生率并无差异,支持甲亢本身引起的高血流动力学状态在肺动脉高压发病中的重要作用。③上皮细胞内源性肺血管舒张物质合成下降,代谢速度加快,而血管收缩物质表达增加,代谢减慢,引起肺血管可逆性收缩反应增加和血管结构重塑,这是形成肺动脉高压的关键因素[22]。④甲状腺激素不足,心肌水肿,心肌细胞缺血、缺氧,心肌收缩及舒张功能下降,为肺动脉压力升高打下了基础。
本研究仍存在不足:本研究为回顾性研究,纳入的对象为肺动脉高压的住院患者,未包括门诊患者,可能存在数据的偏倚。肺动脉收缩压采用超声心动图估测,未采用右心导管检查测定,可能造肺动脉收缩压偏差。另外,由于本研究纳入病例数较少,难以进一步分组分层分析,目前正继续收集病例资料,以期能对甲状腺功能亢进、甲状腺功能减退、低T3综合征等不同类型甲状腺疾病合并肺动脉高压的特点进行进一步分析。
综上所述,肺动脉高压与甲状腺疾病之间关系密切,肺动脉高压合并甲状腺功能异常患者临床指标偏重,因此有必要对肺动脉高压患者常规进行甲状腺功能检测,为早期诊断、治疗及预测和改善预后提供帮助。
