丝氨酸构象异构化机理的密度泛函理论研究
2020-04-16朱立周鲍羽鹤王海光杨笑春于佳璇孟祥军
朱立周,鲍羽鹤,王海光,杨笑春,于佳璇,孟祥军
(1. 唐山师范学院 化学系,河北 唐山 063000;2. 承德技师学院 电气工程技术系,河北 承德 067000)
氨基酸是构成蛋白质的单体,是重要的生命营养物质,参与众多生理反应,发挥着重要生物功能。分子的生物活性与分子的构象变化间存在密切关系,研究氨基酸的构象行为是理解蛋白质、多肽分子动态特征的关键所在。
甘氨酸和丙氨酸的结构较简单,构象研究也较早[1,2],工作较充分[3,4]。丝氨酸分子式为C3H7O3N,官能团除了氨基和羧基外,还有一个侧链羟基;三个官能团均可作为氢键给体和受体,分子内氢键形式多样,构象较复杂,但它是认识构象氢键效应的一个好模型。2004 年Lambie B 等[5]采用B3LYP/6-31++G**理论方法得到了12 种丝氨酸稳定构象,并用矩阵隔离-傅里叶变换红外光谱法观测到了4 种稳定构象;2007 年Blanco S 等[6]采用超音速射流-傅里叶变换微波谱法观测到了7 种丝氨酸稳定构象,并用MP2/6-311++G**方法对观测构象进行了理论计算。2017 年Wang Y 等[7]将低能电子附着在丝氨酸最稳定的4 种构象上得到形态共振体系,然后用量子散射方法进行了分子解离动力学观测。到目前为止,还缺乏丝氨酸构象转化机理的研究,研究构象转化机理可以深入认识构象变化的微观特征和动态信息[8]。
1 计算方法
密度泛函理论(DFT)现已发展为量子化学计算的最重要手段。之前B3LYP 方法较适用于模拟氨基酸体系的性质[9,10],现在较新的M06 方法由于包含了许多校正项,能量计算比B3LYP 准确,并且描述氢键较好[11]。本文采用M06/6-31++G**方法优化丝氨酸结构,对所有构型都进行频率确认,对过渡态的正确性进行反应内禀坐标(IRC)验证。然后对各构型进行零点能(ZPE)校正,得到各构型的能量Ecom,进而计算各构型的相对能ΔEr(ΔEr=Ecom-Ecom,min,Ecom,min是最稳定构象能量)以及反应过程的正(逆)反应能垒Ea(Ea')。所有任务均使用G09 程序完成[12]。
2 结果与讨论
2.1 稳定构象
本文共得到15种丝氨酸稳定构象以及15个过渡态,按照能量升高次序以英文字母对稳定构象命名,过渡态名称由反应物和产物的名称组合而来。稳定构象包含了文献[5]的12 种构象,其中最稳定4 种构象与文献[7]报道的4 种构象一致。为了便于比较和讨论,将这些构象按照转化途径排列于图1,各构象的原子编号一致,参见构象A。
各构象的第一和第二频率值(υ1和υ2)及能量值(相对能ΔE,正逆反应能垒Ea和Ea')列于表1,υ1为正的构象是稳定态,υ1为负而υ2为正的构象是过渡态。最稳定构象A 中含有3 条氢键,分别为BO2-H1、BO2-H2和BN1-H4。前4 种稳定构象的相对能低于4 kJ·mol-1,能量最高构象O 的相对能为16.53 kJ·mol-1。
丝氨酸过渡态主要由 5 个内旋转自由度(C1-C2 键、C2-C3 键、C1-O1 键、N1-C2 键和C3-O3 键)产生。过渡态I-J 和L-M 对应着氨基(N1-C2 键)的旋转,能垒低于10.16 kJ·mol-1。E-L、F-A 和I-N 对应着C1-C2 键的旋转,能垒低于22.78 kJ·mol-1。B-G、D-H 和N-O 对应着C2-C3键的旋转,能垒低于23.31 kJ·mol-1。A-O、C-K、E-K 和G-H 对应着侧链羟基(O3-C3 键)的旋转,能垒低于24.13 kJ·mol-1。B-M、D-J 则对应着羧羟基(C1-O1 键)的旋转,能垒在39.68~54.80 kJ·mol-1之间。A-F 是质子H1 在O1 和O2 原子间迁移的过渡态,能垒高于129.44 kJ·mol-1。
2.2 构象转化途径和机理
丝氨酸构象转化的途径和能级变化见图2。由于A 是最稳定结构,B 是次稳定结构,这里对A转化到B 的微观机理进行详细讨论(其它路径不赘述)。转化路径为
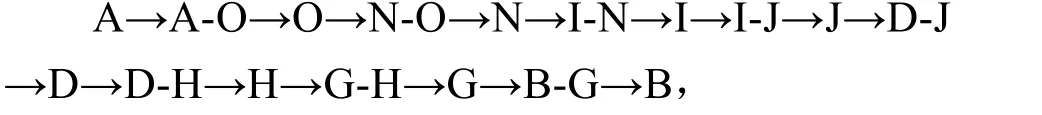
该路径最高能垒为54.8 kJ·mol-1。构象A 中氢键BO2-H1长229.6 pm,BO2-H2和BN1-H4分别为245.3和221.0 pm,二面角ΦH4-O3-C3-C2为43.4°。由C3-O3键的旋转,二面角ΦH4-O3-C3-C2达到-77.3°时得到过渡态A-O,能量升高24.13 kJ·mol-1;达到-82.4°时得到构象O,能量降低7.60 kJ·mol-1。
通过C3-C2 键的旋转,构象O 变为N-O,二面角ΦO3-C3-C2-C1由177.0°变为128.7°,能量升高12.60 kJ·mol-1,该二面角旋转至75.1°得到N,能量降低18.40 kJ·mol-1。构象N 中ΦO2-C1-C2-C3为142.5°,C1-C2 键的旋转导致ΦO2-C1-C2-C3变为68.1°时得到I-N,能量升高18.15 kJ·mol-1。该二面角转至-20.7°时得到I,能量降低20.85 kJ·mol-1。构象I 中ΦH2-N1-C2-C3为-174.3°,N1-C2 键的旋转导致ΦH2-N1-C2-C3变为-117.0°时得到I-J,能量升高6.07 kJ·mol-1。ΦH2-N1-C2-C3转至-64.3°时得到J,能量降低5.69 kJ·mol-1。
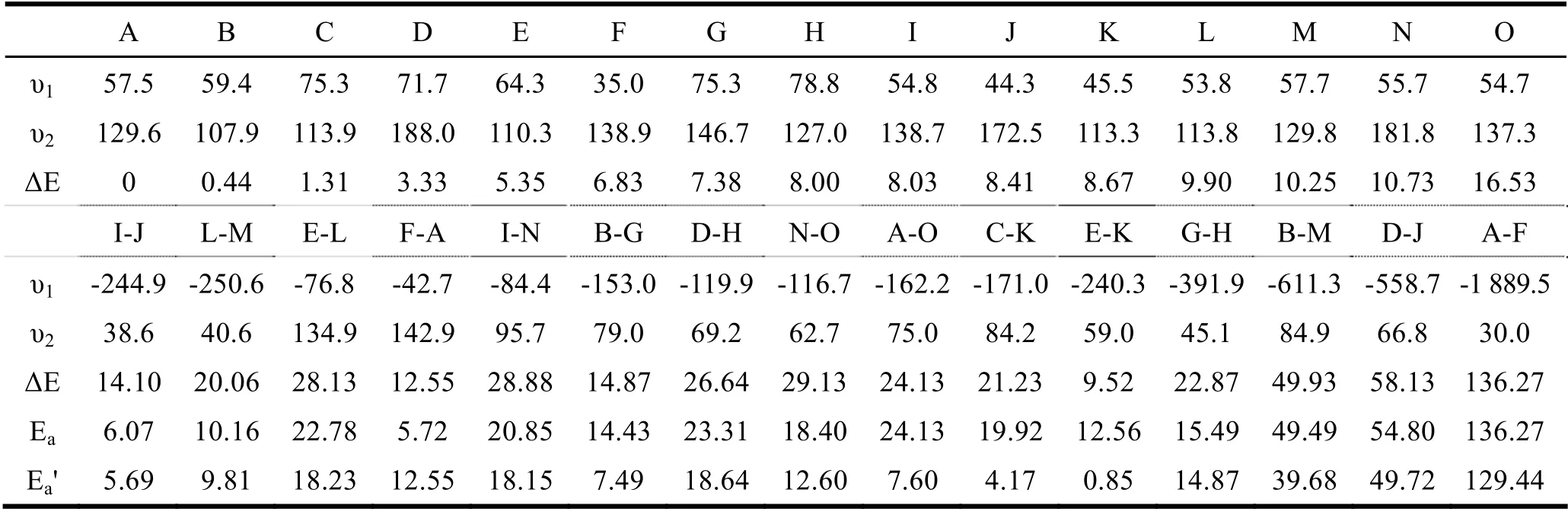
表1 丝氨酸各构象的频率(单位cm-1)及能量(单位kJ·mol-1)
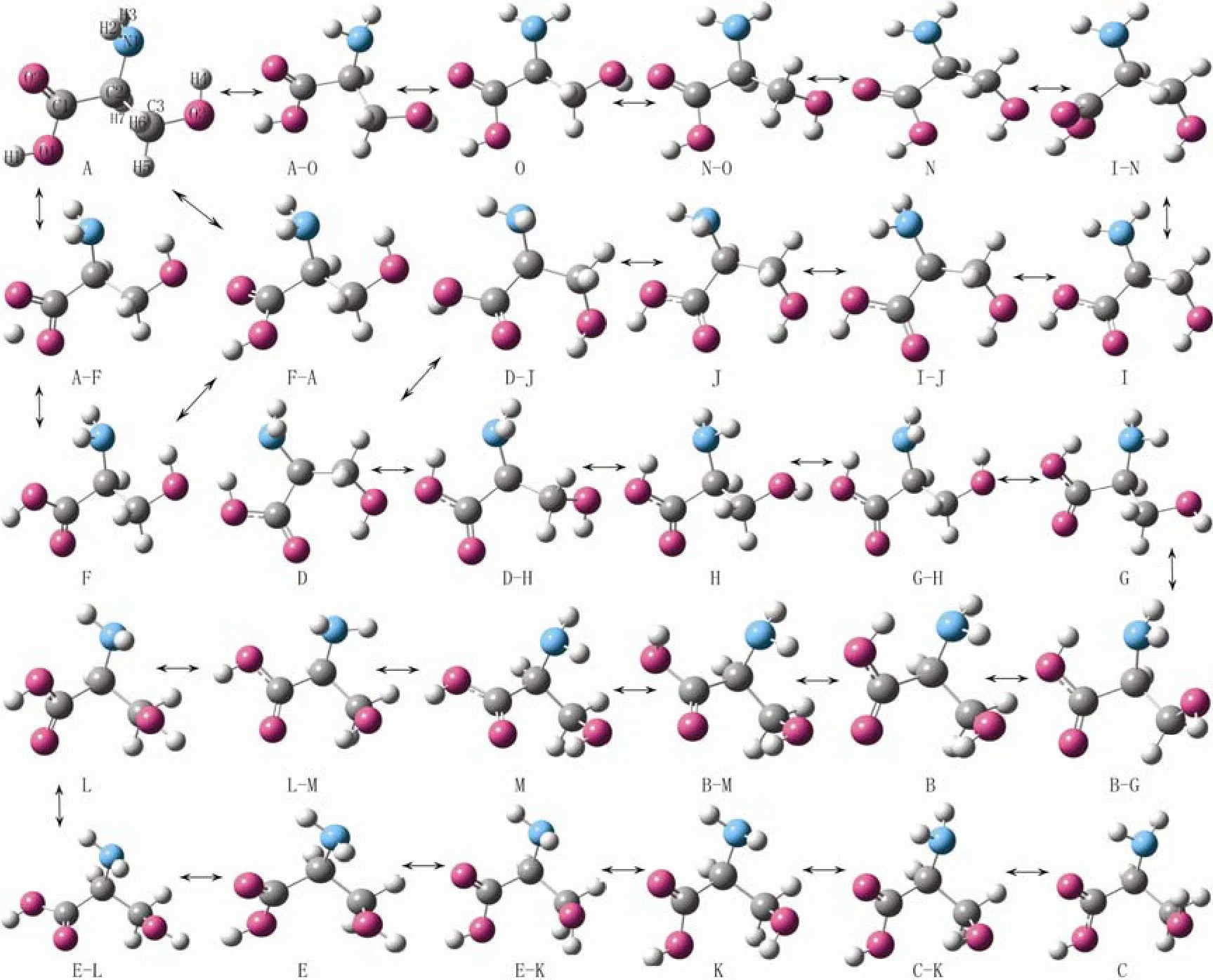
图1 丝氨酸构象及其转化途径
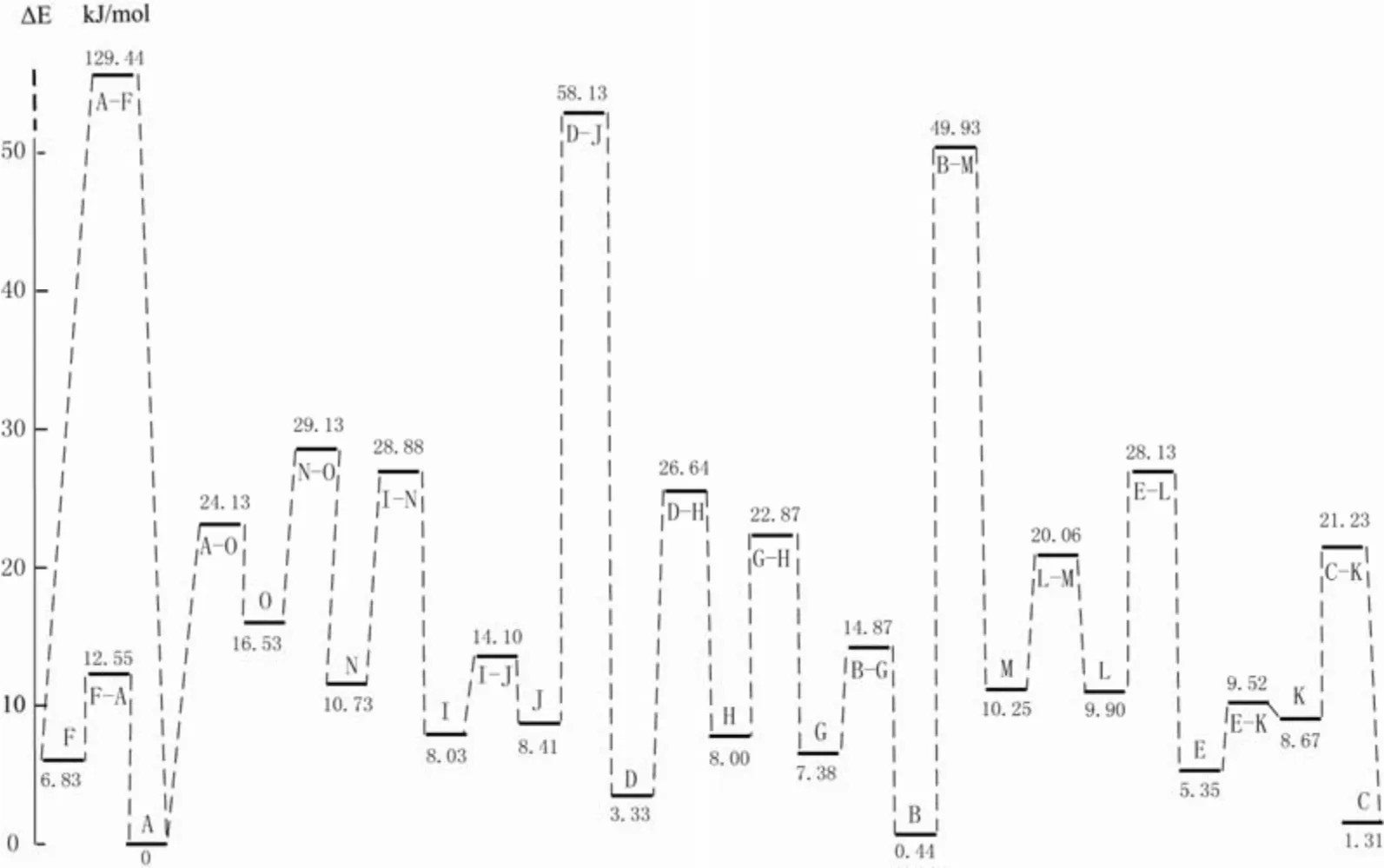
图2 丝氨酸构象转化途径和能级
C1-O1 键的旋转导致J 经由过渡态D-J 转变为D,二面角ΦH1-O1-C1-O2相应地变化,由-0.6°到-97.7°再到176.5°,能量先升高49.72 kJ·mol-1,再降低54.80 kJ·mol-1。C3—C2 键的旋转导致D 经由D-H变为H,二面角ΦO3-C3-C2-C1由64.8°到123.1°再到103.9°,能量先升高23.31 kJ·mol-1,再降低18.64 kJ·mol-1。O3-C3 键的旋转导致H 经由过渡态G-H 转变为G,二面角ΦH4-O3-C3-C2由-123.3°到3.4°再到179.6°,能量先升高14.87 kJ·mol-1,再降低15.49 kJ·mol-1。构象G 通过C3-C2 键的旋转经由B-G 变为B,二面角ΦO3-C3-C2-C1由-179.3°到4.5°再到-63.3°,能量先升高7.49 kJ·mol-1,再降低14.43 kJ·mol-1。
3 结论
运用M06/6-31++G**方法研究丝氨酸构象异构化机理,丝氨酸存在15 种稳定构象,这些构象可以通过分子内化学键的旋转相互转化。氨基旋转的能垒低于10.16 kJ·mol-1,C-C 键旋转的能垒低于23.31 kJ·mol-1;侧链羟基旋转的能垒低于24.13 kJ·mol-1,羧羟基的旋转能垒在 39.68 ~54.80 kJ·mol-1之间。最稳定构象A 转化为次稳定构象B 的路径为A→A-O→O→N-O→N→I-N→I→I-J→J→D-J→D→D-H→H→G-H→G→B-G→B,该路径的最高能垒为54.80 kJ·mol-1。
