贝伐珠单抗联合化疗治疗胶质母细胞瘤的meta分析
2020-04-14赵卓琳周良学周世军
吴 蛟 易 勇 赵卓琳 周良学 周世军
胶质母细胞瘤(glioblastoma,GBM)是一种恶性程度很高的中枢神经系统肿瘤[1]。贝伐珠单抗作为以血管内皮细胞生长因子A(vascular endothelial growth factor A,VEGF-A)为靶点的单克隆抗体,是美国食品药物监督局批准的第一种靶向肿瘤血管生成的药物,自2009 年开始应用于GBM 的治疗[2]。然而,其单独用于治疗GBM的疗效不佳,目前,多与其他疗法联合应用,如放疗、化疗等,但其疗效及不良反应依然众说纷纭[3]。本文采用meta 分析的方法评价贝伐珠单抗联合化疗方案治疗GBM的疗效。
1 资料与方法
1.1 文献检索 以Glioblastoma,Bevacizumab,Chemo⁃therapy 等为英文主题词/关键词检索 Pubmed、Co⁃chrane Central、EMbase;以胶质母细胞瘤、贝伐珠单抗、化疗等为中文主题词/关键词检索中国知网、中国生物医学文献数据库、维普、万方等中文数据库,辅以手工检索相关文献的参考文献,检索日期为从建库至2019年5月所有文献。
1.2 纳入标准和排除标准 临床随机对照试验,研究对象均确诊为GBM,试验组以贝伐珠单抗联合化疗为干预措施,对照组以单独化疗或单用贝伐珠单抗为干预措施。排除非中文或英文的其他语言、无法提供准确的统计学数据、中文非科技核心期刊收录、研究对象每组例数小于30例的研究
1.3 资料提取及质量评价 阅读筛选文献和数据提取由2 位研究者独立完成,存在分歧的文献通过讨论后决定其是否纳入。文献质量按Cochrane 手册5.1.0的方法学质量进行评价。
1.4 统计学方法 采用RevMan 5.3 软件进行数据处理;计量资料采用均数差(mean difference,MD)及其95%置信区间(confidence interval,CI);计数资料采用比值比(odd ratio,OR)及其95%CI表示;纳入研究间的异质性采用χ2检验,P≤0.1、I2≥50%时选择随机效应模型,P>0.1、I2<50%时则选择固定效应模型;P<0.05为差异有统计学意义。
2 结果
2.1 检索结果 初检文献共1 550 篇,阅读标题和摘要剔除1 496 篇,剔除重复文献8 篇、非随机对照试验35篇、不符合评价指标3篇,最终纳入符合标准的文献 8 篇[4~11],共计 2 586 例,其中试验组 1 334 例,对照组1 252例。纳入文献的基本特征见表1。
2.2 meta分析结果
2.2.1 无进展生存期 8项研究[4~11]均报道贝伐珠单抗联合化疗对GBM 病人无进展生存期的影响,共计2 586例,试验组1 334例,对照组1 252例;meta分析结果显示试验组无进展生存期显著长于对照组(MD=2.83;95%CI 1.46~4.20;P<0.0001)。
2.2.2 总体生存期 7 项研究[4~9,11]报道贝伐珠单抗联合化疗对GBM 病人总体生存期的影响,共计1 845例,其中试验组980例,对照组865例;meta分析结果显示,试验组与对照组总体生存期无统计学差异(MD=-0.17;95%CI-1.50~1.15;P=0.80)。
2.2.3 客观反应率 4 项研究[4,7,8,11]报道贝伐珠单抗联合化疗对GBM病人客观反应率的影响,共874例,其中试验组 482 例,对照组 392 例;meta 分析结果显示试验组客观反应率显著高于对照组(OR=2.67;95%CI 1.90~3.76;P<0.00001)。
2.2.4 6 个月无进展生存期 4 项研究[4,5,7,9]报道贝伐珠单抗联合化疗对GBM病人6个月无进展生存率的影响,共 654 例,其中试验组 320 例,对照组 334 例;meta分析结果显示试验组6个月无进展生存期较对照组明显延长(MD=0.25,95% CI 0.14~0.37;P=0.04)。
2.2.5 严重不良反应率 7 项研究报道贝伐珠单抗联合化疗对GBM 病人造成3 级及以上严重不良反应,其中 6 项报道[4,6~9,11]的数据可供 meta 分析使用,共 1 665 例,其中试验组 910 例,对照组 755 例;meta 分析结果显示试验组严重不良反应率明显高于对照组(OR=2.11;95%CI 1.22~3.65;P=0.008)。
3 讨论
本文meta 分析结果显示,与单药治疗相比,贝伐珠单抗联合化疗可以显著改善GBM 病人无进展生存期、6个月无进展生存期,但对总体生存期无明显影响;此外,联合方案的客观反应率更高,但3 级以上不良反应也更频繁。既往有两篇关于贝伐珠单抗联合替莫唑胺和放疗治疗GBM的meta分析,与本文结果一致[12,13]。
联合疗法改善GBM 病人无进展生存期而对总体生存期并无显著影响,可能原因:首先,GBM是一种生长中的肿瘤,贝伐珠单抗预防新生血管的形成可能会导致增生性缺氧,阻碍营养吸收,然而缺氧可能通过多种方式刺激肿瘤进展,如促进血管生成、侵袭肿瘤细胞、抵抗凋亡等;其次,临床前研究证实,使用抗血管生成药物可使肿瘤异常血管正常化,从而减轻肿瘤细胞对放疗和化疗的抵抗,在血管正常化的基础上,使用贝伐珠单抗可以缓解血管源性水肿,虽能改善无进展生存期,但不能充分延长血管正常化的时间,从而提供更长远的益处[12,14,15]。本文结果提示贝伐珠单抗在与化疗联合用于GBM的治疗时,可能是一把双刃剑,在使用贝伐珠单抗与化疗联合治疗后,GBM微环境中序贯性缺氧可能增强了GBM细胞的侵袭性[16]。
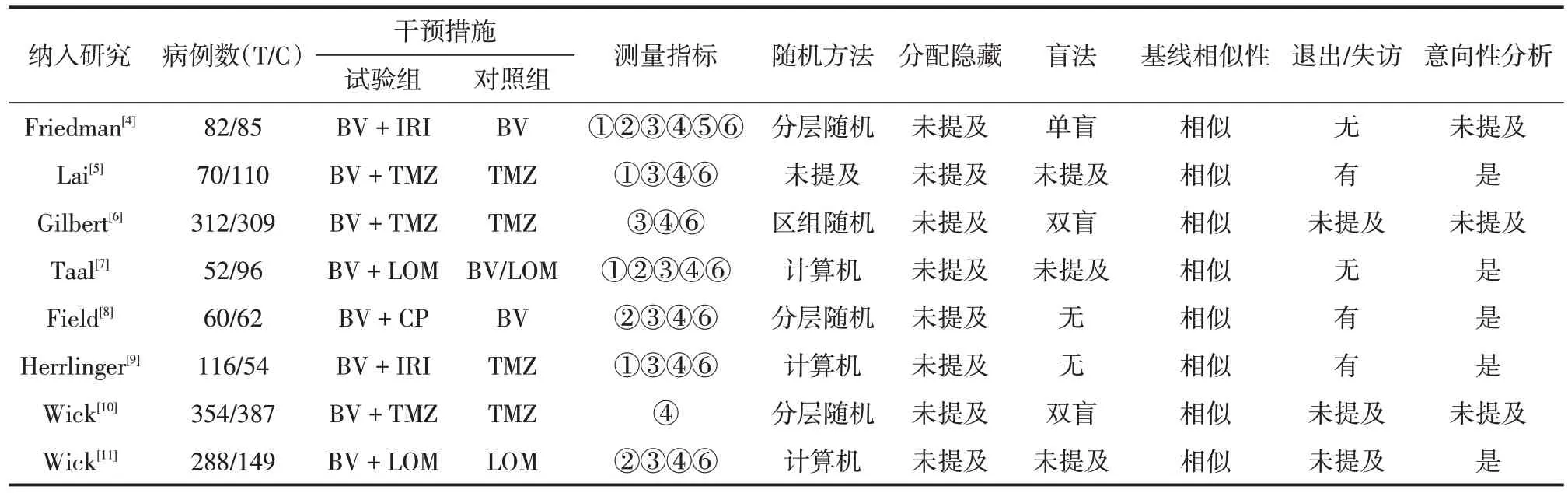
表1 纳入研究的基本特征
此外,由于贝伐珠单抗是一种以VEGF-A 为靶点的单克隆抗体,肿瘤是否高表达VEGF-A 对于疗效有重要影响,而本文纳入的研究并未提及病人肿瘤VEGF-A表达情况,因此,今后的临床研究可探讨对肿瘤VEGF-A表达与贝伐珠单抗疗效的关系。
本文meta 分析存在一些不足:对照组所接受的治疗方案在不同研究间存在差别,可能对贝伐珠单抗联合治疗的评估有影响;此外,由于资料不足,缺乏严重不良反应的亚组分析,未能对特定的严重不良反应在组间的差异进行评估。
综上所述,贝伐珠单抗联合化疗方案可显著改善GBM病人无进展生存期、客观反应率、6个月无进展生存期,但对病人总体生存期无明显影响,其所引起的不良反应比单药治疗更多。
