抗隐孢子虫卵黄抗体制备及间接ELISA方法建立
2020-03-13党秀丽刘珍珍胡苏辉王臣荣菅复春河南农业大学牧医工程学院河南省人兽共患病国际联合实验室河南郑州45000河南农业大学理学院河南郑州45000
张 璐,党秀丽,刘珍珍,胡苏辉,王臣荣,菅复春∗ (.河南农业大学 牧医工程学院/河南省人兽共患病国际联合实验室,河南 郑州45000;.河南农业大学 理学院,河南 郑州45000)
卵黄抗体(immunoglobulin of egg yolk,Ig Y)是通过免疫产蛋鸡,由其生产的蛋黄中提取相应的抗体,并可用于相应疾病的预防和治疗的制剂。Ig Y 具有化学性质稳定、产量高、利于生产、成本低廉,产生有效免疫反应所需抗原量小等优点[1],并可作为捕获或检测抗体用来检测哺乳动物免疫球蛋白,且具有更强的特异性和灵敏度。目前,Ig Y 的应用范围已经扩展到保健品、医药卫生及生物技术等相关领域,应用前景良好[2-4]。
近年来,ELISA 方法以其较强的特异性,高灵敏度,操作简便等优点,在隐孢子虫的检测中得到应用[5-7],但目前仍然没有国产商品化的ELSIA 试剂盒可供使用,因此,建立检测隐孢子虫抗体的间接ELISA 方法很有必要[8-9]。本试验尝试制备抗隐孢子虫的特异性Ig Y 抗体,可用于隐孢子虫病的治疗。在获取特异性Ig Y 过程中,为检测免疫鸡群的抗体水平、Ig Y 抗体产生变化的动态,建立了间接ELISA 检测特异性Ig Y 抗体。
1 材料与方法
1.1 试验动物从郑州市某养鸡场选择并购买8只120日龄开产健康海兰蛋鸡,粪便检查为隐孢子虫阴性,血清学检测显示无抗隐孢子虫抗体。
1.2 仪器及试剂超声波细胞粉碎仪:Cole Parmer Instrument公司;紫外分光光度计:北京普析通用仪器有限公司;全自动酶标仪:Thermo 公司;HRP-兔抗鸡Ig Y:上海艾博抗贸易有限公司;透析袋:北京鼎国昌盛生物技术有限责任公司。
1.3 抗原的制备将提纯后卵囊(108/m L)置液氮(-196℃)和水浴锅37℃反复冻融5次,超声波细胞粉碎仪(100 HZ)2 min×5 次破碎后,10 000 r/min离心15 min,其中,上清作为检测用抗原,沉淀作为免疫用抗原。-20℃保存备用[10]。
1.4 抗原蛋白含量的测定采用紫外分光光度计法测定抗原蛋白含量。
1.5 免疫用疫苗的制备抗原与油佐剂等体积混合,放入50 m L EP管中于漩涡振荡器上振荡,乳化制成“油包水”乳状液;用0~2.5μL 的移液枪吸取0.5μL滴入水面上,如果振荡后的乳剂肉眼看不见扩散,则乳化合格,否则继续振荡直至乳剂滴在水面上肉眼看不见扩散为止。
1.6 蛋鸡的免疫选择8只120日龄开产健康海兰蛋鸡,4只用于隐孢子虫抗原免疫制备Ig Y,4只不免疫作为阴性对照。参照邵兆霞等[11]的方法制定免疫程序和剂量,采取长期多次免疫法,首免剂量卵囊为1×107个/只,二免剂量卵囊为2×107个/只,三免剂量卵囊为2.5×107个/只,免疫方式为翅根部皮下及胸部肌肉多点注射法进行免疫。对照组以空白疫苗做相对应的免疫。
1.7 卵黄的收集与纯化收集免疫前鸡蛋和对照组鸡蛋作为阴性对照。首次免疫7 d后开始收集试验组和对照组鸡蛋并按照分组编号,将收集的鸡蛋清洁消毒后,打破蛋壳,弃蛋清,用医用一次性1 m L注射器吸取卵黄液置试管中,用9倍的灭菌单蒸水稀释,之后采用二步硫酸铵法纯化卵黄液[12]。
1.8 间接ELISA方法的建立
1.8.1 间接ELISA 程序 按常规方法在96孔聚丙乙烯微量板上进行。程序如下:抗原包被,洗涤,封闭,洗涤,加检测样品,洗涤,酶标抗体,洗涤,底物显色,终止,测定吸光度值。
1.8.2 抗原和抗体最佳工作浓度的测定 采用方阵滴定法确定抗原最适包被浓度和一抗的最佳工作浓度。将纯化抗原稀释为1.0,2.0,2.5和3.0 mg/L共4个质量浓度进行包被,每个质量浓度重复4孔,每孔100μL,4℃过夜。用1%明胶进行封闭,阳性和阴性Ig Y 分别做200,400,800倍稀释,每个稀释度重复4孔,37℃孵育1 h。按照1.8.1间接ELISA程序进行操作,记录结果。选取阳性Ig Y 平均D450nm接近1.00,相邻平均D值出现较大变化并且P/N值达到最大的孔,确定抗原最适包被质量浓度和抗体最佳稀释度。
1.8.3 最佳包被条件的选择 将抗原进行2.5 mg/L稀释后包被酶标板,分别在以下3个条件下进行包被:37℃作用1 h后4℃过夜,37℃作用2 h后4℃过夜,4℃过夜,筛选最优包被条件。
1.8.4 最佳酶标抗体工作浓度的选择 96孔酶标板包被、封闭之后,样品作1∶100倍稀释,对酶标抗体进行2 000,3 000,5 000和8 000倍稀释,100μL/孔,确定最佳工作浓度。
1.8.5 最佳一抗反应时间的测定 加入一抗之后,将抗原抗体作用时间依次调整为30,45,60 min,确定最佳作用时间。
1.8.6 最佳酶标抗体反应时间的测定 将酶标抗体做1∶3 000倍稀释,并分别于37℃作用30,45,60 min,确定其最佳反应时间。
1.8.7 最佳显色时间的测定 对抗原作2.5 mg/L稀释后包被酶标板,37℃作用2 h后4℃过夜,样品作1∶400稀释。加底物液后,分别避光显色5,10,15,20 min,确定最佳显色时间。
1.9 检测性试验
1.9.1 特异性试验 采用已建立的间接ELISA 方法,对球虫卵囊,圆线虫虫卵和贾第虫抗原进行检测,同时设立阳性和阴性对照,读取D450nm值、记录结果。
1.9.2 重复性试验 以批内和批间重复性试验来检验间接ELISA 方法的重复性,选取3份卵黄抗体样本在不同时间、相同条件下重复做ELISA 测定,每个样品重复4次,按照已建立的间接ELISA 操作程序测定,计算同一份样本D450nm值的变异系数(CV),比较试验结果。
1.9.3 敏感性试验 将隐孢子虫阳性Ig Y 从1∶400开始做2倍连续稀释至1∶12 800,共做6个稀释度,其他条件不变,按照已建立的间接ELISA 操作方法测定D450nm值,检测其敏感性。以出现阳性的最高稀释倍数推算其最小检出量。
2 结果
2.1 抗原的蛋白含量经紫外分光光度法测得本次制备的隐孢子虫抗原蛋白含量为1.734 g/L。
2.2 抗隐孢子虫卵黄抗体的收集与纯化免疫前后,收集不同时间产出的鸡蛋,按水稀释二步硫酸铵法提取卵黄,纯化Ig Y,获得Ig Y 抗体。
2.3 间接ELISA方法的建立
2.3.1 抗原最适包被浓度及阴、阳性Ig Y 最佳稀释度的确定 方阵滴定结果可知(表1),抗原包被质量浓度为2.5 mg/L,一抗稀释度为1∶400 时,D450nm接近于1.0,且此时P/N最大,故在ELISA检测方法中抗原包被质量浓度确定为2.5 mg/L,被检样品的稀释倍数为1∶400。
2.3.2 最佳包被条件的选择 由表2可知,37℃作用1 h后4℃过夜,37℃作用2 h后4℃过夜,4℃过夜等3种条件下包被,37℃作用2 h后4℃过夜条件下D450nm值最大,故采用此包被条件最佳。
2.3.3 最佳酶标抗体工作浓度的确定 最佳酶标抗体工作浓度的选择结果如表3所示,因此确定最佳酶标抗体工作浓度为1∶3 000。
2.3.4 最佳一抗反应时间的确定 最佳被检卵黄抗体作用时间选择结果如表4所示。试验确定最佳被检卵黄抗体作用时间为37℃孵育60 min。
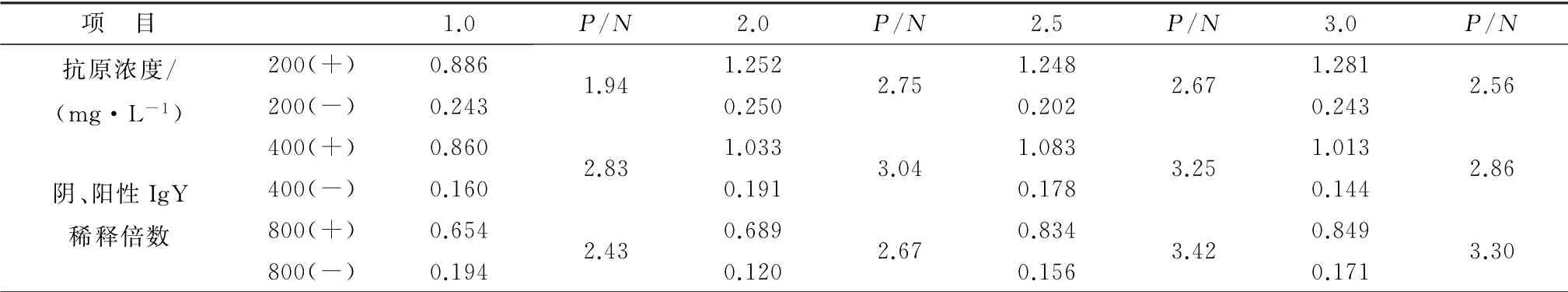
表1 抗原最适包被浓度及阴、阳性Ig Y 最佳稀释度的确定
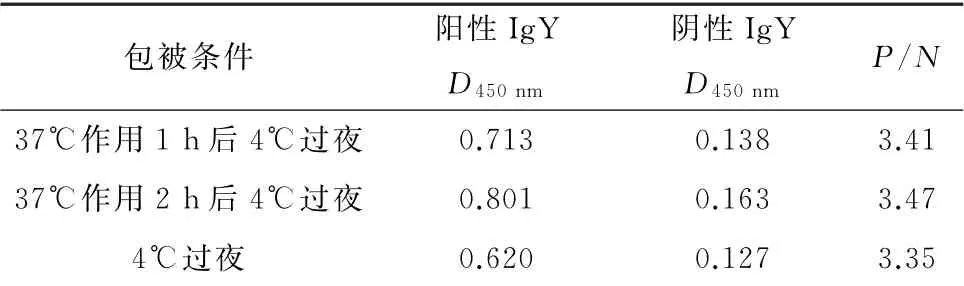
表2 最佳包被条件的确定
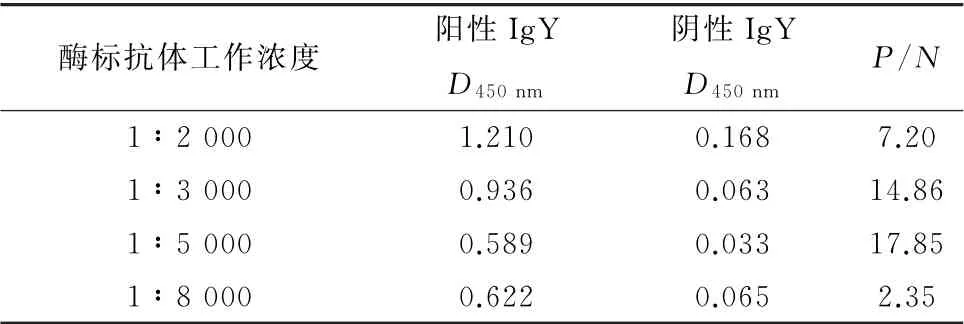
表3 最佳酶标抗体工作浓度的选择
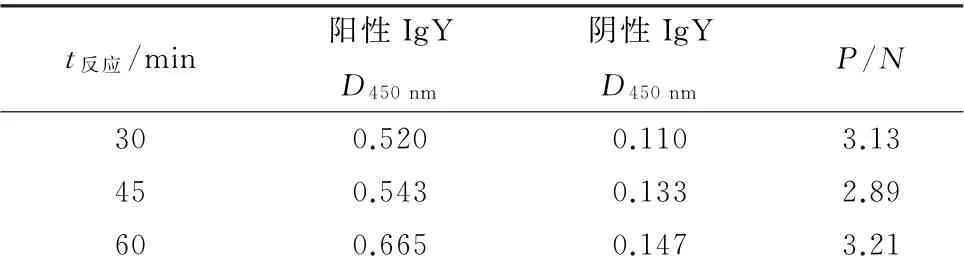
表4 一抗最佳反应时间的的确定
2.3.5 最佳酶标抗体反应时间的确定 最佳酶标抗体作用时间选择结果如表5所示。试验确定最佳酶标抗体作用时间为37℃孵育45 min。
2.3.6 最佳显色时间的测定 最佳被检样品和酶标抗体作用时间选择结果如表6所示,最终确定显色条件为室温显色10 min。
2.4 检测性试验
2.4.1 特异性试验 对已知的圆线虫虫卵,球虫卵囊和贾第虫包囊按照隐孢子虫检测的前处理方法,同样检测这些虫卵的抗原作1∶100稀释,同时设阳性对照和阴性对照,每份样品重复4孔,然后用本试验建立的间接ELISA 检测方法进行测定。除阳性对照外,结果均为阴性,表明Ig Y 抗体间接ELISA方法具有良好的特异性(表7)。
2.4.2 重复性试验 如表8结果所示,随机抽取的3个卵黄样品批内和批间变异系数在2.98%~7.58% 之间,均小于10%,表明方法的重复性好。
2.4.3 敏感性试验 将阳性Ig Y 作倍比稀释后,用建立的间接ELISA 方法检测,结果显示当阳性Ig Y稀释到1∶12 800后,检测结果仍为阳性,显示建立的间接ELISA 方法具有良好的敏感性(表9)。
2.4.4 卵黄抗体的产生规律 蛋鸡在首次免疫后14 d,在卵黄中可以检测到特异性抗体,经过3次免疫之后抗体效价达到1∶12 800(图1)。
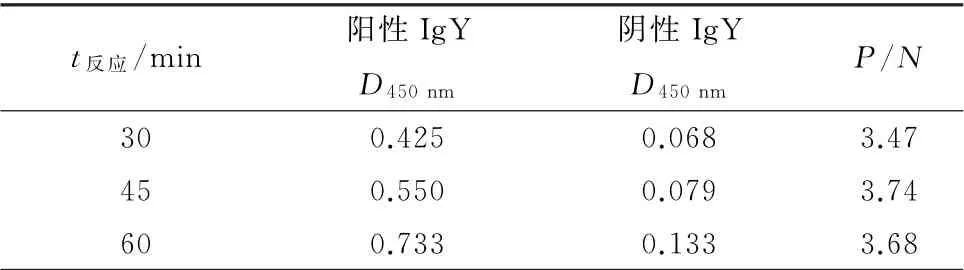
表5 酶标二抗最佳反应时间的的确定
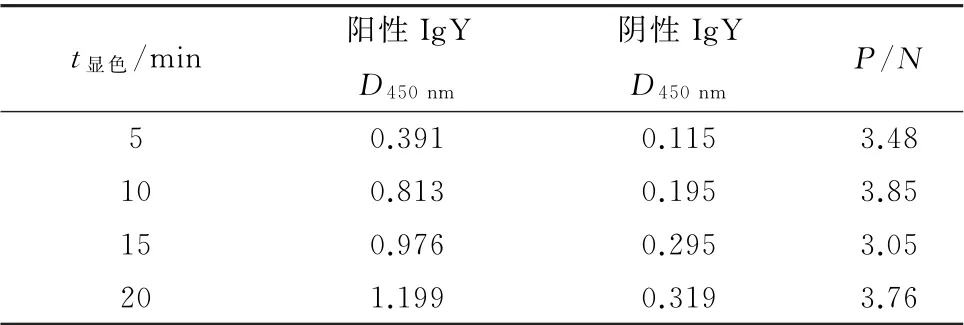
表6 最佳显色时间的确定

表7 特异性试验

表8 批内、批间重复性试验 %

表9 敏感性试验
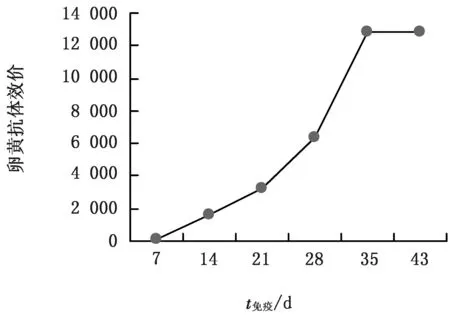
图1 卵黄抗体的产生规律
3 讨论
3.1 IgY抗体比一般哺乳动物来源的IgG 抗体有更多的优点禽类与哺乳动物有一定的种属距离差异,这使得Ig Y 具有很多特性和优点[13-14]。Ig Y 具有良好的耐热、耐酸、耐碱和一定的耐酶解能力;Ig Y 成本低、产量高,易获得;产蛋母鸡易于饲养,无须抽取动物的血液,直接收集鸡蛋,对动物无伤害,符合动物保护规则;同时与IgG 相比Ig Y 产生有效抗体反应所需抗原量较少,3次免疫后,可以连续收取鸡蛋40 d左右,抗体产出比较高。因此在某些动物疾病的预防及治疗中Ig Y 有着更好的优势,从而被称为一种新生代抗体,并且已经越来越多的应用于各种病原的检测,疾病的预防及治疗[15-17]。目前对于Ig Y 的规模化生产和临床推广应用还有一些问题尚未解决,相信随着Ig Y 生产技术的发展和对其研究的不断深入,Ig Y 的应用前景将越来越广阔,有可能成为一类广泛应用的新型生物制剂。
3.2 建立间接ELISA 方法检测卵黄抗体水平常用于检测鸡群抗体水平的方法是ELISA、琼脂扩散、免疫荧光试验,ELISA 方法具有特异性好,灵敏度高,操作简便,易标准定量化等优点,从而获得广泛应用[18-19]。在ELISA 反应中,非特异性吸附和非特异性反应是影响ELISA 方法成败的关键因素。抗原包被浓度、一抗稀释倍数和二抗稀释倍数等也直接影响着试验结果。通过试验条件不断摸索优化,最终确定试验条件为:抗原的工作质量浓度为2.5 mg/L;Ig Y 的最佳稀释倍数1∶400;Ig Y 作用时间为37℃,1 h;1%明胶37℃封闭1 h;HRP-兔抗鸡Ig Y 的最佳工作浓度为1∶5 000,作用时间为37℃,45 min;底物反应的时间为室温显色10 min。本试验建立的间接ELISA 特异性强、灵敏度高、可重复性好。以此方法检测Ig Y 抗体,首免后7 d开始有抗体产生,三免后7 d测得Ig Y 抗体效价即可达到1∶12 800。
3.3 IgY可进一步应用于免疫学检测或治疗中隐孢子虫是最常见的人兽共患虫种之一,主要引起未断奶犊牛严重腹泻甚至死亡,并可导致包括人在内的多种脊椎动物腹泻[20]。免疫学检测方法主要有免疫荧光、酶免疫分析、流式细胞仪技术、免疫磁珠分离、免疫印迹和间接血凝试验等,因其特异性好、敏感性强,便于批量检测等优点,被广泛应用于隐孢子虫病诊断中。
目前,国内外许多学者开辟了免疫学检测方法检测隐孢子虫的新途径,主要用于检测隐孢子虫卵囊抗原,子孢子抗原和特异性抗体,并且有着很好的发展趋势和前景[21]。本试验制得的Ig Y 可以作为捕获或检测抗体用来检测哺乳动物免疫球蛋白,具有更强的特异性和灵敏度,可用于进一步的免疫检测及治疗应用中。
