含离子聚丙烯酰胺/氧化石墨烯的制备及应用
2020-03-06邵亚辉彭双双彭晓宏
邵亚辉,彭双双,彭晓宏
(华南理工大学 材料科学与工程学院,广东 广州 510640)
当前对于工业废水中重金属离子[1-3]的处理通常采用吸附法[4-5],但现有吸附剂[6-7]往往存在吸附效果差、成本高及可循环使用不佳的问题,在考虑吸附效果的前提下,经济成本往往成为制约吸附剂应用最重要的因素。聚丙烯酰胺(PAM)[8]在污水处理方面的应用由来已久。作为絮凝剂的PAM大多为线型高分子,在引入极性第二单体后,阳离子聚丙烯酰胺(CPAM)[9]和阴离子聚丙烯酰胺(APAM)[10]的制备方法获得改进,制备过程更加节能环保,同时对带电污染物的絮凝性能也更加优异。氧化石墨烯(GO)[11-13]广泛应用于污水处理中染料和重金属离子的吸附,吸附效果优异,利用离子型PAM与GO结合制备复合水凝胶吸附剂,将有望达到更好的污水处理效果和良好的经济效益。目前,分别采用GO和含离子聚合物作为吸附染料的吸附剂时有报道[14-16],但将GO与含离子聚电解质结合制备复合材料吸附剂的研究尚未见报道。
本工作以GO,丙烯酰胺(AM)和极性第二单体为原料,通过简单且环境友好的一步自由基聚合法制备了PAM/GO、CPAM/GO和APAM/GO复合水凝胶。利用FTIR、13C NMR、拉曼光谱和XRD等方法对合成产物进行了表征,研究了复合水凝胶对Cr(Ⅵ)的吸附行为,分析了CPAM/GO吸附Cr(Ⅵ)的影响因素。
1 实验部分
1.1 主要试剂与仪器
AM:化学纯,上海润捷化学试剂有限公司;丙烯酸(AA)、甲基丙烯酰氧基乙基三甲基氯化铵(DMC)、N,N’-亚甲基双丙烯酰胺(MBA)、氢氧化钠、重铬酸钾:分析纯,天津福晨化学试剂厂;GO:纯度99.9%,济宁利特纳米技术有限责任公司;过硫酸铵、无水乙醇、盐酸:分析纯,广州化学试剂厂;二苯碳酰二肼:分析纯,麦克林试剂有限公司。
VERTEX70型傅里叶变换红外光谱仪、Bruker-500型核磁共振光谱仪、D8 ADVANCE型X射线衍射仪:德国Brucker公司;Lab RAM Aramis型拉曼光谱仪:法国H.J.Y公司;FD-IA-50型冷冻干燥机:上海利闻科学仪器有限公司;U-3010型紫外可见分光光度计:日本日立公司。
1.2 复合水凝胶的制备
采用自由基共聚一步聚合法制备复合水凝胶:向3等份30.0 mg的GO粉末中分别加入7.5 mL去离子水,超声处理1 h后得到3份分散稳定的GO剥离液。制备PAM/GO时,在1份分散液中加入1.0 g AM;制备APAM/GO时,加入1.0 g AM,2.0 g AA和0.9 g氢氧化钠;制备CPAM/GO时,加入1.0 g AM和0.32 g DMC。将三种混合液搅拌混合至均匀透明后分别倒入带蛇形冷凝器、温度计和磁力搅拌器的三颈烧瓶中。通N2除氧0.5 h,再分别加入7.50 mL 4.2%(w)的过硫酸铵溶液引发剂和20 mg MBA交联剂,在63 ℃下反应8 h得到3种深黄色水凝胶。所得水凝胶分别用去离子水浸泡洗涤数小时,过滤后重复浸泡洗涤3次,得淡黄色凝胶。将凝胶产物切成约1 cm×1 cm×1 cm的小方块冷冻过夜后,放入-50 ℃的真空冷冻干燥机中干燥48 h后得外表蓬松的深黄色干凝胶,置于干燥器中备用。
1.3 吸附表征
1.3.1 Cr(Ⅵ)标准溶液的配制
称取110 ℃下干燥2 h的重铬酸钾0.29 g,用去离子水完全溶解配成1.0 g/L的Cr(Ⅵ)储备液。
1.3.2 复合水凝胶对Cr(Ⅵ)的吸附动力学
288 K下,在40 mg/L的K2Cr2O7溶液中,pH=5的条件下分别加入20 mg复合水凝胶进行静态吸附,每隔10 min取上清液测定Cr(Ⅵ)浓度,直至平衡,计算平衡吸附量。
1.3.3 CPAM/GO吸附Cr(Ⅵ)的影响因素
吸附等温线及吸附热力学均在288,303,313 K下进行,在50 mL重铬酸钾(40 mg/L)溶液中,调节pH=5,用20 mg CPAM/GO进行静态吸附,收集平衡时的吸附数据。
考察288 K下单因素对CPAM/GO吸附Cr(Ⅵ)的影响:1)pH:设定初始Cr(Ⅵ)为80 mg/L,将30 mg CPAM/GO加入50 mL溶液中,在不同pH下进行静态吸附,达到吸附平衡后测定浓度,计算吸附容量;2)Cr(Ⅵ)初始质量浓度:在50 mL的Cr(Ⅵ)溶液中加入30 mg CPAM/GO,在不同Cr(Ⅵ)质量浓度,pH=5下进行静态吸附;3)CPAM/GO用量:在pH=5的80 mg/L的50 mL原始Cr(Ⅵ)溶液中,分别依次加入不同用量的CPAM/GO,静态吸附后,测定铬的质量浓度并计算吸附量。
1.3.4 吸附容量的计算
按GB 7466—1987[17]规定的方法,利用分光光度计在最大波长540 nm处测量吸光度并计算铬的总质量浓度,按式(1)~(2)计算复合水凝胶吸附剂对Cr(Ⅵ)的吸附容量。

式中,Qt为t时的吸附容量,mg/g;Qe为平衡吸附时间下的吸附容量,mg/g;ρ0为初始Cr(Ⅵ)的质量浓度,mg/L;ρt为t时Cr(Ⅵ)的质量浓度,mg/L;ρe为Cr(Ⅵ)平衡状态下的质量浓度,mg/L;V为Cr(Ⅵ)溶液的体积,L;m为干燥水凝胶的质量,g。
2 结果与讨论
2.1 复合水凝胶结构表征
2.1.1 FTIR表征结果
图1为试样的FTIR谱图。从图1可看出,在GO中,1 737 cm-1处的吸收峰归属于羧基的伸缩振动,1 060,1 409 cm-1处的伸缩振动峰归属于C—O—C和C—OH;在PAM中,3 200 cm-1处为N—H的伸缩振动峰,2 930,2 865 cm-1处为—CH2—的不对称和对称伸缩振动吸收峰;PAM/GO在1 107,1 420 cm-1处的吸收峰分别归属于GO上环氧基团和C—OH基团的伸缩振动,2 935 cm-1处为PAM的—CH2—的伸缩振动峰,表明PAM分子与GO键接成功;CPAM/GO的谱图与PAM/GO基本相似,DMC中亚甲基的弯曲振动峰和伸缩振动峰分别出现在1 452,953 cm-1处,表明CPAM分子与GO成功结合;APAM/GO在1 230,1 170 cm-1处出现的新吸收峰归属于AA中羧基的伸缩振动,说明APAM/GO已成功制备。
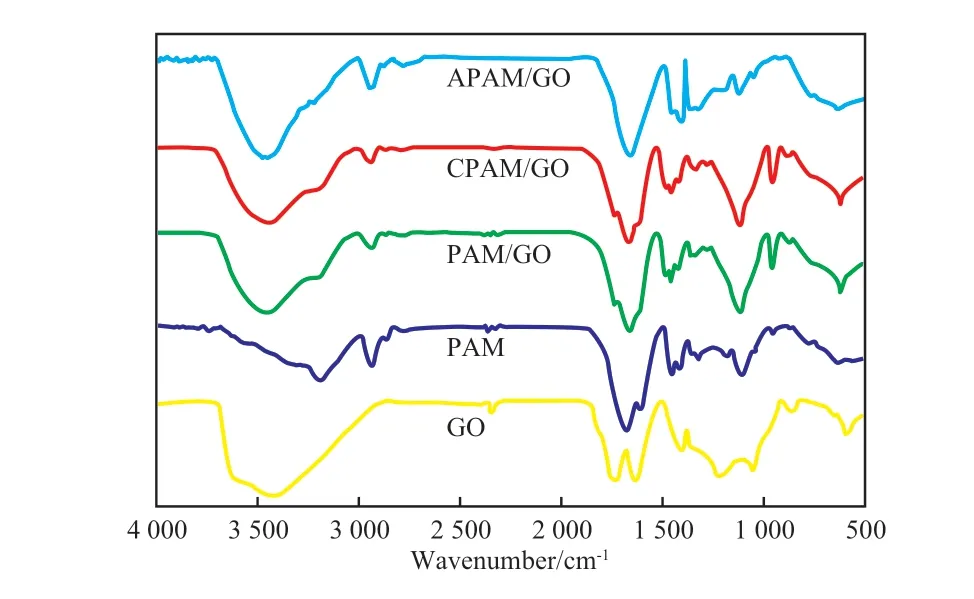
图1 试样的FTIR谱图Fig.1 FTIR spectra of samples.
2.1.213C NMR表征结果
试样的13C NMR谱图见图2。如图2所示,PAM/GO,APAM/GO,CPAM/GO的化学位移δ非常接近,并且在δ=180.35,43.25处均出现两个明显的特征峰,其中,δ=180.35处的特征峰对应于聚合物基体中的—CO—NH2或CO—NH—CO—结构;δ=43.25处的特征峰对应基体中的—CH2或—CH结构。δ=133处的特征峰代表GO的sp2杂化碳(C=C)结构。13C NMR谱中没有出现结合后的共振峰,由此可推断复合水凝胶体系中聚合物与GO之间很可能未发生化学反应或者只有极少量的化学反应发生,因而共价键作用难以显现。GO通过与聚合物基体间的范德华力、物理包覆作用以及大量的氢键结合而稳定分散在基体中,与FTIR的表征结果相对应。
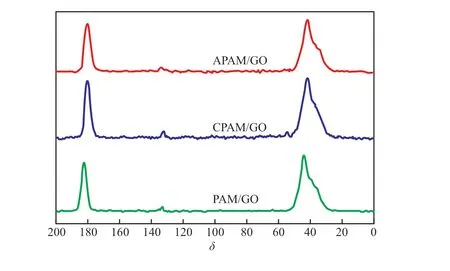
图2 试样的13C NMR谱图Fig.2 13C NMR spectra of the samples.
2.1.3 拉曼光谱表征结果
拉曼光谱可用于确定复合物中石墨烯的存在以及石墨烯在基体中的分布情况[18]。通常对于石墨烯碳基材料,D峰(1 335 cm-1)表示结构缺陷的石墨,G峰(1 585 cm-1)表示结构完整的石墨。图3为试样的拉曼光谱图。由图3可知,4种试样均出现了G峰和D峰,其中,GO在这两个峰处的强度最大,而3种复合水凝胶两峰处的数值均有一定程度的降低。D峰与G峰强度的比值(ID/IG)通常用于评估碳基石墨烯纳米材料的石墨化程度。ID/IG越小表明材料中石墨的还原程度越高,反之表明氧化程度越高[19]。计算结果表明,GO的ID/IG=0.87,而APAM/GO,CPAM/GO和PAM/GO的ID/IG分别为0.85,0.83,0.81。较GO均有不同程度减小,但降幅不大。较小的ID/IG对应较高的还原程度,即在聚合过程中有少量GO被还原。说明聚合物单体聚合对GO化学微观结构的影响很小,该结果与FTIR和13C NMR的表征结果相对应。
2.1.4 XRD表征结果
试样的XRD谱图见图4。层间距(d)根据2dsinθ=nλ(λ为入射波长,nm;θ为衍射角,°;n为衍射级数)计算。如图4所示,GO(001)处的衍射峰对应的衍射角出现在10.93°,层间距为0.86 nm,表明GO是单层结构体,层间距大于原始石墨的层间距(0.335 nm)[19]。这可能是因为,氧化反应后,引入的含氧官能团插入GO层中,使得原始石墨的层间距被拉伸,不同的GO含氧官能团的数量不同,含氧官能团越多,对应完整结构的区域越小,即层间距越大,XRD的衍射峰的半高宽值也越大,层间距0.86 nm也表明GO上含氧官能团的数量较多。APAM/GO,PAM/GO和CPAM/GO的衍射峰对应的衍射角分别为21.86°,21.36°和21.96°,层间距分别为0.41,0.42,0.40 nm,即GO减少,说明在聚合过程中GO的氧化性降低即含氧官能团被部分还原,由此也可说明GO有效地参与了反应过程。
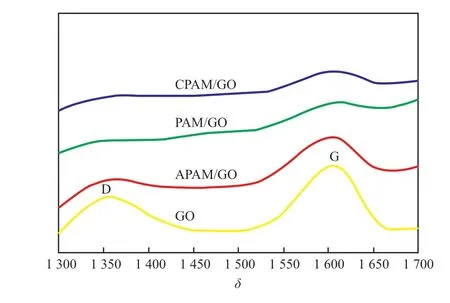
图3 试样的拉曼光谱图Fig.3 Raman spectra of samples.

图4 试样的XRD谱图Fig.4 XRD patterns of samples.
2.2 复合水凝胶对Cr(Ⅵ)的吸附应用
2.2.1 Cr(Ⅵ)标准曲线的绘制
以浓度为x轴、吸光度为y轴作Cr(Ⅵ)标准曲线,得到Cr(Ⅵ)标准液的线性关系为y=-0.102 8+0.524 0x,R2=0.993 6说明线性较好。
2.2.2 复合水凝胶对Cr(Ⅵ)的吸附动力学
吸附动力学可探究吸附过程中主要的速率控制步骤以及复合水凝胶对Cr(Ⅵ)的吸附机理[20]。288 K下研究了复合水凝胶对Cr(Ⅵ)的吸附曲线,结果见图5。从图5可看出,在引入GO以后,复合水凝胶的吸附容量明显增强,三种复合水凝胶对Cr(Ⅵ)的吸附速率均呈先快速增加后趋于平衡的变化趋势。CPAM/GO对Cr(Ⅵ)的吸附量明显高于APAM/GO和PAM/GO,说明DMC的引入提高了CPAM/GO对Cr(Ⅵ)的吸附性能。

图5 复合水凝胶吸附Cr(Ⅵ)的曲线Fig.5 Curves of adsorption Cr(Ⅵ) by composite hydrogel.
采用伪一阶和伪二阶动力学模型考察吸附动力学。伪一阶动力学模型通常对应于物理吸附,假定吸附速率主要由扩散步骤决定;伪二阶动力学模型通常对应于化学吸附,假定吸附之间的相互作用为决定吸附速率的关键。式(3)~(4)分别为伪一阶和伪二阶模型的拟合动力学方程。

式中,Qe1为伪一阶模型中达到平衡时间的吸附量,mg/g;Qe2为伪二阶模型中达到平衡时间的吸附量,mg/g;k1为伪一阶模型的速率常数,min-1;k2为伪二阶模型的速率常数,mg/(g·min2)。
伪一阶和伪二阶动力学模型的参数见表1。由表1可看出,通过伪一阶动力学模型模拟计算的Qe1与实验得到的Qe有较大差距,拟合系数R2在0.875 2~0.977 6之间,表明拟合程度不高,因此伪一阶动力学模型可能不是理想模型;通过伪二阶动力学模型模拟计算的Qe2与实验得到的Qe较接近,R2均在0.99以上,表明伪二阶动力学模型可作为复合水凝胶对Cr(Ⅵ)吸附动力学拟合的理想模型。
2.2.3 CPAM/GO对Cr(Ⅵ)的吸附等温线模拟
CPAM/GO对Cr(Ⅵ)的吸附等温线见图6。从图6可看出,在相同温度下,初始吸附速率均快速增加,接近平衡时吸附速率增速缓慢直至最后达到吸附动态平衡,此时吸附容量达到最大值;随温度的升高,CPAM/GO对Cr(Ⅵ)的吸附量增大。

表1 288 K下复合水凝胶吸附Cr(Ⅵ)的动力学参数Table 1 Kinetic parameters for adsorption Cr(Ⅵ) by composite hydrogel at 288 K

图6 CPAM/GO吸附Cr(Ⅵ)的等温吸附线Fig.6 The adsorption isotherm for adsorption Cr(Ⅵ) by CPAM/GO.
Langmuir等温模拟线和Freundlich等温模拟线见式(5)~(6)[21],对于Langmuir等温线,可以用无量纲平衡参数(RL)描述,见式(7)。


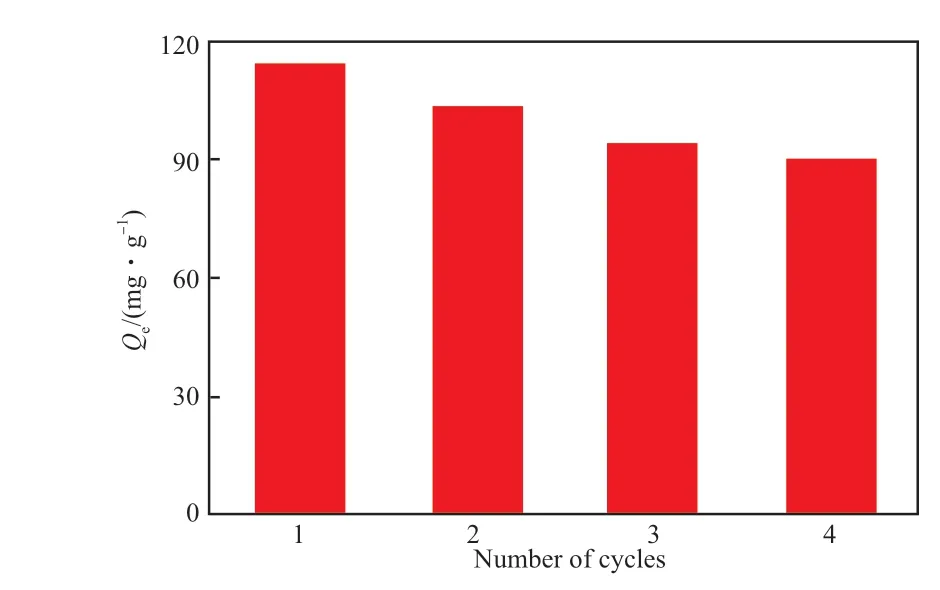
式中,Qmax为最大吸附容量,mg/g;KL为Langmuir常数,L/mg;KF为Freundlich常数,(mg·g-1)/(L·mg-1)1/n;n为与吸附分子和吸附剂表面作用强度有关的参数。RL表示等温线的类型,RL>1为不利,RL=1为线性,0 以Cr(Ⅵ)的ρ0=40 mg/L进行Langmuir和Freundlich等温模拟,结果见表2。从表2可看出,CPAM/GO吸附Cr(Ⅵ)的RL均在0~1的范围内,说明CPAM/GO对Cr(Ⅵ)的吸附为有利过程,吸热性导致Qmax和RL随温度的升高而增加,即高温有利于吸附;Freundlich拟合常数n均小于10,说明吸附具有自发性,另外Freundlich拟合的R2均略小于Langmuir拟合的R2。由此可知CPAM/GO对Cr(Ⅵ)的吸附等温模拟中,Langmuir等温拟合更好,也说明Cr(Ⅵ)在复合水凝胶上的吸附为单层均质吸附。 表2 CPAM/GO吸附Cr(Ⅵ)的等温模拟参数Table 2 The isothermal simulation parameters for adsorption Cr(Ⅵ) by CPAM/GO 2.2.4 CPAM/GO对Cr(Ⅵ)吸附热力学 CPAM/GO对Cr(Ⅵ)的吸附吉布斯自由能用范霍夫方程式(8)~(9)计算。 式中,T为溶液的温度,K;R为气体常数,8.314×10-3kJ/(mol·K);Kd为分配系数;ΔG 为标准吉布斯自由能,kJ/mol;ΔH 为标准焓变,kJ/mol;ΔS 为标准熵变,J/(mol·K)。 根据lnKd~1/K的线性拟合计算得到CPAM/GO对Cr(Ⅵ)吸附的热力学参数见表3。由表3可知,ΔG <0表明吸附Cr(Ⅵ)到CPAM/GO是自发且可行的;ΔH >0表明CPAM/GO对Cr(Ⅵ)的吸附是吸热过程;ΔS >0表明吸附过程为熵增,即自由度增加的热力学自发过程。 表3 吸附Cr(Ⅵ)的热力学参数Table 3 Thermodynamic parameters for adsorption Cr(Ⅵ) 2.2.5 CPAM/GO吸附Cr(Ⅵ)的影响因素 2.2.5.1 pH对吸附的影响 溶液的酸碱度不仅影响Cr(Ⅵ)的稳定性,还影响吸附剂的带电情况,从而影响表面结合位点。pH对CPAM/GO吸附Cr(Ⅵ)的影响见图7。 图7 pH对CPAM/GO吸附Cr(Ⅵ)的影响Fig.7 The effect of pH on the adsorption of Cr(Ⅵ) by CPAM/GO.Reaction conditions:Cr(Ⅵ) initial concentration 80 mg/L,Cr(Ⅵ) solution 50 mL,CPAM/GO 30 mg. 从图7可看出,随pH增大,CPAM/GO吸附Cr(Ⅵ)能力先增强后降低,Qe在pH=5时最大。Cr(Ⅵ)在水溶液中有几种稳定的存在形式,每种存在形式的相对浓度均与Cr(Ⅵ)的初始质量浓度和溶液pH有关。pH<5时Cr(Ⅵ)的优势存在形式为,此时聚合物中的NH质子化后转化为NH2+,和HCrO4-能与NH2+发生强烈的静电相互吸引,从而达到吸附Cr(Ⅵ)的效果。当pH>7时,Cr(Ⅵ)的存在形式主要为CrO42-,此时随溶液pH的升高,聚合物中的NH2+含量降低,导致吸附量降低,因此吸附的最佳pH=5。 2.2.5.2 Cr(Ⅵ)初始质量浓度对吸附的影响 Cr(Ⅵ)初始质量浓度对CPAM/GO吸附Cr(Ⅵ)的影响见图8。从图8可看出,随初始质量浓度的增加,吸附量增加,但金属离子的吸收率从85.94%(57.29 mg/g)降至72.24%(120.40 mg/g)。表明吸附量依赖初始质量浓度,但对于固定的吸附剂质量,总可用吸附位点是有限的,因此随着吸附剂初始质量浓度的增加,去除率降低。 图8 Cr(Ⅵ)初始质量浓度对CPAM/GO吸附Cr(Ⅵ)的影响Fig.8 The effect of Cr(Ⅵ) initial mass concentration on adsorption of Cr(Ⅵ) by CPAM/GO. 2.2.5.3 CPAM/GO用量对吸附的影响 CPAM/GO用量对吸附Cr(Ⅵ)的影响见图9。从图9可看出,当CPAM/GO的用量从12 mg增加到45 mg时,Qe从200.33 mg/g降至80.01 mg/g,说明能够被吸附的铬的容量有限,大量有效吸附位点未能吸附Cr(Ⅵ),即单位质量CPAM/GO吸附的铬的量会降低。但吸附效率随吸附剂用量的增加而增加,这是由于增加的吸附剂为Cr(Ⅵ)提供了更多的吸附活性位点和更大的比表面积。本工作选取CPAM/GO的最佳用量为30 mg。 2.2.6 吸附剂的再生性能 在温度为288 K下研究了CPAM/GO对吸附Cr(Ⅵ)的循环使用性能。用50 mL 0.10 mol/L的NaOH作解吸剂进行吸附-解吸实验,经过4个循环后,结果见图10。由图10可知,经过4次吸附解吸循环后,Qe从113.43 mg/g降至89.87 mg/g,相对于初始Qe仍保持了80%的吸附能力,表明CPAM/GO对Cr(Ⅵ)具有较好的循环吸附性能。 图9 CPAM/GO用量对吸附Cr(Ⅵ)的影响Fig.9 The effect of CPAM/GO amount on the adsorption of Cr(Ⅵ).Reaction conditions:Cr(Ⅵ) initial concentration 80 mg/L,Cr(Ⅵ) solution 50 mL,pH=5. 图10 CPAM/GO对Cr(Ⅵ)的循环吸附性能Fig.10 Recyclability of CPAM/GO for adsorption Cr(Ⅵ).Reaction conditions:CPAM/GO 30 mg,Cr(Ⅵ) initial concentration 80 mg/L,pH=5. 1)采用一步自由基聚合法制备了PAM/GO、CPAM/GO和APAM/GO复合水凝胶。GO通过与聚合物基体间的范德华力、物理包覆作用和氢键结合稳定分散在基体中,聚合物单体聚合对GO化学微观结构的影响很小。 2)伪二阶动力学模型能更好地模拟复合水凝胶对Cr(Ⅵ)的吸附过程。Langmuir等温拟合是合适的等温拟合方式,Cr(Ⅵ)在复合水凝胶上的吸附是单层均质吸附。 3)288 K下,CPAM/GO对Cr(Ⅵ)的吸附量高于APAM/GO和PAM/GO。CPAM/GO对Cr(Ⅵ)的最佳吸附条件为:Cr(Ⅵ)初始质量浓度80 mg/L,CPAM/GO用量30 mg,溶液pH=5。在经过4个吸附-解吸循环后,CPAM/GO吸附Cr(Ⅵ)的Qe仍能保持初始Qe的80%。






3 结论
