培美曲塞联合洛铂治疗晚期肺腺癌的临床观察
2020-01-10张瑞清肖克安
张瑞清 肖克安
广东省中山市黄圃人民医院内二科,广东中山 528429
根据国家癌症中心发布的最新癌症报告,肺癌已经成为发病率、死亡率最高的恶性肿瘤,其中非小细胞肺癌占全部肺癌的85%以上[1],而肺腺癌为非小细胞肺癌主要类型。循证医学证据显示,在肺癌的治疗中,不同病理类型的生物学特性不同,并直接对化疗药物的药理学活性产生影响,因此依照病理学亚型确定治疗方案成为新的趋势。肺腺癌恶性程度高、易转移及复发,预后较差,且大部分患者在确诊时多为晚期,因此全身化疗成为临床主要治疗手段。培美曲塞联合顺铂为晚期肺腺癌治疗的基础方案,然而在实际治疗过程中,顺铂引起的强烈毒性反应严重影响患者治疗耐受性及依从性,因此探讨毒性更小的化疗药物成为近年来医务工作者的主要研究目标。国内外相关医学研究发现,洛铂在抗癌活性方面与顺铂相似,然而其引起的胃肠道反应及肾毒性相对较轻。为进一步明确洛铂与培美曲塞联合治疗肺腺癌的应用价值,笔者选取我院收治的90 例晚期肺腺癌患者进行分组研究,现报道如下。
1 资料与方法
1.1 一般资料
选取2016 年2 月~2018 年2 月在我院接受化疗的90 例肺腺癌患者作为研究对象,均符合以下纳入标准:(1)经肺部CT 确诊,病理细胞学诊断为晚期肺腺癌;(2)预计生存期>半年;(3)患者均知晓本次研究且签署知情同意书;(4)完成全程治疗及随访。排除标准:(1)早、中期肺癌;(2)肝肾功能异常、血常规异常者;(3)中途失访者。按照随机数字表法将其分为观察组(45 例)与参考组(45 例)。观察组:男25 例,女20 例,年龄44 ~76 岁,平均(60.6±3.3)岁;病程0.5~5年,平均(2.01±0.75)年;其中ⅢB 期22 例,Ⅳ期23 例;其中肿瘤转移28 例(骨转移17 例,腹部转移6 例,中枢神经系统转移5例)。参考组:男23 例,女22 例,年龄45 ~76 岁,平均(60.4±3.3)岁;病程0.5 ~5 年,平均(2.1±0.8)年;其中ⅢB 期23 例,Ⅳ期22 例;其中肿瘤转移26 例(骨转移15 例,腹部转移7 例,中枢神经系统转移4 例)。研究经医院伦理委员会审核通过,两组患者临床资料比较差异无统计学意义(P >0.05),具有可比性。
1.2 方法
两组患者接受化疗前7d 肌内注射维生素B12(海南制药二厂,H41023607)1000μg,口服叶酸(常州制药厂,H20067437)400μg 直至化疗结束后21d。化疗前1d、当天以及开始后1d,患者口服地塞米松(广州白云山制药股份有限公司,H44024666)8mg/d。观察组:第1 天静脉滴注培美曲塞(江苏豪森药业集团有限公司,H20093996)500mg/m2以及洛铂(海南长安国际制药有限公司,H20050308)30mg/m2,连续治疗21d 为1 个疗程。参考组培美曲塞用法、用量、生产厂家及批次与观察组相同,在第1 ~ 3 天静脉滴注顺铂(齐鲁制药有限公司,H37021358 )常规水化利尿,连续21d。化疗期间,每周对血尿常规、心电图及生化治疗进行复查,若出现血小板减少、Ⅲ~Ⅳ白细胞减少,则给予IL-11或者G-GSF 治疗。
1.3 观察指标
(1)记录两组治疗期间胃肠道反应、皮疹、骨髓抑制、血小板及白细胞减少等不良反应发生情况;以NCI-CTCAE 评分[2]评价毒副反应严重程度,采用0 ~4 分评价,分数越高则毒副反应越严重。(2)治疗后,对患者CEA、β2微球蛋白、CYFRA21-1、NSE 水平进行观察;(3)随访1 年,观察两组死亡率、远处转移、局部复发率发生情况,并采用QOL 评分[3]对患者生活质量进行评价。从食欲、精神、睡眠、疲乏、疼痛、家庭理解与照顾、自身对癌症认识、同时及朋友的照顾、对治疗的态度治疗副作用及日常生活等方面进行评价,满分60 分,分数越低表明生活质量越差。
1.4 疗效判定
化疗2 个周期后进行效果评价,参考2000 年版RECIST 实体瘤疗效评价标准[4],将治疗效果分为4 级:完全缓解:病灶完全消失,肿瘤标志物水平恢复正常,至少维持4 周;部分缓解:目标病灶体积缩小50%以上,至少维持4 周以上;稳定:肿瘤病灶两径乘积缩小不足25%或增大小于25%,未见新病灶;进展:肿瘤病灶两径乘积增加25%以上,或者由新病灶出现。若得到有效评价,则在4周后再次进行疗效再确认。
1.5 统计学分析
2 结果
2.1 两组患者治疗效果比较
观察组治疗总有效率为84.44%(38/45,其中完全缓解20 例,部分缓解18 例),无变化5 例,进展2 例;参考组治疗总有效率为82.22%(37/45,其中完全缓解19 例,部分缓解18 例),无变化6 例,进展2 例,两组治疗效果比较,差异无统计学意义(χ2=0.080,P=0.777)。
2.2 两组患者毒副反应发生情况比较
两组治疗期间均有患者出现消化道反应、血液学毒性等表现,观察组与参考组发生率分别为11.11%、28.89%,差异有统计学意义(P <0.05)。两组毒副反应分布见表1。

表1 两组毒副反应发生情况比较[n(%)]
2.3 两组患者肿瘤标志物水平比较
观察组患者CEA、β2-MG、CYFRA21-1、TPA 水平明显低于参考组,差异有统计学意义(P<0.05)。见表2。
表2 两组患者肿瘤标志物水平比较
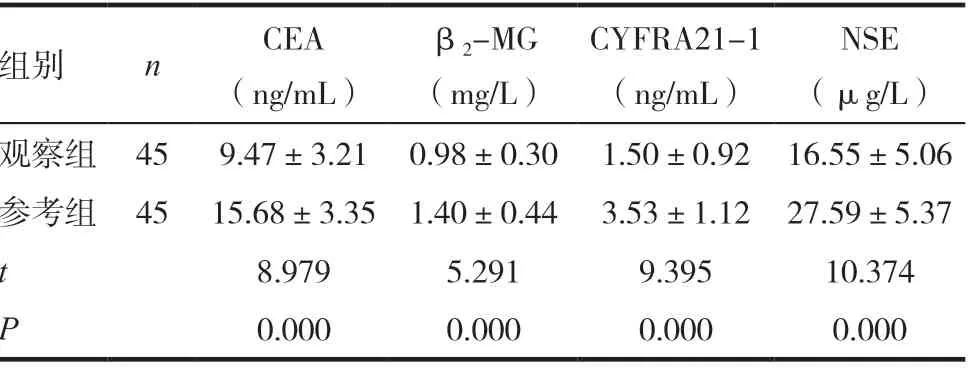
表2 两组患者肿瘤标志物水平比较
?
2.4 两组远期治疗效果比较
1 年随访期内,观察组与参考组全因死亡率、远处转移、局部复发率比较差异无统计学意义(P >0.05),见表3。
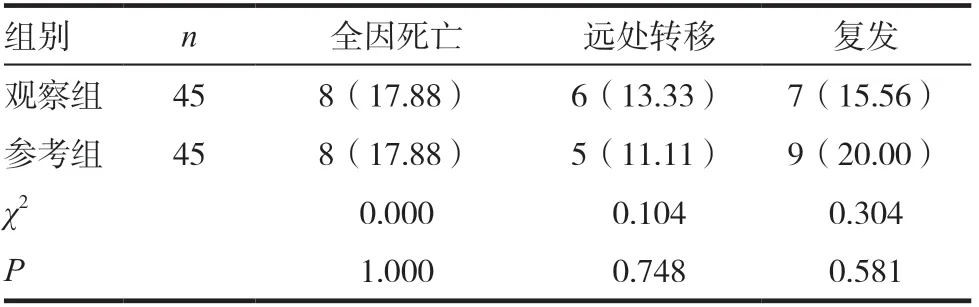
表3 两组死亡率、远处转移及局部复发率比较(n/%)
2.5 两组患者QOL评分比较
观察组QOL 评分为(40.09±3.55)分,参考组QOL 评分为(30.51±3.65)分。两组比较差异有统计学意义(t=12.622,P=0.000)。
3 讨论
医院统计数据显示,由于大部分肺腺癌患者确诊时已经为晚期,因此患者5 年生存率仅为5%,在延长患者生命时间的同时提高其生存质量成为现代医学治疗的主要原则[5]。NSCLC 协作组在1995年分析并明确了铂类药物为主的化疗方案[6],而顺铂治疗效果明显优于卡铂,因此在2009 年,NCCN指南推荐培美曲塞+顺铂为肺腺癌的一线化疗方案。然而随着治疗方案的推广,人们发现顺铂虽然治疗效果较为理想,然而药物自身的肾毒性、耳毒性以及胃肠道较为严重,患者耐受性较差,甚至放弃治疗,因此探讨毒性更小的化疗替代药物成为临床研究的重点。
洛铂为第三代新型铂类抗癌药物,主要用于慢性粒细胞性白血病、小细胞肺癌等,具有抗瘤谱广及活性强、水溶性号等特点,在临床应用中表现出明显优势。在肺腺癌治疗中,药物能够形成Pt-GG、Pt-AG 链内交叉连接,对DNA 转录、复制过程形成阻滞,进而干扰肿瘤细胞周期运行,发挥与顺铂相似的治疗效果。周宇、张纪良等[7-8]在研究中发现,洛铂联合吉西他滨、多西他赛治疗肺癌中均取得良好效果,而药物肾毒性较轻,因此无需水化,患者的治疗依从性显著提高。本次研究中,观察组患者化疗期间毒副反应发生率明显低于参考组,且NCICTCAE 评分明显低于参考组(P <0.05),证实了洛铂联合培美曲塞在肺腺癌治疗中毒副作用更小。通过对两组毒副反应分析,可以发现参考组主要集中在胃肠道反应、血小板减少、口腔黏膜溃疡等,查看病历发现患者多是在化疗第2 个周期后出现,因此随着化疗时间的延长,医护人员必须通过有效手段干预化疗毒副反应,从而帮助患者建立治疗的信心。观察组患者毒副反应中以口腔黏膜溃疡为主,分析认为与个体基因多态性影响、药物协同作用等有关,考虑与洛铂毒性、培美曲塞造成的叶酸消耗有关,因此在治疗期间需告知患者做好口腔卫生护理。在随访期内,观察组QOL 评分明显高于参考组(P <0.05),在QOL 调查量表的编制中,心理、躯体反应及不良反应占据较大比例,由此可见反应化疗的副作用可能对癌症患者的生活质量产生直接或间接的影响,化疗期间毒副反应越明显,则患者的精神压力越大、自我感受越差,甚至对治疗缺乏信心;此外,化疗毒副反应引起的食欲减退、呕吐恶心、疼痛等均可对患者生活质量产生影响[9-10],因此在化疗药物的选择中,采用培美曲塞联合洛铂治疗,可减少药物毒副反应对患者生活质量的影响,对其治疗依从性的提高有积极意义,而这同时与现代医学人文理念相符合。
培美曲塞为新型抗叶酸化疗药物,能够通过对细胞复制过程中叶酸代谢进行干扰,从而有效发挥自身抗肿瘤作用[11]。相关研究发现,培美曲塞可抑制甘氨酰胺核苷甲酰基转移酶、胸苷酸合成酶,从而多靶点抑制,抑制胸腺嘧啶核苷及嘌呤生物合成,进而影响肿瘤RNA 及DNA 合成[12-14]。CEA、β2-MG、CYFRA21-1、TPA 等为恶性肿瘤主要标志物[15],能够反应肿瘤控制效果,观察组治疗后各指标水平明显低于参考组(P <0.05),分析认为采用培美曲塞联合洛铂治疗肺腺癌,二者作用机制、代谢过程不同,因此能够发挥协同作用,优势互补,达到显著的治疗效果。本次研究中,观察组与参考组近期治疗总有效率、随访期内死亡率、远处转移、局部复发率比较无显著差异(P >0.05),表明两者联合治疗可达到理想的治疗效果。
总之,在晚期肺腺癌的治疗中,培美曲塞联合洛铂可达到理想效果,药物毒副反应对患者耐受性、生活质量等影响较小,因此可作为一线治疗方案推广使用;然而本研究受时间限制,患者随访时间较短,因此需更长时间研究进行验证。
