超声引导介入治疗动静脉内瘘狭窄的临床应用
2020-01-07孙淑良钟小亮刘海兰
孙淑良,宋 嫣,钟小亮,刘海兰,肖 颖,汪 晨
(南昌大学第三附属医院超声科,南昌330000)
动静脉内瘘(arteriovenous fistulas,AVF)是终末期肾病患者行血液透析治疗的主要血管通路,而动静脉内瘘狭窄是许多终末期肾病患者长期血液透析后发生的最常见的并发症,也是造成内瘘血栓形成及最终失功的首要病因[1],良好的血管通路是保证患者透析质量、提高其生活质量、延长其生命的最重要条件。过往治疗动静脉内瘘狭窄常采用外科手术重建或放射引导下介入治疗[2],但是两者均有诸多的局限性,例如创伤大、需特殊设备场地、患者及医护人员均暴露于X线辐射下等。近年来,随着超声技术的提升及超声仪器的更新,超声下经皮腔内血管成形术(percutaneous transluminal angioplasty,PTA)介入治疗动静脉内瘘狭窄产生了非常良好的反应及疗效,已成为透析通路血管狭窄的一线治疗方法[3]。南昌大学第三附属医院于2018年2月起开展此项技术,临床成功率达95%,效果显著,现对符合纳入标准的50例患者进行报告如下。
1 资料与方法
1.1 一般资料
选取2018年2—12月于本院就诊的AVF狭窄患者50例,其中自体动静脉内瘘44例,人工血管动静脉内瘘6例,狭窄部位主要位于静脉段、吻合口段、动脉段(表1);男32例,女18例,年龄29~89岁,平均(59.10±12.68)岁。50例患者均行超声引导下PTA术,手术适应证如下:1)血液透析穿刺困难,无法抽取血液,或透析时血流量<200 mL·min-1;2)触诊发现内瘘血管震颤减弱或消失,听诊杂音消失;3)彩色多普勒超声血流成像检查显示血管狭窄≥50%并肱动脉血流量<500 mL·min-1,狭窄处血流速度增快。

表1 狭窄部位及内瘘类型
1.2 手术方法
PTA术前,使用彩色多普勒超声诊断仪对动静脉内瘘进行详细检查,常规采用高频探头,明确动静脉内瘘狭窄的部位、管径及狭窄长度,在检查前需将超声探头及连线置于无菌透明塑料袋内。嘱患者取仰卧位于手术床,术肢外展伸直,超声医生及彩超仪放置于患者术肢的一侧,常规消毒铺巾、局部麻醉,在超声引导下选取合适位置对瘘管进行穿刺,可选择静脉端或动脉远心端,穿刺成功后置入导丝,再将穿刺针退出,沿导丝置入穿刺鞘管,并退出导丝,经鞘管注入普通肝素20 mg,经导管鞘置入0.035英寸超滑泥鳅导丝,若狭窄部位血管角度过大或者分支较多时可使用指引导管辅助,导丝通过狭窄部位后,根据超声图像显示下的血管直径选择适宜外周血管球囊(狭窄相连正常的血管直径与球囊直径比率为1.0:1.1为宜),沿导丝置入PTA球囊至狭窄病变部位进行分次扩张,一个部位反复扩张3次左右,每次持续30 s左右,球囊压力需缓慢增加,可每2 atm(202.65 kPa)增加1次,直至球囊压迹消失。经PTA治疗后复查彩超,观察狭窄部位的血管有无回缩,若原狭窄处残余狭窄仍>30%,可选择直径比首次扩张球囊大1 mm的球囊进行扩张。确认无并发症后,拔出血管鞘并加压包扎。
1.3 评估方法
手术成功:术后超声评估残余狭窄内径<30%,内瘘血管震颤增强,肱动脉血流量增大等,临床上可顺利完成血液透析治疗,每周2~3次,维持1个月以上[4]。
1.4 统计学方法
2 结果
50例患者手术均成功,成功率达100%,术后次日即可正常进行常规血液透析治疗。与术前相比,术后狭窄处内径、肱动脉血流量和临床透析血流量均明显增大,差异均有统计学意义(均P<0.001),见表2。术前术后均行常规超声评估,可见术后狭窄处内径、肱动脉血流量均较术前有显著改善,见封四图1—2。

A:术前超声显示头静脉流出道血管内膜增生,局部管腔狭窄,彩色多普勒成线状血流,最窄处内径1.3 mm;B:术后即刻超声评估可见头静脉流出道较术前内径明显增宽,彩色血流充盈良好,原狭窄处内径3.8 mm。
图1 超声评估术前术后狭窄处内径(患者,女,55岁,行维持性血液透析7年余)

A:术前超声测得肱动脉血流量64 mL·min-1,峰值血流速度49.5 cm·s-1;B:术后即刻超声测得肱动脉血流量417 mL·min-1,峰值血流速度119.4 cm·s-1,较术前明显增大。
图2 术前术后超声评估肱动脉血流量(同图1患者)
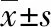
表2 PTA术前术后各参数比较
3 讨论
血管通路是维持性血液透析患者的重要生命线,肾脏病预后质量倡议(Kidney Disease Outcomes Quality Initiative,KDOQI)指南建议终末期肾病患者的血管通路首选自体AVF[5],对于该病维持性血液透析患者来说,建立动静脉內瘘是血液透析的根本,也是永久性通路的最佳选择,但因血管内膜增生、血栓形成、血管壁钙化等原因常导致AVF狭窄或闭塞。永久性血管通路故障是相关疾病发病和死亡的主要原因,同时也会增加终末期肾脏病患者进行慢性维持性血液透析治疗所需的费用。以往常采用外科手术来治疗AVF狭窄或闭塞,近些年来,PTA技术的应用使得AVF狭窄有了更新的治疗方式选择,已成为透析通路血管狭窄的一线治疗方法。PTA技术可以在超声引导下或DSA引导下进行,本文主要探讨超声引导下PTA的临床应用。
本研究50例患者均行超声引导下PTA,均取得了良好的疗效,与术前相比,术后内瘘血管内径、肱动脉血流和临床透析血流量均明显增大(均P<0.001),患者术后次日即可行血液透析治疗,部分患者手术当天即可正常行血液透析,且透析血流量良好。超声引导下PTA仅需一台具备高频探头的彩色多普勒超声诊断仪,操作简便,可重复观察,能直观观察血管管腔和管壁等结构、狭窄的部位和程度以及相邻血管的毗邻关系,术中操作时可引导静脉血管的穿刺,实时清楚地显示导丝、球囊导管的行进,并指导球囊导管放置的位置及观察球囊扩张的情况,大大减少血管穿孔等并发症的发生,并且能随时观察血流情况,及时发现可能的血栓,血肿的形成,术后还可立即评估再狭窄情况,减少并发症的发生,更利于评估手术完成的效果。同时超声对于动静脉内瘘血流量的评估也起着至关重要的作用,血管通路临床实践指南[6]推荐每月监测血流量。内瘘狭窄早期可引起超声血流量和血流动力学相关参数的改变,高频超声定期监测能够对其早期发现和诊断[7]。因超声引导下PTA具有简便、无创、可重复性等优点而成为首选的方法。有研究[8]认为肱动脉可作为超声血流量参数的最佳测量部位。本研究对每一例患者均于PTA术前和术后采用超声进行血流量的测定,并对比前后血流量差异,发现术后均有较大提升。由于超声测量血流量相关技术的局限性,本研究得出的血流量数据并非完全等同于真实的血流量,但是只要操作规范,尽量减少测量的一些误差,如测量血流频谱时取样线与血管角度尽量小、选择较为平直的血管段进行测量等。需要特别指出的是,对于不同类型的内瘘,本研究测量血流量时有所区别,以自体桡动脉-头静脉内瘘为例,一般以肱动脉血流量为最终测值;而人工动静脉内瘘,以肱动脉-贵要静脉为例,则以肱动脉吻合口近心端血流量值减去肱动脉吻合口远心端血流量值为最终测值。通过大量的临床实践得知,超声可作为衡量内瘘功能的一个重要手段[9]。但是超声无法监测中心静脉的相关情况,使其有一定局限性。
在PTA术中,有时会有一些并发症的发生,如血肿、静脉破裂、血栓形成等[10]。本研究中共有7例发生不同的并发症,术中均进行了相应的处理,如对血肿处进行适当的球囊扩张压迫,可进行多次,但需要注意压力的选择,不可过大。血栓形成及静脉破裂也可使用该方法进行局部的扩张压迫,并注入少许肝素以预防血栓的形成。本研究发现绝大多数术中并发症均可获得显著治疗效果,同时发现对于静脉极度扭曲、血管钙化严重的患者,PTA术后效果相对较差。对于静脉极度扭曲患者,导丝及球囊的置入面临较大困难,会极大增加PTA术失败的风险,因此对需球囊扩张的静脉段极度扭曲患者,不建议将PTA作为治疗首选;而血管的钙化也可能导致上述问题,或者出现球囊不能完全将狭窄处扩开的情况。血管钙化可能与患者高磷血症、继发性甲状旁腺功能亢进有关[11],甲状旁腺激素分泌过多可导致患者全身多系统损害,高磷、高甲状旁腺激素是导致患者血管钙化的重要因素之一,也是导致心血管事件死亡率升高的危险因素之一[12],因此调节患者血电解质的稳定也很重要,不仅可减少患者血管钙化及心血管并发症的发生,也对远期行PTA术有益。
综上所述,超声引导下PTA治疗AVF狭窄是一种微创、疗效显著、安全方便、术中及术后并发症少的优良方法,可保留患者珍贵的血管资源,另外超声对于远期效果的评估及预后发挥着重要的作用。
