液相色谱-质谱联用法测定罂粟壳中5种生物碱的含量
2019-12-27黄宁唐丽君黄恩堂苏星王毅梅杨希
黄宁,唐丽君,黄恩堂,苏星,王毅梅,杨希
1.鹰潭市综合检验检测中心,江西 鹰潭 335000;2.江西省食品检验检测研究院,江西 南昌 330001
罂粟壳为罂粟科植物罂粟的干燥成熟果壳,具有敛肺、涩肠、止痛的功效,用于久咳,久泻,脱肛,脘腹疼痛。收录在《中国药典》2015年版一部(以下简称药典),但本品易成瘾[1],需严格控制用量,所以罂粟壳的定量检测显得尤为重要。罂粟壳的活性成分主要是吗啡、罂粟碱、可待因、那可丁、蒂巴因等生物碱,目前大多研究性文献[2-20]研究罂粟壳成分主要从以上5种生物碱中选择1~5种作为分析对象,不同产地、批号的罂粟壳中生物碱的含量差异较大。药典中罂粟壳的【含量测定】项目仅对吗啡进行了控制。
笔者通过大量试验,建立了液相色谱-质谱联用法同时测定罂粟壳中吗啡、罂粟碱、可待因、那可丁、蒂巴因的含量。该方法高效快捷,分离效果好,定量准确稳定。
1 仪器与材料
1.1 仪器液相色谱/质谱联用仪(三重串联四级杆质谱)LC/MS QQQ(配四元泵、自动进样器、柱温箱、ESI电喷雾离子源,美国Agilent Technologies 1290 InfinityⅡ/6460 Triple Quad LC/MS);电子天平(赛多利斯科学仪器上海有限公司MSE125P-1CE-DU)
1.2 材料罂粟壳药材来源于甘肃农垦医药药材有限责任公司,批号:20170304、20171210、20 171213;对照品来源见表1。
三氯甲烷、浓氨、醋酸、正丁醇、乙酸铵、磷酸二氢钾、磷酸氢二钠、甲酸为分析纯;甲醇、乙腈为色谱纯,水为超纯水。过滤用0.22μm滤膜。
2 方法与结果
2.1 色谱条件色谱柱:以十八烷基硅烷键合硅胶为填充剂(规格为2.1×100mm,5μm),以乙腈-0.1%甲酸水(7:3)为流动相,流速0.4mL/min,柱温40℃,进样量5μL。
2.2 质谱条件ESI离子源干燥气温度300℃,干燥气流速11 L/min,毛细管电压4000V,正扫描模式,MRM多反应监测,待测化合物监测母离子、子离子、碎裂电压、碰撞能等质谱参数见表2。
2.3 标准曲线的制备分别精密称取吗啡、可待因、那可汀、蒂巴因、罂粟碱对照品,用甲醇稀释至约250μg/mL的溶液,吗啡、可待因用乙腈稀释成系列浓度25、50、100、150、250ng/mL,罂粟碱、那可汀、蒂巴因用乙腈稀释成系列浓度5、10、20、30、50ng/mL,分别精密吸取标准曲线溶液各5μL,注入液-质联用仪分析,记录色谱质谱图,以响应值为纵坐标,罂粟壳生物碱浓度(ng/mL)为横坐标,分别线性回归分析。
2.4 供试品溶液的制备取样品粉末(过三号筛)约1g,精密称定,置250mL具塞锥形瓶中,精密加入50mL含5%醋酸的20%甲醇溶液,密塞,称定重量,超声处理(功率250W,频率20kHz)30min,取出,放冷,再称定重量,用含5%醋酸的20%甲醇溶液,补足减失重量,摇匀,静置,吸取上清液滤过,即得。
2.5 测定法分别精密吸取供试品溶液和标准曲线溶液各5μL,注入液相色谱-质谱联用仪,记录色谱质谱图。
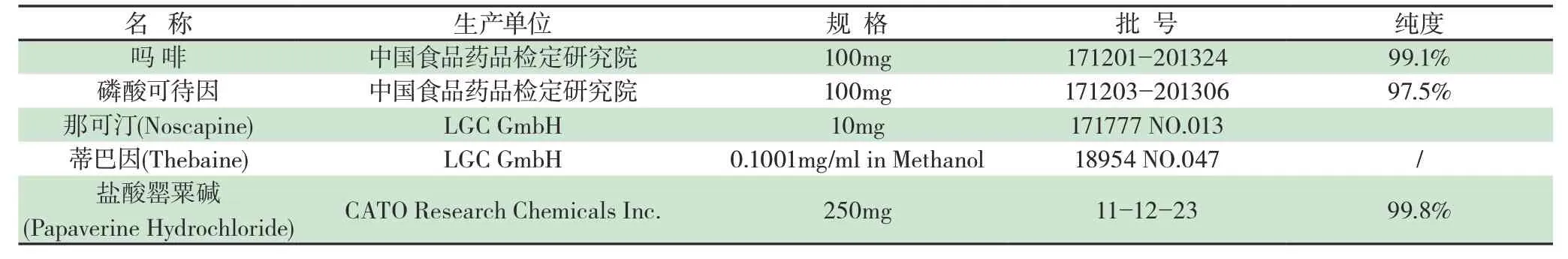
表1 对照品来源

表2 各种化合物质谱条件
2.6 结果计算公式:X (%)=(ρ×V×n×100×10-9/m)%
X——试样中待测组分的含量,单位为%;
ρ——从标准曲线得到的试样中待测组分的含量,单位为ng/mL;
V——试样的体积,单位为mL;
m——试样的质量,单位为g;
n——样品稀释倍数。
2.7 线性关系考察如图5所示,按2.3制备好标准曲线,进行线性回归,吗啡、可待因、罂粟碱、蒂巴因、那可汀回归方程分别为y=4.607561x+136.665908、y=27.198157x+476.925291、y=508.526038x+286.535574、y=81.784540x+181.455263、y=241.356278x+717.213296,相关系数r分别为0.99597、0.99686、0.99998、0.99905、0.99762,各生物碱在线性范围内的浓度与峰面积均呈良好线性关系,吗啡、可待因的线性范围是25~250ng/mL,罂粟碱、蒂巴因、那可汀的线性范围是5~50ng/mL。
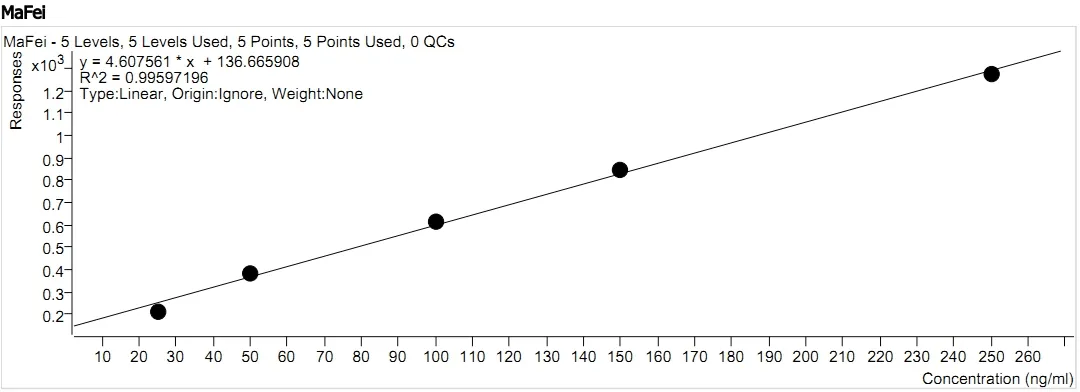
图1 吗啡标准曲线及线性方程

图2 可待因标准曲线及线性方程

图3 罂粟碱的标准曲线和线性方程
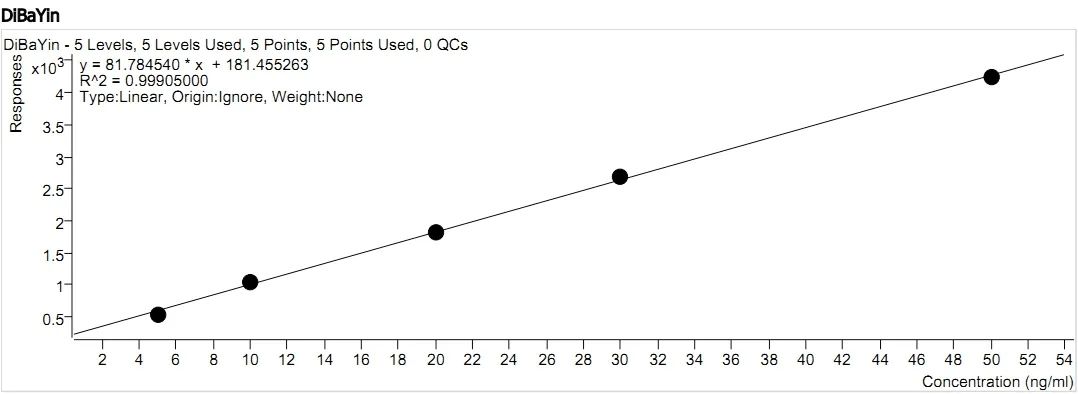
图4 蒂巴因的标准曲线和线性方程
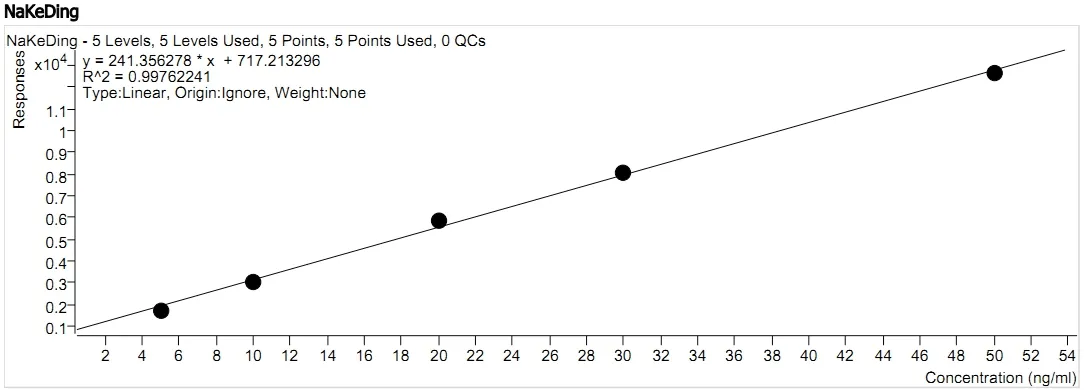
图5 那可汀的标准曲线和线性方程
2.8 定量限将已知低浓度的罂粟壳生物碱对照品溶液,按方法测定,以信噪比(S/N)约为10:1时相应浓度确定为定量限(LOQ),吗啡、可待因、罂粟碱、蒂巴因、那可汀的定量限分别为2.4×10-2mg/kg、2.4×10-2mg/kg、6×10-4mg/kg、6×10-4mg/kg、6×10-4mg/kg。
2.9 精密度将混合标准品连续进样6次,记录其峰面积,精密度用峰面积变化的相对标准偏差(RSD)表示,吗啡、可待因、罂粟碱、蒂巴因和那可汀的峰面积的RSD值分别为1.32%、4.63%、1.11%、0.56%、1.77%,RSD均小于5%,表明精密度良好。
2.10 稳定性试验在室温条件下,将同一份样品溶液每隔几小时(0h、2 h、4 h、8 h、12 h)测定一次,计算吗啡、可待因、罂粟碱、蒂巴因、那可汀峰面积变化的相对标准偏差(RSD),分别为3.38%、1.38%、4.44%、4.99%、3.60%。说明样品在12h内稳定性好。
2.11 回收率试验分别精密称取相同质量的样品10份,一份不加标准品,作为测定本底值的样品。另外9份分别加入高、中、低三种浓度的标准品制备供试液,每种浓度重复3次,按方法测定,计算其样品加标回收率,吗啡的平均加标回收率是78.28%~103.62%,可待因的平均加标回收率是80.86%~108.80%,罂粟碱的平均加标回收率是84.21%~101.61%,蒂巴因的平均加标回收率是74.63%~96.40%,那可汀的平均加标回收率是76.26%~91.08%。表明本法准确度良好。
2.12 样品测定取3批罂粟壳样品(批号:20170304、20171210、20171213),按本法测定,结果含量见表3。
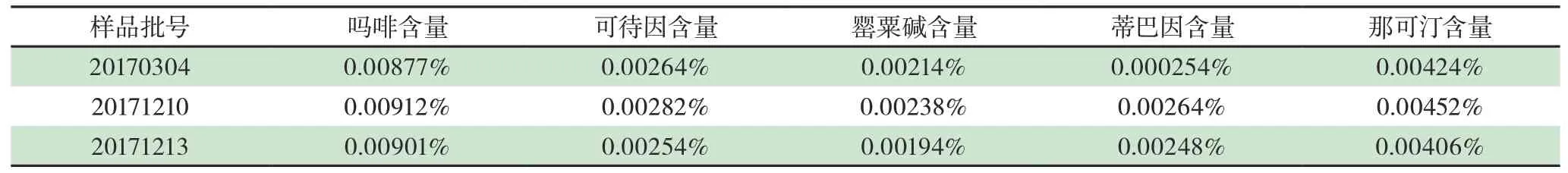
表3 样品测定结果
3 试验条件的选择
3.1 提取溶剂的选择试验分别用水、甲醇、含5%醋酸的20%甲醇、70%乙醇、水饱和的正丁醇(浓氨调pH值至11)、三氯甲烷(用浓氨调pH值至9)做为溶剂提取罂粟壳生物碱,实验表明各种溶剂提取5种生物碱的效果各有优劣,综合考虑5种生物碱的提取效果以及响应值、检出限和线性范围,最后确定用含5%醋酸的20%甲醇作为提取溶剂。
3.2 流动相的选择试验尝试多种流动相:甲醇-0.02mol/L乙酸铵溶液、乙腈-0.02mol/L磷酸二氢钾+0.02mol/L磷酸氢二钠溶液、以乙腈-0.1%甲酸水(7:3)为流动相、乙腈-0.01mol/L乙酸铵溶液(pH3.0、3.5、3.8、4.0、4.3),试验表明以乙腈-0.1%甲酸水(7:3)为流动相洗脱分离效果最好,如图6~10所示。
3.3 柱温的选择分别在30℃、35℃、40℃柱温下进行试验,结果在柱温40℃时峰分离度和峰型最好,如图6~10所示。

图6 吗啡质谱图
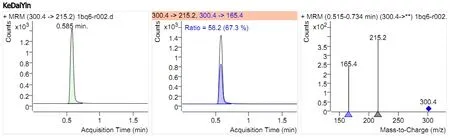
图7 可待因质谱图

图8 罂粟碱质谱图

图9 蒂巴因质谱图
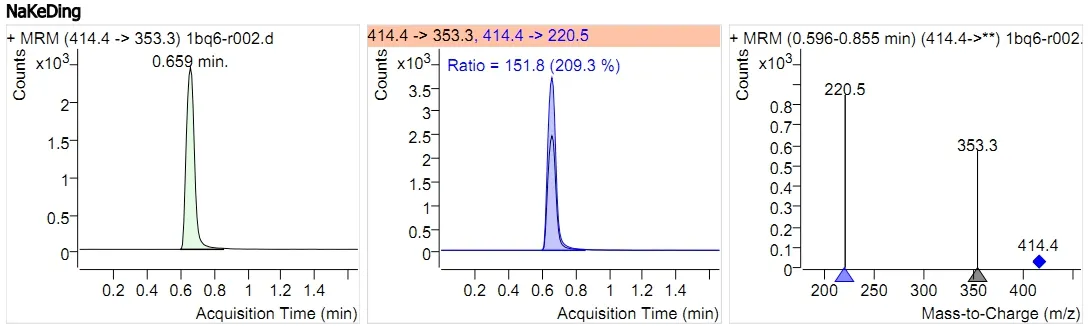
图10 那可汀质谱图
4 讨论
药典中吗啡的含量限度为0.06%~0.40%[1],由于罂粟壳是管制药品,想获得多批次的药材比较困难,需要进一步对不同产地、不同批次的罂粟壳药材进行多次试验,方可确定含量限度范围。
