贝伐珠单抗联合参芪扶正注射液在晚期非鳞非小细胞肺癌老年患者中应用对生存质量的影响
2019-12-23张悦华王志伟
侯 欣,张悦华,杨 芳,王志伟
(河南大学第一附属医院 肿瘤科,河南 开封 475001)
大多非鳞非小细胞肺癌的老年患者就诊时病情大多已发展至中晚期,失去手术机会,只能通过药物治疗延长生存期,改善生活质量。临床数据显示,长期化疗、放疗或靶向治疗易导致免疫功能降低,诱发多种病变,缩短生存期[1]。本文就贝伐珠单抗联合参芪扶正注射液治疗晚期非鳞非小细胞肺癌的临床效果,现报告如下。
资料与方法
一、临床资料 选择河南大学第一附属医院2014年2月-2019年2月收治的非鳞非小细胞肺癌患者152例,按治疗方法的不同分为对照组和观察组,各76例。观察组患者男33例,女43例,年龄67~74岁,平均年龄(70.5±3.3) 岁;对照组患者男36例,女40例,年龄65~76岁,平均年龄(71.0±4.3)岁。所有患者性别、年龄均无统计学差异(P>0.05)。纳入标准:a.所有患者均符合《中国常见恶性肿瘤诊治规范》中非鳞非小细胞肺癌诊断标准[2],且经CT、病理学等检查明确诊断,分期标准符合第7版美国癌症联合委员会(AJCC)癌症分期标准[3],TNM分期Ⅳ期;b.预计生存期>3个月;c.初次治疗,无放疗、化疗等治疗史;d.无法接受手术治疗;e.无EGFR、ALK ROS1等阳性驱动基因突变;f.均经患者及家属同意自愿参与本次研究,签署知情同意书。排除标准:a.肿瘤无转移,有心、脑、肝、肾等脏器严重器质性病变者;b.存在感染、凝血功能异常和严重免疫系统疾病者;c.中药制剂过敏史者;d.存在放化疗禁忌症者;e.肿瘤侵犯大血管,或有咯血等出血表现或者出血倾向者。
二、治疗方法 所有患者均予以培美曲塞联合卡铂化疗方案,培美曲塞500mg/m2d1+卡铂AUC=5d2/q21d静脉滴注;对照组在此基础上予以贝伐珠单抗7.5mg/kg,加入250m L 0.9%NaCl溶液中,静滴,第1周期第1d 90m in完成滴注,第2周期第1d 60min完成滴注,每21d应用1次,共2个周期;观察组在对照组基础上联合应用参芪扶正注射液250m L/次,1次/d,静滴,周期同对照组,化疗前3d开始用药,用药42d(2个周期)。
三、疗效分析 生存质量采用肺癌患者生存质量测定量表(FACT-L)[4]进行评估,包括生理状态、社会/家庭状况、情感状况、功能状况和肺癌附加关注等5个维度,共36项,总分144分,分数与生存质量呈正比例相关;肿瘤标志物包括糖类抗原-125(CA125)、细胞角蛋白19片段抗原(CYFRA21-1) 和癌胚抗原(CEA),采用电化学发光免疫分析法进行检测;免疫功能包括CD3+,CD4+和CD4+/CD8+,采用流式细胞仪进行检测;以上指标均于治疗前和治疗2个周期后分别进行检测,肿瘤标志物和免疫功能于空腹状态下取静脉血5m L进行离心分离后检测。
四、统计学方法 采用SPSS21.0对所有数据进行统计学处理,计量资料结果用(¯±s),采用t检验,以P<0.05为差异有统计学意义。
结 果
一、2组FACT-L评分和免疫功能比较
治疗后观察组FACT-L评分高于对照组,CD3+,CD4+和CD4+/CD8+水平高于对照组,差异均具有统计学意义(P<0.05),见表1。
二、2组肿瘤标志物比较
观察组治疗后CA125,CYFRA21-1和CEA水平低于对照组,差异具有统计学意义(P<0.05),见表2。
讨 论
对于非鳞非小细胞肺癌的老年患者,双药联合化疗虽可使病情得到控制,总的客观缓解率约30%~40%,但血液毒性和长期神经毒性严重影响患者的生活质量。近年来,我院应用贝伐珠单抗联合化疗治疗非鳞非小细胞肺癌,客观缓解率可提高至54%。我国多名临床研究人员证实联合治疗晚期非鳞非小细胞肺癌,能够明显延长生存期,耐受性较好,但免疫功能仍然受到明显影响[5]。祖国医学认为,非小细胞肺癌发病属正虚邪盛,其根本原因是正气虚衰,因此,扶正固本是治疗该病的重要原则[6]。因此本研究采用参芪扶正注射液联合治疗非鳞非小细胞肺癌。
表1 2组FACT-L评分和免疫功能比较 (±s)
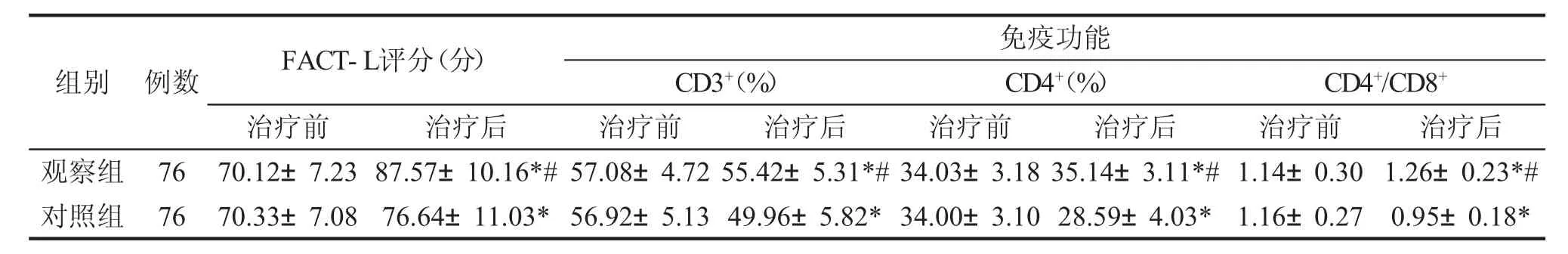
表1 2组FACT-L评分和免疫功能比较 (±s)
免疫功能CD3+(%)CD4+(%)CD4+/CD8+治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组 76 70.12±7.23 87.57±10.16*#57.08±4.72 55.42±5.31*#34.03±3.18 35.14±3.11*#1.14±0.30 1.26±0.23*#组别 例数FACT-L评分(分)对照组7670.33±7.08 76.64±11.03*56.92±5.13 49.96±5.82*34.00±3.10 28.59±4.03* 1.16±0.27 0.95±0.18*
表2 2组肿瘤标志物比较 (±s)

表2 2组肿瘤标志物比较 (±s)
注:表1、2中,与本组治疗前比较,*P<0.05;与对照组治疗后比较,#P<0.05。
CA125(U/mL)治疗前观察组 76 83.17±8.02组别 例数 治疗后50.55±7.15*#对照组76 82.86±7.9267.18±8.24*治疗前12.01±4.20 11.89±3.93 CYFRA21-1(pg/L)治疗后8.41±1.96*#10.07±2.13*CEA(ng/mL)治疗前 治疗后24.16±7.07 12.29±4.13*#23.88±6.54 17.08±5.36*
FACT-L评分量表在目前临床中专门用于肺癌患者生存质量的测定,从上述结果中可见,观察组治疗后FACT-L评分高于对照组,表明中西医联合治疗可有效提高患者的生存质量,延长有效生存期;CD3+和CD4+在抗肿瘤免疫反应中具有重要调控作用,CD4+/CD8+比值可维持免疫功能平衡,从上述结果中可见,观察组CD3+,CD4+和CD4+/CD8+水平高于对照组,表明中西医联合治疗可有效避免免疫指标下降,改善免疫功能;CEA和CA125在非鳞非小细胞肺癌患者中大多呈高表达状态,CYFRA21-1是临床诊断非鳞非小细胞肺癌的重要依据,从上述结果可见,观察组治疗后CA125,CYFRA21-1和CEA水平低于对照组,表明中西医联合治疗可有效降低肿瘤标志物水平,加强治疗疗效。诸多报道显示,中医药在治疗肿瘤病变中,可有效缓解毒副作用,可多靶点、多环节、多途径的发挥抗肿瘤作用[6]。参芪扶正注射液以益气扶正、活血化瘀、消症散结、固本补虚为主要功效;该药与抗肿瘤药物联合应用,可有效缓解化疗和靶向药的毒副作用,降低肿瘤负荷,增强治疗疗效,减轻免疫系统抑制性,延长生存期,改善生活质量。因此,参芪扶正注射液在非鳞非小细胞肺癌治疗中具有辅助支持作用,但可能并不是控制肿瘤发展的决定因素。
综上所述,贝伐珠单抗联合参芪扶正注射液治疗晚期非鳞非小细胞肺癌老年患者可有效降低肿瘤标志物水平,改善免疫功能,提高生存质量,推荐临床推广应用。
