土三七致肝小静脉闭塞综合征2例并文献复习
2019-12-16邵素娥马于林李佳玲
李 亚 邵素娥 马于林 陈 炎 李佳玲 万 静
肝小静脉闭塞综合征(hepatic veno-occlusive disease,HVOD)是由某种原因引起的肝小叶中央静脉和肝小静脉支内皮肿胀、纤维化,导致管腔狭窄甚至闭塞而产生的肝内窦后性门脉高压症[1]。临床表现多为:高胆红素血症、肝区疼痛、腹水、体重增加。HVOD最初于1920年由Willmot和Robertson报道因服用含有吡咯烷类生物碱(PA)Senecio tea引起[2]。目前国内外报道多例服用土三七诱发的HVOD。本文对2例服用土三七后导致的HVOD患者报道如下。
1 病例资料
1.1病例1 患者,男,68岁。因“腹胀40余天,乏力纳差1月”于2017年6月30日入院。患者诉40余天前进食土三七后出现腹胀、皮肤黄染,1月前出现乏力、纳差,并间断出现恶心、呕吐。既往有肠切除手术史。入院体检:全身皮肤巩膜重度黄染,腹膨隆,上腹部可见明显静脉曲张,腹部移动性浊音阳性。
入院后辅助检查:血、尿、粪便常规+潜血均正常。肝功能:谷丙转氨酶(ALT)63 U/L,谷草转氨酶(AST)96 U/L,总胆红素(TBIL)215.9μmol/L,直接胆红素(DBIL)91.0μmol/L,间接胆红素(IDBIL)124.9μmol/L,葡萄糖(GLU)9.28 mmol/L,白蛋白(ALB)29.7 g/L,γ谷氨酰转肽酶(GGT)218 U/L,碱性磷酸酶(ALP)199 U/L;肾功能正常、血脂、心肌酶、脑钠肽、甲功均正常。凝血象:凝血酶原时间15.6秒,凝血酶原时间活动度53%,活化部分凝血活酶时间39.1秒。感染指标:乙肝全套、丙肝、HIV、梅毒均阴性。肿瘤标志物:甲胎蛋白正常。血氨(AMON):60.3μmol/L。腹水常规及生化检查提示为漏出液,腹水肿瘤标志物(CEA、AFP、CA199)阴性。腹水细菌培养阴性。腹部CT:肝脏轮廓规整,肝叶比例正常,肝实质内不均匀密度减低;增强:肝静脉纤细,其分支显示不清。门静脉血管成像:门静脉主干及分支未见明显异常,肝静脉纤细,肝静脉分支未见明显显示,胃底静脉曲张(见图1)。腹部大血管B超正常。
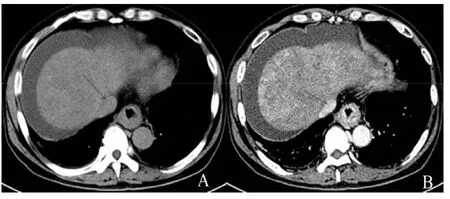
图1 患者1腹部CT结果
诊断考虑:HVOD,病程中予护肝退黄、改善循环、抗凝、减轻水钠潴留、抗感染(头孢哌酮钠他唑巴坦)、输注白蛋白、口服乳果糖等对症支持治疗。治疗后复查肝功能:谷丙转氨酶(ALT)24 U/L,谷草转氨酶(AST)51 U/L,总胆红素(TBIL)94.8μmol/L,直接胆红素(DBIL)47.2μmol/L,间接胆红素(IDBIL)47.6 μmol/L,白 蛋 白 (ALB)37.0 g/L,谷 氨 酰 转 肽 酶(GGT)103 U/L,碱性磷酸酶(ALP)108 U/L;凝血象:凝血酶原时间12.8秒,凝血酶原时间活动度81%,活化部分凝血活酶时间37.5秒。病情稳定好转后出院。
1.2病例2 患者,男,83岁。因“腹痛半月余”于2018年9月17日入院。患者半月前无明显诱因出现全腹部疼痛,为胀痛,剑突下疼痛明显,症状于进食后加重,伴有反酸嗳气,恶心不适,偶有心慌。既往服用土三七病史,2013年肠息肉切除术史。入院查体:剑突下轻度压痛。
入院后辅助检查:血常规:血小板66×10-9/L;尿、粪便常规+潜血均正常。肝功能:谷丙转氨酶(ALT)88 U/L,谷草转氨酶(AST)162 U/L,总胆红素(TBIL)131.4μmol/L,直接胆红素(DBIL)65.6μmol/L,间接胆红素(IDBIL)65.8μmol/L,白蛋白(ALB)24.5 g/L,γ谷氨酰转肽酶(GGT)194 U/L,碱性磷酸酶(ALP)216 U/L。肾功能、血脂、心肌酶、脑钠肽均正常。凝血象:凝血酶原时间19.1秒,凝血酶原时间活动度42%,活化部分凝血活酶时间33.5秒。感染指标:乙肝全套、丙肝、HIV、梅毒均阴性。肿瘤标志物:甲胎蛋白正常。自身免疫性肝病、肝纤维化检查正常。腹水常规及生化检查提示为漏出液,腹水肿瘤标志物(CEA、AFP、CA199)阴性。腹水细菌培养、抗酸染色、脱落细胞液基检查均正常。胃镜:十二指肠球炎;糜烂性胃炎III级;糜烂性胃炎。腹部CT示:腹盆腔积液;所及双侧胸腔少许积液(见图2)。腹部血管检查:肝左、中、右静脉内径分别约为0.3 cm、0.3 cm、0.6 cm。下腔静脉仅见肝段、内径约2.0 cm,余被气体遮盖显示不清。CDFI:上述可显示血管内彩色血流信号连续,未见明显充盈缺损。门静脉血管成像:门静脉主干直径约8 mm,门静脉主干及分支血管显示清晰,未见明显狭窄、扩张及充盈缺损影。肝静脉主干及分支、肝段部分下腔静脉显示欠清(见图2)。所及腹腔积液,左侧胸腔少量积液。
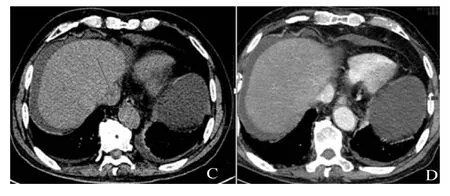
图2 患者2腹部CT结果
诊断考虑:HVOD。入院后予护肝退黄、改善循环、减轻水钠潴留、抗感染(头孢米诺)、护胃、输注白蛋白等对症支持治疗。治疗后复查:血小板98×10-9/L;肝功能:谷丙转氨酶(ALT)37 U/L,谷草转氨酶(AST)40 U/L,AST/ALT:1.09,总胆红素(TBIL)35.3μmol/L,直接胆红素(DBIL)12.2μmol/L,间接胆红素(IDBIL)23.1μmol/L,白蛋白(ALB)27.7 g/L↓,球蛋白(GLB)39 g/L,γ谷氨酰转肽酶(GGT)60 U/L,碱性磷酸酶(ALP)104 U/L;凝血象:凝血酶原时间15.6秒,凝血酶原时间活动度56%,活化部分凝血活酶时间29.7秒。病情好转出院。
综上所述,2例患者病例具有以下共同特点:①患者均为老年男性;②均有明确的土三七服用史;③均有较为典型的临床症状和体征[3];④影像学表现均有肝静脉及其分支显示不清。入院后均给予以下治疗:①护肝降酶;②退黄;③改善循环;④抗感染:根据患者的病情选择不同的抗生素;⑤控制腹水。根据病情予补充白蛋白、利尿及腹腔穿刺放液治疗。根据具体病情同时给予其他对症支持治疗。
2 讨论
土三七是广泛使用的草本植物,内含有吡咯烷类生物碱,具有活血化瘀、消肿止痛的功效,常用于外伤、骨折及骨关节疾病的治疗。土三七导致HVOD的机制尚不明确,目前研究报道由于土三七内含有的PA在肝内经过CYP(P450细胞色素)代谢生成有毒的代谢产物,可交联肝细胞DNA造成肝细胞损坏[4]。此外,PA可以减少谷胱甘肽(GSH)在窦内皮细胞中的表达[5]。Maioli M A等报道含有PA的植物可能通过损伤肝细胞的线粒体引起肝脏损伤[6]。PA可通过脂质过氧化损伤[7]及诱导肝细胞凋亡等途径造成肝脏的细胞凋亡[8]。有文献报道,如果PA摄入过多还能导致肺水肿和胸腔积液。
HVOD最初由 Dr.Stillman和 Lawrence报道[9,10],目前主要由服用土三七、猪屎豆等含PA的中草药引起,且服用剂量越大、服用时间越长病情越重。土三七所含有的PA对肝脏的毒性在老鼠实验中也得到了证实[11]。少量文献报道,HVOD是干细胞移植和肝移植的少见并发症[12]。HVOD的临床表现主要为腹胀、肝区疼痛、腹水等,诊断相对较为困难,需结合详细的病史、临床表现及影像学表现仔细鉴别。HVOD的确诊依靠活组织检查作为金标准,但由于此类患者多伴有大量腹水、凝血功能差、血小板减少,肝穿刺活检的风险较大,临床上较少穿刺。HVOD的主要病理变化是肝小静脉闭塞、偏心性狭窄、肝小叶3带(1区)细胞损伤坏死、肝窦纤维化[13]。HVOD的影像学表现具有以下特点:平扫可有腹水,肝大,密度不规则形减低;动脉期表现为血管增粗、扭曲,轻度不均匀强化;门静脉期表现为斑片状、地图状低密度影,肝静脉变细或显示不清,门静脉内无改变,下腔静脉段变窄,内无阻塞及远端扩张,无侧支循环形成。下腔静脉、门静脉周围“晕征”或“轨道征”,胃肠道多无淤血表现[13,14]。
HVOD应该与布-加综合征(Budd-Chiari syndrome,BCS)鉴别:BCS是由肝静脉和其开口以上段下腔静脉阻塞性病变引起的常伴有下腔静脉高压为特点的一种肝后门脉高压症,临床表现可有右上腹痛、迅速出现大量腹腔积液、黄疸、肝大,肝区有触痛,少尿等,腹部血管超声可发现肝静脉后及下腔静脉阻塞,HVOD影像学主要为肝小静脉的闭塞。因此,可通过下腔静脉及肝静脉造影来鉴别BCS和HVOD。
HVOD的治疗目前主要为对症支持治疗,包括限制液体入量、减轻水钠潴留、护肝退黄、维持水电解质平衡、营养支持治疗、透析治疗及TIPS等。药物治疗目前推荐:①去纤苷:能够保护内皮细胞,具有抗炎作用[15];②低剂量的低分子肝素:具有抗凝作用[16];③前列腺素:用于改善循环;④甲泼尼龙:抑制细胞因子产生,不良反应较多,仍需大量临床试验[17]。有学者推荐有条件情况下早期肝移植能够改善患者预后。对于土三七所致的HVOD,尽早诊断、及时对症支持治疗能够防止疾病进展及改善预后。
综上所述,以土三七为代表的含有PA的中草药,在中国民间应用广泛,但对其毒性的认识不够。临床医师应加强对PA所致HVOD疾病的认识,及早诊断和治疗,同时应该加强对该类中草药的宣教,减少该类疾病的发生。
