高硫醇含量天然气净化用MDEA复配溶剂的研究
2019-12-06黎志敏
黎志敏,沈 俊,刘 伟
(1.中国石油化工股份有限公司西北油田分公司,新疆 乌鲁木齐 830001;2.四川大学化学工程学院,四川 成都 610065)
从井站开采出来的天然气均含有酸气 (CO2及H2S)及各种有机硫化合物,有机硫化合物通常以硫醇(R-SH)、硫醚R-S-R、羰基硫(COS)、二硫化碳(CS2)为主,且不同区域以及不同地质年代的气层产出的天然气中酸气及有机硫的组成和含量不尽相同[1]。天然气送入商品管道之前必须进行脱碳、脱硫等净化处理,使得CO2、H2S、总硫含量等指标达到国家标准。国内广泛使用的是以MDEA、MEA、DEA等醇胺溶剂为吸收剂的醇胺工艺,经过多年使用、对比以及研究人员的调整优化,目前占主导地位的是以MDEA为主吸收剂的净化工艺[2]。由于MDEA具有的位阻效应能在一定程度上选择性脱除H2S,因此在宽的CO2/H2S比情况下都能适用[3]。MDEA溶剂的推广使用显著提升了我国天然气净化领域的技术水平,然而,随着各种复杂井站气体的开采,单一的MDEA溶剂显得无法适应,其中最为突出的是对于井站气中高含量甲硫醇(MeSH)、乙硫醇(EtSH)、羰基硫、二硫化碳的脱除效果较差,导致高浓度有机硫存在时净化气总硫含量难以达标,大量的研究及井站运行情况也证实了这一情况[4]。
中国石油化工集团在新疆开展天然气开采及处理业务使用的正是MDEA溶剂净化工艺。该工艺在大部分情况下运行状况良好,但是在轮台县的二号联处理站出现了总硫无法达标的情况,经过对气样的分析发现,原料气中甲硫醇体积分数高达0.0725%,乙硫醇体积分数也达到了0.0083%。从分析结果推测,现有单纯的MDEA溶剂无法有效脱除高含量的甲硫醇及乙硫醇,最终导致无法使净化气总硫含量达到要求;为了保障净化气质量,急需解决高硫醇含量天然气的净化难题。考虑到现有净化装置是针对MDEA溶剂进行设计、建造和运行,因此,最为合理的解决方案是在现有设备基础和工艺条件上实现对甲硫醇和乙硫醇的高效脱除,可采取的方法是对MDEA溶剂进行复配优化,在不改变现有工艺流程和设备的基础上,利用复配溶剂增加对甲硫醇及乙硫醇的脱除能力。
我国幅员辽阔,地质结构复杂,随着不同地域及不同地质年代天然气井站的开采,天然气硫组分出现显著差异。因此,有必要针对不同的组分情况有针对性的开发脱硫剂,以解决单一MDEA溶剂无法适应的情况,实现最为经济环保的天然气净化处理。
1 实验部分
1.1 实验装置
使用自制的耐压等级2.0MPa的不锈钢气液相平衡釜作为评价装置,该装置如图1所示。电磁搅拌仪(巩义予华仪器公司,型号规格为85-1A)转速控制在300~350r/min;电加热控制器(CLION公司,型号规格为HNG1-1/032F-38 10Z)为PID温度控制,驱动可控硅进行电加热升温,温控精度为±0.1℃,最大功率为300W;冷凝回流管在溶剂再生时使用25℃水作为冷却介质;压力变送器(Rseries公司,型号规格为PCM300D)量程范围是-0.1~2.5MPa,测量精度为0.5%FS;温度传感器为PT100型,精度为0.3%℃。气相色谱为GC-7820,使用FPD火焰光度检测器,色谱柱采用北京中科惠分仪器有限公司硫化物分析专用柱,规格为50m*0.53mm*7μm;采用程序升温方式进行分离,初始温度为50℃,终点温度为150℃,程序升温速率为10℃/min。使用六通阀配合定量管进行气体的进样,用N3000色谱数据采集及分析,分析计算方法是气相色谱面积外标法。
1.2 实验材料
所使用的试剂MDEA、二甲基亚砜(DMSO)、环丁砜(SUL)、N-甲基吡咯烷酮(NMP),分析纯,由阿拉丁公司提供;实验气体为混合酸性天然气(甲硫醇、乙硫醇、硫化氢的体积分数分别为0.0751%、0.0089%、3.7500%,简称“酸性气”),由大连大特气体有限公司提供。
1.3 实验过程
将物理溶剂(二甲基亚砜、环丁砜、N-甲基吡咯烷酮)和蒸馏水以及MDEA以质量比进行复配,用移液管移取一定体积的溶液加入平衡釜中。使用聚四氟乙烯密封圈进行平衡阀的密封,用氮气进行气密性实验,确认无泄漏后对系统抽真空,同时开启磁力搅拌。磁力搅拌的目的在于强化传热及气液相的传质,缩短平衡时间。同时开启温度控制及加热器,待系统温度达到设定温度、系统表压达到-0.095MPa后,切换至样品气管路,向平衡釜中通入酸性气,通过压力传感器及二次仪表读取系统压力数据。此时开始计时,并每隔一定时间,通过平衡釜出气阀及色谱六通阀将釜内气体通入气相色谱进行气相样品的分析。
2 结果讨论
2.1 气液相平衡时间的影响
实验中综合考虑了塔式连续吸收及静态平衡吸收的特点,使用静态气液相平衡的方法评价各溶剂对有机硫的脱除率。在静态平衡釜中存在气液接触面积小、平衡时间长的问题,因此,确定硫醇、硫化氢在不同溶剂中的平衡时间是开展实验的重要前提。图2是压力1MPa、气液体积比(标准状态,以下简称气液比)150:1、在m(物理溶剂):m(MEDA):m(水)=3:5:2形成的复配溶剂下、吸收温度40℃时,甲硫醇、乙硫醇在各溶剂中的吸收率变化曲线。

图2 不同硫醇在不同溶剂中的吸收率变化曲线
由图2可看出,所有曲线在20min位置都出现了明显的拐点,即在20min前体系处于较快速率的吸收状态,而20min后吸收速率开始下降,直至在大约150min时吸收接近平衡。该曲线是吸收过程气相液相浓度梯度与吸收速率关系的具体体现,在实际生产中为了使生产装置达到最经济的运行状态,吸收塔都处于偏离气液相平衡的状态,任何运行参数的改变都会导致系统重新建立平衡。由于连续吸收装置这种非稳态平衡不利于基础平衡数据的获取,本研究使用静态平衡方法,并根据图2的结果选取150min作为平衡时间进行其他参数的研究。
2.2 吸收温度的影响
吸收温度是影响硫醇脱除率的重要因素,图3在气液比150:1,m(物理溶剂):m(MEDA):m(水)=3:5:2形成的复配溶剂下,吸收压力1MPa,平衡时间为150min时在不同温度下复配溶剂对甲硫醇、乙硫醇的吸收率曲线。所有的吸收溶剂无论是吸收甲硫醇或乙硫醇时都呈现出随着体系温度的降低吸收率升高的现象,这符合物理溶解的规律,即降低温度有利于增加气体在溶剂中的溶解量,低温甲醇法脱硫工艺即利用了这一原理[5]。但MDEA为基础的净化工艺在实际使用中通常只是使用循环冷却水对吸收液进行降温,当需要使吸收液温度降低至现有操作温度以下时必须使用冷冻系统,这会增加冷冻能耗成本及设备成本。因此,从经济性以及MDEA吸收工艺适应性和设备的兼容性考虑,现有装置的运行温度是考察复配溶剂吸收性能的推荐温度。在复配溶剂的开发过程中尽可能接近现有的系统运行温度。由图3还发现,在全部温度范围以及所有溶剂类型中甲硫醇的吸收率均高于乙硫醇,在相关的研究中也发现了这一现象[6]。
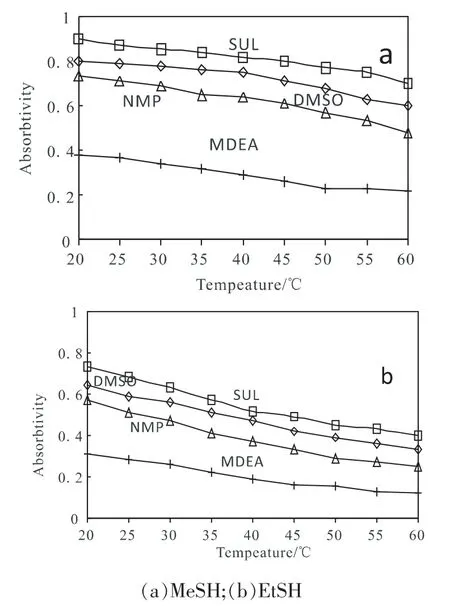
图3 不同温度下复配溶剂对甲硫醇、乙硫醇的吸收率曲线
2.3 气液比的影响
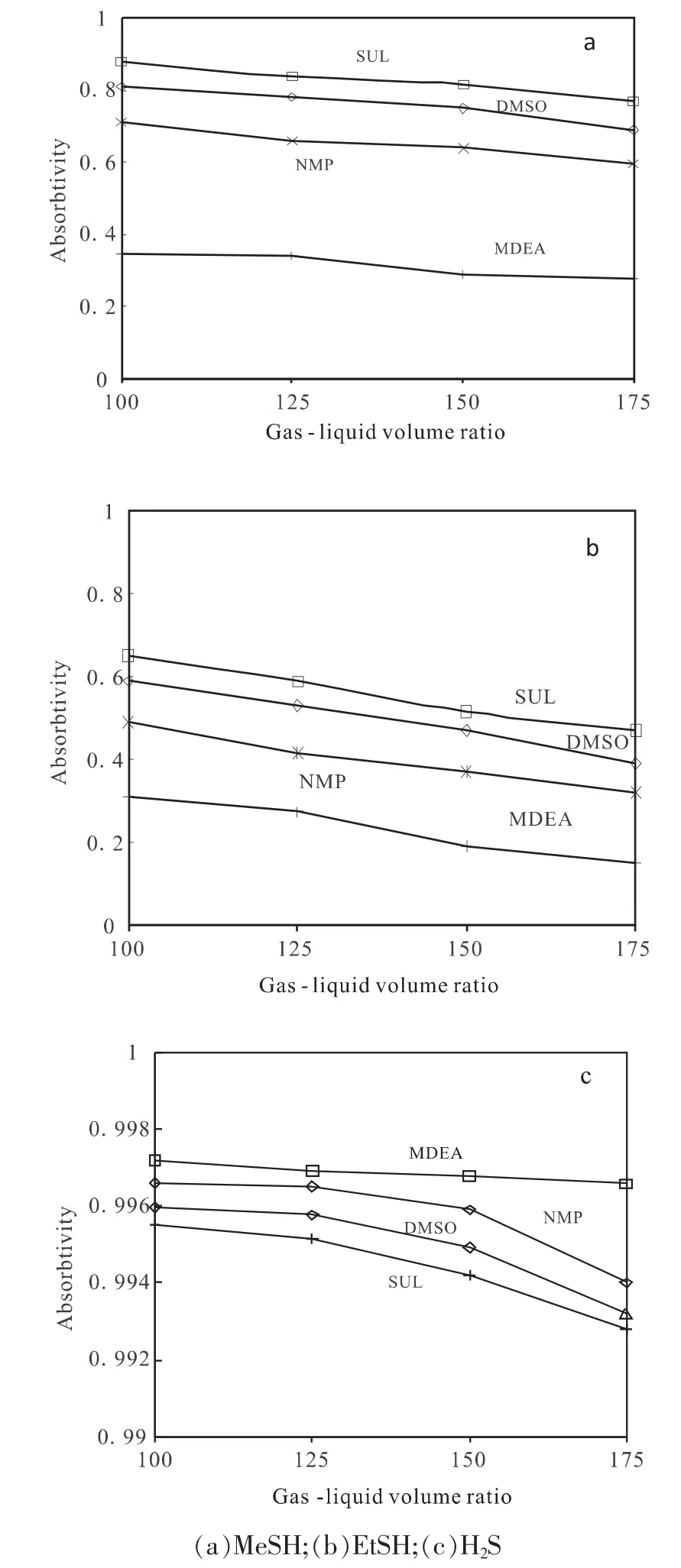
图4 不同气液体积比时的吸收率曲线
气液比是吸收系统中一个重要的参数,直接影响净化气中总硫含量、系统处理能力、系统运行动力消耗、能耗等参数。在生产中总是希望在净化气总硫含量达标的情况下使用最大的气液比以获得最经济的运行成本和实现最大的设备处理能力。但由于各种原因都会使系统偏离设计值,最终导致处理气无法达标或为了达标而降低系统处理能力(即降低气液比),因此,对于一个新开发的吸收溶剂就必须严格考察和选取适宜的气液比。图4的a,b,c是在m(物理溶剂):m(MEDA):m(水)=3:5:2形成的复配溶剂下、吸收压力1MPa、平衡时间为150min时不同气液比情况下复配溶剂对甲硫醇及乙硫醇和硫化氢的脱除率曲线。可见随着气液比的增加,脱除率呈现接近线性的下降趋势,这符合物理溶解的一般规律,同时也表明在该体系中甲硫醇及乙硫醇的吸收以物理溶解为主。除此之外,复配型溶剂对于H2S的脱除都出现了一个下降的拐点,而单纯的MDEA溶剂则未出现该拐点。从现有的研究可知,H2S与MDEA以化学吸收为主[7]。而物理溶剂的加入减少了复配溶剂中MDEA的含量,从而在高气液比时H2S与MEDA的化学吸收达到饱和,继续增加气液比迫使H2S以物理溶解的方式进入溶剂。H2S的物理溶解度远低于其形成的化学吸收量。使用复配溶剂时由于MDEA含量的降低会导致对H2S吸收能力的减弱。因此,在调整和优化复配溶剂组成时必须综合考虑原料气中H2S含量、溶剂中MDEA含量以及系统运行气液比之间的关系,使其达到最佳的组合。就本研究使用的H2S含量以及复配药剂组成而言,比较合适的气液比在150左右,过高的气液比会导致H2S脱除率下降。
2.4 溶剂配比的影响
表1、表2、表3分别列出了二甲基亚砜、环丁砜、N-甲基吡咯烷酮3种物理溶剂与MDEA及水按不同比例(A:m(物理溶剂):m(MEDA):m(水)=3:5:2,B:m(物理溶剂):m(MEDA):m(水)=4:4:2,C:m(物理溶剂):m(MEDA):m(水)=5:3:2)复配后得到的复配溶液对硫醇及硫化氢的吸收率数据。
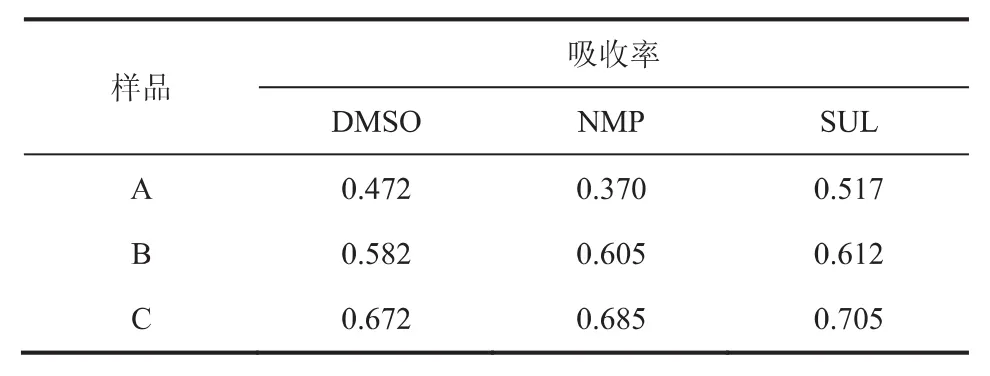
表1 不同配比溶剂对乙硫醇的吸收率
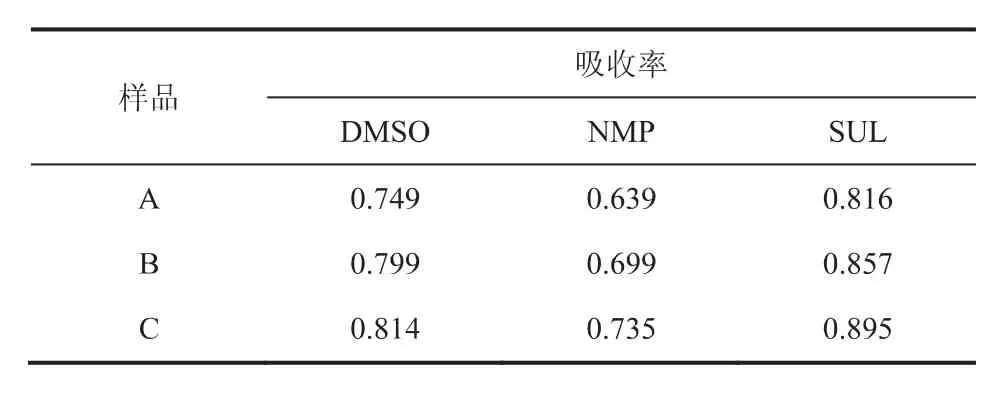
表2 不同配比溶剂对甲硫醇的吸收率
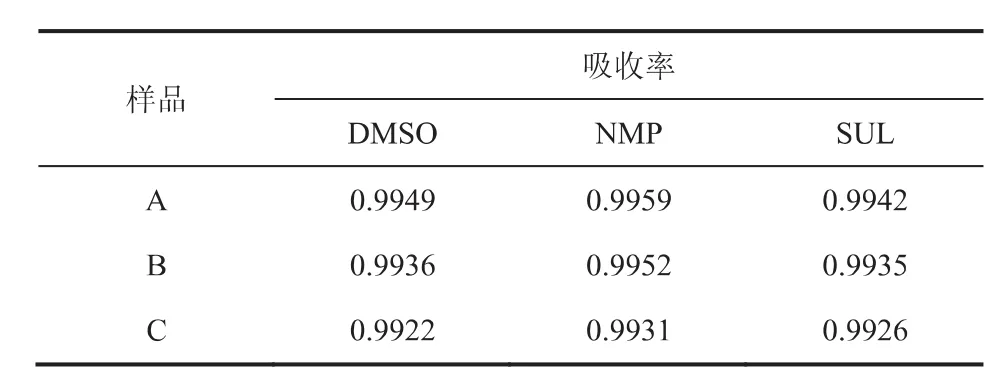
表3 不同配比溶剂对硫化氢的吸收率
由表1~表3数据可见,在全部复配浓度范围内环丁砜复配溶剂显示出对甲硫醇及乙硫醇最好的脱除效果,二甲基亚砜复配溶剂对硫醇的脱除效果次之。可见砜类化合物的添加有效改善了溶剂体系对硫醇的溶解能力。壳牌公司开发的Sulfinol工艺所使用的溶剂即是以环丁砜为辅助成分与胺类药剂混合得到,并在行业中得到了广泛的应用[8]。环丁砜和二甲基亚砜结构中的S=O键具有强的电子诱导效应,使得含有该基团的分子呈现出强极性特征,赋予这类化合物对极性化合物优良的溶解性能。从3个表中也可发现,随着物理溶剂添加量的增加,对硫醇的脱除率也随之增大,但与此同时对H2S脱除率出现下降。尤其是环丁砜样品对H2S的吸收率下降的最为明显,这与图4(c)中的结果一致。因此,物理溶剂一方面增强了对甲硫醇和乙硫醇的溶解吸收,另外一方面由于物理溶剂对H2S的吸收能力小于MDEA,复配溶液中物理溶剂的增加降低了MDEA的含量,导致对H2S吸收能力的下降。因此,针对天然气中不同的H2S及有机硫含量,有必要对复配溶剂进行组分的调整和优化,使其能达到同时脱除H2S和有机硫的目的。
3 结论
使用二甲基亚砜、环丁砜、N-甲基吡咯烷酮这三种强极性非质子溶剂与MDEA及水进行复配得到了复配型MDEA脱硫溶剂,复配溶剂相对单纯的MDEA溶剂显著增强了对甲硫醇和乙硫醇的脱除能力。环丁砜显示出对硫醇最高的脱除效果,N-甲基吡咯烷酮次之。提高强极性非质子溶剂的加入比例有利于增强对甲硫醇和乙硫醇的脱除,但同时也导致对H2S脱除率的下降。
