氨基糖苷类抗生素的拓展应用研究进展
2019-12-03卢明陈代杰
卢明 陈代杰
(1 中国医药工业研究总院,上海 201203;2 上海交通大学药学院,上海 200240)
氨基糖苷类抗生素是较早被发现并应用于临床的一类抗生素。自1944年Waksman从灰色链霉菌中分离得到链霉素,大量氨基糖苷类抗生素相继被发现并应用于细菌性感染的临床治疗[1]。链霉素发现近20年后,研究表明氨基糖苷类抗生素能够抑制提前终止密码子PTC(premature termination codon)的阅读并恢复大肠埃希菌中的全长蛋白质产生[2]。在人体中5%~70%的遗传疾病是由框内无义突变引起的,其在致病基因内引入提前终止密码子(PTC)。因此,在翻译过程中形成了具有病理学意义的无功能或功能缺陷的截短蛋白。PTC抑制可以描述为一种以基因和疾病非依赖性方式治疗突变的治疗策略,该方法旨在抑制蛋白质合成过程中核糖体的保真度,以便可以将共享PTC 3个核苷酸中2个核苷酸的近同源氨基tRNA插入肽链,从而继续翻译,并完整翻译等长度的功能蛋白[3]。因此,对许多遗传性疾病的治疗,抑制PTCs是一种可行的策略。
随着RNA催化潜力的发现,许多氨基糖苷被报道与各种RNA分子相互作用并干扰其功能。其中除了原核蛋白翻译抑制位点16S rRNA,还包括第一组内含子自我剪接酶、RNase P和锤头状核酶[4]。此外,这些抗生素还通过干扰必要的RNA蛋白接触抑制人类免疫缺陷病毒(HIV)的复制[5-6]。在过去的几年里,关于RNA结构和功能的信息迅速增加,对RNA结合抗生素的作用模式有了更详细的了解。本文将从氨基糖苷类抗生素作用机制及应用两方面综述其拓展研究进展。
1 氨基糖苷类抗生素作用机制
1.1 氨基糖苷类抗生素抑制PTCs的作用机制
氨基糖苷类抗生素是一类由单个或多个糖基取代的氨基环醇类化合物。其杀菌作用是通过与原核生物30S核糖体16S rRNA的A1408部位结合,导致蛋白质错译,从而促使细菌细胞的死亡[7]。在真核生物的翻译过程中(图1),同源氨基酰基-tRNA(完全匹配的碱基对)和近同源氨基酰基-tRNA(包含3个碱基对中的2个)都可以与A位点相互作用。同源氨基酰基- tRNA进入A位点后,氨基酸添加到多肽链上后易位到P位点,空出A位点,从而允许下一个密码子信使RNA序列的碱基配对和翻译[8]。当一个核糖体遇到一个终止密码子的信使RNA序列,没有同源氨基酰基-tRNA可以与A位点序列碱基配对。此时,真核释放因子eRF1和eRF3通过二者之间的相互作用促进肽- trna的水解,并通过形成“终止复合物”来释放新形成的多肽。eRF1识别并结合A位点的终止密码子,改变了核糖体肽转移酶的活性。eRF3以依赖于GTP的方式通过eRF1刺激肽的释放[9-10]。
近同源的氨基酰基-tRNA能够与eRFs竞争A位点上的终止密码子的结合[11]。这导致相应的氨基酸被整合到延长的多肽链中,并将这种tRNA-肽链复合物转移到P位点,有效地允许终止密码子的“通读”。每个终止密码子都可以通过使用一组特定的近同源氨基酸进行无义抑制来翻译(图1)。正常情况下,人体内PTCs的通读概率<1%,自然终止密码子的抑制概率<0.1%[12]。无义突变的基础水平过低,无法恢复功能,但功能蛋白的进一步增加可能缓解疾病[13]。多种氨基糖苷类药物在体内外及多种组织和疾病模型中均已表现出无义抑制活性,包括庆大霉素、帕洛霉素、G418、链霉素、利维霉素、妥布霉素等,通过增加PTCs通读恢复少量的功能活性蛋白,在缓解多种遗传疾病方面具有广阔的临床应用前景[14-17]。在氨基糖苷介导的无义抑制过程中,通读效率与诱导A位点结构变化之间的关系尚不完全清楚。目前上述氨基糖苷类抗生素中,G418、庆大霉素和帕洛霉素具有最广泛和最有效的PTC通读活性[19-21]。PTCs通读效能不仅因基因而异,还取决于相关基因中终止密码子的类型和位置以及周围的mRNA序列。一些终止密码子比其他密码子更容易被通读,尽管有一项研究表明终止密码子的类型和庆大霉素治疗效果之间没有相关性,但对于UGA>UAG>UAA的偏爱确已被报道[11,22]。
1.2 氨基糖苷类抗生素抑制RNA酶作用机制
氨基糖苷类抗生素由氨基糖与氨基环醇通过氧桥连接而成,是具有高度柔韧性的多电荷化合物。RNA链上的负电荷与氨基糖苷上的正电荷结合,从而有助于将其容纳在RNA螺旋内部环内的结合袋中或核酶核心中,以进行特定的接触。研究发现,核酶中存在两种类型的氨基糖苷结合位点:第一种由不对称内部环组成,如HIV的RRE和Tar结构域中的解码位点[23-24]。第二种结合位点是核酶催化核心中的金属离子结合口袋[25]。在I型结合位点时,作用方式可能是通过RNA结构的轻微扭曲和干扰功能性底物的结合而实现的,而在II型结合位点中,氨基糖苷类则通过置换必要的二价金属离子起作用。核糖核酸酶P(核糖核酸酶P)是一种依赖Mg2+的核糖核酸内切酶,负责tRNA前体5'端加工。在Mikkelsen等[26]研究发现RNase P在有或无RNase P蛋白时均可被几种氨基糖苷类抑制。
在过去的几十年中,氨基糖苷类抗生素对抗HIV-1的功效已经被广泛证明。HIV-1基因表达是由Tat激活的,Tat是一种病毒编码的转录激活蛋白,它与一种称为TAR的病毒RNA序列相互作用,位于所有病毒mRNA的5-末端。Lapidot等[27]基于HIV-1 RNA结合的肽模型,基于Tat反应元件-配体复合物和氨基糖苷- RNA相互作用的NMR结构,以及HIV-1 Tat结构,设计合成了氨基糖苷-精氨酸偶联物(AACs)和氨基糖苷多精氨酸偶联物(APACs)作为Tat的模拟物,这些化合物通过与HIV-1 Tat反应元件(TAR)RNA和HIV-1 Rev反应元件(RRE)RNA相互作用调节RNA参与病毒生命周期的各个阶段。除了作为Tat拮抗剂,它们还可以通过阻断HIV-1细胞进入的几个步骤来抑制HIV-1的感染性。AACs和APACs通过在cd4结合位点与gp120相互作用,通过在CXCR4 mAb 12G5结合位点与CXCR4相互作用,以及通过与gp41外区瞬时结构相互作用抑制HIV-1细胞的进入(图1)[27-30]。
2 氨基糖苷类抗生素的拓展应用
2.1 氨基糖苷类抗生素抑制PTCs的应用研究
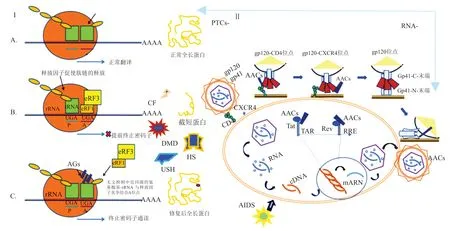
图1 蛋白质翻译和氨基糖类抗生素(AGs)作为无义抑制剂的作用机制Fig.1 The mechanism of protein translation and aminoglycoside antibiotics as nonsense inhibitors
框内无义突变引起的遗传性疾病,主要包括囊性纤维化(CF)[31],Duchenne肌营养不良症(DMD)[32],Usher综合症(USH)[33]以及Hurler综合征(HS),其分别涉及CFTR、dystrophin、PCDH15和IDUA蛋白基因的突变,导致翻译过早终止并最终形成错误截短的非功能性蛋白质(表1)。氨基糖苷类抗生素能够抑制提前终止密码子PTC的阅读并恢复全长蛋白质的翻译。
目前国外主要用于慢性铜绿假单胞菌肺部感染的囊性纤维化患者和非CF性慢性支气管扩张患者的药物有妥布霉素吸入溶液(国外已批准上市)、阿米卡星注射液和庆大霉素注射液。Du等[32]研究发现庆大霉素可以部分恢复DMD和CF[31]小鼠模型中功能蛋白的表达。CFTR蛋白的合成从正常水平的<1%增加至5%,这可能会大大降低CF疾病的严重性[34-35]。2017年2月13日,FDA批准了Vertex医药公司的Symdeko(tezacaftor/ivacaftor+ivacaftor)上市,用于治疗12岁及以上的囊性纤维化患者。这也是Vertex获得FDA批准的第3种针对囊性纤维化根本病因的治疗药物。Duchenne肌营养不良症发病机制主要为编码抗肌萎缩蛋白(dystrophin)基因DMD的无义突变过早地停止了抗肌萎缩蛋白的翻译,由此导致的紊乱使得蛋白质不能全部表达而不再起作用。Translana(Ataluren或PTC-124,CFTR-G542X 无义等位基因抑制剂)是欧洲药品管理局(EMA)于2014年7月31日批准的蛋白表达修复新药,靶向致病基因编码蛋白,通过促进核糖体通读来治疗,允许绕过致病变异体并继续翻译过程以产生功能性蛋白质[36]。

表1 氨基糖苷类抗生素的应用Tab.1 Application of aminoglycoside antibiotics
自1957年Schuknecht[37]首先提出氨基糖苷类抗生素治疗梅尼埃病并逐渐用于临床,其治疗效果也逐渐得到肯定。双盲随机对照的前瞻性研究以及循证医学研究均已经证实了鼓室注射庆大霉素对梅尼埃病患者眩晕控制的有效性[38]。Watson等[39]分析认为鼓室内注射低剂量的庆大霉素治疗对控制梅尼埃病患者的症状有效,同时可以保留听力。Pullens等研究发现,在双盲、安慰剂对照的关于鼓室内庆大霉素对眩晕症状影响的随机临床试验中,与安慰剂组相比,这两项试验均发现庆大霉素组的眩晕症状明显减少。鼓室注射庆大霉素(ITG)可能是根除梅尼埃病患者眩晕最有效的非手术治疗,但也是具有不可忽视的听力损失风险的破坏性治疗方法。ICON推荐对侧前庭功能良好的患者在听力受损时优先使用ITG作为破坏性治疗方法[40]。
Usher综合征是一种常染色体隐性遗传病,患者先天性、双侧性耳聋,伴有视网膜色素变性(RP)引起的视力损害。迄今已经鉴定出14个与user综合征相关的致病基因,包括MYO7A、USH1C、USH1G、CDH23和PCDH15等。29%~50%的USH1型是由MYO7A表达不正常引起的。该基因含有49个外显子,编码2215个氨基酸。c.4513G> T (p.Glu1505Ter)突变会导致蛋白质截短,激活无义介导的衰败(NMD)途径。目前已经开始使用TranslarnaTM(也称为ataluren或PTC124)进行无虹膜的试验(NCT02647359)。同样,贺勒氏症主要由编码α-L-艾杜糖醛缩酶(IDUA)的基因突变导致的,酶替代疗法(ERT)目前正在使用或正在测试中。Aldurazyme是首个用于治疗包括Hurler综合征在内的黏多糖贮积症I(MPS-I)的生物制剂。Wang等[41]利用重组腺病毒相关载体,通过Cas9/sgRNA系统进行基因编辑。
尽管氨基糖苷类抗生素已显示出对PTCs抑制治疗应用具有相当大的潜力,但实际应用过程中仍然存在一些问题。氨基糖苷类(如庆大霉素)不易溶于脂质,全身给药时难以穿透细胞[42]。最值得注意的是,这些药物仍难以穿过血视网膜或血脑屏障,有效全身性输送至视网膜或脑脊液的挑战仍然存在。目前已经在尝试利用脂质体包囊氨基糖苷以实现细胞内递送,以期通过增加药物向细胞质的递送来优化治疗效果[43]。2009年,Nudelman等[19]报道了与庆大霉素相比,新型氨基糖苷类衍生物(NB54)的开发具有更好的通读效率和更低的毒性。该化合物在体外模拟针对具有引起疾病的无义突变的基因的DNA片段进行测试。NB54表现出针对DMD、HS以及CF等病症有关的基因的增强的PTC抑制能力。Nudelman等的研究基于优化药物潜在的抑制功效和毒性,为开发氨基糖苷的新型结构提供了新的方向。而在这个方向上的进一步发展可能为治疗由无义突变引起的许多遗传疾病提供更多的可能性。
2.2 氨基糖苷类抗生素抑制RNA酶的应用研究
除了干扰遗传密码的翻译外,氨基糖苷类抗生素在体外还能抑制几种核酶的活性。第一组内含子自剪接[44]、锤头状核酶自剪接[45]、人类肝炎病毒(HDV)核糖酶[46]、发夹状核酶Mg2+诱导的自我剪接[47]以及RNase P RNA的tRNA加工活性[48]都可被相同的氨基糖苷类抑制,最显著的是新霉素B和妥布霉素。关于锤头状核酶的抑制,研究发现新霉素B至少与一个Mg2+竞争,且抑制效率依赖于pH值,即与抗生素的质子化氨基相关[49]。在没有金属离子的情况下,氨基糖苷类抗生素还可以促进发夹状核酶的裂解反应。发夹状核酶不依赖于二价金属离子进行催化,但Mg2+会极大地促进其折叠。新霉素B可以替代折叠所需的Mg2+,因此可以强烈刺激核酶的活性[47,50]。这与新霉素B对锤头状核酶的作用相反,后者通过从催化核心置换必需的Mg2+而被抗生素抑制。但Chia等[51]也发现HDV的核酶在体内对氨基糖苷不敏感,尽管该核酶在体外是敏感的。
2018年11月,雷鸣团队成功解析了酵母内源RNase P全酶及其与底物pre-tRNA的复合物结构,他们发现RNase P以一种“双锚定(double anchor)”的机制来识别tRNA前体。tRNA的5'端被特异的锚定在催化中心以促使其完成切割反应。底物tRNA的结合诱导了该酶催化中心一个关键残基的巨大的构象变化。结合分子动力学模拟,他们提出了RNase P催化反应的双镁离子模型[52]。新霉素B的结合会干扰二价金属离子进入RNA。综上可知,氨基糖苷与Mg2+离子竞争重要的二价金属离子结合位点。因此,RNase P作为一种重要的酶,是一种潜在的药物靶点,可作为多种氨基糖苷类先导化合物开发新药。
Lapidot等[27]基于HIV-1 RNA结合的肽模型,设计合成了氨基糖苷-精氨酸偶联物(AACs)和氨基糖苷多精氨酸偶联物(APACs)作为Tat的模拟物。这些化合物分子靶向HIV-1 TAR或RRE,在较低的微摩尔范围内以50%的有效浓度抑制HIV-1的病毒复制,最有效的化合物是六精氨酸-新霉素B和九烷基-精氨酸-新霉素偶联物。它们除了充当Tat拮抗剂外,还通过阻止HIV-1细胞进入的几个步骤来抑制HIV-1感染性。用同一种化合物针对病毒生命周期中的几个关键过程不仅可能提高其抗病毒功效,更重要的是,可能降低病毒对该化合物产生耐药性的能力。因此,AACs和APACs可能成为开发多靶点新型HIV-1抑制剂的先导化合物。
目前,人们已经通过不同的方法,包括组合合成、高通量筛选和对现有氨基糖苷类药物的化学修饰等,来解决分离对独特RNA基序特异性增强和对细胞毒性降低的新药物的障碍[53-54]。通过化学修饰增加氨基糖苷的电荷和降低它们的碱度,可以增加它们对目标RNA的亲和力[55]。氨基糖苷的二聚体也可以增强对锤头状核酶的结合亲和力[56]。所有这些新技术最终将有助于更好地理解抗生素与靶标之间的相互作用,从而在已有抗生素的基础上开发出更高效低毒的抗生素。
