T2-FLAIR增强在颅脑转移瘤MRI 中的应用
2019-12-03刘传现黄绍翠黎良山周冰李斌
刘传现,黄绍翠,黎良山,周冰,李斌
(浙江中医药大学附属嘉兴中医院,浙江 嘉兴314001)
MRI 增强检查是颅脑转移瘤的首选检查,其优势明显, 可多方位成像, 为颅脑转移瘤的定位、定量、定性提供了显著帮助。 近年来研究发现[1],这种技术在检查颅底病灶及脑膜转移时易漏诊,对于靠近皮层的小血管易误诊为病灶。 T2-FLAIR 增强在病毒性脑膜炎诊断中的优势明显,而其在颅脑转移瘤中的报道尚少,现探讨其在脑转移瘤患者中是否可作为T1WI 增强检查的补充序列,报道如下。
1 资料与方法
1.1 一般资料 选择本院2016 年8月-2019 年2月诊断为脑转移瘤的患者32 例, 其中男14 例,女18 例,年龄41-80 岁,平均(56.2±10.2)岁,所有病例均行T1WI 增强和T2-FLAIR 增强扫描,其中肺癌脑转移22 例,结肠癌脑转移5 例,胃癌脑转移3例,乳腺癌脑转移2 例;共392 个病灶,5 例为原发病诊断明确后行颅脑排查发现,余病例均有不同程度的脑实质损害的临床表现。
1.2 检查方法 使用美国GE1.5 T 超导型磁共振扫描仪,头颅线圈。 常规序列为轴位DWI、 T1WI、T2WI 和T2-FLAIR、矢状位T2WI 平扫,经肘静脉注入15mL 钆喷酸葡胺 (Gd-DTPA) 后, 均先行T1WI 增强,再行T2-FLAIR 增强检查,所有病例保持一致性。 具体扫描参数为:FOV 22cm×22cm,层厚6mm,层间距1mm,矩阵256×256,激励次数(NEX)1。T1WI:TR 1800ms,TE 20ms;FLAIR:TR 8000ms,TE 145ms。 由2 名副高以上职称的放射科医师按照脑表浅区、颅底区、大脑半球白质区、基底节区分部位对T1WI 增强序列和T2-FLAIR 增强序列扫描图像中所示脑转移病灶的数目、大小、位置及病灶强化形态等进行独立分析。 通过和常规扫描比较,在T1WI 增强与T2-FLAIR 增强扫描中任一个序列上有强化者即为转移病灶。
2 结果
2.1 T2-FLAIR 增强结果 32 例共392 个病灶,单发者3 例,多发者29 例,其中1 例最多56 个病灶;脑实质内病灶T1WI 增强检出率为96.9%(380/392),其中4 个病灶为假阳性,在T2-FLAIR 增强上为脑表面小血管影;漏诊12 个,其中8 个位于颅底, 受血管搏动伪影影响显示不清,4 个病灶位于皮质区,无明显强化,而在T2-FLAIR 增强上较明显强化。 T2-FLAIR 增强检出率为89.8%(352/392),漏诊40 个,其中26 个病灶位于侧脑室旁,长径≤3mm,4 个病灶位于侧脑室壁,长径≤5mm,10个病灶被水肿湮没。 7 处脑膜转移灶中T1WI 增强显示1 处,T2-FLAIR 增强皆显示。
2.2 典型表现 脑转移瘤T2-FLAIR 增强的典型影像学表现详见图1-6。
3 讨论
T1WI 主要反映组织间T1 值的差别,用顺磁性对比剂如钆喷酸葡胺(Gd-DTPA)可缩短T1 值,使T1WI 图像上病灶与正常组织的信号强度对比增加,以达到诊断的目的。 FLAIR 为液体反转恢复序列,抑制脑脊液及脑组织的自由水,突出其长T2 效应,使病变显示更清楚,已成为颅脑病变检查中的常规序列。 另外,T2-FLAIR 反转时间较长,具有一定的T1 效应[2],使其可用于增强检查,其为IR 序列,相对于SE 序列对低剂量Gd-DTPA 更敏感,主要原理是T2-FLAIR 可抑制脑表面微小血管血流慢所引起的高信号,而病变的微小血管可使少量小分子的造影剂漏出,T2-FLAIR 增强后可呈高信号[3],因此,其可显示脑膜、脑表面的小病灶。
脑转移瘤好发于脑皮质区及脑皮髓质交界区,结合临床病史,T1WI 增强检查明显提高了颅脑转移瘤的检出率和诊断准确率,通过多方位、多序列结合扫描,可明确转移瘤的位置、大小、数目及形态,但由于靠近脑表面、脑沟附近的小血管较丰富,血流速度相对较慢,增强后的血管断面在T1WI 上表现为点状高信号,易造成假阳性,而T2-FLAIR 增强可弥补这方面的不足[4-5]。本组4 个病灶在T1WI 增强上表现为脑表面点状强化, 而行T2-FLAIR 增强皆为血管留空信号(图1),避免了误诊。 另外,T1WI 序列难以避免颅底血管内血流搏动引起的伪影[6],对于出现在相应位置的小病灶及脑膜病变易受伪影影响而显示不清,尤其是脑转移瘤的判断[7],T2-FLAIR 可有效避免此类伪影, 本组8 个病灶受血管搏动伪影影响而显示不清, 经T2-FLAIR 增强后病灶显示较清晰(图2)。 本组另有4 个病灶位于皮层下,长径均<5mm,周围无水肿,在T1WI 增强上未显示,在T2-FLAIR 增强上均有强化(图3A-3B),而在T2-FLAIR 增强漏诊的40 个病灶中,以侧脑室旁白质区居多,有26 个病灶,长径均≤3mm,有4 个病灶位于侧脑室壁,T2-FLAIR 增强均无强化,T1WI 增强可见强化,和文献[8-9]报道不一致,可能与病灶本身体积小、强化程度低,与正常脑白质对比度下降有关。 小的转移灶可以轻度水肿,甚至周围无水肿[10-11],但本组仍有10 个病灶在T2-FLAIR 增强上因被肿瘤水肿湮没而未显示,其中9 个病灶长径≤3mm,1 例长径约13mm(图3C-3D), 此病灶在T1WI 增强上表现为较均匀强化;此征象文献报道较少, 作者认为其与病灶小且受邻近较大病灶的水肿影响有关, 或者与肿瘤本身血供特点有关,因此即使为同一患者、同一类型的转移瘤,在T2-FLAIR 增强上也会出现不同的表现。
脑转移瘤的发生、发展具有脑恶性肿瘤特征,往往破坏血脑屏障,周围水肿明显,在T1WI 增强上多表现为环形强化, 病灶中央多无强化, 而在T2-FLAIR 增强序列上有部分病例除表现为环形强化外,其中央可见“云絮状”浅淡强化区(图4),病灶越大此征象越明显, 作者分析其与病灶内部仍有微小血管供血,少量对比剂漏出有关;另外,有部分病灶在T2-FLAIR 增强上表现与T1WI 增强相反,为中央区明显强化,原在T1WI 增强上强化的环却强化不明显(图5),作者认为此征象仍与病灶血管粗细不一、分布不均有关,对比剂漏出的越多强化越不明显。 对于单发的转移瘤, 影像上需要与高级别胶质瘤相鉴别,T2-FLAIR 增强在其中能否有帮助尚待总结。
当出现脑膜转移时,T2-FLAIR 增强存在一定的优势,病变可引起蛛网膜、软脑膜处血管充血、扩张,小分子对比剂(如钆喷酸葡胺)漏出,当造影剂浓度低时,T1WI 增强不强化,而T2-FLAIR 增强则表现出高信号。 另外,T1WI 增强时,小血管强化与脑膜强化难以区别,但T2-FLAIR 增强时小血管无强化,使脑膜强化更清晰。 本组7 例脑膜转移患者在T2-FLAIR 增强上皆有强化(图6),但只有1 例在T1WI 增强上显示明确。

图1 男,45 岁,肺癌脑转移。1A:T1WI 增强示右侧颞叶表面见一点状高信号(白箭);1B:T2-FLAIR 增强后呈低信号,实为血管影。

图2 男,67 岁,肺癌脑转移。 2A:受颅底血管搏动伪影影响,T1WI 增强对部分病灶显示不清;2B:T2-FLAIR 增强则表现出高信号(白箭)。

图3 女,59 岁,乳腺癌脑转移。 3A:T1WI 增强时左侧颞叶皮层下部分小病灶未显示;3B:T2-FLAIR 增强表现出强化(白箭);3C:T1WI 示右侧额叶见结节样强化灶;3D:T2-FLAIR 增强则示病灶湮没在水肿中,无明显强化。

图4 男,70 岁,肺癌脑转移。 4A:T1WI 增强示大脑脚及左侧颞枕叶交界区见环形强化, 其内强化不明显;4B:T2-FLAIR 则示其内见“云絮状”强化影(白箭)。

图5 男,62 岁,肺癌脑转移。5A:T1WI 增强示右侧顶枕叶交界区见环形强化灶;5B:T2-FLAIR 增强则表现为中央结节样强化,周围环强化不明显(白箭)。
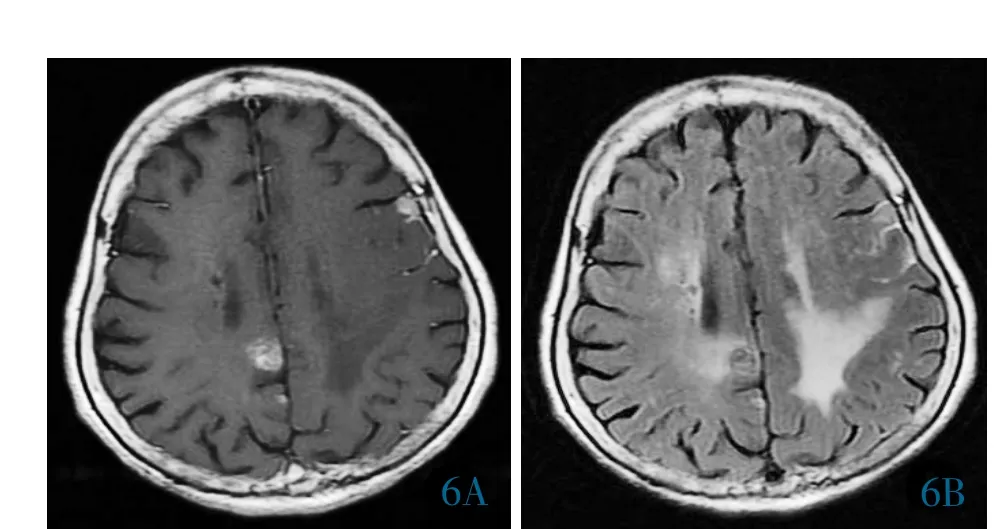
图6 女,76 岁,肺癌脑转移。6A:T1WI 增强可见脑实质内病灶;6B:T2-FLAIR 增强显示左侧额叶部分脑沟内线样强化灶。
综上所述,T2-FLAIR 增强对皮质区小病灶和颅底受血管搏动伪影影响的小病灶的显示有一定优势,可提高检出率。 另外,T2-FLAIR 增强可有效鉴别脑表面小血管与小转移灶,对脑膜转移的检出明显优于T1WI 增强, 而T1WI 增强则对于脑室旁白质区以及侧脑室壁的小转移灶显示明显。 因此,T2-FLAIR 增强可与T1WI 增强互为补充, 以提高颅脑或脑膜转移瘤的检出。
