以寨卡病毒NS3解旋酶为靶点的海洋天然产物库的虚拟筛选与成药性评价
2019-11-29曾志平
曾志平
(厦门大学药学院,福建省药物新靶点研究重点实验室,厦门大学高通量药物筛选平台,福建 厦门 361102)
寨卡病毒是一种虫媒病毒,于1947年从非洲乌干达寨卡森林中的恒河猴体内分离;虽然其致死率较低,但是2015年在巴西爆发寨卡病毒疫情后,发现孕妇如果感染寨卡病毒,可能会导致新生儿发生小头畸形而影响后期的发育(已超过4 000例)[1].除此之外,近期研究表明它还与成人的格利-巴利综合征[2]、急性脊髓炎[3]、眼葡萄膜炎症[4]及脑膜炎[5]等疾病密切相关.更为严重的是,2017年有研究报道寨卡病毒容易发生变异,使其更具有攻击性及毒性,从而在未来可能对人类的公共卫生安全构成较大的隐患[6].此外,由于人类对寨卡病毒基础研究的滞后,迄今为止仍没有相关治疗寨卡病毒病的药物上市,因此,如何开发一类治疗寨卡病毒病的药物已成为紧迫的课题[7].
寨卡病毒是由11 kb的碱基组成的一类RNA病毒,编码3 419个氨基酸,经过水解后可以得到以下一系列蛋白:衣壳蛋白(capsid)、包膜蛋白(envelope)、M蛋白、蛋白水解酶(NS1、NS2A、NS2B和NS3)、解旋酶(NS3)、甲基转移酶(NS4、NS4B和NS5)及聚合酶(NS5)等[7].除M蛋白、NS2A、NS4和NS4B外,其他蛋白都有大量的晶体数据报道.随着NS2B和NS3蛋白水解酶[8-9]、NS3 解旋酶[10]及NS5甲基转移酶[11]等结构的解析,基于晶体结构的药物虚拟筛选研究也相继开展[12-16],但目前还没有得到令人兴奋的结果.2017年有研究发现PrM蛋白上第139位丝氨酸变为天冬酰胺可能会导致病毒攻击性增强[6],值得庆幸的是,除此之外,寨卡病毒并未发生变异,这可能与目前仍没有药物治疗寨卡病毒病相关.NS3解旋酶在寨卡病毒基因组的复制及病毒RNA的合成过程中发挥重要作用,因此成为治疗寨卡病毒病的重要靶点.
NS3解旋酶主要由3个结构域组成.最近,Munawar等[17]利用碎片库及核磁共振(NMR)等手段发现了2个可供药物结合的新口袋(图1和2),引起广泛的关注:口袋A(RNA结合位点)是一个表面结合口袋,它对于NS3解旋酶与NS5聚合酶2个病毒蛋白的相互作用起到非常重要的调控作用,如果有化合物占据此口袋,可能使二者的相互作用消失,从而影响病毒复制复合体的形成,抑制病毒的复制;口袋B(ATP结合位点)位于NS3解旋酶3个结构域的交叉点,是一个柔性但高度保守的变构调节口袋,使NS3解旋酶的结构具有动态性,而小分子在口袋B的结合会使NS3解旋酶稳定在一个特定的构象,从而可能破坏NS3解旋酶的正常功能.因此,口袋A和口袋B成为全新的调控NS3解旋酶生物学活性的重要口袋.
近年来,海洋天然产物由于其化学结构的多样性,越来越受到药物化学家们的青睐[18-20].本研究拟对寨卡病毒的NS3解旋酶蛋白的上述2个口袋开展海洋天然产物的药物虚拟筛选分析,并对结合较好的海洋天然产物进行初步的成药性分析,以期为寻找治疗寨卡病毒病的化合物提供新思路.

(a)口袋A的表面结合部分及重要氨基酸;(b)口袋A的位置示意图.图1 NS3解旋酶的结构生物学模型与口袋A的位置Fig.1 Structure biological model of NS3 helicase and the position of site A
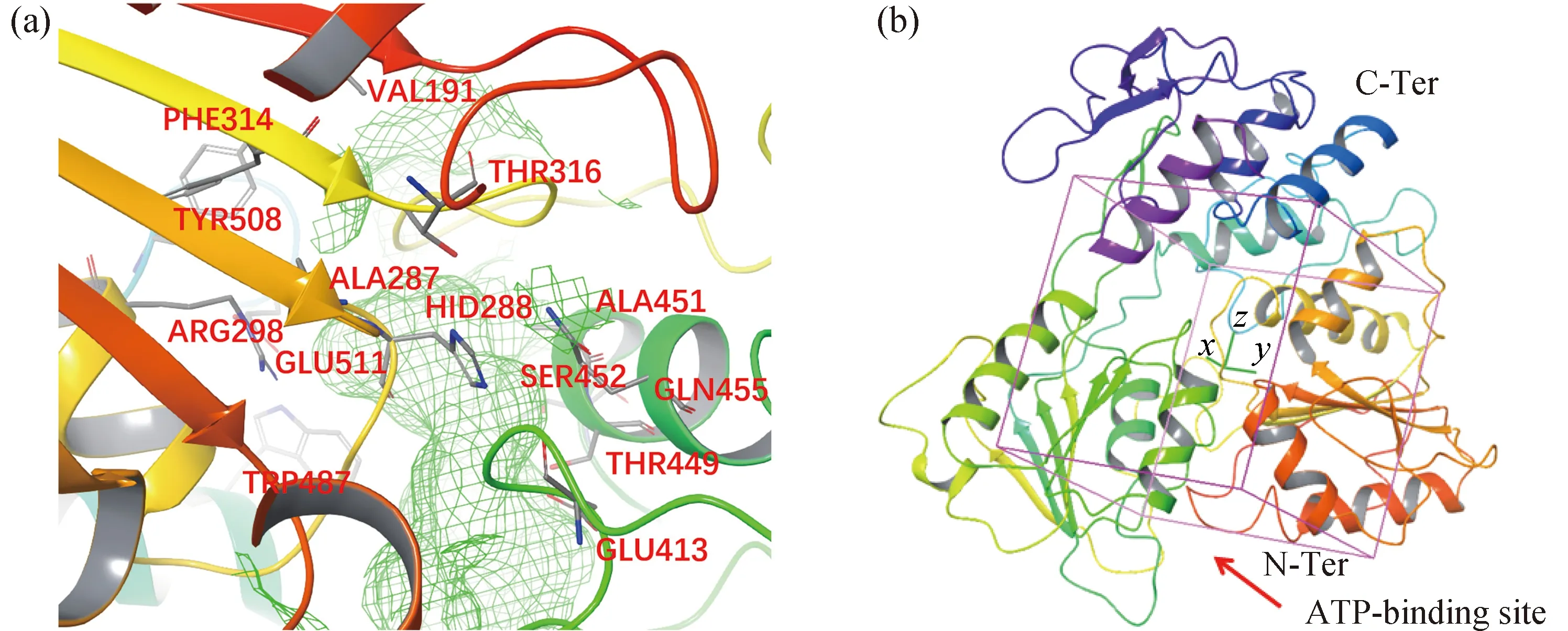
(a)口袋B的结合部位及重要氨基酸;(b)口袋B的位置示意图.图2 NS3解旋酶的结构生物学模型与口袋B的位置Fig.2 Structure biological model of NS3 helicase and the position of site B
1 研究方法
1.1 蛋白准备与结合口袋分析
虽然文献[17]中已报道了NS3解旋酶的2个新颖的结合口袋,但是它们与碎片分子结合的核磁结构尚未上传到蛋白质晶体数据库(PDB)以供下载,因此本研究采用文献[17]中口袋A(图1)和口袋B(图2)附近的关键氨基酸来定义分子对接所需的格点盒子(grid box)位置,并用本课题组自行构建的海洋天然产物库的分子结构在此口袋进行打分评估.根据PDB ID:5Y4Z下载到NS3解旋酶的晶体结构[21],并用薛定谔软件中的蛋白准备模块(protein preparation wizard)进行蛋白的预处理,如除去晶体水分子、加上氢原子,在pH 7.0下用PROPKA程序计算每个氨基酸侧链的质子化状态;然后用薛定谔软件自带的OPLS3e力场及impref脚本进行蛋白复合体的结构优化,除去不合理的碰撞接触等.
1.2 配体准备
5 969个海洋天然产物的初步数据来源为海藻代谢物数据库(Seaweed Metabolite Database,http:∥www.swmd.co.in/)、UNPD(Universal Natural Products Database,http:∥pkuxxj. pku. edu. cn/UNPD)天然产物数据库中的海洋来源小分子及《中华海洋本草:海洋天然产物》[22].将前两个数据库的分子直接导入薛定谔软件套装并进行三维结构转换;而对于《中华海洋本草:海洋天然产物》中的化合物,先用ChemDraw构建二维结构分子,再用Chem3D把二维结构分子转换为三维结构分子,优化的力场参数为MM2.搜集到的分子最后用配体准备模块(LigPrep)优化计算后重新进行化合物编码,依次命名为MNPD000001~MNPD005969.
1.3 口袋A和口袋B结合位点的成药性分析
用薛定谔软件套装的Sitemap 2.3模块对口袋A和口袋B的结合位点进行成药性分析.以siteA-1和siteB-3两个NMR测定的小分子位点作为结合口袋区域,配置参数如下:Site Point个数设置为最少15个;对疏水相互作用采用更加严格的条件算法,同时用经典的格点文件进行计算.
1.4 分子对接分析
基于口袋A的分子对接分析:以口袋A覆盖的10个重要氨基酸(ARG439、VAL440、ILE441、ASN568、ILE571、MET572、MET595、ALA597、CYS600和SER601)为关键氨基酸(图1(a)),首先定义这些氨基酸的坐标中心为分子对接口袋的中心;同时,定义格点盒子形状为立方体,边长为2 nm,用受体格点文件程序(receptor grid generation)产生格点文件.为了提高虚拟筛选的效率,采用薛定谔软件中的HTVS、SP及XP模块进行逐级筛选.HTVS与SP的打分函数(Glidescore)相同,但HTVS算法通过降低寻找配体的构象数来加速对接的过程;而XP算法的打分函数比HTVS与SP的更精细(主要增加了配体与受体的去溶剂化惩罚项等,从而降低了虚拟筛选过程中的假阳性率),并充分考虑了配体与受体口袋的性状补偿等,因此将耗费较长的计算时间.本研究中用HTVS算法对5 969个海洋天然产物的小分子库进行初步筛选;对于得到的排名前200个化合物,进一步用SP算法进行中等精度的筛选;最后对于排名前50个化合物,利用高等精度的XP算法筛选并分析结果.所有筛选方法如无提及均采用默认参数.以文献[17]中的碎片分子9H-嘌呤-2,6-二胺化合物作为参照物进行XP分子对接.
基于口袋B的分子对接分析:以口袋B覆盖的14个重要氨基酸(VAL191、ALA287、HID288、ARG298、PHE314、THR316、GLU413、THR449、ALA451、SER452、GLN455、TRP487、TYR508和GLU511)为关键氨基酸(图2(a));格点盒子的产生及参数设置、分子对接的过程及方法与口袋A的完全一致.以文献[17]中的碎片分子N-(4-氯乙基)肼甲酰胺作为参照物进行XP分子对接.
1.5 海洋天然产物的吸收、分布、代谢、排泄及毒性预测分析
在薛定谔软件中的QikProp v5.7模块下,采用正常模式对化合物进行了基于配体的ADMET预测(ligand-based ADME/Tox prediction).QikProp v5.7主要根据95%已经上市的药物进行模型训练,同时也对30个可能导致假阳性的反应官能团进行了注释,基本满足本研究对成药性的评价要求.对筛选得到的海洋天然产物进行成药性评估,计算的描述符及参数包括:经典的成药五规则评价(# stars、# rotor、donorHB、acceptHB、SASA、PSA、QPlogP油水分配系数o/w、QPlogS及违反五规则数目rule of five)、药物代谢能力评价#metab、药物与血浆蛋白结合能力评价QPlogKhsa、药物人体口服吸收能力评价human oral absorption、药物透皮吸收能力评价QPPCaco以及药物心脏毒性评价QPlogHERG等.
2 结果与分析
2.1 基于口袋A的虚拟筛选结果分析
口袋A位于NS3和NS5蛋白的交界处,是蛋白间相互作用的重要区域,该配体结合位点浅,根据Sitemap 2.3模块的计算结果表明:其成药性计算参数如Sitescore、Dscore及Size均不如口袋B,这可能与口袋A倾向于表面结合同时缺少一个稳固的疏水口袋相关.尽管如此,此位点却在病毒复制复合体的形成过程中具有非常重要的作用,其中ASN569若突变为ALA,则病毒复制复合体无法形成,从而阻止病毒RNA的复制与传染;而此位点在寨卡病毒、登革热病毒等黄病毒属病毒中高度保守.类似地,高度保守的碱性强极性氨基酸ARG439可以通过降低溶剂可极化表面极性来介导NS3解旋酶与其他蛋白的相互作用.此外,形成口袋A边界的非极性氨基酸如ILE571、ILE441和ALA597也在黄病毒属病毒中高度保守[17,23].上述关键氨基酸能与筛选所得的化合物产生重要的相互作用.首先把9H-嘌呤-2,6-二胺化合物进行XP对接(图3(a)),对接的结合能为-19.640 kJ/mol,且发现它能很好地重复文献[17]中的结果,即主要氨基酸的氢键长度均与NMR数据一致,证明了本研究中对接参数设置的准确性;但其分子较小,因此无法与关键氨基酸ARG439、ASN568发生明显的相互作用.最终进入XP对接的化合物结合能范围为-6.280~-41.307 kJ/mol,因此本研究取优于9H-嘌呤-2,6-二胺化合物(即结合能低于-19.640 kJ/mol)且与口袋的关键氨基酸有重要相互作用的分子进行分析;由于篇幅有限,本文中仅展示最具有结构代表性的5个化合物的对接分析结果(图3(b)~(f),附录(http:∥jxmu.xmu.edu.cn/upload/html/20190605.html)表S1).

化合物分子中绿色表示碳原子,蓝色表示氮原子,灰色表示口袋的氨基酸,红色表示氧原子,黄色表示硫原子(下同).图3 海洋天然产物与寨卡病毒NS3解旋酶口袋A的分子对接分析Fig.3 Molecular docking analyses of marine natural products towards the binding site A of NS3 helicase of Zika virus
1) divanchrobactin(MNPD001378):该化合物为棕黄色油状物,由Sandy等[24]于2010年报道,从海洋弧菌Vibriosp.DS40M4中分离得到,目前尚无生物学活性的相关报道.通过XP算法计算,divanchrobactin的结合能为-41.307 kJ/mol,远低于碎片分子9H-嘌呤-2,6-二胺化合物的结合能,原因可能是该分子类似于四肽分子,分子质量和体积较大,官能团丰富,与口袋A表面结合位点的氨基酸存在较多的相互作用(图3(b)),如:2个精氨酸侧链和丝氨酸侧链能与口袋A的CYS600、ASN568、ASN569、THR570、ILE571和MET572等主链酰胺键存在不同程度的相互作用,这与9H-嘌呤-2,6-二胺化合物的相互作用类似但更丰富;此外,其首尾的苯二酚结构能与SER365的侧链羟基形成键长0.293 nm的强氢键,与ALA443的酰胺键形成键长0.271 nm的强氢键,同时苯环区域还能与口袋A中保守的关键疏水氨基酸ILE441等形成疏水相互作用.上述这些使divanchrobactin获得了额外的结合能.
2) bromophenol(MNPD005219):该化合物为白色针状物,属于含溴多酚类化合物,由Fan等[25]于2003年从红藻(Rhodomelaconfervoides)中提取分离得到;它含有5个溴原子,是海洋天然产物的一个典型特征,有降糖及抗肥胖作用[26].该化合物与NS3解旋酶的结合能为-27.888 kJ/mol,其中主要的相互作用为5个酚羟基均与氨基酸主链形成较强的氢键,而5个溴原子对结合能的作用不明显;与divanchrobactin不同的是,其中一个溴原子能与口袋A中关键氨基酸ARG439的胍基有较好的接触,这可能类似于同主族的氟原子有类氢键的相互作用;与此同时,该化合物还与保守氨基酸ALA597和ILE571具有较强的疏水相互作用(图3(c)).
3) 2-hydroxy-1′-methylzeatin(MNPD000865):该化合物为细胞分裂素(cytokinin),来源于绿藻[27-28],其结构较小,与碎片分子9H-嘌呤-2,6-二胺化合物具有相同的母核,因此结合方式也与之非常类似.由于cytokinin的五六元环上缺少氨基,所以它的羟基代替氨基可与CYS600、MET572的羰基形成较强的氢键(键长分别为0.386和0.279 nm),而五六元环上的2个氢键与9H-嘌呤-2,6-二胺化合物的几乎一致;不同的是,cytokinin的烯丙位的羟基与LEU442的羰基形成额外的氢键(键长0.266 nm),这也是cytokinin稍优于9H-嘌呤-2,6-二胺化合物的原因;此外,该化合物还与关键氨基酸ALA597和ILE571形成较强的疏水相互作用(图3(d)).
4) garveatin E(MNPD002933):该化合物于2006年从东北太平洋海洋水螅体Garveiaannulata中分离得到[29],并被证明是吲哚胺2,3-双加氧酶的抑制剂.该化合物是三环结构,且没有氮原子的存在,这大大削弱了类似于9H-嘌呤-2,6-二胺化合物的氢键相互作用,因此其结合能不低(-21.817 kJ/mol);其作用方式主要是利用母核上的羰基与羟基分别与ARG439的胍基、MET572和ASN569的酰胺键形成强氢键;与此同时,三环结构能与CYS600、ALA597、MET595、ILE571和ILE441发生疏水相互作用从而促进garveatin E与口袋A的结合(图3(e)).
5) 2-hydroxy-6-methylaminopurine(MNPD000958):该化合物早期从绿藻和蓝珊瑚中分离得到,属于细胞分裂素的一种[30],与cytokinon及9H-嘌呤-2,6-二胺化合物的结构很类似.目前它已被开发为单磷酸腺苷依赖型蛋白激酶(AMPK)的激动剂[31],用于治疗代谢性疾病.其结合能为-19.720 kJ/mol,与9H-嘌呤-2,6-二胺化合物的相当,且结合方式分析表明两者的氢键相互作用几乎一致,但此化合物的2位羟基由于氢键的饱和性,只能与MET572形成单氢键,而难以与CYS600的酰胺基再形成氢键;还有一处不同的是,此化合物6位氨基的甲基化可能与保守且重要的ALA597存在疏水相互作用而会稍微改善结合能,这是由于它附近无氢键受体能与之相互作用,而杂芳香环可与保守的ILE571发生疏水相互作用从而增强其结合能力(图3(f)).
综上,共剖析了5个海洋天然产物在口袋A的相互作用:由于口袋A的可开放性,它能容纳分子质量较大的小分子;该口袋主要通过氢键网络来维持配体的相互作用,且这些相互作用在5个海洋天然产物中较保守,与文献[17]的结果类似.因此,上述证据暗示这5个化合物可能是寨卡病毒NS3解旋酶的配体.
2.2 基于口袋B的虚拟筛选结果分析
与口袋A完全不同,口袋B的结合位点深埋在蛋白内部且空间狭长,位于NS3解旋酶3个结构域的交界处(图2),但与RNA结合位点又有所差别.该结合位点的氨基酸呈疏水区(THR316、VAL191、ALA287、PHE314、TYR508和TRP487)和亲水区(HID288、GLU413、SER452、THR449和GLN455)两极分布,且在人类所有的黄病毒属病毒(如登革热病毒、昆津病毒、谷脑炎病毒等)中高度保守,暗示口袋B可能是非常重要的影响NS3解旋酶结构与功能的结合口袋.这也与文献[17]中N-(4-氯乙基)肼甲酰胺的分子结构形状相互匹配.基于Sitemap 2.3模块的口袋成药性分析表明:对于优化后的NS3解旋酶,口袋B具有比口袋A更好的成药性.Sitescore作为判断药物结合与否的重要依据,默认计算值大于0.8的即可作为药物结合口袋,而口袋B的计算值为1.14,暗示该处是一个强的药物结合口袋.而作为区分成药性与非成药性的Dscore参数,口袋B的计算值也达到0.96,满足口袋成药性的要求.对该化合物进行重新对接分析(图4(a)),其结合能为-21.227 kJ/mol,稍优于9H-嘌呤-2,6-二胺化合物在口袋A的结合能.其结合方式主要依靠疏水的苯环区域及极性末端与极性氨基酸的相互作用;而进入XP算法对接的化合物结合能范围为-6.816~-35.173 kJ/mol,因此本研究取优于N-(4-氯乙基)肼甲酰胺化合物(即结合能低于-21.227 kJ/mol)且与口袋的关键氨基酸有重要相互作用的结果进行分析;由于篇幅有限,本文中也仅展示最具有结构代表性的5个化合物的对接分析结果(图4(b)~(f)与附录表S2).

图4 海洋天然产物与寨卡病毒NS3解旋酶口袋B的分子对接分析Fig.4 Molecular docking analyses of marine natural products towards the binding site B of NS3 helicase of Zika virus
1) aromatic polyketides(MNPD001827):该化合物为黄色针状物,属于芳香聚酮类化合物,由Du等[32]于2008年从海洋真菌白曲霉(Aspergillusglaucus)中分离得到.该类化合物有一个芳香性的疏水双环,同时以多羟基糖环作为极性基团结尾,这样的结构与N-(4-氯乙基)肼甲酰胺化合物很类似,这也是它用Glide计算所得结合能最低(-35.173 kJ/mol)的原因.相互作用分析表明:芳香环能与口袋B的关键氨基酸如PRO320和HID288等存在疏水相互作用;与此同时,芳香环的羟基能与THR318主链的羰基形成键长0.337 nm的中等强度氢键;而五元糖环能与THR449和SER452等关键氨基酸形成至少4个氢键(图4(b)).正是如此多的相互作用才使该化合物在口袋B上对NS3解旋酶具有很强的结合能力.
2) dimeric terrestrols(MNPD001354):该化合物由Chen等[33]于2008年从海洋真菌青霉菌(Penicilliumterrestre)中分离得到,其分子结构特征也与N-(4-氯乙基)肼甲酰胺化合物类似,但结合能较低(-28.558 kJ/mol).其苯环上的4个羟基均能与口袋B的关键极性氨基酸(如GLU413和SER452等)形成强氢键(键长0.276~0.313 nm),这与aromatic polyketides类似(图4(c));但由于疏水作用对象由萘环变为苯环,该部分的贡献值降低,这也是该化合物的结合能高于aromatic polyketides的根本原因.
3) 6-(methylamino)-3,7-dihydro-2H-purin-2-one(MNPD005912):该化合物可以看作2-hydroxy-6-methylaminopurine的互变异构体.该化合物在口袋B上的结合能却比在口袋A上的要低6.808 kJ/mol,说明该化合物可以选择性地结合到口袋B而非口袋A.虽然此类化合物的分子质量较小,但是相互作用分析表明:它与口袋B的关键且保守极性氨基酸(如THR449和HID288等)可形成5个强氢键(图4(d)),远超过与口袋A的3个氢键;此外,口袋B的芳香性氨基酸TRP487能与其五六元环存在π-π堆积作用,这也是它具有结合位点偏好性的根本原因.
4) 4,5-dibromopyrrole-2-carbonamide(MNPD000526):该化合物早期从海绵Agelasdendromorpha中获得[34],虽具有芳香性基团,但由于溴原子参与形成氢键的能力较弱(图4(e)),其结合能(-25.900 kJ/mol)略高于6-(methylamino)-3,7-dihydro-2H-purin-2-one.
5)R-allantoin(MNPD001587):该化合物从沿海植物紫草(Mertensiamaritima)中分离得到[35],虽然有氢键给体与受体能力,但是分子没有芳香性且分子体积较小,无法达到与极性氨基酸相互作用的程度(图4(f)),这也是它结合能较高的根本原因.
综上,口袋B的虚拟筛选结果表明:此口袋偏好芳香性官能团及氢键给体与受体官能团;同时口袋B属于隧道形结构,因此无法容纳分子体积较大的分子,这也是它与具有表面结合性质的口袋A不同的地方.
2.3 筛选化合物的ADMET预测与分析
对上述10个海洋天然产物进行药物ADMET(即吸收、分配、代谢、排泄和毒性)预测分析,结果表明(表1):大部分化合物满足成药性的各项指标要求,但divanchrobactin (MNPD001378)的成药性偏差,有3条违反成药五原则.其属于拟四肽,氢键给体与受体偏多,且在代谢过程中极有可能发生代谢反应,口服吸收利用率低,虽然它能很好地与口袋A结合,但是从成药性来看反而不是最佳的化合物.而与口袋B结合最好的化合物aromatic polyketides(MNPD001827)有人类果蝇相关基因(hERG)编码的K+通道阻断的风险,可能具有一定的心脏毒性.R-allantoin(MNPD001587)的QPPCaco值低于25,暗示该化合物经过肠道吸收不好.而另外2个化合物4,5-dibromopyrrole-2-carbonamide(MNPD000526)与MNPD004936的肠道吸收指标都很好(QPPCaco值大于500),这也与它们对应有较高的人体口服吸收度(80.260%和89.293%)一致.
3 结 论
本研究针对寨卡病毒NS3 解旋酶的2个新颖结合位点,运用分子对接技术对包含5 969个海洋天然产物的自建库开展虚拟筛选,并根据打分函数及结构多样性的原则,挑选了10个化合物进行对接口袋的详细分析,结果发现这些化合物的结合方式与报道的碎片分子一致,但结合能力却有大幅度提升,暗示它们可以更好地靶向NS3解旋酶,从而成为潜在治疗寨卡病毒病的海洋天然产物;且初步的成药性评估表明除divanchrobactin(MNPD001378)外,本文中所述的海洋天然产物都满足成药性要求,为后期这些化合物进行实验测试提供了理论支撑.
致谢:薛定谔公司提供了薛定谔软件套装,海洋天然产物库由刘诗婷、杨灿原、鞠芮及王鑫构建提供,在此一并感谢.
