不同吻合技术应用于低位直肠癌手术的疗效及安全性
2019-11-14丁博文权红光
丁博文 权红光 王 隽
直肠癌是一种常见恶性肿瘤,目前其发生率及死亡率均不断上升[1]。在我国,直肠癌的发病率逐年升高,其中中下段直肠癌发生占直肠癌的85%,称为低位直肠癌[2]。手术治疗是低位直肠癌的主要方法[3]。传统手术方法为Miles手术[4],随着手术技巧的不断完善及手术器械的不断改进,DST双吻合技术及支撑吻合技术已逐渐应用于低位直肠癌中[5],但目前2种技术应用于低位结肠癌手术的研究较少。因此,本文回顾性分析了2种吻合方式应用于低位结肠癌手术的疗效及安全性,现报告如下。
1 资料与方法
1.1 一般资料
选择我院2011年1月至2015年12月收治的79例低位结肠癌患者,所有患者均要求行保肛手术,其中男性49例,女性30例,年龄范围为45~72岁,平均年龄为(59.2±5.8)岁;病程范围为1~7年,平均病程为(4.2±1.0)年;体重范围为47.8~87.3 kg,平均体重为(64.3±5.9)kg;术前病理分型:乳头状腺癌共16例,管状腺癌51例,黏液腺癌6例,印戒细胞癌6例。根据随机数字表法,将所有患者分为观察组及对照组,2组患者的性别、年龄、病程、体重、病理分型等资料对比,差异无统计学意义(P>0.05),见表1。本研究所有患者知情同意,且经医院伦理委员会批准同意。
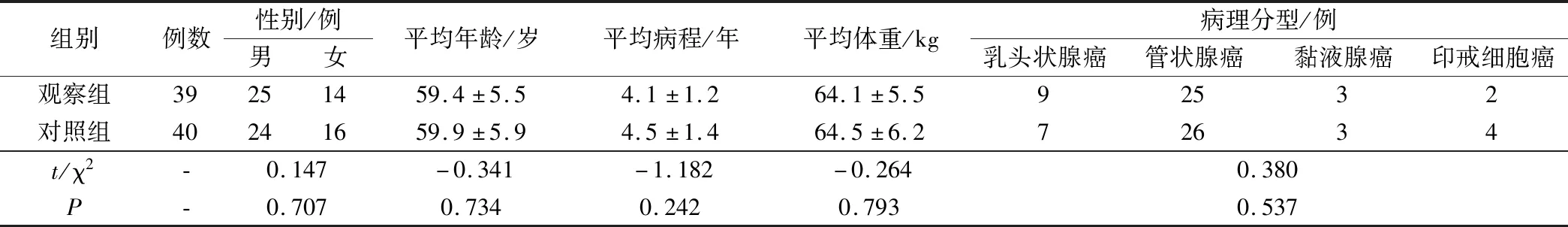
表1 2组患者的一般资料对比
1.2 方法
观察组患者给予支撑吻合技术,先将肿瘤及直肠肛管进行游离,在距离肿瘤下缘2~4 cm处用直角钳,并采用2%碘伏棉球经肛管进行消毒、冲洗,之后在直角钳的下缘将近侧肠管切断,在游离拖下近侧的结肠内8 cm处,置入支撑吻合管,采用双7号线结扎1次,再用单7号线进行缝扎固定。待充分扩肛后,在骶前置入2根引流管。在远侧肛管及直肠残端0.5~1.0 cm处,采用7号线连续荷包缝合1周,再经肛将近侧结肠及支撑吻合管经盆腔肛管拖出,之后将荷包线收紧、打结;外固定支撑吻合管,术后10 d左右,将外固定线拆除,肛门支撑吻合管脱落。术后14 d,对吻合口情况进行检查。
对照组患者采用DST双吻合技术,线将乙结肠游离至盆底并超越尾尖,在肿瘤下2~4 cm处,用肠道弧形切割闭合器将直肠闭合,在近侧切断直肠,将肿瘤段的直乙结肠进行切除,在近端结肠给予荷包缝合,置入肠道管状吻合器。待充分扩肛后,经患者肛门置入一管状吻合器,使其头端将直肠闭合段顶住,将吻合器杆身尾端螺栓逆时针旋转,使锥形导头从直肠盲段的钉合部中央的后方刺出后套入抵钉座内,将吻合器杆身尾端螺栓进行顺时针旋转,将直肠断端与结肠进行靠拢,当杆身红色标记进入绿色区时,表明完成对合。之后打开保险,握紧手柄,用力进行击发,听到咔嚓声时,表明结肠直肠吻合完成;之后将吻合器退出,经肛门注气,对吻合口的严密性进行检查,若漏气则立即加强缝合。
2组术后均给予静脉抗感染、禁饮禁食,止血、营养支持等治疗,术后14 d观察患者的吻合口情况。
1.3 观察指标
(1)根据《结肠癌诊疗规范》中的相关标准[6],对比2组患者的治疗效果,经治疗后患者临床症状、伤口愈合及肿块消失为显效;治疗后患者临床症状及体征均改善为好转;治疗后患者临床症状或体征无改善甚至加重为无效;(2)对比2组患者的肿瘤情况(肿瘤下缘跟底部距肛缘的长度、肿瘤下界距断端的最短距离)、住院时间及住院费用;(3)对比2组患者治疗期间的不良反应及术后3年的局部复发率。
1.4 统计学方法
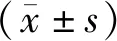
2 结果
2.1 2组患者的治疗效果对比
观察组的总有效率为97.4%,对照组为70.0%,观察组总有效率明显高于对照组(χ2=10.872,P=0.001),见表2。

表2 2组患者的治疗效果对比/例
2.2 对比2组患者的肿瘤情况、住院时间及住院费用
2组的肿瘤下缘跟底部距肛缘的长度及住院时间对比,差异无统计学意义;观察组的肿瘤下界距断端的最短距离明显长于对照组,住院费用明显少于对照组,见表3。

表3 对比2组患者的肿瘤情况、住院时间及住院费用
2.3 2组患者术后3年的局部复发率及治疗期间并发症对比
观察组的并发症发生率为0.0%,对照组预防性造瘘3例、吻合口瘘3例,并发症总发生率为15.0%(6/40),观察组明显低于对照组(χ2=6.331,P=0.026)。观察组术后3年无局部复发,复发率明显低于对照组的12.5%(5/40),差异有统计学意义(χ2=0.023,P=0.048)。
3 讨论
低位直肠癌是一种常见的恶性肿瘤,多是因不良的生活习惯造成的[7-8]。直肠癌发生率位于癌症的第2位,且在直肠癌中,约有60%患者为低位结肠癌[9]。目前,有越来越多的患者存在低位结肠癌[10]。目前,随着结肠癌治疗技术的不断进步及人们对生活质量要求的提高,低位结肠癌手术已逐渐改为在彻底切除肿瘤的前提下,尽量将肛门的排便、控制功能进行保留[11]。在低位结肠癌的治疗中,即可使用DST双吻合技术,又可使用支撑吻合技术,目前,二者在低位结肠癌的治疗中研究较少,因此本文分析了二者用于低位直肠癌患者的疗效及安全性。
本文结果表明,观察组的总有效率明显高于对照组,表明支撑吻合技术用于低位结肠癌的疗效优于DST双吻合技术,主要是由于支撑吻合技术可对DST技术残端进行有效补救,当吻合器不能将远端肠管闭合时,可改为经肛行荷包缝合远端肠管残端,在吻合过程中充分利用支撑管[12];观察组的肿瘤下界距断端的最短距离明显长于对照组,主要是由于应用支撑吻合技术时,可在直视下缝合肛门。此外,支撑吻合技术的缝合线距离肠管断端为0.2~0.3 cm,对远端肠管的游离长度较DST吻合器短,其肿瘤下界距断端的最短距离较对照组长。观察组的住院费用明显少于对照组,主要是由于支撑吻合技术的材料成本低于10元,价格低廉,材料费用较DST双吻合器低1万元,从而降低了住院的费用[13]。观察组的并发症发生率明显低于对照组,主要是由于支撑吻合法可扩张、挤压吻合口周围组织,减少盆腔空腔,有利于肉芽的填充。此外,支撑肠管的内镜为3 cm时,有利于肠内容物的充分引流,从而避免了由于引流不畅导致的吻合口漏[14];同时支撑吻合技术在出现吻合口漏时,有利于引流及吻合口漏的愈合;而对远端直肠进行处理时,DST吻合器需消耗0.7 cm的远端肠管,且在患者存在肌肉强度大、肥胖、残端距离齿状线低于1 cm或盆腔太窄时,需反复性吻合操作,其会加重局部损伤,从而增加了吻合口漏的发生率,同时对于严重的肿瘤梗阻,不能对患者行清洁灌肠时,会有粪便在近端的肠腔残存,而使用支撑吻合技术时,在保肛的基础上,可以降低预防性造口瘘的发生[15]。观察组术后3年局部复发率明显低于对照组,主要是由于支撑吻合技术的手术适应范围较大,可彻底切除肿瘤,从而降低低位结肠癌术后3年的肿瘤复发情况。
综上所述,与DST双吻合技术相比,支撑吻合技术可提高低位直肠癌手术的疗效,降低患者并发症的发生率及术后3年肿瘤的局部复发率。本研究病例资料较少,有待进一步扩大样本量,进行下一步研究。
