不同剂量催产素对剖宫产产妇心排量及子宫张力影响的比较
2019-11-12陶怡怡杜唯佳宋玉洁刘志强徐振东
陶怡怡, 杜唯佳, 李 江, 宋玉洁, 刘志强, 徐振东
(同济大学附属第一妇婴保健院麻醉科,上海 200040)
产后出血是发展中国家产妇死亡的首要原因,而子宫收缩乏力是导致产后出血的最主要因素[1]。催产素是预防和治疗子宫收缩乏力性产后出血的一线药物,但其心血管副反应的发生率较高,剂量使用不当可使循环系统发生剧烈变化,严重者可致产妇心跳骤停[2]。如何选择合适的催产素剂量,达到满意子宫张力同时,对血流动力学影响最小,是产科医师以及麻醉医师共同追求的目标[3]。既往有关催产素对循环影响的研究仅观察产妇心率和血压等的变化,信息有限[4]。随着监测技术的发展,目前可以通过无创的技术全面了解血流动力学的变化特点。本研究拟借助新型无创的功能性血流动力学监测设备(NICOM监测仪),比较剖宫产术中静脉推注不同剂量的催产素对心输出量和其他血流动力学参数的影响,同时评估子宫张力状况。
1 资料与方法
1.1 一般资料
选择2015年10月—2016年5月同济大学附属第一妇婴保健院单胎、足月(孕周>37周)产妇,ASAⅠ~Ⅱ级,年龄20~40岁,未进入产程的择期剖宫产初产妇149例,术前均签署知情同意书。排除标准: 已知胎儿异常,产妇心脏病史,妊娠期高血压,妊娠期糖尿病,多胎妊娠,胎膜早破,巨大儿,前置胎盘,拒绝加入试验研究者。本研究经同济大学附属第一妇婴保健院院伦理委员会批准(KS1538)。
采用双盲的方法,产妇随机分为4组,每组40例。其中3组为实验组: P1、P2和P3,分别在胎儿娩出后静注1、2、3IU催产素,另一组为对照组P0,使用安慰剂即生理盐水。所有推注药物均用生理盐水稀释到2mL。
1.2 麻醉方法
产妇入室后予开放静脉,麻醉前补充晶体液500mL。按照说明书在产妇体表连接NICOM监测仪电极片。产妇取右侧卧位实施腰硬联合麻醉,于L3~4或L2~3穿刺,蛛网膜下腔注入0.5%盐酸罗哌卡因(耐乐品)12mg后,硬膜外置管,剔除穿刺困难者。麻醉后产妇取左倾15°仰卧,调节麻醉平面至T6,平面不足T6者剔除。监护脉搏氧饱和度(SpO2)和心电图。胎儿娩出后立即缓慢静注试验药物。同时500mL平衡液内加入20IU催产素静脉滴注,速度为10IU/h,即4mL/min。
1.3 观察指标
采用NICOM监测仪监测不同时间点的心率(haret rate, HR)、血压(blood pressure, BP)、心指数(cardiac index, CI)、每搏输出指数(stroke volume index, SVI)、总外周血管阻力(total peripheral resistance, TPR),取得基础值、注射试验药物后数值、追加补救药物后数值。产妇入室后,左倾15°静卧5min后测得基础值(TB)。T0为胎儿娩出即刻的测量值,之后每隔1min记录CI、HR、SVI值,分别记为T1……T12,由于监测仪测量无创血压需时较长,每隔1.5min 记录TPR和BP的数值1次,相应的记录时间点为T1.5、T3、T4.5……T12。
手术医生在药物推注完毕后的2、4、6、8、10、12min 分别评估子宫张力。使用数字评定量表评估子宫张力,范围从0到10,其中0分表示“无效果”,7分表示“临床满意的收缩”,10分为“最大强度的子宫收缩”[5]。若于各评估时间点评估子宫张力<7,则予以其他缩宫药物或物理按摩加强宫缩(具体方式由术者决定)。记录各组需给予加强宫缩的补救方式、药物种类及剂量,记录术中失血量。
1.4 统计分析
2 结 果
各组实际纳入分析为: P1(n=36)、P2(n=37)、P3(n=36)、P0(n=40)。部分病例最终未纳入分析的原因包括: 脊椎麻醉失败改为单纯硬膜外麻醉、NICOM电极片术中脱落或遭羊水和血液浸湿、数据采集缺失。
2.1 各组一般情况及基础值的比较
实验组(P1、P2、P3)与对照组(P0)产妇年龄、身高、体质量等一般情况差异无统计学意义(均P>0.05),见表1。实验组(P1、P2、P3)与对照组(P0)产妇的各个血流动力学参数基础值比较,差异无统计学意义(P>0.05),见表2。

表1 一般情况比较

表2 血流动力学参数基础值比较
1mmHg=0.133kPa
2.2 主要指标的比较
实验组(P1组、P2组、P3组)与对照组(P0组)产妇的HR、CI、SVI在分娩后1min内均升高,2min左右达到最高峰;4组HR、CI、SVI比较,差异无统计学意义(P>0.05),见图1A、1B、1C。图1D为产妇TPR变化图。4组TPR在胎儿娩出后1.5min均较基础值降低,P3组TPR在1.5min与P0组比较,差异有统计学意义(P<0.05)。图1E为产妇各时间点血压的变化图,同TPR的变化相似,P2组和P3组自推注实验药物后第1.5min即发生变化,两组SBP、MAP和DBP都呈现一过性下降,然后迅速回升。P2组和P3组SBP、DBP、MAP在1.5min时与P0组比较,差异均有统计学意义(P<0.05)。各组间以上数值在不同时点比较,差异均无统计学意义(P>0.05)。
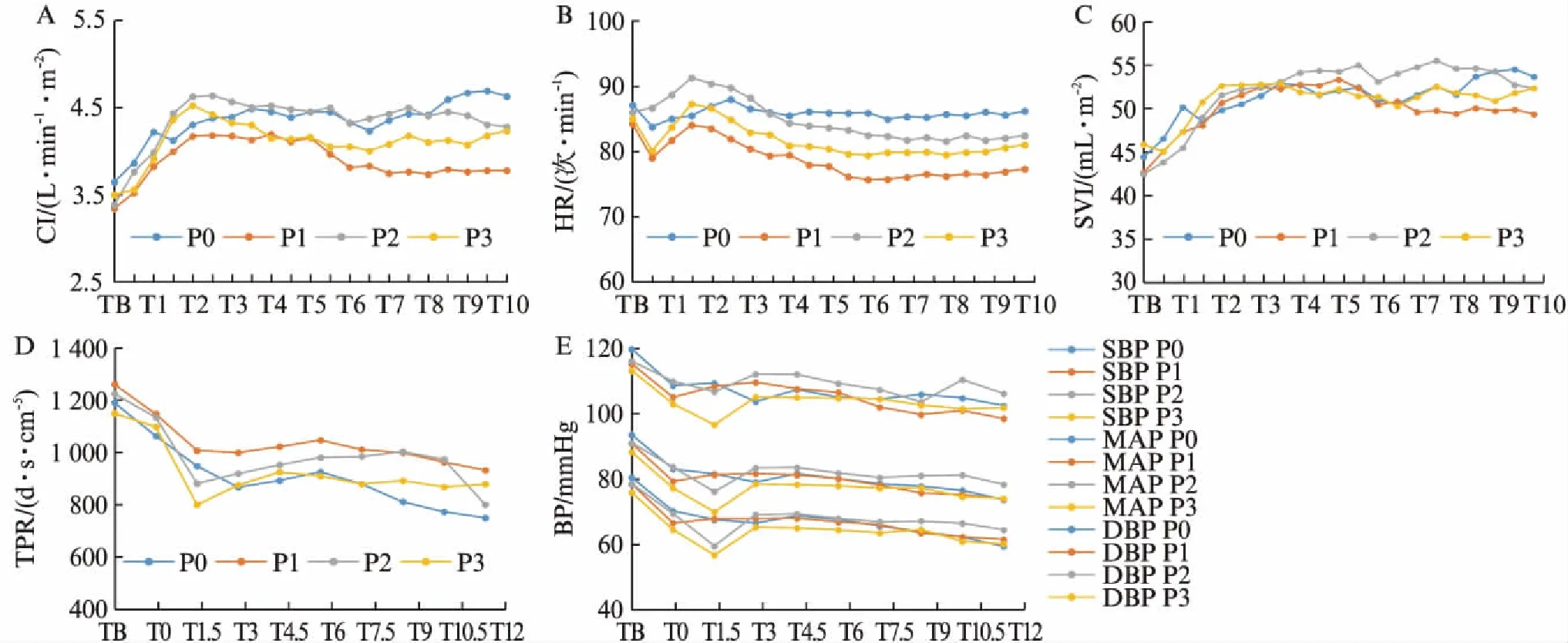
图1 不同时点血流动力学参数变化趋势图Fig.1 Changes in hemodynamics after intervention
2.3 次要指标的比较
次要指标之一的术中出血量,对照组及P1、P2、P3组分别为(243.02±33.77)、(247.22±55.99)、(241.89±55.92)、(222.22±34.73)mL,其中P1、P2与对照组差异无统计学意义(P>0.05),但是P3组术中出血量与对照组相比,差异有统计学意义(P=0.033)。
由表3可见,推注3IU实验药物后的第2、4、6、8min时间点显示,P3组中子宫收缩强度评分明显高于对照组;P2组子宫收缩强度也高于P0组,但差异无统计学意义(P>0.05);而P1组子宫收缩强度评分与对照组相似。由此可见,胎儿娩出后静注3IU催产素才能明显增加子宫收缩强度。

表3 各时间点子宫收缩强度评分比较表
与P0组比较,*P<0.05,**P<0.01
各组在追加使用额外的缩宫药物或缩宫措施情况比较发现,P3组干预措施均少于对照组(表4)。
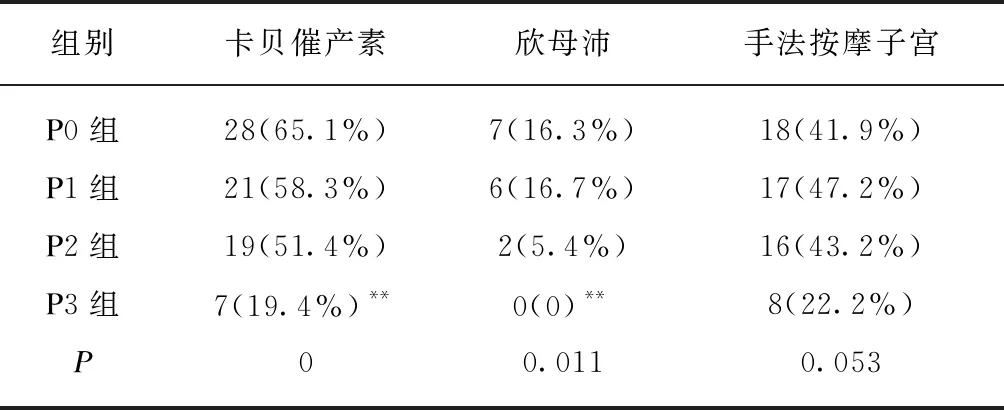
表4 各时间点补救宫缩剂使用
P1、P2、P3均与P0组比较,**P<0.01
3 讨 论
本研究发现,推注1~3IU的催产素不会导致心输出量以及外周血管阻力的显著改变,但是3IU组的子宫张力评分显著高于其他组。
催产素是分娩后促进子宫收缩的一线药物。剖宫产术中催产素的用量还存在很大分歧: 从0.5IU/次到10~30IU/次,有的则主张静脉滴注[6-7]。剂量偏小子宫张力不足,导致产后出血;剂量过大可致剂量相关的低血压、心动过速和心肌缺血[4]。催产素产生低血压机制可能是通过钙依赖的途径刺激血管内皮释放一氧化氮,促进血管舒张,还可促进ANP和BNP的释放,对心肌产生负性肌力的作用[8]。因此如何确定合适的催产素剂量,保持最大的子宫张力同时,产生最小的心血管副作用,是临床一直关注的重要问题。
美国和澳大利亚推荐的剖宫产术中静注催产素5IU。然而Sartain等[4]发现,与静脉滴注5IU相比,静注2IU催产素继以持续滴注,即可产生足够的子宫张力,但5IU的催产素显著升高心率,降低动脉压。本研究借助NICOM比较了1、2和3IU催产素对CI等血流动力学参数的影响,并评估子宫张力。NICOM技术是利用心脏射血时生物电阻抗变化的原理,动态、连续的追踪产妇在分娩过程中CI、SVI以及HR等的变化趋势[9-12]。本研究的结果发现,试验组在胎儿娩出后即刻给予静注1~3IU催产素,CI、SVI和HR均增加,但与对照组比较无显著差异。这主要是因胎儿娩出后,下腔静脉的压迫解除,且每次子宫收缩约有300~500mL血液进入母体循环,回心血量增加,导致SVI和CI增加[9,13]。而TPR在1.5min时均下降,但仅3IU催产素组有显著差异。3组血压同步下降,2IU和3IU催产素组下降显著。推测可能是催产素的直接扩血管作用导致动脉压下降,1~2IU催产素仅导致外周阻力轻度下降,3IU使外周阻力变化显著。这提示临床上对有心血管合并症产妇需谨慎静注3IU以上催产素。
对宫缩强度影响的比较发现,3IU催产素在静注后10min以内,产生的宫缩强度明显强于对照组,而1~2IU影响不显著。3IU组额外追加其他缩宫药物或措施,以及术中出血等显著少于对照组,提示催产素促进子宫收缩是剂量依赖性的,3IU催产素可能是有效剂量。目前文献资料和实践都证明: 剖宫产术中静注5IU催产素已经足够,更大剂量只会加剧副作用的发生[14]。有研究指出静注催产素的最低有效剂量(ED90)是0.35IU(95%CI: 0.18~0.52)[15];0.5~3IU的催产素足以在2min内达到足够的子宫张力,大剂量应用并不能获得更明确的子宫张力[14]。
综上所述,剖宫产术中胎儿娩出后缓慢推注3IU催产素,既可以达到满意的子宫张力又对产妇的血流动力学影响较小,有利于加强产后子宫收缩,减少剖宫产术中出血量,减少额外缩宫药物的使用。
