高级别宫颈上皮内瘤变宫颈锥切术后病理升级的多因素分析及临床处理措施
2019-10-30陈超彭珊珊陆洋陈芳芳刘筑玉
陈超 彭珊珊 陆洋 陈芳芳 刘筑玉
[摘要]目的 探讨高级别宫颈上皮内瘤变(CIN)宫颈锥切术后病理升级的多因素及临床处理措施。方法 选取2015年1月~2017年12月我院收治的77例高级别CIN宫颈锥切术患者作为研究对象,上述患者中25例术后病理升级,52例未有术后病理升级,对上述患者的临床资料进行回顾性分析,总结导致术后病理升级的因素及相应的处理措施。结果 术后病理升级患者的年龄45岁以上占比、绝经占比、阴性部位宫颈管占比明显高于未有术后病理升级组,差异有统计学意义(P<0.05);年龄、人乳头瘤病毒(HPV)DNA水平等同术后病理升级成正相关关系;出现病理升级占32.47%,未出现的占67.53%,另外有11例患者接受二次手术治疗。结论 病理升级同患者的年龄、HPV DNA水平、初次宫颈锥切的宽度、绝经状态和阴性部位等因素有密切关联,上述因素中,患者的年龄、绝经状态、HPV DNA水平及阴性部位等属于高危因素。临床中对切缘阳性患者应开展个体化的二次手术治疗。
[关键词]高级别;宫颈上皮内瘤变;宫颈锥切术;病理升级
[中图分类号] R737.33 [文献标识码] A [文章编号] 1674-4721(2019)8(a)-0104-03
[Abstract] Objective To investigate and analyze the multi-factors and clinical management measures of high-grade cervical intraepithelial neoplasia (CIN) after cervical conization. Methods A total of 77 patients with high-level CIN after cervical conizatio after admitted to our hospital from January 2015 to December 2017 were enrolled. Of these, 25 patients had postoperative pathological escalation, and 52 patients had no postoperative pathological escalation. The clinical data were retrospectively analyzed to summarize the factors leading to postoperative pathological escalation and the corresponding treatment measures. Results The age of patients over 45 years old, the proportion of menopause, and the proportion of cervical tube in the negative site were significantly higher than those without postoperative pathological improvement (P<0.05). Age and human papillomavirus (HPV) DNA levels were positively correlated with pathological upgrading after operation. At the same time, pathological changes accounted for 32.47%, and 67.53% did not appear. In addition, 11 patients underwent secondary surgery. Conclusion Pathological escalation are closely related to the patient′s age, levels of HPV DNA, width of primary cervical conization, menopausal status and negative site. Among the above factors, age, menopausal status, HPV DNA levels and negative part and so on are high risk factors. In the clinical practice, patients with positive margins should undergo individualized secondary surgery.
[Key words] High grade; Cervical intraepithelial neoplasia; Cervical conization; Pathological escalation
宮颈上皮瘤变(CIN)是一种同子宫颈癌有密切关联的一组子宫颈癌变,临床中约5%的CIN可发展为浸润癌,因此对高级别CIN,应及时开展积极有效的治疗,以避免疾病进一步发展而影响患者的身体健康及预后。宫颈锥切术包含冷刀锥切术与环形电切术等,为目前临床治疗高级别CIN的首选措施[1]。但临床中部分有高危因素的患者在手术治疗后仍有病灶残留及病理升级的情况,本研究主要分析高级别CIN宫颈锥切术后病理升级的因素和临床处理措施,特抽选部分患者进行比较分析,现报道如下。
1资料与方法
1.1一般资料
选取2015年1月~2017年12月我院收治的77例高级别CIN宫颈锥切术患者作为研究对象,患者年龄28~65岁,平均(48.85±4.68)岁;其中绝经25例,未绝经52例;已婚62例,未婚15例。上述患者的子宫颈活检病理学诊断均确诊为高级别,初次子宫颈锥切和病理学诊断,切缘阳性;再次开展子宫颈锥切和子宫切除手术的患者。纳入标准:经规范系统的肿瘤学专科培训,且经过本院专家组考核后,具备入组资格的患者;经病理检查提示病变累及切缘或刚到达切缘;本研究经医院医学伦理委员会审查批准开展,且所有患者与家属均对本研究知情,且自愿参加。排除标准:意识不清晰、无一定表达能力,不能完整表达自身诉求的患者;精神病史患者。
1.2方法
77例患者二次手术治疗后开展病理检查,同时对年龄、绝经情况等进行分析,所有患者在初次锥切术前均给予第二代杂交捕获法检测,获得高危人乳头癌病毒(HPV)DNA负荷量和初次宫颈锥切宽度、高度,分析切缘阳性部位等;对二次手术方案进行分析,分析实施再次锥切术、子宫全切术及宫颈癌改良根治术的差异性与实施的必要性等。
1.3观察指标
分析研究病理升级相关因素的单因素(是否绝经、年龄、孕次、阳性部位、手术方式、初次锥切高度、HPV DNA、宫颈液基细胞学检查结果和手术出血量)和多因素(年龄、初次锥切宽度、HPV DNA水平)[2]。
1.4统计学方法
采用SPSS 22.0版统计学软件进行数据处理分析,计量资料以均数±标准差(x±s)表示,采用t检验;计数资料以率表示,采用χ2检验,指标间相关性分析采用Pearson线性相关分析,以P<0.05为差异有统计学意义。
2结果
2.1高级别CIN宫颈锥切术后病理升级占比情况
经统计77例高级别CIN宫颈锥切术患者中,25例出现病理升级,其占比为32.47%;未有病理升级52例,其占比为67.53%。
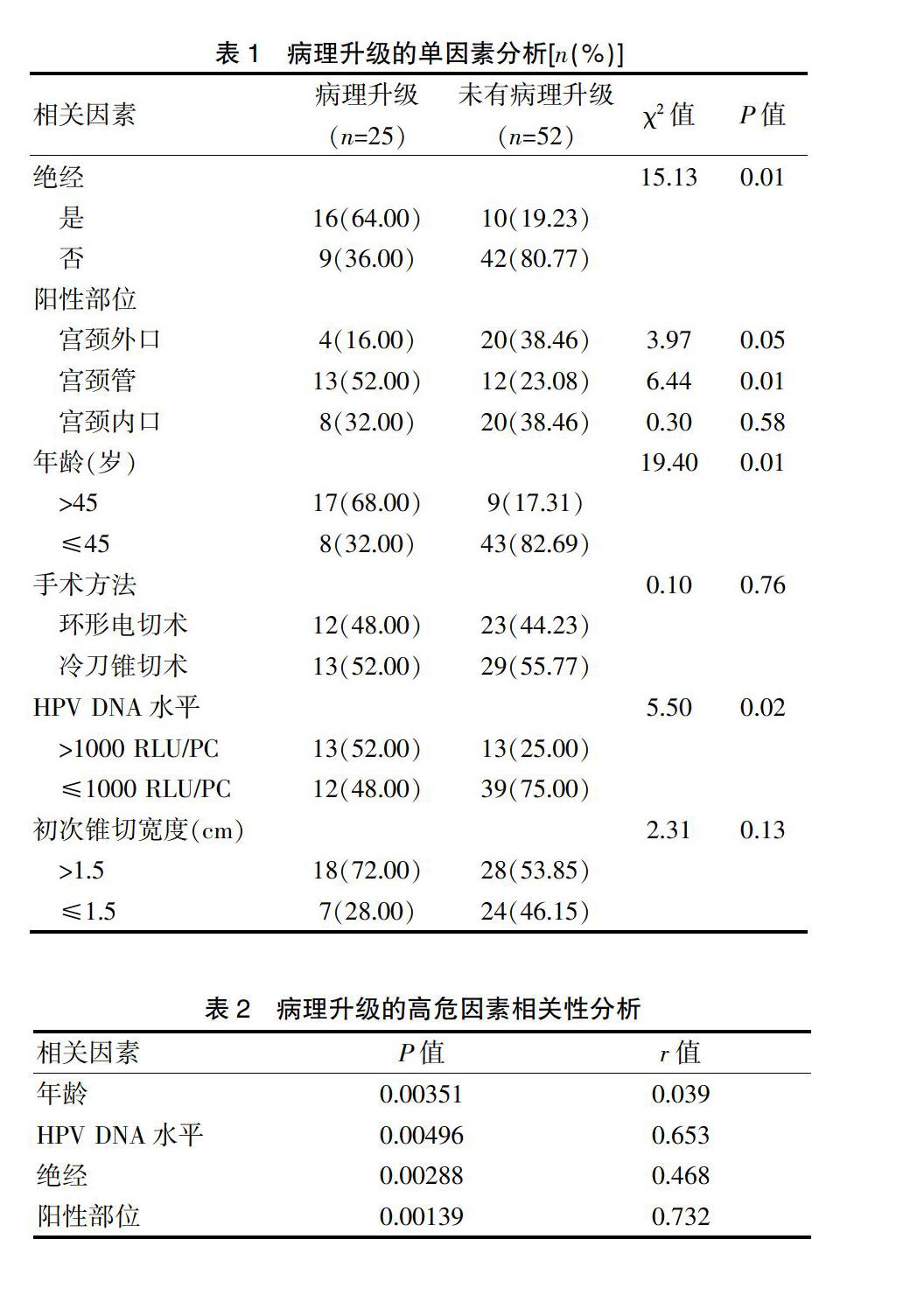
2.2病理升级的单因素分析
病理升级組的绝经占比、宫颈管占比、年龄>45岁、HPV DNA>1000 RLU/PC占比均明显高于未有病理升级组,差异有统计学意义(P<0.05)(表1)。
2.3病理升级的高危因素相关性分析
年龄、HPV水平、绝经及阳性部位和病灶残留成正相关关系(P<0.05)。
2.4高级别CIN宫颈锥切术后二次手术方式
77例高级别CIN宫颈锥切术患者中,有11例患者接受二次手术治疗,其中宫颈锥切术占比最高,其次即为子宫切除术、宫颈癌改良根治术。11例患者中,宫颈锥切术6例,其占比为54.55%;子宫切除术3例,占比为27.27%;宫颈癌改良根治术2例,其占比为18.18%。
3讨论
近年来,CIN的临床发病率呈现逐年递增的趋势,且患病人群逐渐年轻化,多数年轻患者在接受治疗时,对生殖器官完整及生育功能的保留有较高的要求。宫颈锥切术是目前临床治疗CIN和宫颈原位癌的常用措施。因CIN的病灶通常为多中心型发展,开展子宫颈切除术后,可能仍然有部分病理升级,且术后十分必要为患者开展切缘病理检查。目前临床认为术后病理升级的独立性危险因素即为切缘阳性,此类患者常要接受二次手术治疗。临床相关研究指出[3],CIN患者接受宫颈锥切术治疗后,经随访发现,切缘阳性的病灶有较多的残留和复发率,且其残留率与复发率明显较切缘阴性高。本研究主要分析切缘阳性患者的相关临床因素,目的在为今后临床工作提供参考,研究发现,患者的年龄、绝经状况、术前HPVDNA及初次宫颈锥切宽度同病理升级有密切关联,而初次手术治疗的方式同病理升级无较大关联。
进一步展开多因素回顾模型分析,发现病理升级同患者的年龄、是否绝经及术前HPV DNA等因素有密切关联,且临床相关研究表明[4],预测高级别CIN患者术后是否有病理升级或疾病复发的一项可靠指标即为检测HPV DNA,若患者术前HPV DNA检测结果显示在1000 RLU/PC以上,则其术后发生病理升级或疾病复发的风险提升3倍。宫颈锥切术治疗过程中,临床中多数学者提倡尽可能达到切缘阴性,临床中亦有部分学者提出[5],通过适当减小锥切的范围,降低术后相关并发症及妊娠相关并发症的发生率。患者接受宫颈锥切术治疗后,其发生早产的概率较未接受手术者高2~3倍。亦有研究指出[6],锥切高度<1 cm,锥切体积<2.1 cm3为病理升级的重要因素,亦有研究指出[7],依据锥切体积评估病理升级的可靠性欠佳。近年来,伴随着二孩政策的开放,部分有生育要求或再生育要求者,使CIN适合的切除范围临界值成为临床中的重点关注问题。本研究中发现,病理升级同锥切宽度和高度间有密切关联存在[8-9]。
由美国阴道镜和宫颈病理协会指南和美国国立综合癌症网络指南可知,目前临床主张初次锥切术后,针对切缘阳性的患者,可为其展开密切的随访,或为其再次实施宫颈病变诊断性切除、子宫切除,但具体的治疗方案应当结合患者的具体情况而定[10],以此充分体现针对性和个性化特征。本研究中所有切缘阳性患者均接受二次手术治疗,且认为对锥切术后切缘阳性患者必须开展二次手术治疗。二次手术治疗中开展的宫颈癌改良根治术的手术范围较大,且对患者机体存在的损伤较大,应慎重开展该术式治疗[11-12]。再次宫颈锥切术治疗可有效减小手术治疗对患者生育功能产生的影响,但仍然有再次病理升级的风险存在。为此患者二次手术治疗的方案应当结合其具体情况而定,针对具有生育要求的年龄患者,应尽可能保留其生育功能,可为其开展宫颈锥切术治疗,减小手术治疗对其生育功能产生的影响[13-15]。针对年龄较大、无生育要求、随访条件欠佳的患者,在获得其同意后,开展子宫全切术治疗。
综上所述,病理升级同患者的年龄、HPV DNA、初次宫颈锥切的宽度、绝经状态、HPV水平和阴性部位等因素有密切关联,上述因素中,患者的年龄、绝经状态、HPV水平及阴性部位等属于高危因素。临床对切缘阳性患者应开展个体化的二次手术治疗。
[参考文献]
[1]刘延超.子宫颈上皮内瘤变锥切术后残留或复发因素的分析及监测[D].青岛:青岛大学,2018.
[2]朱远航.HPV E6/E7 mRNA检测对ASCUS患者宫颈高级别上皮内瘤变和宫颈癌的诊断价值[D].郑州:郑州大学,2018.
[3]程其会.宫颈冷刀锥切术和LEEP刀锥切术治疗高级别宫颈上皮内瘤变的疗效分析[J].中国社区医师,2018,34(14):22-23.
[4]金明杨.273例宫颈上皮内瘤变患者术后切缘阳性的危险因素及预后分析[J].中国妇幼保健,2018,33(5):997-1000.
[5]林洁,刘彬,陈桂林,等.宫颈冷刀锥切术和宫颈环形电切术治疗宫颈高级别上皮内瘤变临床疗效对比分析[J].福建医药杂志,2018,40(3):37-39.
[6]陈惠华,金文芳,黄宝英.HPV E6/E7 mRNA在宫颈高级别上皮内瘤变诊断及LEEP术后中的价值[J].中国妇幼保健,2017,32(23):6006-6008.
[7]贾丽华,胡玉玲,杨国华,等.宫颈冷刀锥切术联合子宫动脉下行支结扎在治疗高级别宫颈上皮内瘤变中的应用价值[J].中国妇产科临床杂志,2017,18(5):443-444.
[8]聂小毳,史玉林,丛建萍,等.宫颈上皮内瘤变锥切术切缘阳性的相关因素分析[J].中华肿瘤防治杂志,2016,23(4):262-265.
[9]宗丽菊,高绍凤,韩赛,等.75例宫颈上皮内瘤变锥切术后病变残留或复发的临床特点及诊治分析[J].实用妇产科杂志,2016,32(9):676-680.
[10]王秋红,杜桂清,邓桂霞,等.宫颈上皮内瘤变患者活检与锥切术后病理结果比较[J].贵阳医学院学报,2016,41(2):234-237.
[11]陈微微,石琨,易丽莎.宫颈上皮内瘤变锥切术后切缘阳性高危因素分析[J].中国妇幼保健,2017,32(12):2550-2552.
[12]李銀姬,邓燕杰,张佳宁.宫颈上皮内瘤变Ⅲ患者宫颈冷刀锥切术后腹腔镜下全子宫切除术101例分析[J].中国医师进修杂志,2017,40(3):247.
[13]蒋燕明,王鹤,贺红英,等.不同手术方式治疗宫颈上皮内瘤变的近、远期疗效分析[J].现代妇产科进展,2018, 27(1):28-32.
[14]郝敏,蔺莉.绝经后妇女宫颈上皮内瘤变Ⅱ级及以上患者临床特点分析[J].中国微创外科杂志,2017,17(2):155-158.
[15]陈燕,江维,曾四元,等.阴道镜活检对宫颈低级别鳞状上皮内病变(CIN1)的诊断分析[J].实用癌症杂志,2016, 31(11):1818-1821,1830.
(收稿日期:2019-01-08 本文编辑:崔建中)
