[N2,2,2,2]BF4的合成及其对双水相体系成相行为的影响
2019-10-14朱新儒张海德
余 垒,朱新儒,曾 颖,李 雄,张海德
(海南大学食品学院,海南海口570228)
离子液体(ILs)是一种完全由离子组成,在室温或者接近室温下呈液体状态的低温熔融盐,是一类新型的绿色溶剂,近年来已在化工反应、环境保护、制备新型材料等方面获得了突飞猛进的发展[1],但常见的咪唑型、吡啶型离子液体昂贵的价格在一定程度上也限制了它们的应用范围,而价格较低的季铵型离子液体具有制备简单、电导率高、熔点低、热稳定性和电化学稳定性好等优点,越来越得到广大研究者的关注[2-3]。
聚乙二醇(PEG)具有很高的生物降解性、低毒、低熔点、低成本等优点,通常被用作双水相系统中的一种成相剂[4],但是,富含PEG的一相较低的极性及PEG本身只能通过改变相对分子质量或分子结构的这种特点限制了它的应用范围[5]。为突破这种局限,R.C.S de Sousa 等[6]研究了不同离子液体作为助剂对PEG-盐双水相系统分离生物分子分配行为的影响,得出离子液体作为助剂能改变共存相的特性和生物分子的分配行为,且更适合于分离疏水性较高的生物分子;S.Hamzehzadeh等[7]研究了1-丁基3-甲基咪唑溴化物离子液体作为辅助剂对PEG-磷酸盐成相面积的影响,得出添加5%的离子液体为辅助剂增大了PEG400-磷酸盐和PEG600-磷酸盐双水相的成相面积,且得出离子液体与富含PEG的上相具有更好的亲和性的结论;R.L.de Souza等[8]研究了使用离子液体作为助剂萃取分离两种探针染料,增加了双水相区域的面积,离子液体的存在改变了染料在双水相体系的分配系数,使得探针染料富集于PEG相,并得出离子液体与疏水相间存在更强烈的相互作用的结论;I.V.Lucena等[9]通过添加5%质子型离子液体为PEG-硫酸铵双水相系统的辅助剂,大大增加了辣根过氧化酶的纯化效果;S.Hamzehzadeh 等[10]通过在 PEG400-柠檬酸钾双水相体系中加入5%的[Bmim]Br,发现L-色氨酸的萃取效率得到了明显提高;A.M.Ferreira等[11]通过分别添加5%咪唑型和季铵型离子液体为PEG-柠檬酸钾双水相体系的辅助剂,与不含离子液体的双水相体系相比,富含PEG相中免疫球蛋白G的纯度增加了37%;H.Yang等[5]通过添加4%不同咪唑型离子液体为PEG600-NaH2PO4·2H2O双水相体系的辅助剂,提高了L-苯丙氨酸的萃取效率。
本文合成了季铵型离子液体[N2,2,2,2]BF4,并对其进行1H NMR表征和纯度验证。通过研究加入少量的[N2,2,2,2]BF4对 PEG-NaH2PO4·2H2O 双水相系统成相面积的影响,旨在寻找一种低成本有效的双水相体系,该体系将适合在常温下较稳定的亲水性生物活性物质的分离纯化研究。
1 实验部分
1.1 材料与仪器
PEG400、PEG600、PEG2000、PEG4000、PEG6000,均为化学纯;NaH2PO4·2H2O、三乙胺、溴乙烷等,均为分析纯。
双束紫外可见分光光度计(TU-1901);旋转蒸发仪(RE-2000A);节能型智能恒温槽(DC-1006);恒温磁力搅拌器(85-1);离心机(CenceL500);油浴锅(DF-2A);数显恒温水浴锅(HH-8);核磁共振仪(DP-FD-CNMR-I);全自动水分测定仪(KF-4)。
1.2 实验方法
1.2.1 两步法合成季铵型离子液体[N2,2,2,2]BF4
1)合成中间体[N2,2,2,2]Br。 在 250 mL 圆底烧瓶内加入 0.1 mol的乙腈(ACN),0.2 mol的三乙胺,用恒压滴液漏斗加入0.2 mol的溴乙烷,常温密闭反应72 h,抽滤,置于真空干燥箱干燥48 h得到中间体产物[N2,2,2,2]Br。 合成路线见图1。
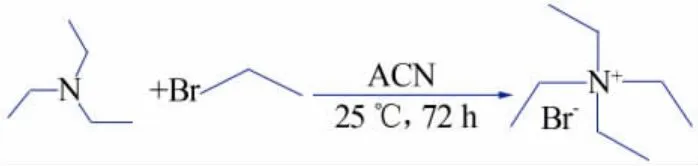
图1 [N2,2,2,2]Br合成路线
2)以中间体[N2,2,2,2]Br为反应物合成季铵型离子液体[N2,2,2,2]BF4。 在 250 mL 圆底烧瓶内加入 0.1 mol[N2,2,2,2]Br和 0.11 mol NaBF4,加入100 mL乙腈溶剂,装好冷凝回流装置,油浴锅温度设置为80℃,冷凝回流6 h,抽滤,除去下层沉淀;然后将溶液于60℃旋转蒸发仪内蒸干,得白色晶体,此为粗目标产物;然后向烧瓶内加入80 mL异丙醇,油浴锅温度设置为120℃,冷凝回流,待烧瓶内固体全部溶解,停止重结晶,抽滤得白色针状湿品[N2,2,2,2]BF4,重复上述步骤,进行二次重结晶;真空干燥48 h,进行纯度检测,待固体质量不再变化,称重,计算产率。合成路线见图2。

图2 [N2,2,2,2]BF4合成路线
产率计算公式见式(1):

式中:X为产率,%;Wa为实际产物量,g;Wp为理论产物量,g。
3)[N2,2,2,2]BF4的结构表征。 用 95%的氘代二甲基亚砜溶剂和5%的四甲基硅烷(TMS)溶解[N2,2,2,2]BF4,由核磁共振仪对其结构进行表征。
4)[N2,2,2,2]BF4水溶液标准工作曲线的绘制及纯度的检测。 准确称量[N2,2,2,2]BF4标准样品0.01 g,在容量瓶中定容到100 mL,得到质量浓度为100 mg/L 的[N2,2,2,2]BF4标准样品水溶液,将其分别稀释至 10、20、30、40、50、60、70、80、90 mg/L,以去离子水为参比,在190~300 nm波长范围内进行扫描,确定[N2,2,2,2]BF4水溶液在紫外光区的最大吸收波长,并以离子液体水溶液的浓度为横坐标,以吸光度为纵坐标,绘制标准曲线[12];准确称量实验室自制的[N2,2,2,2]BF4离子液体,用去离子水稀释配成不同浓度的[N2,2,2,2]BF4水溶液,以去离子水为参比,测定最大吸收波长处的吸光度,通过标准曲线计算所得 [N2,2,2,2]BF4离子液体的实际浓度,计算所得实际浓度与理论配制浓度之比,即可得到该离子液体的纯度。
1.2.2 单因素实验
以[N2,2,2,2]Br的物质的量、乙腈用量及反应时间 3 个因素为研究对象,以[N2,2,2,2]BF4的产率为指标进行单因素实验。
1.2.3 正交优化实验
为获得合成 [N2,2,2,2]BF4的最佳工艺条件,在单因素实验的基础上,以[N2,2,2,2]BF4的产率为指标,设计三因素三水平的正交优化实验。
1.2.4 相图的绘制
在25℃条件下采用浊点法[13]绘制双水相体系相图。制备质量分数为 4%的[N2,2,2,2]BF4原溶液,质量分数为60%不同相对分子质量的PEG原溶液、质量分数为40%的NaH2PO4·2H2O原溶液,备用。分别称量一定质量的 PEG 原溶液及[N2,2,2,2]BF4溶液于试管中,边振荡边逐滴滴加盐溶液,直至混合液刚好出现混浊,接着逐滴滴加蒸馏水,直至混合液变澄清,重复上述操作。每次实验重复3次,计算平均质量。
1.2.5 数据处理
每组实验均为3次重复实验求平均值,采用origin8.5处理实验数据。
2 结果与分析
2.1 [N2,2,2,2]BF4的 1H NMR 及纯度分析
用95%的氘代二甲基亚砜溶剂和5%的TMS溶解[N2,2,2,2]BF4,由核磁共振仪对其结构进行表征,所得结果如图3所示;由紫外分光光度计测得标准 [N2,2,2,2]BF4溶液的紫外吸收光谱图及标准[N2,2,2,2]BF4溶液浓度与吸光度的标准曲线如图4和图5所示。
由图3可知,δ=2.47~2.53为溶剂峰,在1H NMR中对谱图峰进行了归属[14],数据如下:δ=1.01~1.31为—CH2—CH3甲基上的 12个氢,δ=3.03~3.39为—CH2—N—乙基上的8个氢,两个峰面积的比值为1.45∶1≈3∶2 与理论值符合,说明目标化合物[N2,2,2,2]BF4结构正确。
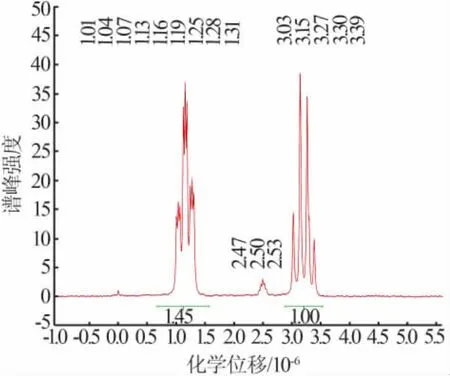
图3 [N2,2,2,2]BF4的核磁氢谱图

图4 [N2,2,2,2]BF4水溶液的紫外吸收光谱图
由图4 可知,[N2,2,2,2]BF4离子液体水溶液在190~300 nm之间有单一吸收峰,最大吸收波长在205 nm处附近。因此在该最大吸收波长上利用紫外分光光度计测定离子液体的浓度符合朗伯-比耳光吸收定律,可获得较高的准确性[12]。

图5 标准[N2,2,2,2]BF4水溶液浓度与吸光度标准曲线
如图5所示,线性标准工作曲线方程为y=0.01057x+0.02677,相关系数R2=0.9987,由此判断此标准曲线可用来进行实验室自制[N2,2,2,2]BF4离子液体浓度检测。分别配制30、70、100 mg/L的实验室自制[N2,2,2,2]BF4溶液,测得的吸光度代入标准曲线计算得离子液体的纯度分别为:98.46%、98.51%、98.48%,经过与AgNO3反应,未发现任何沉淀,由此可知,实验合成的离子液体纯度较高[15],经真空干燥后通过KF-4型全自动水分测定仪测定[N2,2,2,2]BF4的含水量, 使含水量在使用前保持在 6×10-4以内。
2.2 合成[N2,2,2,2]BF4的单因素与正交优化实验
2.2.1 [N2,2,2,2]Br的物质的量对产率的影响
固定NaBF4的量为1.1 mol不变,乙腈用量为100 mL,反应时间为6 h,反应温度为80℃,考察[N2,2,2,2]Br的不同物质的量对产率的影响。当反应物[N2,2,2,2]Br的物质的量小于 1.0 mol时,反应产率呈上升趋势;当反应物[N2,2,2,2]Br的物质的量等于1.0 mol时,反应产率达到高值,为89.9%;当反应物[N2,2,2,2]Br的物质的量大于 1.0 mol时,反应产率呈下降趋势,而且,过量的[N2,2,2,2]Br会导致生成杂质产物NaBr,并且很难处理[16]。所以,最终选择[N2,2,2,2]Br的物质的量为 1.0 mol。
2.2.2 乙腈用量对产率的影响
固定 [N2,2,2,2]Br 的 物 质 的 量为 1.0 mol、NaBF4的量为1.1 mol不变,反应时间为6 h,反应温度为 80 ℃,考察不同乙腈用量对[N2,2,2,2]BF4产率的影响。当反应物乙腈的用量小于100 mL时,反应产率呈上升趋势;当反应物乙腈用量为100 mL时,反应产率达到最高,为90.4%;当反应物乙腈的用量大于100 mL时,反应产率呈下降趋势,说明溶剂的量对离子液体产率影响较大[17]。综合比较,最终选择乙腈的用量为100 mL。
2.2.3 反应时间对产率的影响
固定 [N2,2,2,2]Br的物质的量为 1.0mol、NaBF4的量为1.1 mol不变,溶剂的量为100 mL,反应温度为 80 ℃,考察不同反应时间对[N2,2,2,2]BF4产率的影响。当反应时间小于8 h时,反应产率呈上升趋势;当反应时间为8 h时,反应产率达到最高,为91.2%;当反应时间大于8 h时,反应产率呈下降趋势。而且,过短或者过长的反应时间都会对反应产率的结果造成不利的影响,综合比较,最终选择的反应时间为8 h。
2.2.4 正交实验结果与极差分析
根据不同单因素对产率的影响结果,以原料配比(A)、溶剂用量(B)、反应时间(C)为因素,以[N2,2,2,2]BF4的产率为指标,采用 L9(34)进行正交实验,优化[N2,2,2,2]BF4产率的最佳影响条件。影响[N2,2,2,2]BF4产率的因素水平表见表 1,正交实验结果与极差分析表见表2。

表1 正交实验因素水平表

表2 正交实验结果与极差分析表
由表2可知,反应条件的选择对产品收率有明显的影响,产率可由59.7%提高至89.8%。通过极差分析可以得出:影响该反应的最主要的因素是反应时间,此外四乙基溴化铵与四氟硼酸钠的物质的量比和溶剂用量对产率也有不同程度的影响;其中,溶剂用量影响最小。最佳反应条件为:A1B1C2,即n([N2,2,2,2]Br)∶n(NaBF4)为 1∶1.1,溶剂 用量为100 mL,反应时间为8 h。选择该反应条件做3次平行实验,最终得到[N2,2,2,2]BF4的产率为(90.70±4.0)%。实验结果表明,正交实验筛选出的最佳合成条件可操作性强,重复性好,适用于季铵型离子液体[N2,2,2,2]BF4的合成。
2.3 相图的绘制与双节点数据的关联
2.3.1 相图的绘制
由浊点法[13]绘制双水相的相图,结果如图6所示。由图6可知,随着PEG相对分子质量的增加,双水相区域逐渐增大,这主要是因为在PEGNaH2PO4·2H2O双水相系统中,由于静电斥力的作用,PEG相对分子质量的增大使得体系中水化离子与PEG分子间的水不溶性增强,PEG的疏水性随着相对分子质量的增大而增强。相同聚乙二醇浓度的条件下,聚乙二醇的相对分子质量越大,双水相成相所需的 NaH2PO4·2H2O含量越少,双水相相图越靠近原点[14]。所以,各相对分子质量的PEG成相能力由大到小分别为:PEG6000+4%IL(IL代表[N2,2,2,2]BF4)、PEG4000+4%IL、PEG2000+4%IL、PEG6000、PEG4000、PEG2000、PEG600+4%IL、PEG600、PEG400+4%IL、PEG400。 由此可知,PEGNaH2PO4·2H2O双水相系统加入4%具有疏水性的[N2,2,2,2]BF4,能够替代双水相中的部分 PEG,增加双水相区域的面积,扩大成相剂成相的选择范围[9]。 J.B.Pereira 等[18]的研究结果也表明,离子液体自身的疏水性是双水相成相的驱动力。
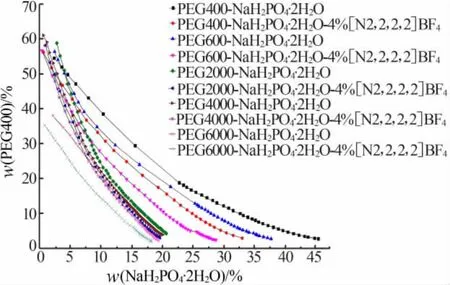
图6 25℃下三元与四元体系组成的双水相体系的相图
2.3.2 相图数据的关联
近年来,Merchuk方程已成功应用于PEG/盐和离子液体/盐双水相双节点数据的关联。Merchuk经验方程形式简洁,比Pitzer、Cabezas等半经验半理论热力学模型具有更广泛的实际应用价值[19]。
由Merchuk方程[20]对相图数据进行关联,结果见表3和表4。Merchuk方程如式(2)所示。

式中:Y和X分别代表PEG和NaH2PO4·2H2O的质量分数;A,B和C为通过回归方程得到的常数。

表3 25℃下通过Merchuk方程获得的PEG-NaH2PO4·2H2O体系的标准偏差及决定系数R2
通过非线性拟合得出的相关系数A、B和C由标准偏差σ及决定系数R2对其进行评估,由表3和表4可知,R2接近于1,关联度很好,这表明,所有相图实验数据能很好地适用于Merchuk方程,为后续的双水相体系的选择与优化奠定了理论基础。

表4 25℃下通过Merchuk方程获得的PEG-NaH2PO4·2H2O-4%[N2,2,2,2]BF4体系的标准偏差及决定系数 R2
3 结论
通过单因素及正交优化实验合成了[N2,2,2,2]BF4,经1H NMR谱图分析得知其结构正确;通过标准曲线计算得知,实验室合成的[N2,2,2,2]BF4纯度较高,产率为 90.7%;通过研究添加 4%的[N2,2,2,2]BF4对 PEG-NaH2PO4·2H2O双水相成相面积的影响可知,随着PEG相对分子质量的增加,成相面积逐 渐增加,其 中 ,PEG6000-NaH2PO4·2H2O-4%[N2,2,2,2]BF4双水相的成相面积达到最大, 有利于后续双水相成相体系的选择。通过对相图数据进行非线性拟合得出,决定系数R2接近于1,关联度很好;与离子液体-盐双水相体系相比,PEG-盐-离子液体双水相体系在一定程度上减少了成本,为后续双水相分离纯化生物分子奠定了理论基础。
