液相色谱-质谱串联法测定人血浆中羟尼酮浓度的不确定度评定*
2019-10-12马林杨春晓周嘉黎吴健鸿师少军刘亚妮
马林,杨春晓,周嘉黎,吴健鸿,师少军,刘亚妮
(1.华中科技大学同济医学院附属协和医院药学部,武汉 430022;2.武汉药品医疗器械检验所,武汉 430075)
羟尼酮(hydronidone)为吡啶酮类小分子化合物,化学名为N-(4-羟基苯基)-5- 甲基-2-吡啶酮;由上海睿星基因技术有限公司研发的抗肝纤维化一类新药,目前处于临床研究阶段[1-2]。其衍生物吡非尼酮(pirfenidone)已被国内外批准上市,用于治疗特发性肺纤维化[2-4]。羟尼酮通过有效抑制肝脏中星状细胞的增殖,减少胶原合成,从而减少细胞外基质在肝脏中过多堆积,遏制肝纤维化进程,但并不影响正常细胞外基质的生成。羟尼酮口服给药后,吸收迅速,0.33~0.63 h达血药浓度峰值,并快速在体内消除,t1/2为1.72~3.10 h。高脂饮食会延缓其体内的吸收速度,并降低其吸收程度[1]。I期临床研究表明羟尼酮在15~120 mg剂量呈现良好的耐受性和安全性[1]。
本实验室建立液相色谱-质谱串联(LC-MS/MS)法测定人血浆中羟尼酮的浓度,为其临床药动学研究提供方法学依据。该方法测定结果的可靠性直接决定羟尼酮临床药动学研究结果的准确性,并影响其安全性和有效性的评价。不确定度是指对测量结果正确性的可疑程度,用于表征合理地赋予被测量值的分散性,是目前国际上普遍推荐使用的定量评估检测结果质量的参数[5-7]。通过评估测定方法的不确定度大小,可衡量测定结果准确性的可疑程度,客观评价测定结果的质量[7-8]。为此,有必要对LC-MS/MS法测定人血浆中羟尼酮浓度的不确定度进行评定,有助于改进检测步骤并提高检测质量;如实反映测量的置信度和准确度,为羟尼酮人血浆药物浓度测定方法的改进提供指导依据。
1 仪器与试药
1.1仪器 岛津液相色谱系统(日本岛津公司,配备DGU-20A3 脱气机、LC-20AD 型二元输液泵、SIL-20AC型自动进样器、CTO-20AC 型柱温箱),API 4000型三重四极杆串联质谱仪(美国AB Sciex公司),Analyst 1.5.1数据处理系统(美国AB Sciex公司),BS110S 型分析天平(北京赛多利斯天平有限公司),VORTEX GENIUS 3型微型旋涡混合仪(德国IKA公司),Legend Micro 21R 高速冷冻离心机(美国Thermo Scientific 公司),Simplicity超纯水仪(美国Millipore公司)。
1.2试药 羟尼酮对照品(上海睿星基因技术有限公司提供,批号:20120101,含量:99.1%),内标吡非尼酮对照品(上海睿星基因技术有限公司提供,批号:20120807,含量:100%),甲醇和醋酸(色谱纯,美国Tedia公司)、乙腈(色谱纯,美国Fisher公司),人空白血浆(武汉市血液中心提供)。
2 方法
2.1测定条件 色谱条件:采用Aglient ZORBAX 300 Extend-C18色谱柱 (2.1 mm×150 mm,3.5 μm,美国Aglient公司)和Security GuardTMC18保护柱(4 mm×2.0 mm,5 μm,美国Phenomenex公司);柱温设定为40 ℃;以水-乙腈(78:22)为流动相;流速为0.20 mL·min-1;进样体积为10 μL;进样器温度设定为4 ℃。
质谱条件:采用电喷雾离子源(ESI),正离子模式,多重反应监测(MRM)扫描模式;离子喷射电压(IS):5500 V;离子源温度(TEM):500 ℃;雾化气(Gas1,N2):344.75 kPa;辅助气(Gas2,N2):344.75 kPa;气帘气(CUR,N2):172.375 kPa;去簇电压(DP):84 V(羟尼酮),80V(吡非尼酮);碰撞能量(CE):39 V(羟尼酮),35 V(吡非尼酮);定量分析监测离子对分别为:羟尼酮 [M+H]+,m/z202.2→92.0,吡非尼酮[M+H]+,m/z186.1→92.1。
2.2工作溶液的配制
2.2.1羟尼酮工作溶液的配制 平行称取2份羟尼酮对照品10 mg,精密称定,置10 mL量瓶中,用甲醇溶解并定容,再分别用甲醇进一步稀释为10.0 μg·mL-1的储备液(标准曲线储备液和质控储备液)。取标准曲线储备液用流动相依次稀释配制成含羟尼酮4 000 (C8),2 000(C7),1 000 (C6),500 (C5),200 (C4),100 (C3),40(C2),20(C1)ng·mL-1的系列标准曲线工作溶液。取质控储备液用流动相依次稀释配制成含羟尼酮3000 (H),600 (M),60 (L)ng·mL-1的质控工作溶液。
2.2.2内标工作溶液的配制 取吡非尼酮对照品10 mg,精密称定,用甲醇溶解,配制成1.01 mg·mL-1的内标储备液。稀释该储备液至101.20 ng·mL-1作为内标工作溶液。
2.3含药血浆样品的配制 用移液器(量程2~20 μL)分别精密吸取“2.2.1”项下羟尼酮系列标准曲线工作溶液(C1~C8)和低(L)、中(M)、高(H)浓度质控工作溶液各20 μL,置2.0 mL离心管中,然后用移液器(量程20~200 μL)分别精密加入空白血浆200 μL,涡旋30 s,混匀,配制成相当于羟尼酮浓度为2,4,10,20,50,100,200和400 ng·mL-1的系列标准曲线血浆样品以及浓度为6,60,300 ng·mL-1的低(L)、中(M)、高(H)浓度质控样品。
2.4血浆样品处理 采用蛋白沉淀法进行血浆样品前处理。精密吸取血浆样品50 μL,置1.5 mL离心管中,分别精密加入吡非尼酮内标工作溶液20 μL、流动相5 μL、10%醋酸溶液20 μL,涡旋30 s后,再精密加入甲醇200 μL,涡旋震荡5 min,于16 000 r·min-1离心10 min,分别精密吸取上清液和纯化水各100 μL,置于进样瓶中混匀后,吸取10 μL进样测定。
2.5样品测定与计算 将“2.3”项下系列标准曲线血浆样品按“2.4”项方法处理后,在“2.1”项条件下测定羟尼酮与内标吡非尼酮的响应信号峰面积。以羟尼酮与内标吡非尼酮的峰面积比值(R)对羟尼酮血药浓度(C)进行加权最小二乘法线性拟合,得标准曲线方程:R=aC+b。则质控样品和待测血浆样品中羟尼酮浓度的计算公式为:C=(R-b)/a,其中:C为羟尼酮最终血浆测定浓度,R为羟尼酮与内标吡非尼酮的峰面积之比,a为拟合标准曲线方程的斜率,b为截距。
3 结果
3.1测量不确定度的来源 羟尼酮血浆样本测定过程中,对测定结果产生影响的每一个因素都是不确定度的来源,其来源主要包括:①工作溶液和含药血浆样品的配制,涉及的影响因素包括:羟尼酮对照品的纯度及称量,量瓶允差,移液管允差,吸量管允差,移液器允差,样品均匀性,温度;②血浆样品的处理;③标准曲线拟合;④仪器测定;⑤重复性测定等。
3.2各分量不确定度的评定[5-10]
3.2.1A类不确定度评定 重复性引入的不确定度采用A类评定程序。按照“2.3”项下方法分别配制2,4,10,20,50,100,200和400 ng·mL-1系列标准曲线血浆样品,并平行配制6,60,300 ng·mL-1质控样品各5份,重复配制3批,按“2.4”项下方法处理后,进行LC-MS/MS测定,将羟尼酮与内标峰面积比值带入相应分析批的标准曲线方程,计算得质控样品的浓度,结果见表1。

表1 羟尼酮血浆样品重复测定结果
根据贝塞尔公式计算各组浓度的合并样本标准偏差:
测定结果的标准不确定度分别为:
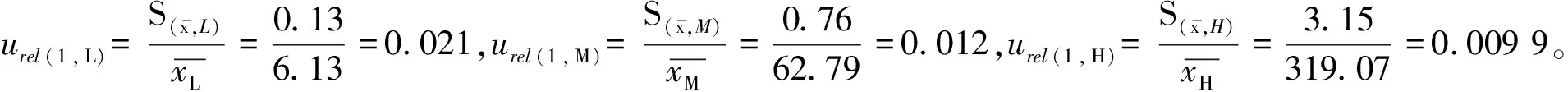
3.2.2B类不确定度评定

内标称量引入的不确定度对羟尼酮浓度测定结果的影响很小,可忽略不计。羟尼酮称量的质量为10.30 mg,则称量羟尼酮引入的相对标准不确定度为:
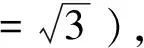
溶液配制过程中用到10 mL量瓶10次、5 mL单标移液管5次、5 mL分度吸量管3次,20~200 μL量程移液器1次,其相对不确定度为:
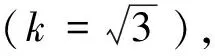
3.2.2.4血浆样品提取过程和基质效应引入的不确定度 按“2.4”项下处理低、中、高浓度的质控样本,进行LC-MS/MS测定所得峰面积为A1;空白血浆按“2.4”项处理后加入相同浓度的质控及内标工作溶液进行测定所得峰面积为A2;流动相同法操作后进行测定所得峰面积为A3,则提取回收率=A1/A2×100%,基质效应=A2/A3×100%,结果见表2。
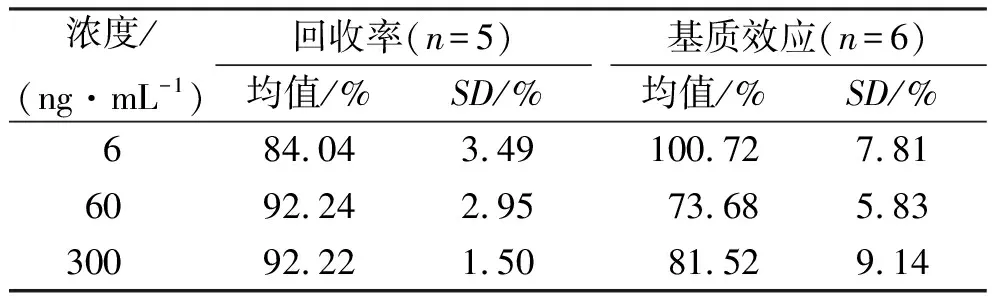
表2 提取回收率和基质效应
各组浓度回收率的相对标准不确定度分别为:
各组浓度基质效应的相对标准不确定度分别为:
3.2.2.5仪器量化不确定度 质谱仪为API 4000,定量允差为3%;液相色谱仪为岛津液相系统,吸样允差为1%。按均匀分布,仪器量化的相对标准不确定度为:
3.2.2.6线性拟和过程引入的不确定度 羟尼酮血浆样品的浓度根据拟合的标准曲线方程计算所得,标准曲线的建立对浓度测定的结果至关重要。按“2.3”项下方法配制8个不同浓度的标准曲线血浆样品,每个浓度配制3份;以羟尼酮血浆浓度(C)为横坐标,羟尼酮与内标吡非尼酮的峰面积比值(R=As/Ai)为纵坐标,采用加权最小二乘法进行线性回归,权重系数为1/C,共拟合3条标准曲线方程,结果见表1。

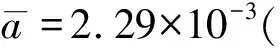
经计算,各质控浓度的相对标准不确定度分别为:
3.3合成不确定度的评定 羟尼酮浓度测定的相对标准不确定度为:
经计算低、中、高浓度的相对标准不确定度分别为:uc,rel,L=0.051,uc,rel,M=0.043,uc,rel,H=0.052
羟尼酮浓度测定的标准不确定度分别为:
3.4扩展不确定度的评定 采用简易评定,取k=2,对应的置信概率为95%,则低、中、高浓度的扩展不确定度分别为:
UL=kuc,L=2×0.31=0.63 ng·mL-1
UM=kuc,M=2×2.73=5.46 ng·mL-1
UH=kuc,H=2×16.70=33.40 ng·mL-1
血浆中羟尼酮各浓度质控测定结果可分别表示为:低浓度(6.13±0.63)ng·mL-1,中浓度(62.79±5.46)ng·mL-1,高浓度(319.07±33.40)ng·mL-1。
4 讨论
笔者建立LC-MS/MS法测定人血浆中羟尼酮的浓度,并对方法学进行验证,各项指标(线性、精密度、准确度、回收率、基质效应、等)均满足测定要求。为了评估测定结果的可靠性、提高检测质量,参考相关文献和指南[5-10],对该方法进行不确定度评定。通过对测定过程中不确定度来源的各分量进行分析,计算各来源不确定度分量值评估各分量值的贡献大小,以期为测定方法的改进提供参考和指导。结果表明,基质效应对各质控浓度不确定度贡献最大,因处理后的血浆样品中残留的基质成分在进行LC-MS/MS分析时会对检测响应信号产生明显的干扰,应尽可能的优化完善样品的前处理方法、减少基质干扰。标准曲线拟合对低浓度测定结果的影响远大于高浓度,故需进行加权线性拟合以保证低浓度测定的准确性。血浆样品的处理(回收率)及重复性(精密度)对低、中浓度不确定度贡献均较大,故应制定样品前处理标准操作规程,并对操作人员进行充分培训并严格按规范操作。此外,仪器允差对各质控浓度不确定度的贡献也不容忽视,应对仪器定期进行核查、维护和计量检定。根据不确定度评定结果,在实际分析测定过程中对不确定度贡献较大的各分量来源应加以关注和严格控制,找出影响因素和解决办法,尽可能地减小不确定度,为测定方法提供科学指导并提高检测结果的准确性和可靠性。
