基质辅助激光解吸电离飞行时间质谱临床检测微生物的专利及行业发展分析
2019-10-08曹克浩吴文英葛永奇
曹克浩,吴文英,葛永奇
(国家知识产权局专利局复审和无效审理部,北京 100088)
临床上检测微生物是一个复杂的过程。当患者疑似微生物感染时,临床医生需要收集其流行病学信息、症状和体征,并及时采集患者样本(如血液、尿液、痰等)送微生物实验室进行鉴定。目前病原菌的鉴定方法主要包括表型鉴定法和基因型鉴定法。前者需要对样本进行培养、分离,检测周期长且操作繁琐,已经不适合快速鉴定致病微生物的临床需要。后者通过分子生物学方法将细菌的检测与鉴定引入核酸和蛋白质等大分子水平,虽然准确率高,但操作复杂,成本昂贵,易受干扰物影响[1]。因此,快速而高效的微生物诊断技术对于确定患者治疗方案、缓解患者病痛至关重要。
基质辅助激光解吸电离飞行时间质谱(MALDI TOF MS)检测微生物技术是近年来发展起来的鉴定病原微生物的新技术,可通过对供试病原微生物的生物活性分子的指纹图谱进行同源分析而快速鉴定菌种,对疾病诊断具有重要意义[2]。MALDI TOF MS检测微生物主要是利用已知的菌种建立数据库,通过对待测微生物进行检测,获得蛋白质或核酸特征指纹图谱,再将所得的质谱图与数据库中的微生物参考图谱进行比对,从而得到鉴定结果。因此,与传统病原微生物鉴定方法相比,MALDI TOF MS技术具有灵敏度较高、准确率较高、耗能较低、高通量等优点。
目前国际上使用较为广泛的MALDI TOF MS的主要生产商有德国布鲁克公司、法国梅里埃公司、日本岛津公司等。截至2019年2月19日,全球涉及MALDI TOF MS质谱仪及其部件的相关专利申请已经达到2 269件(同族专利扩展为10 396件),其中中国受理的专利申请为399件(数据来自国家知识产权局专利检索系统、DWPI数据库、CNABS数据库)。虽然国内已有北京东西分析、北京普析通用、江苏天瑞、舜宇恒平、聚光科技、郑州安图、北京毅新、厦门质谱等企业提交了一系列涉及质谱仪产品的专利申请[3],但这些专利申请多是基于上述国外生产商的产品及其部件进行改进,原创型专利数量过少,在相关技术的推广应用中易于受到国外产品专利的限制。
根据中华检验医学网的预测,未来的临床微生物检测的市场空间将达到400亿元[4]。鉴于MALDI TOF MS临床上检测微生物的潜在应用价值,可以预期相关检测技术和产品(例如检测试剂、芯片、载体、指纹图谱库或质谱模型、分析软件及试剂盒等)即将成为专利申请的热点。因此,在全球范围内分析MALDI TOF MS临床上检测微生物的专利申请进展,可以了解相关检测技术和产品的创新现状和发展趋势,对于我国在该领域上绕开质谱仪器专利的限制而实现“弯道超车”提供指导作用。
1 专利分析的数据来源
本文以国家知识产权局收录的德温特世界专利索引数据库(DWPI)和中国专利文摘数据库(CNABS)为数据来源,利用关键词检索式“MALDI”“time s flight s mass s spectrometry”“matrix assisted laser desorption / ionization”“ CLIN-TOF”,结合“Microbe or microb+ or microorganism+”“bacil+(= bacilus or bacillus or bacilli) or bacter+(= bacteria or bacterial or bacterium)”“germ or microphyte or pathogen+,fung+(=fungi or fungus or fugal)”“virus”,截至2019年2月13日,共得到涉及MALDI TOF MS技术检测微生物的508件专利(同族专利扩展为2 750件专利)。在分析大量文献的基础上,从上述结果中筛选和去除主要发明目的在于改进质谱仪装置、部件以及用于诊断非微生物病症的数据,共获得发明主题涉及上述检测技术和产品的279件专利申请,其中以中国作为受理国的专利申请共122件,包含中国申请人提交的83件专利。所有结果导入数据分析的专业平台进行分析。
此外,以主题关键词“MALDI”“ time s flight s mass s spectrometry”“ matrix assisted laser desorption / ionization”“ CLIN-TOF结合分类号G01N”进行检索,共得到涉及MALDI TOF MS技术的2 269件专利(同族专利扩展为10 396件专利),其中以中国作为受理国的专利申请为399件。
虽然中国专利申请的公开周期普遍短于国外专利申请的公开周期,但国外专利申请到公开通常有18个月周期,因此2018年的数据仅供参考。
2 涉及MALDI TOF MS临床检测致病微生物的专利申请分析
2.1专利申请趋势分析 图1显示了世界范围及中国范围内MALDI TOF MS临床检测微生物的专利逐年申请情况。从图1中可以看出,该技术从1996年首次出现专利申请后,之后呈缓慢增长的态势,其中申请人以外国申请人为主。进入2008年之后,中国范围内提交的专利申请呈现快速增长的态势,并逐渐缩小与世界范围内专利申请的数量差距,尤其是2016-2018年,虽然二者的申请数量均不高,但申请数量差距达到最小值。这初步表明国外申请人尚未重视将MALDI TOF MS临床检测微生物的技术提交专利申请,而中国已经成为将该检测技术提交专利申请的主要国家。

图1 世界范围及中国范围的专利逐年申请情况
2.2技术来源国的专利申请趋势分析 图 2 、3分别为世界范围内、中国范围内提交专利申请的主要国家及地区。虽然美国在世界范围内的专利申请数量最多,但其进入中国的专利申请仅位居第二。事实上加上中国台湾的申请量,中国申请人提交的专利申请数量已经位居世界第一。这表明,相比于以中国作为受理国的申请量(399件)占世界范围内涉及所有MALDI TOF MS技术的专利申请量(共2 269件)的较小比例而言,中国申请人在临床检测微生物的专利申请已经超过外国申请人,进一步表明国外申请人并未重视MALDI TOF MS技术临床检测微生物在中国的市场前景,这意味着无论是从研究的角度,还是市场运营的角度,对于中国申请人都是难得的科学研究与专利保护的“窗口期”。
2.3专利申请人的申请趋势分析 图4显示世界范围内MALDI TOF MS临床检测微生物的主要专利申请人的数量排名。数据显示,国外申请人中,德国布鲁克公司、法国梅里埃公司、美国安捷伦公司作为MALDI TOF MS仪器的核心技术的拥有者,对于临床检测微生物的应用技术也给予一定的关注;知名的国际生物仪器及试剂公司,如美国BD公司、美国ISIS制药公司、美国西昆诺姆公司,也开始涉及质谱临床检测微生物的应用中。然而,同样作为MALDI TOF MS仪器的核心技术的拥有者,日本岛津公司(含在中国的合资企业)并未提交MALDI TOF MS临床检测微生物的专利申请。
国内申请人中,北京毅新(含北京毅新博创公司、北京毅新兴业公司)的专利申请及授权数量远远超过其他国内申请人和国外申请人,这表明该公司在该研究领域已经处于垄断地位。担负传染病预防和检疫职责的中国疾控中心亦已经开始使用质谱用于临床诊断致病微生物。而较早研究和开发MALDI TOF MS仪器的厦门质谱、浙江和谱、郑州安图,亦开始涉及临床诊断微生物的研究和应用。这表明我国在该领域的主体并不是以研究机构为主,已经涌现出以北京毅新为代表的企业积极参与技术转化,并在该领域的专利布局中与国外申请人保持同步、甚至超越,保持均衡的态势。
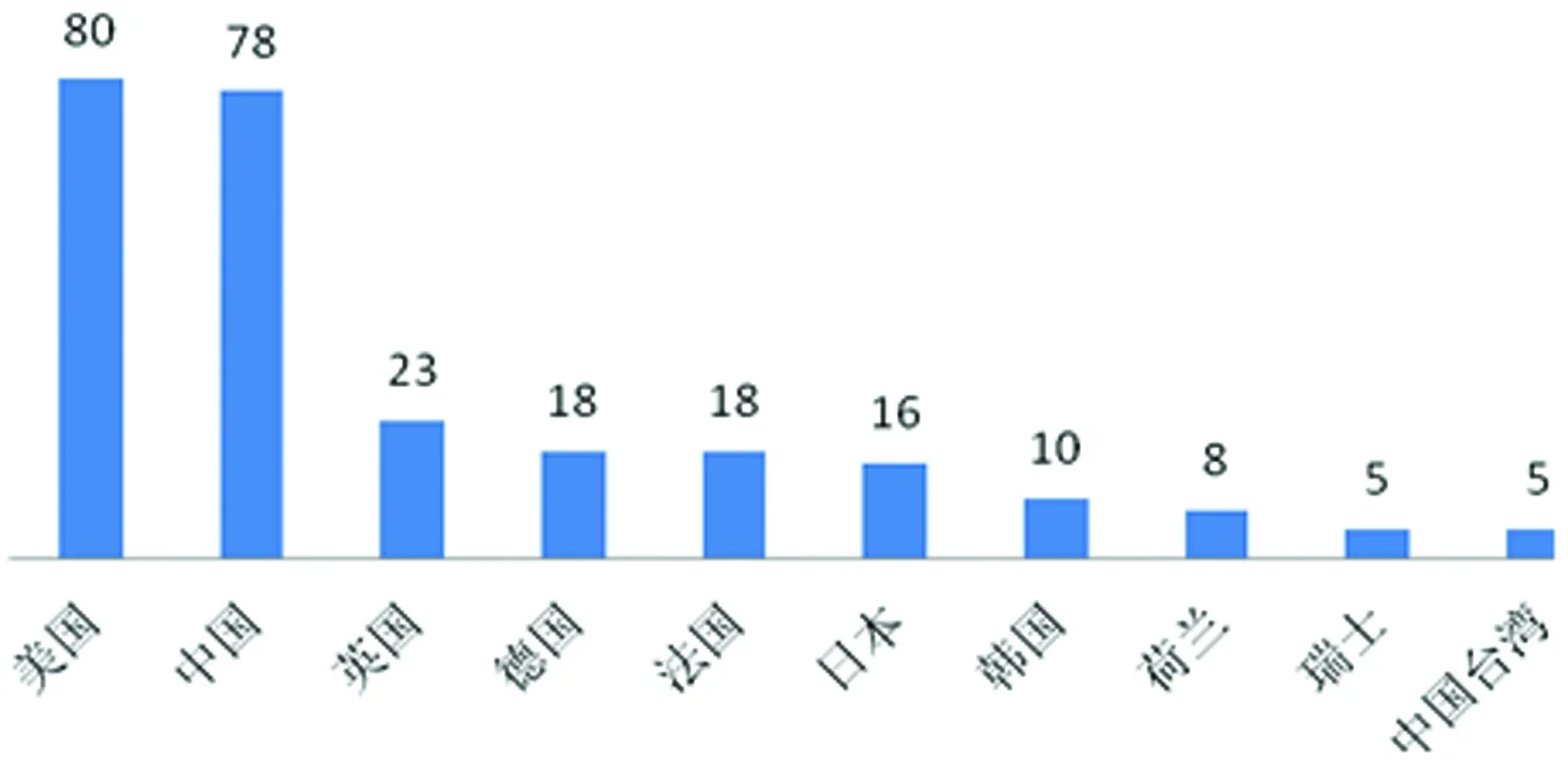
图2 世界范围内提交专利申请的国家及地区(前10名)

图3 中国范围内提交专利申请的主要国家及地区

图4 世界范围内主要申请人的专利申请数和授权数排名
2.4MALDI TOF MS临床检测微生物的特征标志物的专利分析 微生物包括细菌、病毒、真菌和酵母菌等。针对微生物的特征标志物主要是具有生物活性的蛋白质和核酸。从分子生物学的角度看,由于核酸(基因)决定蛋白的表达,而蛋白质的表达决定生物体的表型。因此,通常认为基于蛋白质指纹图谱进行的微生物鉴定分析,相比核酸水平进行的鉴定更为准确和便捷[5]。在专利分析中,以蛋白或多肽作为待检特征标志物的专利分类号IPC小组为C07K,以核酸或基因作为鉴定标志物的专利分类号IPC小组为C12N。
然而, 以世界范围的专利申请(279件)的分类号C07K、C12N(包括主分类号、副分类号)进行分析,结果显示:涉及分类号C07K的专利申请数量(共101件)与涉及分类号C12N的专利申请数量(共178件),二者比例接近4∶7。这表明,目前使用MALDI TOF MS技术用于临床鉴定微生物,已经越来越倾向于以微生物的核酸或基因作为待检特征标志物。这种变化主要与MALDI TOF MS联合PCR扩增技术的检测技术取得突破发展有关。该技术或是使用通用引物扩增微生物16S rDNA后,通过特定核酸内切酶将扩增产物酶切成长度不一、丰度不一的核酸片段,然后进行激光质谱获得待测微生物的核酸指纹图谱;或是联合多重PCR技术扩增微生物的核酸目的基因,然后将扩增的目的基因片段经质谱检测后的峰图与数据库中的峰图进行比对后得出鉴定结果[6]。
此外,利用MALDI TOF MS检测核酸标志物,还具有双保险的特点,一旦有序列发生变化,质谱就可以发现变化的产物,可以是峰的迁移或是出现新的质谱峰,抑或是理论值峰的消失,因此特别适用于检测耐药性突变位点、微生物分型。甚至有报道使用该技术转用于检测生物组织SNP位点、甲基化分型、产前诊断中的胎儿游离循环DNA,这都预示着MALDI TOF MS技术中选择核酸作为特征标志物,相比于选择蛋白作为特征标志物,将具有更为广泛的应用前景[7]。
2.5MALDI TOF MS临床检测微生物的专利申请的授权情况分析 图5显示世界范围内MALDI TOF MS临床检测微生物的专利申请状态。其中授权的专利申请数量为84件,占总数30%。未授权(包括驳回、主动撤回、视为撤回)的专利申请数量为46件,占总数17%。在审案件(包括处于申请公开、进入实质审查)的案件为149件,占总数53%。通过比较,授权的比例明显超过未授权的比例,说明MALDI TOF MS临床检测微生物的技术具有较高的可专利性,这与该技术受到临床检验人员的认可保持一致。
然而,根据专利法第25条第1款的规定,对于疾病的诊断和治疗方法不能获得专利权。同时,《专利审查指南》第二部分第一章第4.3.1.1节“属于诊断方法的发明”指出,“如果一项发明从表述形式上看是以离体样品为对象的,但该发明是以获得同一主体疾病诊断结果或健康状况为直接目的,则该发明仍然不能被授予专利权”[8]。虽然MALDI TOF MS用于临床鉴定微生物的发明方法,从表述形式上看是以离体致病菌样品为对象的,但该发明方法是以获得同一主体(即患者)疾病诊断结果或健康状况为直接目的,因此,对于这类方法的发明主题不能被授予专利权。
因此,对授权专利的发明主题进行分析可知,如图6显示,一方面,发明主题涉及检测微生物方法的授权专利(共13件)全部为用于鉴定微生物耐药性的专利,具体是通过MALDI TOF MS 技术分析抗菌药物及被修饰后的产物、分析给药后待测细菌的代谢物、分析微生物的核糖体DNA 甲基化、分析微生物的突变位点等。这种对致病微生物的耐药性机理的保护,由于不能以产品的形式进行运营,难以引起资本市场的兴趣。同时在专利侵权鉴定过程中难以认定被控侵权的方法是否落入专利的保护范围,因此该类主题的授权专利难以获得有效的专利运营和市场保护。

图5 世界范围内MALDI TOF MS临床检测微生物的专利申请状态

图6 授权专利的发明主题
另一方面,发明主题涉及核酸引物组试剂盒的专利为27件,蛋白标志物试剂盒的专利为17件,涉及对鉴定核酸或蛋白标志物中改进所用载体、基质及试剂的专利为24件。由此可见,通过提交涉及核酸和蛋白标志物的试剂盒的专利申请,既有利于获得专利授权,同时能够间接地保护MALDI TOF MS临床检测微生物的用途。此外,改进上述试剂盒中所用的载体(如承载蛋白或核酸样品的芯片载体、靶托)、基质(用于匹配样品点样的基质溶液)、试剂(如样品预处理试剂等)也具有较高的可专利性。可以预期这类发明主题的专利更会受到市场的认可,同时也为研究人员的技术开发提供指导作用。
3 结论与建议
3.1结论 本文通过国家知识产权局收录的德温特世界专利索引数据库(DWPI)和中国专利文摘数据库(CNABS),从世界及中国范围的专利申请趋势、技术来源国、专利申请人的分布、检测特征标志物、专利授权情况、授权的发明主题类型等方面对全球MALDI TOF MS临床检测致病微生物的研究现状和发展态势进行了专利信息分析。
研究表明:(1)涉及研发和生产MALDI TOF MS产品及其部件的核心技术仍然掌握在美、日、德等国,国内并未出现类似于类型布鲁克公司和英国质谱公司这类型的大型质谱研发和生产企业[9];(2)当前国外MALDI TOF MS质谱研发企业的研究热点包括离子源、离子阱、离子导入装置、真空泵、宽动态范围以及微通道板为主的电子倍增器[10],对于使用该技术用于临床检测致病微生物的应用并未引起重视,因而在专利申请和授权数量上并未占据优势。(3)相比于国外的MALDI TOF MS质谱仪器的企业,国内相关企业已经形成利用该技术应用于临床检测致病微生物的趋势,并涌现以北京毅新为代表的国内科技创新企业进行专利布局,其中无论是申请数量还是授权数量,已经能与国外企业形成均衡态势。(4)该领域的研究成果中,对于发明主题涉及涉及核酸和蛋白标志物的试剂盒以及载体、基质、试剂的专利申请,既有利于获得授权,同时在专利运营过程中具有较低的生产成本和诊断准确率高的优点,易于获得市场认可。因此,在国外MALDI TOF MS产品的专利技术垄断的情况下,属于难得的专利申请空白,值得国内科技创新企业引起关注。
3.2建议 为全面贯彻十九大报告提出的“实施健康中国战略”的精神,同时响应“中国制造 2025”的发展规划,坚持创新驱动、智能转型、强化基础、绿色发展,加速我国在应用MALDI TOF MS临床诊断新技术的发展,为人民群众提供全方位全周期的健康服务,可以从以下几方面进行努力。(1)鼓励国内企业和科研院所利用我国临床样本资源丰富的优势,积极投入MALDI TOF MS临床诊断致病微生物的研究,不断提高自身的技术创新能力,研发一系列针对中国人特有的微生物病症的诊断技术,并积极申报专利申请,实现专利保护。(2)国家及地方政府在科研政策、市场采购、专利资助、知识产权保护等方面出台相关政策,以鼓励国内申请人积极抢占技术制高点,推进诊断技术的创新,为将来国外专利进入中国诊断市场而提前做好准备。(3)国内企业和科研院所要不断努力拓展MALDI TOF MS临床诊断致病微生物的新领域,并根据中国现阶段的国情,例如微生物对环境和食品安全的影响的检测需要,积极研发和申报关于非诊断目的的检测微生物的专利方法申请,从而获得更为全面的专利保护力度。(4)根据该技术需要大样本的微生物标准指纹质谱图谱数据的特点,利用互联网将众多医院、检疫机构的微生物标准数据样本进行共享,并通过大数据技术进行处理分析,从而研发出一系列“互联网+”的质谱诊断技术和相关产品,并积极进行国内外专利布局,以实现我国在该诊断领域中“弯道超车”。(5)在承接成熟的MALDI TOF MS质谱诊断微生物的基础上,将实验数据的处理分析与人工智能结合,形成MALDI TOF MS智慧质谱(即MALDI TOF MS智谱)诊断微生物技术。该智谱技术极大提高了谱图稳定性与谱库分辨率,并智能读取质谱产生的数据并做出判定,实现了效率的极大提升,大量节省了医疗成本[11]。
