喜炎平注射液治疗儿童呼吸道合胞病毒肺炎有效性及安全性的Meta分析
2019-09-05马明星王雪峰张秀英李林峰姜俊爽宋立超
马明星, 王雪峰, 张秀英, 李林峰, 姜俊爽, 宋立超
呼吸道合胞病毒肺炎系儿童常见的间质性肺炎之一,临床多表现为发热、咳嗽、咳痰、喘息等症状,尤以6个月以下婴儿最为常见[1]。本病如不及时控制,严重时可引起心力衰竭,进而危及患儿生命[2]。临床上对此病治疗尚无特效药物,有研究发现喜炎平注射液在防治儿童病毒性肺炎中有显著优势[3]。近年来喜炎平注射液临床应用于儿童呼吸道合胞病毒肺炎的研究越来越多,但尚缺乏较系统的Meta分析对其疗效及安全性进行评价。因此,开展本研究,对喜炎平注射液治疗儿童呼吸道合胞病毒肺炎的有效性及安全性进行Meta分析,以期为其临床应用提供依据。
1 资料与方法
1.1 纳入标准 (1)临床随机对照试验,语种不限;(2)研究对象:均符合《实用儿科学》中呼吸道合胞病毒肺炎诊断标准[4];(3)干预措施:治疗组采用喜炎平注射液,对照组采用常规治疗;(4)纳入患者无其他合并疾病;(5)疗效评价主要结局指标包括:总有效率(痊愈率+显效率+有效率)、住院时间、不良反应情况,次要结局指标包括:退热时间、咳嗽消失时间、肺部啰音消失时间、胸片炎症吸收时间及治疗后的血清炎性因子水平。
1.2 排除标准 (1)动物实验或临床药动学研究或综述;(2)重复发表的文献;(3)联合采用其他药物治疗;(4)非静脉注射给药;(5)无法获取有效数据。
1.3 检索策略 计算机检索CNKI、VIP、CBM、Wanfang Data、PubMed、Web of Science、EMbase及The Cochrane Library,检索时限均为建库至2019年4月30日。同时,手工检索纸质期刊及会议论文等灰色文献,以补充获取相关文献。中文检索词为“喜炎平”“呼吸道合胞病毒肺炎”;外文检索词为“Xiyanping”“Respiratory syncytial virus pneumonia”“RSV pneumonia”,根据不同数据库的检索特征使用主题词联合自由词的方法进行检索。
1.4 文献筛选和资料提取 文献筛选和资料提取均由2名研究员严格按照检索方法、纳入标准、排除标准独立进行。纳入及筛选的过程中如遇分歧则进行讨论决定,如仍不能解决则引入第三方进行讨论后仲裁。文献筛选时首先通过检索获得文献,再选用NoteExpress软件进行查重与去重,最后依次通过阅读题目、摘要及全文,确定最终是否纳入。使用Excel软件设计文献信息提取表,主要内容为:(1)基本信息:研究题目、第一作者、时间等;(2)研究类型和偏倚风险评价;(3)干预措施;(4)结局指标。
1.5 纳入研究的偏倚风险评价 2名研究员使用Cochrane协作网针对随机对照试验制定的偏倚风险评估工具进行评价。主要评价内容有:随机序列的产生、分配隐藏、是否盲法及盲法形式、结果数据完整性、选择性报告偏倚和其他可能的偏倚风险。最终对各指标做出“低风险”“高风险”“不确定”的评价。
1.6 统计学方法 采用Cochrane协作网提供的RevMan 5.3软件进行Meta分析。计数资料采用相对危险度(RR)表示,计量资料采用均数差(MD)表示,效应量采用95%CI表示。采用I2检验进行异质性分析,纳入结果异质性较小(I2≤50%,P>0.1)时采用固定效应模型分析;反之,存在较大异质性进行敏感性或亚组分析,明确异质性原因,再采用随机效应模型分析。对于不能合并的资料,用定性描述。采用倒漏斗图分析文献是否存在潜在的发表偏倚。
2 结果
2.1 文献检索 数据库及其他途径初步检出64篇相关文献,经去重和筛选排除不符合纳入标准的文献,本研究最终纳入9个RCTs。见图1。
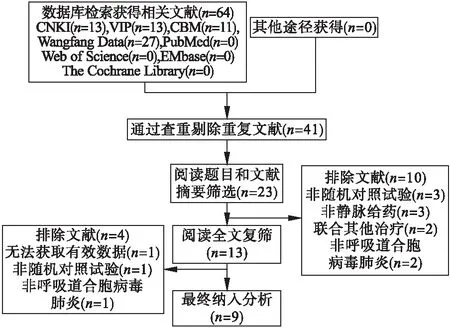
图1 文献检索流程图
2.2 纳入研究的基本特征及文献质量评价 共纳入9个研究[5-13],686例呼吸道合胞病毒肺炎患儿。所有文献均描述基线可比。1个研究[6]未详细记录患儿性别。纳入文献仅有3个研究[5,8,12]提及采用“随机数字表法”,所有研究均未提及随机化隐藏、是否盲法等方面。5个研究报告患者均签署知情同意书[5-6,9,12-13],所有研究均未报告有脱落情况。纳入研究的基本特征见表1,偏倚风险评价见表2。
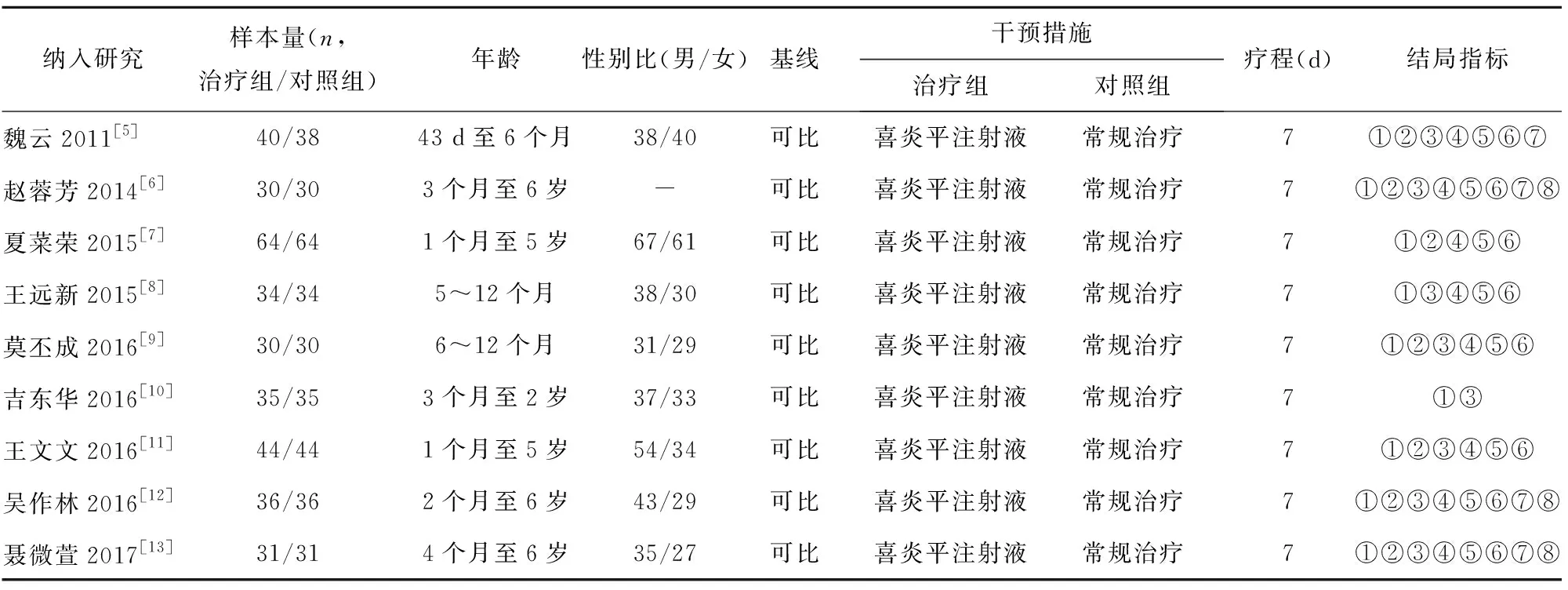
表1 纳入研究基本特征
注:①总有效率,②住院时间,③不良反应情况,④退热时间,⑤咳嗽消失时间,⑥肺部啰音消失,⑦胸片炎症吸收时间,⑧血清炎性因子分析
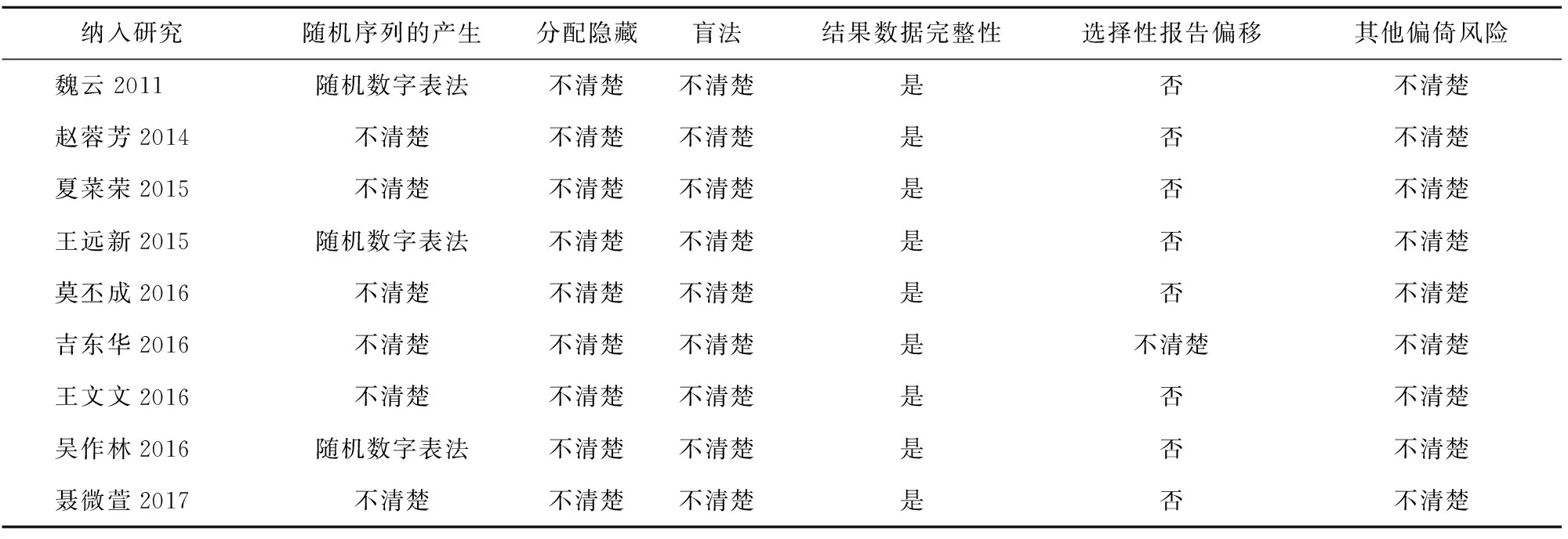
表2 纳入文献偏倚风险评价
2.3 Meta分析
2.3.1 主要结局指标
2.3.1.1 总有效率 纳入的9个研究均记录了总有效率,共686例患儿,其中喜炎平注射液组344例,常规治疗组342例。异质性检验分析显示,各研究无异质性(I2=0%),可采用固定效应模型合并。Meta分析结果显示,两组差异有统计学意义[RR=1.18,95%CI(1.12,1.25),P<0.000 01],提示喜炎平注射液治疗儿童呼吸道合胞病毒肺炎的总有效率高于对照组。见图2。
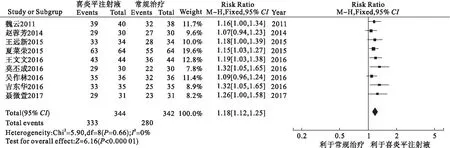
图2 总有效率的Meta分析森林图
2.3.1.2 住院时间 7个研究记录了住院时间,共548例患儿,其中喜炎平注射液组275例,常规治疗组273例。异质性检验分析显示,各研究存在较大异质性(I2=94%),可采用随机效应模型合并。Meta分析结果显示,两组差异有统计学意义[MD=-3.01,95%CI(-3.82,-2.61),P<0.000 01],提示喜炎平注射液治疗儿童呼吸道合胞病毒肺炎的住院时间显著短于对照组。见图3。
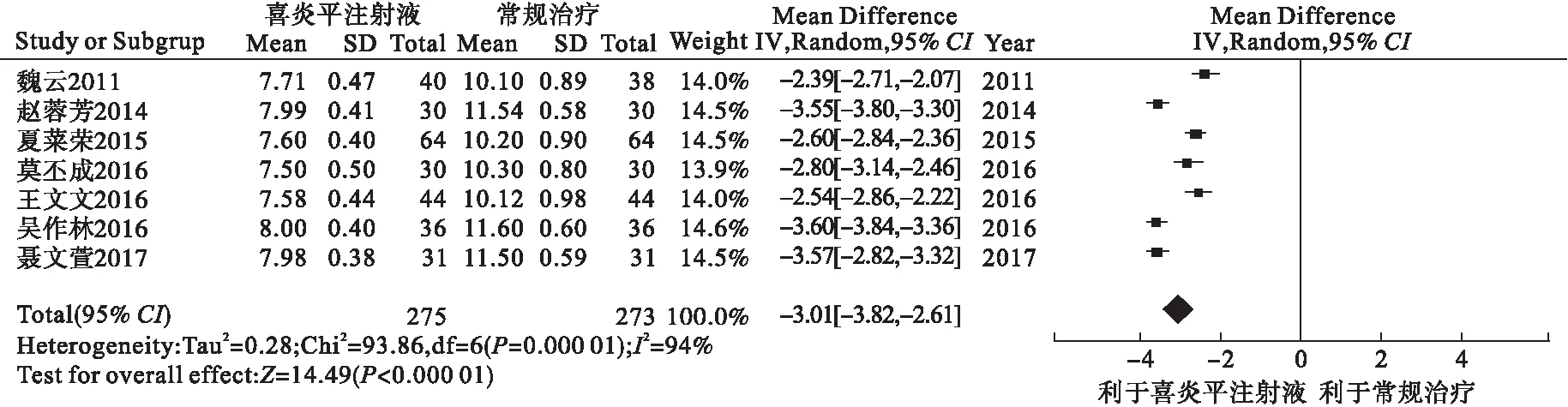
图3 住院时间的Meta分析森林图
从图3森林图可以看出,有3个研究[6,12-13]与其他4个研究有明显异质性,追溯原文发现,此3个研究试验组用量与其他4个有明显差异,剔除3个研究后,将其他4个研究重新分析显示[MD=-2.58,95%CI(-2.73,-2.43),I2=3%,P<0.000 01]。
2.3.1.3 不良反应发生率 8个研究报道不良反应发生情况,其中1个研究[10]报道两组均无严重不良反应发生,对不良反应发生情况描述不准确,故排除。最终对7个研究进行分析,共470例患儿,其中喜炎平注射液组236例,常规治疗组234例。异质性检验分析显示,各研究无异质性(I2=0%),可采用固定效应模型合并。Meta分析结果显示,两组差异有统计学意义[MD=0.45,95%CI(0.25,0.82),P<0.010],提示喜炎平注射液治疗儿童呼吸道合胞病毒肺炎的不良反应发生率低于对照组。见图4。

图4 不良反应情况的Meta分析森林图
2.3.2 次要结局指标
2.3.2.1 退热时间 8个研究记录了退热时间,共616例患儿,其中喜炎平注射液组309例,常规治疗组307例。异质性检验分析显示,各研究存在较小异质性(I2=36%),可采用固定效应模型合并。Meta分析结果显示,两组差异有统计学意义[MD=-1.11,95%CI(-1.22,-1.00),P<0.000 01],提示喜炎平注射液治疗儿童呼吸道合胞病毒肺炎的退热时间短于对照组。见图5。
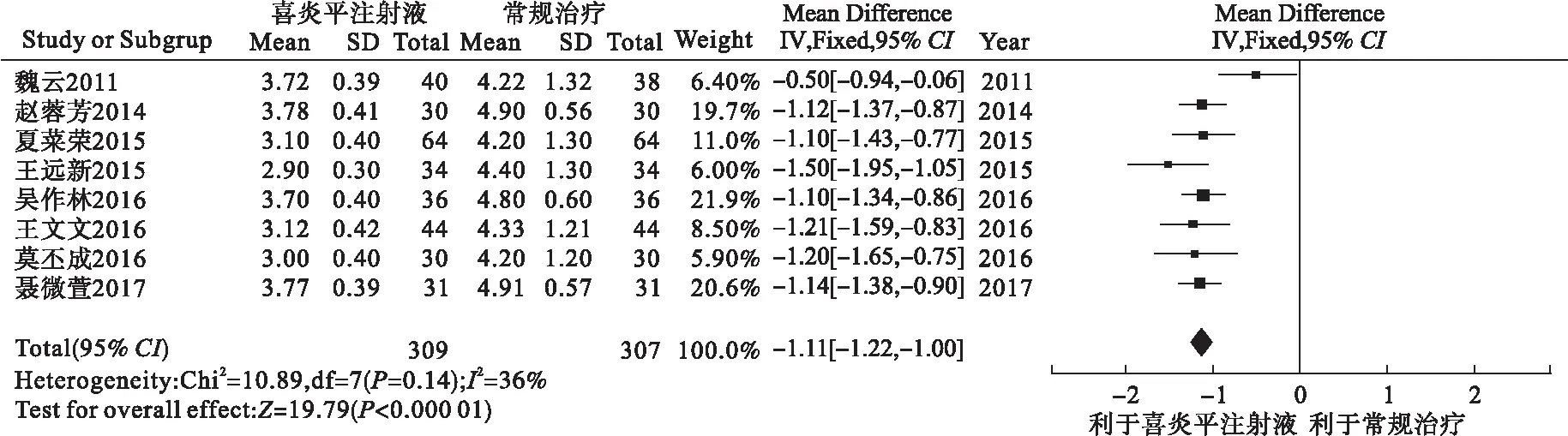
图5 退热时间的Meta分析森林图
2.3.2.2 咳嗽消失时间 8个研究记录了咳嗽消失时间,共616例患儿,其中喜炎平注射液组309例,常规治疗组307例。异质性检验分析显示,各研究存在较大异质性(I2=86%),可采用随机效应模型合并。Meta分析结果显示,两组差异有统计学意义[MD=-1.02,95%CI(-1.14,-0.91),P<0.000 01],提示喜炎平注射液治疗儿童呼吸道合胞病毒肺炎的咳嗽消失时间短于对照组。见图6。
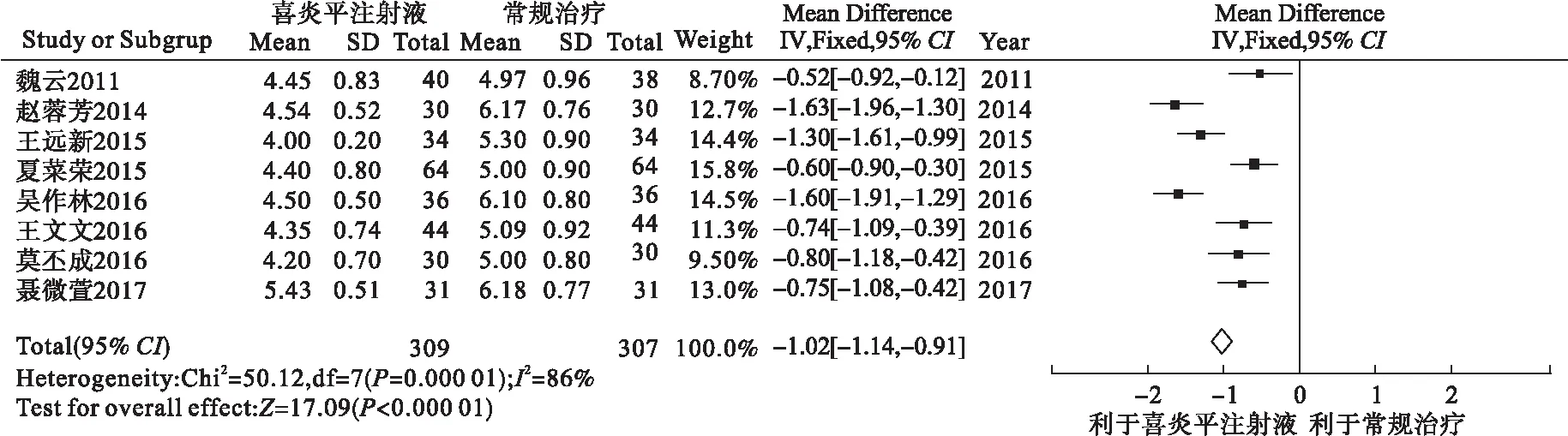
图6 咳嗽消失时间的Meta分析森林图
从图6森林图可以看出,有3个研究[6,8,11]与其他5个研究有明显异质性,追溯原文,未发现产生异质性原因,故无法进行敏感性分析。
2.3.2.3 肺部啰音消失时间 8个研究记录了肺部啰音消失时间,共616例患儿,其中喜炎平注射液组309例,常规治疗组307例。异质性检验分析显示,各研究有异质性(I2=94%),可采用随机效应模型合并。Meta分析结果显示,两组差异有统计学意义[MD=-1.34,95%CI(-1.63,-1.06),P<0.000 01],提示喜炎平注射液治疗儿童呼吸道合胞病毒肺炎的肺部啰音消失时间短于对照组。见图7。从森林图可以看出,有1个研究[5]与其他7个研究有明显异质性,追溯原文发现,此研究试验组年龄与其他7个研究中年龄有明显差异,剔除此研究后,将其他7个研究重新分析显示[MD=-1.50,95%CI(-1.60,-1.39),I2=2%,P<0.000 01]。
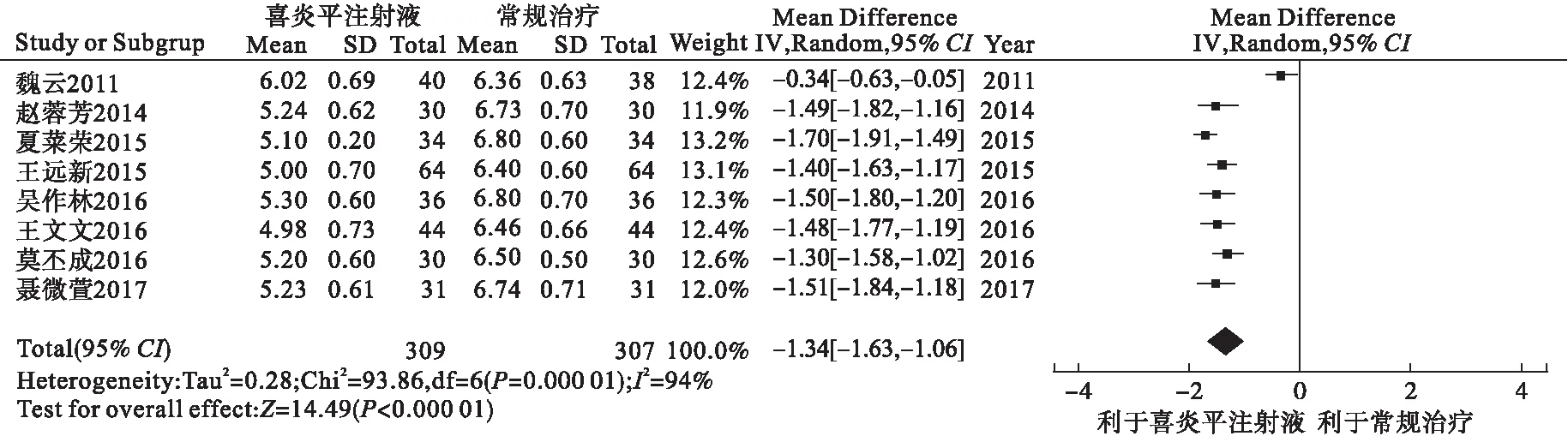
图7 肺部啰音消失时间的Meta分析森林图
2.3.2.4 胸片炎症吸收时间 4个研究记录了胸片炎症吸收时间,共272例患儿,其中喜炎平注射液组137例,常规治疗组135例。异质性检验分析显示,各研究存在较小异质性(I2=25%),可采用固定效应模型合并。Meta分析结果显示,两组差异有统计学意义[MD=-1.21,95%CI(-1.39,-1.04),P<0.000 01],提示喜炎平注射液治疗儿童呼吸道合胞病毒肺炎的肺内炎症吸收快于对照组。见图8。
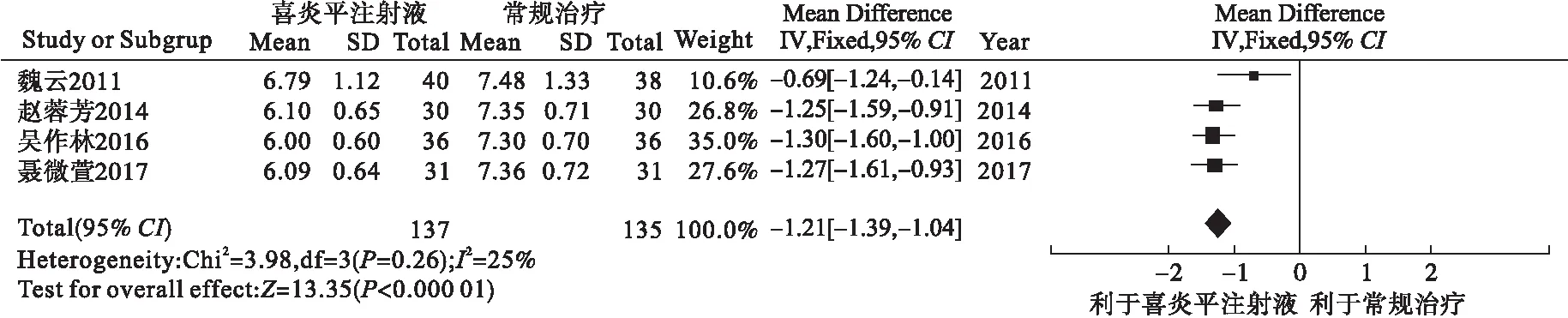
图8 胸片炎症吸收时间的Meta分析森林图
2.3.2.5 血清炎性因子水平 3个研究记录了治疗前后的血清炎性因子(IL-6、IL-8及TNF-α)水平,对治疗后的IL-6、IL-8及TNF-α水平进行亚组分析,异质性检验显示,各研究均无异质性(I2=0%),可采用固定效应模型分析。Meta分析结果显示,治疗后IL-6、IL-8及TNF-α水平分别为[MD=-7.79,95%CI(-9.48,-6.10),I2=0%,P<0.000 01]、[MD=-4.39,95%CI(-5.50,-3.28),I2=0%,P<0.000 01]及[MD=-15.59,95%CI(-17.03,-14.16),P<0.000 01],差异均具有统计学意义。提示喜炎平注射液治疗儿童呼吸道合胞病毒肺炎后血清炎性因子水平低于对照组,即喜炎平更能有效控制机体的炎性反应。见图9。
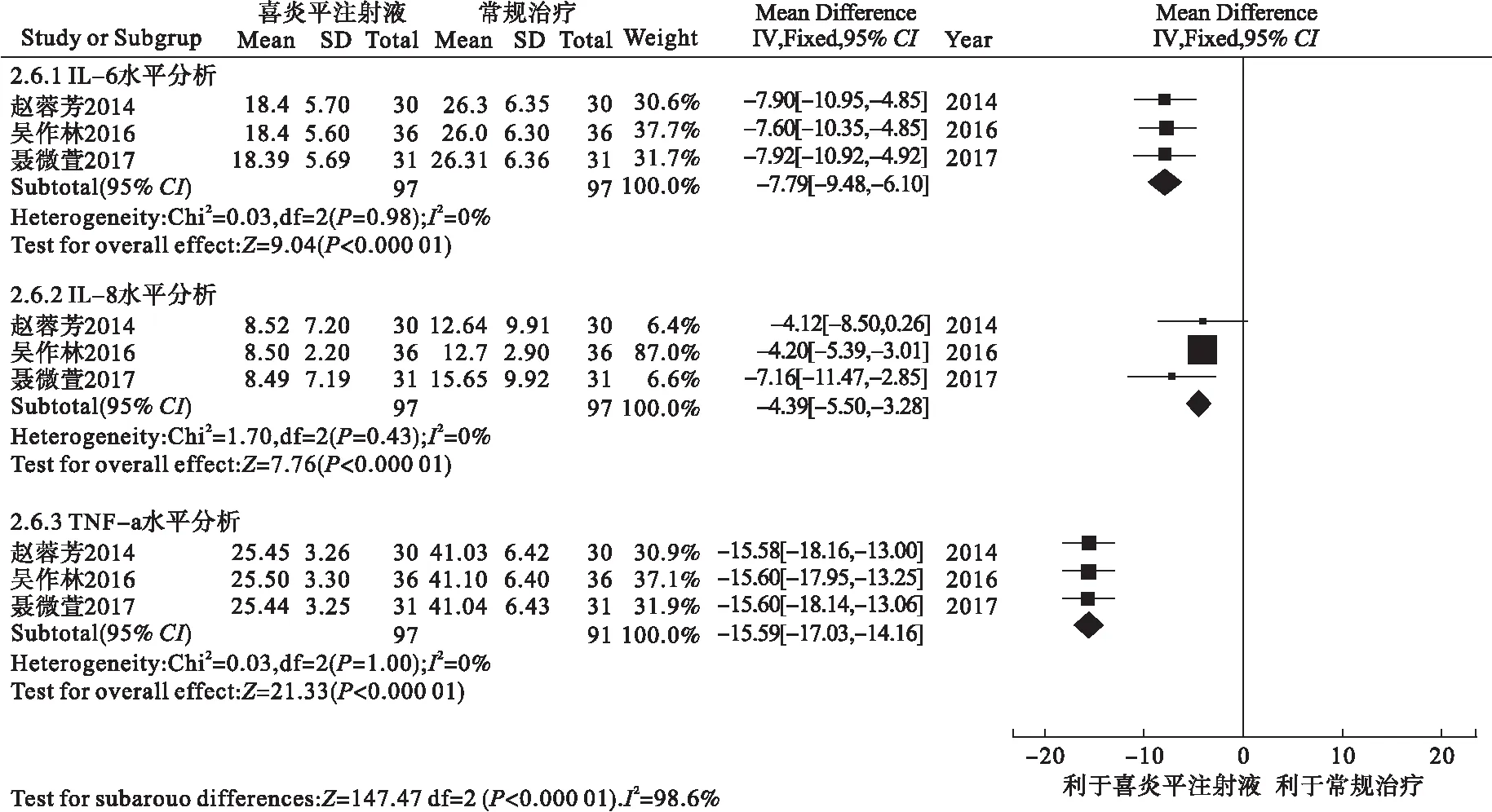
图9 治疗后IL-6水平分析的Meta分析森林图
2.4 发表偏倚 分别以纳入研究的RR值为横坐标,以SE[log(RR)]为纵坐标,对喜炎平注射液治疗儿童呼吸道合胞病毒肺炎的总有效进行漏斗图分析,发现其显示不对称,提示可能存在发表偏倚,阴性结果的试验可能未发表。见图10。
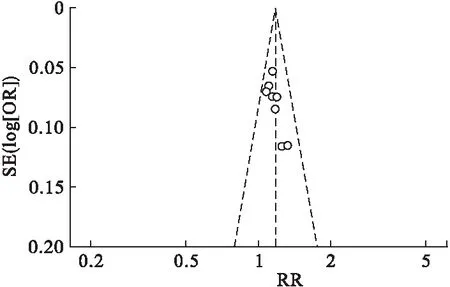
图10 总有效率的漏斗图
3 讨论
3.1 研究结果分析及临床价值 呼吸道合胞病毒是一种RNA病毒,通过与跨膜蛋白发生作用,使Th1/Th2失衡,在患儿下呼吸道位置产生免疫性损伤[14]。临床上常由空气飞沫或密切接触的形式进入口鼻,进而侵入肺部形成呼吸道合胞病毒肺炎。西药治疗该病常用利巴韦林等抗病毒药物,临床发现此类药物治疗疗效不佳,且不良反应多。有研究发现,中医清热解毒类注射剂在治疗儿童病毒性肺炎中有明显疗效及特色,且疗效均以喜炎平最佳[3]。喜炎平注射液属于穿心莲的中药提纯剂,穿心莲内酯磺化物是其主要成分,具有疏风清热、凉血解毒的功效。近年来研究表明喜炎平注射液的药理作用有以下特点:(1)抗病毒作用,喜炎平能够阻碍病毒组装过程中DNA与蛋白质的结合,调节体液免疫和细胞免疫,达到直接抑制病毒生存和繁殖作用[15]。(2)可加快退热速度,王云等[16]认为喜炎平具有调节体温的功效,可能与IL-12、TNF-α等血清炎性因子的释放减少有关。(3)良好的止咳、祛痰作用,喜炎平能通过舒张气道平滑肌,缓解平滑肌痉挛,抑制腺体分泌,从而发挥止咳、祛痰作用[17]。(4)避免过度抗炎反应,改善其免疫功能,本药能有效抑制体内促炎、抗炎因子过度释放,使TNF-α、IL-6和IL-8因子在机体内达到平衡状态,改善其免疫功能[18]。(5)本药能够有效抑制和杀灭大多数革兰阳性菌和阴性菌,有较高的广谱抗菌效应,且不良反应较少[19]。
本研究采用循证医学的方法,对喜炎平治疗儿童呼吸道合胞病毒肺炎的有效性及安全性进行了Meta分析。通过文献检索及筛选,最终纳入9个研究,686例患者。Meta分析结果显示,喜炎平注射液与常规治疗儿童呼吸道合胞病毒肺炎相比,前者在有效性方面,可以明显提高总有效率,显著缩短住院时间,同时可缩短退热时间、咳嗽消失时间及肺部啰音消失时间,加快胸片炎症吸收时间,降低血清炎性因子水平;在安全性方面,本药不良反应发生率较低。以上数据充分说明了喜炎平在治疗儿童呼吸道合胞病毒性肺炎中发挥良好的应用效果,这与谢辉辉等[20]的研究结果相似。
3.2 不良反应 本研究中共8个研究报道了不良反应发生情况,其中1个研究不良反应描述不准确无法统计。故对7个研究的不良反应进行Meta分析,最终统计不良反应共45例,喜炎平组14例,常规治疗组31例。分析证明喜炎平注射液应用于儿童呼吸道合胞病毒性肺炎治疗时,不良反应发生率低于对照组。喜炎平组14例不良反应中涉及胃肠道症状6例,皮肤瘙痒4例,未详细记录过敏反应4例。常规治疗组31例不良反应中涉及皮疹5例,胃肠道症状14例,贫血6例,未详细记录过敏反应6例。两组治疗中不良反应情况均以胃肠道症状居多,提示临床治疗时应注意防范胃肠道症状。以上8个研究中均未出现严重的不良反应,且其不良反应均可自行消退或对症处理后消失。儿童脏器发育尚未成熟,对药物的吸收、分布、代谢及排泄能力较差,临床用药易出现不良反应[21-22],故儿童用药的药量和给药方式需谨慎对待。
3.3 展望 本研究证明了喜炎平注射液应用于儿童呼吸道合胞病毒性肺炎治疗时,其有效性及安全性均优于常规治疗,但本研究仍存在一定局限性:(1)方法学质量上,纳入的9篇文献提及随机分配,但其中6篇文献未详细描述随机分组方法,只有3篇文献使用了正确的“随机数字表法”,易导致选择性偏倚;且所有研究均未提及分配隐藏和盲法,易导致选择性和实施偏倚。(2)均未报告研究方案注册及样本量估算等情况。(3)所有研究均未报告有脱落情况。(4)本研究中仅1篇文献样本量≥100,大部分研究因样本量少,可能造成疗效指标不稳定。(5)根据漏斗图呈非对称性分布显示,存在潜在的发表偏倚。
综上所述,喜炎平注射液治疗儿童呼吸道合胞病毒肺炎有效性及安全性均优于常规治疗,能明显提高临床总有效率,显著缩短住院时间,改善症状体征,降低不良反应发生率。但纳入文献数量及质量有限,还需开展更多大样本、高质量的随机对照试验对其有效性及安全性予以验证。
