生物滤池同步净化低温高铁锰氨氮地下水
2019-08-28王刘煜曾辉平
王刘煜,李 冬*,曾辉平,张 杰,2
生物滤池同步净化低温高铁锰氨氮地下水
王刘煜1,李 冬1*,曾辉平1,张 杰1,2
(1.北京工业大学水质科学与水环境恢复工程北京市重点试验室,北京 100124;2.哈尔滨工业大学城市水资源与水环境国家重点试验室,黑龙江 哈尔滨 150090)
为实现低温(5~6℃)高铁锰氨氮[TFe:9~15mg/L,Fe2+:6~12mg/L,Mn2+:0.8~1.2mg/L,NH3-N:0.9~1.4mg/L]地下水的生物同步净化,以水厂实地滤柱进行实验.结果表明,在该种水质下,以1.0,3.0m/h滤速启动生物滤柱,分别历经128,91d启动成功.铁和氨氮自启动之初出水即合格,锰的去除仍然是滤池成熟的决定性因素.溶解氧(DO)充足条件下,净化所需滤层厚度随氨氮浓度的升高而加厚,氨氮极限去除浓度为1.60mg/L.进水DO不足是限制氨氮继续提升的主要因素.滤速越大,锰的去除量越少,净化所需滤层越厚,滤柱极限运行滤速为8.0m/h.沿程分析发现,铁和锰的氧化去除存在显著分级,铁和氨氮在滤层内可同步氧化去除,锰的高效氧化去除区间相对滞后.
低温;高铁锰氨氮;地下水;同步净化;溶解氧;滤层厚度
目前,很多国家和地区的地下水中均存在不同程度的铁锰污染[1].铁锰过量会危害人体健康[2].生物除铁除锰工艺因运行成本低、操作简单、可以同步去除铁锰等优势[3],在国内外工程中得到广泛应用[4-5],但处理的原水水温多在12℃以上[6-7],关于我国东北高寒地区低温地下水的生物除铁除锰研究鲜有报道.温度会显著影响生物酶的催化氧化速率和基质传递到细胞的速率,温度越低,锰氧化菌(MnOB)除锰活性越差[8].课题组前期研究[9]采用“一级曝气+一级过滤”工艺,经120d自然挂膜,成功实现了低温高铁锰(T:5~6℃,TFe:10~14mg/L,Fe2+: 8~ 10mg/L,Mn2+:0.8~1.2mg/L)地下水的同步净化去除,但是近年来,受高浓度氨氮污染的地下水及土壤通过渗流、雨淋等作用补给地下水,造成地表水氨氮浓度不断升高[10],由于铁锰氨的氧化去除是以DO(溶解氧)为电子受体的氧化还原过程,氨氮的升高势必会大量消耗水体中的DO,而影响锰的去除效果.所以对于哈尔滨(水温7~9℃)、佳木斯(水温5~6℃)等地的低温高铁锰氨氮地下水而言,滤池的快速启动及铁锰氨的同步高效去除是需要解决的难题.本实验立足于以上背景,在佳木斯某水厂搭建中试试验装置,探究了该水质(:5~6℃,TFe:9~15mg/L,Fe2+:6~ 12mg/L,NH3-N:0.9~1.4mg/L,Mn2+:0.8~1.2mg/L)条件下滤池的快速启动和净化规律,并优化滤层厚度和运行滤速,以期为低温高铁锰氨氮复合污染地下水的生物净化和实际生产提供技术支持.
1 材料与方法
1.1 实验装置
实验装置如图1所示,以有机玻璃滤柱模拟生产滤池,直径200mm,高3000mm,装填双层滤料,装填总高度1500mm,上层为无烟煤滤料,厚度300mm,级配1.0~1.2mm;下层为锰砂滤料,厚度1200mm,级配0.6~1.2mm;承托层采用鹅卵石,级配1.8~20mm,厚度300mm;另设有取样口和取砂口.

图1 实验装置示意
1.2 实验水质
实验前期进水采用水厂跌水曝气后原水:TFe 9~15mg/L,Fe2+6~12mg/L,NH3-N 0.9~1.4mg/L,Mn2+0.8~1.2mg/L,根据实验目的与方法,实验后期用蠕动泵添加适量硫酸铵配置成反应器进水,NH3-N: 1.4~2.3mg/L,pH:6~7,水温:5~6℃DO:9.10~9.30mg/L.实验水质属于罕见的低温高铁锰氨氮地下水.
1.3 实验方法
两根滤柱R1、R2分别以1.0,3.0m/h的滤速启动,根据出水水质提高滤速,每次提升1.0m/h,当滤速下降至无法调节时进行反冲洗,滤速达到水厂运行滤速6.0m/h,出水水质合格并稳定超过7d,即视为生物滤柱启动成功[11].后续进行提速培养和浓度提升,期间适当调整反冲洗强度和时间.实验进程中,通过沿程分析,明晰铁锰氨的去除区位,对培养方式和滤层厚度进行优化.
1.4 分析项目及方法
按照《生活饮用水标准检验方法》(GB5750- 2006)规定[12],分别采用邻菲罗啉分光光度法、过硫酸铵分光光度法、纳氏试剂分光光度法、N-(1-奈基)-乙二胺光度法、紫外分光光度法检测铁、锰、氨氮、亚硝酸盐氮、硝酸盐氮浓度. DO、pH值(温度)、的测定使用便携式测定仪(Qxi 315i-WTW).为了确保数据的准确性,反冲洗4h以后进行取样,每次测量设置3组平行实验.空床接触时间(EBCT)和进水锰负荷分别用式(1)、式(2)计算;锰的氧化动力学方程如式(3)所示:
(1)
L=´(2)

式中:为EBCT,min;为滤料装填高度,m;此处为定值1.5;为滤柱的运行滤速,m/h;L为进水锰负荷,单位为g/(m2∙h);为锰进水质量浓度,mg/L;0为锰氧化动力学系数.
2 结果与讨论
2.1 生物滤柱的快速启动
如图2所示, Fe2+的去除不存在启动期,自第1d起R1、R2的出水铁均达标,但R2出水Fe2+浓度初始几天里稍高于R1,分析认为滤料刚装填入滤柱,滤层结构尚不稳定,对污染物的截留性能稍差,R2的滤速较大,所以表现的更加明显.但在整个启动期均远低于国家饮用水标准限值,似乎并未受到低温环境和启动滤速的影响,验证了铁主要通过化学氧化作用去除[13].

滤料对NH3-N具有较好的吸附作用,初始一段时间里R1、R2对氨氮去除效果良好, 氨氮主要依靠物理吸附去除,但滤料的吸附位点有限[14],滤料的吸附能力逐渐趋于饱和,由于R2的进水氨氮负荷远高于R1,所以R2更早的达到吸附饱和,而此时生物硝化去除NH3-N的进程尚未培养成熟,所以出水NH3-N逐渐升高,出水水质持续恶化,且受进水水质影响而波动较大.此后,随着培养时间的延长,生物的硝化作用逐渐增强,代替物理吸附成为NH3-N主要去除途径.R2的滤速高于R1,反冲洗周期短于R1,较为频繁的反冲洗不利于硝化菌的生长繁殖,所以R2的生物硝化成熟过程稍长于R1.每次滤速提升后的几天里出水波动, NH3-N质量浓度升高,这可能是因为滤速增大,水流剪切力增大,滤料表面的部分硝化细菌脱落,又由于滤速增大,氨氮负荷增大,生物量不足所致,亦有可能是因为滤速增大, EBCT缩短,硝化反应时间缩短所致,但是当培养一段时间后,氨氮的去除效果又恢复至之前水平,说明跟硝化反应时间缩短无关,主要受滤速提升, NH3-N负荷增大,生物量不足影响.另外,R1出水波动大于R2,分析认为R2启动滤速较大,滤柱在高滤速下运行一段时间后,老化的硝化细菌脱落,耐滤速冲击强的硝化细菌得到驯化富集,生物量达到新的平衡,高氨氮负荷条件下,中下部滤层成熟,滤料表面披覆的生物量增加,受水流剪切力影响相对较小,抗滤速冲击能力优于R1,所以能更快适应滤速的提升.
滤料对锰同样具有吸附作用,自启动之初R1、R2出水锰便降至痕量,滤柱对锰的去除率高达100%,滤料对锰的吸附去除表现良好.但是分别自24d、16d起,R1、R2出水锰开始超标,并且随着滤料对锰的吸附能力逐渐趋于饱和,出水水质持续恶化,出水锰浓度逐渐升高,但在此过程中滤料表面的MnOB逐渐生长繁殖和富集,生物固锰除锰逐渐发挥效能,R1、R2分别自39,34d起出水锰浓度反转降低,并逐渐降至国家饮用水卫生标准限值以下.实验后期,每次滤速提升出水水质虽略有波动,但R1、R2出水锰连续49d、23d均合格,抗冲击负荷能力较强,MnOB进入第二活性增长期[15].
为进一步明晰培养过程中R1、R2生物滤层的成熟情况及启动时间的差异,对二者的除锰、除氨氮耗氧量进行核算.在生物滤层中,铁锰氨的氧化去除都是在pH值约为6~7的中性条件下进行的,DO消耗量可根据氧化还原反应中的电子得失计算得到,除铁理论耗氧量为Fe=0.143[Fe2+][16].由图2可知,R1、R2分别自24d、16d起,出水Mn2+开始超标, NH3-N质量浓度也逐渐升高,因此认为24d、16d之前滤料吸附容量
未达到饱和,假设24d、16d之前Fe2+在2个滤柱中全部通过化学接触氧化去除,Mn2+和NH3-N全部由物理吸附去除,即Mn2+和NH3-N耗氧量为0,分别对24d、16d之前2个滤柱的实际DO消耗量取平均值平均,作为水中Mn2+和NH3-N外的铁和其他还原物质实际消耗的DO量,则锰和氨氮实际耗氧量为=[O2]实际-平均,其中[O2]实际为滤柱DO总的消耗量.
所得除锰、除氨氮耗氧量如图3所示,前期两个滤柱的除锰、除氨氮耗氧量与假设的0基本符合,只存在微小偏差,分析是由于每天的进水Fe2+波动较大,导致耗氧量取平均值之后,求出的氨氮和锰耗氧量出现负值和不为零的情况,但初期的趋势仍与之前的假设一致,佐证了前期氨氮和锰主要依靠滤料的物理吸附作用去除.随着培养时间的延长,两个滤柱的除锰、除氨氮耗氧量明显提高,生物硝化和生物固锰除锰作用逐渐加强,生物滤层渐渐趋于成熟.但注意到R2的除锰除氨氮耗氧量增长速率高于R1,亦更早的到达峰值并趋于稳定,分析是由于R2的启动滤速较大,较大的滤速将更多的DO及锰和氨氮带向了滤层深处,为MnOB和硝化细菌的生长繁殖提供了充足的基质,加速了中下部滤层的成熟.
上述实验表明,以达到水厂的设计滤速6m/h,并在该滤速下出水铁、锰和氨氮浓度连续达标7d为启动成功标准,通过对运行参数的调控,模拟生物滤柱R1、R2分别历时128d、91d,在水温5~6℃的高铁锰氨氮地下水质下实现了生物净化铁锰氨工艺的快速启动,R2相对R1启动滤速较大,启动时间缩短了1个月左右,相比兰西镇水厂, Fe2+含量为10~ 14mg/L, Mn2+含量为0.65~1.1mg/L,水温9℃左右,培养期缩短了5个月,课题组之前实验的鞍山、抚顺、长春地区的地下水温度在10℃以上, Fe2+含量仅为5~7mg/L, Mn2+含量为0.4~0.5mg/L,生物滤层的成熟期也在0.5~3个月之间[1].说明本实验的调控措施不仅在低温条件下成功实现了铁锰氧化细菌和硝化细菌的富集,在5~6℃的水温且高铁锰氨氮更为恶劣的条件下,启动工艺所用时间更短.
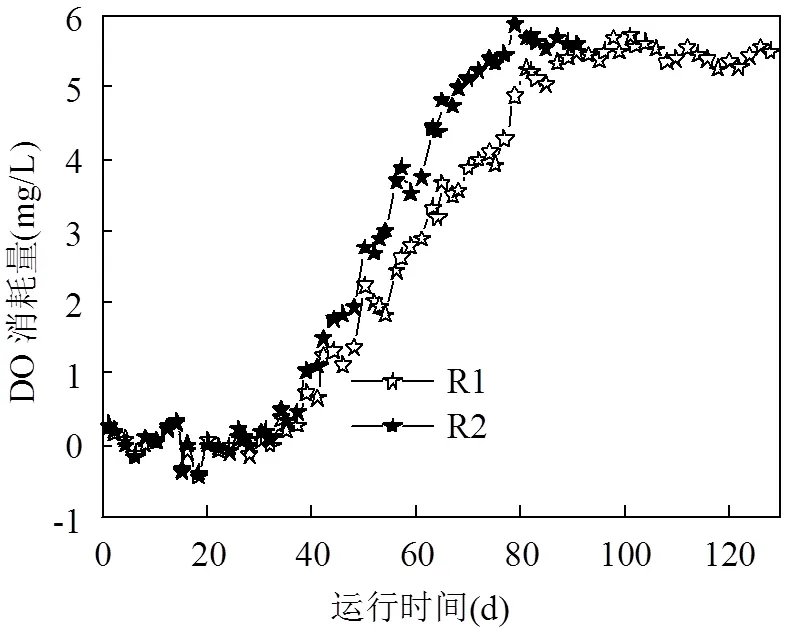
图3 DO消耗量
2.2 生物滤柱极限氨氮浓度与极限滤速探究
如2.1节所述,模拟生物滤柱实现了低温高铁锰氨氮地下水的快速启动,对铁锰氨净化效果良好.为了增加实验的普适性且进一步开发工艺的净水效能,对工艺的极限氨氮浓度与极限滤速进行了探究.如图4所示,在逐级提高氨氮浓度和滤速过程中,出水铁浓度未出现波动,滤柱对铁的氧化去除表现良好.说明铁的接触氧化速率很快,受氨氮浓度和滤速变化影响较小,在该水质条件下,铁不是运行滤速和氨氮浓度提升的限值因素.
自133d起,实验进水恢复为水厂曝气后原水,如图5所示,氨氮的去除效果良好,但出水锰依然超标,此时出水DO尚有富余,可见除锰恶化与DO无关,但经过一周左右的培养至143d,出水锰浓度下降至0.1mg/L以下.有研究认为,可能在高氨氮的负荷条件下,较大的滤速携带了大量的氨氮至滤层内锰的氧化去除区间,MnOB的活性受到抑制[18-20],而这一现象具有滞后性和积累效应[21],所以当氨氮负荷降低后,抑制作用并不会立刻解除,但经过一段时间的运行培养,抑制作用逐渐弱化,锰的去除效果恢复至较好水平.提升滤速至7.5m/h,出水连续一周合格,继续提升至9.0m/h,出水锰超标近2倍,在此工况下,连续培养了20d,出水锰浓度依然维持较高水平,调低滤速至8.0m/h,出水锰浓度再次达标,但已经接近0.1mg/L,至此认为,在该水质条件下,生物滤柱达到极限滤速8.0m/h.

图4 滤速提升过程中进出水铁浓度变化
整个提速培养过程,DO充足,出水锰超标与DO无关.不同滤速和EBCT条件下,滤柱稳定运行阶段,锰的平均去除量如表1所示,由于锰的去除遵循零级反应[22-23],锰的去除与进水锰浓度无关,出水锰浓度是时间的减函数,如式(3)所示.即锰的去除仅与EBCT有关.在6.0,7.5m/h条件下,虽然EBCT缩短,但锰的平均去除量却极为接近,似乎违背了锰的去除所遵循的零级反应规律.分析是由于式(3)用来表征锰在滤柱沿层都有去除即穿透滤层时才适用的,而此时锰尚未穿透滤层,滤层内MnOB含量丰富,滤柱的除锰性能良好,能完成锰的净化去除,出水锰合格.当滤速提升至9.0m/h后,此时锰穿透了滤层,锰的去除量下降,出水锰超标.降低滤速至8.0m/h,锰的平均去除量升高,但小于6.0和7.5m/h滤速下锰的平均去除量,出水锰浓度也趋近于达标线,此时滤柱已经达到极限滤速.综上,滤速增大,锰穿透滤层出水锰超标是限制滤速继续提升的主要因素.


表1 不同滤速和EBCT条件下锰去除量
本实验表明,在水温5~6℃,总铁9~15mg/L,锰0.8~1.2mg/L水质条件下,以水厂设计滤速6m/h运行模拟生物滤柱,氨氮的极限净化浓度为1.60mg/L,进水DO浓度是滤柱净化氨氮极限浓度多少的决定性因素;通入水厂原水,维持进水氨氮在0.9~1.4mg/L,逐级提升滤速,受滤速增大,锰穿透滤层所限,滤柱所能达到的极限滤速为8.0m/h.
2.3 铁锰氨氧化活性去除区位分析
2.3.1 质量浓度对铁锰氨氧化活性去除区位影响 铁、锰、氨氮各自发生氧化还原的电位值不同,分别为铁<200mV、200mV<氨氮<400mV、锰>400mV[24],因此铁优先在滤层中去除,且化学接触氧化速率较快,如图6所示,在滤柱的0~20cm段高效去除,在40cm处降至痕量,受氨氮浓度变化影响较小.氨氮的生物硝化反应过程和铁的化学接触氧化过程两者是相互独立的,滤层上部DO充足,氧分压较高,氨氮也在0~40cm段高效氧化去除.锰的氧化还原电位值较高,且高浓度的亚铁离子对锰具有还原作用[25],二者的高效氧化去除区间存在显著分级,在铁的高效去除段锰几乎没有去除,自40cm起,锰的去除速率才逐渐加快.图6中,随着氨氮浓度的升高,滤柱上部DO消耗量增加,滤层中下部氧分压降低,锰的氧化去除速率下降,滤柱出水达标深度也逐渐下移,所需滤层越厚.但当进水氨氮提高至较高水平,滤柱净化铁锰、氨氮需氧量大于进水DO时,低温高铁锰氨氮地下水的生物同步净化与滤柱内生物量无关,即与滤层厚度无关.在实际生产中,针对此类水质,建议采用喷淋等强曝气措施,尽可能的提升进水DO,且DO越高,氨氮和锰的去除越彻底,滤池的整体抗冲击负荷能力越强,运行也更加稳定.
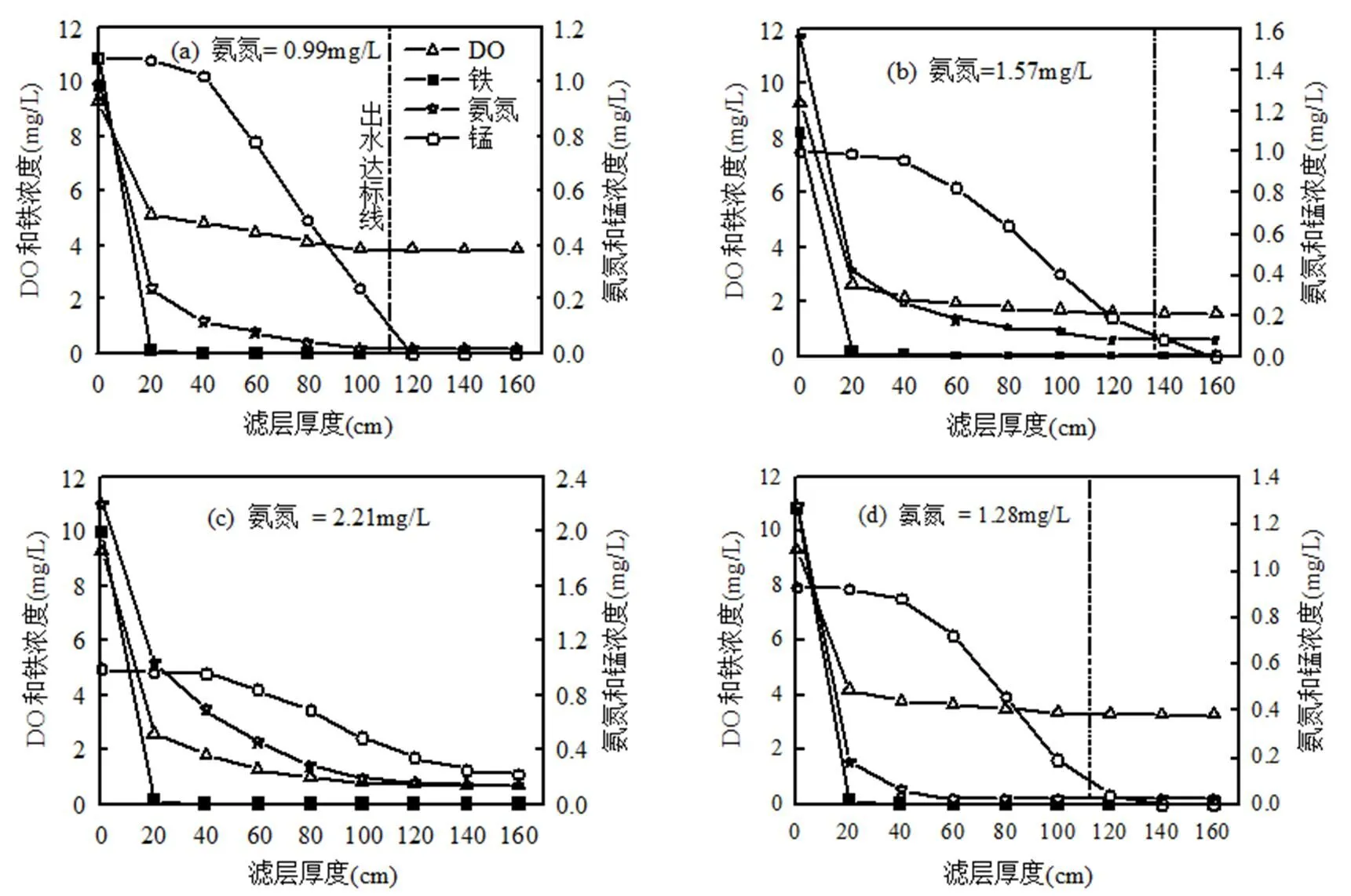
图6 不同水质铁锰氨沿程去除情况
2.3.2 滤速对铁锰氨氧化活性去除区位影响 铁的去除遵循化学氧化动力学规律,即氧化接触时间越长,铁的去除量越高,所以当EBCT由15min缩短为10min时,去除铁所需要的滤层厚度由20cm增加至60cm.滤速增大,生物对氨氮和DO的网捕利用率下降,氨氮去除速率下降,但进水DO充足,滤层中以铁、锰氧化菌为优势菌群的多种微生物群系构成的生态系统是一个不断趋于更加成熟与稳定的动态平衡的生态系统[18],滤柱的抗滤速负荷冲击能力较好,氨氮达标所需滤层厚度稍有增加.图7中,随着滤速的提升,在滤层的20,40cm处出现了锰浓度大于进水浓度的锰“溶出”现象,由2.3.1知, Fe2+对锰具有还原作用,锰的去除只能发生在Fe2+充分氧化之后,滤速提升,铁的氧化去除区间向滤层深处延伸,压缩了锰的高效氧化去除区间,高效去除起始位置向滤层深处位移了近40cm,直至滤层80cm处才开始大量去除,至8.0m/h时,直至承托层方才达标,此时,锰是滤速提升的限制条件,与2.2节研究一致.由图知,滤速越大,EBCT越小,锰的去除量越少,验证了锰的去除遵循零级反应规律,所以,在实际生产中,为了实现出水锰达标,可以通过增加滤层厚度,增大EBCT来实现.

图7 不同滤速铁锰氨氮沿程去除情况
3 结论
3.1 以1和3m/h滤速启动生物滤池均可实现低温高铁锰氨氮地下水的同池净化,分别经128,91d启动成功,后者的启动时间缩短了1月左右.锰的去除是滤池成熟的决定性因素.
3.2 在6m/h滤速工况下,氨氮的极限去除浓度受进水DO影响较大,为1.60mg/L,面对高浓度氨氮地下水,可以通过喷淋等强曝气措施来解决.DO充足条件下,滤速增大,锰的去除所需滤层厚度加厚,受锰穿透滤层所限,滤柱极限滤速为8.0m/h,实际生产中,适当增加滤层厚度可以提高锰的去除率.
3.3 铁锰氨的去除存在显著分级.DO充足条件下,铁和氨氮在滤层上部相互独立且同步去除.锰的高效去除带相对滞后,只有在亚铁去除至一定浓度时才开始大量去除.因此,实际生产中应尽量避免滤速突然的大幅提升.
[1] 张 杰,李 冬,杨 宏,等.生物固锰除锰机理与工程技术 [M]. 北京:中国建筑工业出版社, 2005. Zhang J, Li D, Yang H, et al. Biological manganese stabilization and removal mechanism and engineering technology [M]. Beijing: China Architecture & Building Press, 2005.
[2] 周鑫辉.饮用水生物氧化除锰特性、机理与动力学研究 [D]. 长沙:湖南大学, 2006. Zhou X H. Study on characteristics, mechanism and kinetics of biological oxidation and manganese removal from drinking water [D]. Changsha: Hunan University, 2006.
[3] 蔡言安,李 冬,曾辉平,等.生物滤池净化含铁锰高氨氮地下水试验研究 [J]. 中国环境科学, 2014,34(8):1993-1997. Cai Y A, Li D, Zeng H P, et al. Removal of iron, manganese and high ammonia from groundwater by biofilter [J]. China Environmental Science, 2014,34(8):1993-1997.
[4] Gouzinis A, Kosmidis N, Vayenas D V, et al. Removal of Mn and simultaneous removal of NH3, Fe and Mn from potable water using a trickling filter [J]. Water Research, 1998,32(8):2442-2450.
[5] Du X, Liu G, Qu F, et al. Removal of iron, manganese and ammonia from groundwater using a PAC-MBR system: The anti-pollution ability, microbial population and membrane fouling [J]. Desalination, 2016,403:97-106.
[6] Vries D, Bertelkamp C, Kegel F S, et al. Iron and manganese removal: recent advances in modelling treatment efficiency by rapid sand filtration [J]. Water Research, 2017,109:35-45.
[7] Tekerlekopoul A G, Vayenas D V. Ammonia, iron and manganese removal from potable water using trickling filters [J]. Desalination, 2007,210(1-3):225-235.
[8] Hoyland V W, Knocke W R, Falkinham J O, et al. Effect of drinking water treatment process parameters on biological removal of manganese from surface water [J]. Water Research, 2014,66:31-39.
[9] 李 冬,路 健,梁雨雯,等.低温生物除铁除锰工艺快速启动与滤速的探求[J]. 中国环境科学, 2016,36(1):82-86. Li D, Lu J, Liang Y W, et al. Quick start-up and filter speed searching of biological iron and manganese removal process [J]. China Environmental Science, 2016,36(1):82-86.
[10] 危润初,肖长来,梁秀娟.吉林市城区地下水污染时空演化 [J]. 中国环境科学, 2014,34(2):417-423. Wei R C, Xiao C L, Liang X J. Spatio-temporal evolution of groundwater pollution in the urban areas of Jilin city [J]. China Environmental Science, 2014,34(2):417-423.
[11] Isaka K, Date Y, Kimura Y, et al. Nitrogen removal performance using anaerobic ammonium oxidation at low temperatures [J]. FEMS Microbiol Lett, 2008,282(1):32-38.
[12] GB/T5750-2006 生活饮用水标准检验方法 [S]. GB/T5750-2006 Standard examination methods for drinking water [S].
[13] 白筱莉,黄廷林,张瑞峰,等.铁锰复合氧化膜同步去除地表水中氨氮和锰 [J]. 中国环境科学, 2017,37(12):4534-4540. Bai X L, Huang T L, Zhang R F, et al. The simultaneous removal of ammonium and manganese from surface water by iron-manganese co-oxides film [J]. China Environmental Science, 2017,37(12):4534- 4540.
[14] Cai Y A, Li D, Liang Y W, et al. Effective start-up bio-filtration method for Fe, Mn, and ammonia removal and bacterial community analysis [J]. Bioresource Technology, 2015,176:149-155.
[15] 李 冬,曹瑞华,曾辉平,等.高铁锰氨氮地下水净化试验及氧化动力学 [J]. 中国环境科学, 2017,37(11):4140-4150. Li D, Cao R H, Zeng H P, et al. Analysis of the removal and oxidation kinetics of high-iron manganese and ammonia nitrogen from groundwater [J]. China Environmental Science, 2017,37(11):4140- 4150.
[16] 曾辉平.含高浓度铁锰及氨氮的地下水生物净化效能与工程应用研究[D]. 哈尔滨:哈尔滨工业大学, 2010.Zeng H P. Biological purification of iron,manganese and ammonia with high concentration in groundwater and engineering application [D]. Harbin:Harbin Institute of Technology, 2010.
[17] GB5749-2006 生活饮用水卫生标准 [S]. GB5749-2006 Standards for drinking water quality [S].
[18] 程庆锋.高铁锰氨氮地下水净化工艺优化及菌群结构研究 [D]. 哈尔滨:哈尔滨工业大学, 2014. Cheng Q F. Optimization of purifying filter of groundwater containing high concentration of iron, manganese and ammonia and microbial community structure [D]. Haerbin:Harbin Institute of Technology, 2014.
[19] Tekerlekopoul A G, Vayenas D V. Simultaneous biological removal of ammonia,iron and manganese from potable water using a trickling filter [J]. Biochemical Engineering Journal, 2008,39(1):215-220.
[20] 蔡言安,李 冬,曾辉平,等.氨氮与亚硝酸盐对含铁锰地下水生物净化影响[J]. 哈尔滨工业大学学报, 2014,46(8):96-101. Cai Y A, Li D, Zeng H P, et al. Influence of ammonia and nitrite on performance of Fe and Mn removal by biofilter [J]. Journal of Harbin Institute of Technology, 2014,46(8):96-101.
[21] 李 冬,曹瑞华,杨 航,等.低温高铁锰氨氮地下水生物同池净化[J]. 环境科学, 2017,38(12):5097-5105. Li D, Cao R H, Yang H, et al. Removal of high concentration of iron, manganese and ammonia nitrogen from low temperature groundwater using single bio-filter [J]. Environmental Science, 2017,38(12):5097- 5105.
[22] Andersson A, Laurent P, Kihn A, et al. Impact of temperature on nitrification in biological activated carbon (BAC) filters used for drinking water treatment [J]. Water Research, 2001,35(12):2923-2934.
[23] 禹丽娥.地下水生物除铁效果及其动力学研究[J]. 供水技术, 2009,3(3):19-21. Yu L E.Efficiency and kinetics of iron removal by biofilter in groundwater [J]. Water Technology, 2009,3(3):19-21.
[24] Cai Y A, Li D, Liang Y H, et al. Autotrophic nitrogen removal process in a potable water treatment biofilter that simultaneously removes Mn and NH4+-N [J]. Bioresource Technology, 2014,172:226-231.
[25] 曾辉平,李 冬,高源涛,等.生物除铁、除锰滤层中铁、锰的氧化还原关系[J]. 中国给水排水, 2010,26(9):86-88. Zeng H P, Li D, Gao Y T, et al. Redox relationship between Fe and Mn in biological filter layer for iron and manganese removal [J]. China Water & Wastewater, 2010,26(9):86-88.
Simultaneous purification of high-iron,manganese and ammonia nitrogen from low temperature groundwater in biological filter.
WANG Liu-yu1, LI Dong1*, ZENG Hui-ping1, ZHANG Jie1,2
(1.Key Laboratory of Beijing Water Quality Science and Water Environment Recovery Engineering, BeijingUniversity of Technology, Beijing 100124, China;2.State Key Laboratory of Urban Water Resource andEnvironment, Harbin Institute of Technology, Harbin 150090, China)., 2019,39(8):3300~3307
A pilot-scale bio-filter was constructed for the removal of high concentrations of iron (TFe: 9~15mg/L, Fe2+: 6~12mg/L), manganese (Mn2+: 0.8~1.2mg/L), and ammonia nitrogen (NH3-N: 0.9~1.4mg/L) simultaneously from low temperature (5~6℃) groundwater.Pilot-scale bio-filter were started separately by using the 1.0m/h and 3.0m/h were started successfully after 128d and 91d, respectively. Iron and ammonia nitrogen were removed at the beginning of the bio-filter start-up, Mn removal remains a decisive factor in filter maturity.The required thickness of the bio-filter required for purification increased as the concentration of ammonia nitrogen increased when dissolved oxygen (DO) was sufficient.The maximum removal of ammonia nitrogen was about 1.60mg/L.DO deficiency was the main factor limiting the further increase of ammonia nitrogen.For higher filtration rates, the removal of manganese was less, and the thicker the filter layer required for purification.The maximum filtration rate of the single bio-filter was 8.0m/h. Analysis along the way,there were significant removal classification between Fe and Mn during the oxidation-removal process, iron and ammonia nitrogen in the filter layer can be oxidized and removed simultaneously,manganese is oxidized and removed after the iron and ammonia nitrogen.
lowtemperature;high iron manganese and ammonia nitrogen;groundwater;simultaneous purification;dissolved oxygen;thickness of filter layer
X523
A
1000-6923(2019)08-3300-08
王刘煜(1995-),男,河南周口人,北京工业大学硕士研究生,主要研究方向为水环境恢复理论及关键技术.发表论文1篇.
2019-01-17
国家自然科学基金资助项目(51678006)
* 责任作者, 教授, lidong2006@bjut.edu.cn
