影响腹腔镜下无阻断肾部分切除术实施的危险因素分析
2019-08-21许言徐从云沈德赟陶陶刘义迅肖峻黄涛
许言 徐从云 沈德赟 陶陶 刘义迅 肖峻 黄涛
肾部分切除术(partial nephrectomy, PN)已经逐渐成为小肾癌患者治疗的标准术式[1],具有和根治性肾切除相同的控瘤效果和较好的肾功能保护。随着微创技术的不断发展,腹腔镜下肾部分切除术(laparoscopic partial nephrectomy, LPN)已被证明可以替代开放肾部分切除术(open partial nephrectomy, OPN)[2-6]。一项大样本研究证实,与OPN相比,LPN能够缩短患者住院时间,减少入住重症监护室的风险[7]。随着LPN手术经验的逐渐增多,LPN相对于OPN能更好地保护肾功能,改善患者预后[8]。
传统PN术中在肿瘤切除前需要阻断肾门血管,目的是控制出血,保持术野清晰。Tachikake等[9]发现缺血时间过长会对肾功能造成显著损害。虽然引起肾功能不可逆损伤的确切缺血时间尚未达成共识,但应尽可能减少PN术中肾脏的缺血时间[10]。为了减少缺血对肾功能的影响,包括选择性动脉分支阻断[11]和控制性低血压[12]等在内的多种方法曾被尝试。
无阻断肾部分切除首次报道于2011年[13],已被证实具有良好的安全性和控瘤效果,并可以显著改善远期肾功能[14-15],特别是肾功能较差的患者更能从此技术中获益[16]。随着腹腔镜器械的改进和技巧的提升,更复杂的肿瘤也可以通过无阻断技术成功切除[14]。但无阻断技术存在增加术中出血、影响切除/缝合质量等风险[17],目前无明确标准用于合适患者的术前筛选。
本研究回顾性分析拟行无阻断LPN患者的术前资料,寻找导致无阻断失败的危险因素,试图为术前选择合适患者进行无阻断LPN提供建议。
对象与方法
一、一般资料
本研究收集了2016年7月至2018年6月于我院接受治疗的94例肾占位患者,纳入标准:①单发,单侧肿瘤;②肿瘤分期T1aN0M0;③无既往患肾手术史;④无严重心脑血管、肺部、肝肾功能障碍。所有患者均接受常规实验室检查及心肺功能评估,并根据MDRD方程计算估算肾小球滤过率(estimated glomerular filtration rate, eGFR)。行3 mm薄层肾CT扫描,以评估肿瘤大小、位置、深度及与集合系统的关系,并计算R.E.N.A.L.评分。并由同一术者和助手完成所有手术。
二、手术步骤
经腹腔途径建立穿刺通道。游离肾蒂,显露肾动脉、静脉及供应瘤体区域的分支动脉并以血管吊带提起以便辨识。电灼标记肿瘤边缘外5 mm为切除范围,冷刀钝、锐性沿标记切除瘤体,吸引器保持术野清晰。切除瘤体外周,保留薄层正常肾脏组织。小血管采用百克钳,5 mm双极棒状电凝止血。切除位置深达髓质时降低血压至80/50 mmHg,将分离出的较大血管以钛夹或Hem-o-lok夹闭。3-0可吸收线缝合破裂的集合系统,2-0可吸收线单层或双层连续缝合肾脏创面。一旦难以控制的出血发生,及时夹闭肾动脉。
三、观察指标
记录术中估计失血量(estimated blood loss volume, EBL)、术前术后血色素差值、手术时间(operative time, ORT)及输血情况。记录术后住院时间、并发症发生率及病理诊断、标本切缘。术后7 d及3个月复查eGFR并计算其变化率[eGFR变化率=(eGFR术前-eGFR复查)/eGFR术前× 100%]。
四、统计学方法
将患者分为无阻断组和阻断组,采用拟合优度检验确定变量分布。Studentt检验、Mann-Whitney U检验或χ2检验挑选出组间差异显著的变量。再采用Logistic多元回归分析对变量进行进一步筛选,寻找独立危险因素。最后利用受试者工作特征曲线(receiver operator characteristic curve, ROC)计算出独立危险因素的临界值和曲线下面积(area under curve, AUC)。所有统计学处理均使用SPSS 19.0软件,在评价组间差异时,由于变量数量多,并存在相互影响,为了避免遗漏,将P值阈值设置为0.3,其他除特别说明外,P<0.05为差异有统计学意义。
结 果
94例患者纳入本研究,所有患者均接受LPN,无患者中转开放。32例患者因术中出血较多而终止无阻断,并常规阻断肾动脉完成手术,围手术期无严重并发症发生。经t检验和χ2检验,阻断组和无阻断组在年龄、体重指数、糖尿病史、术前eGFR、肿瘤直径、肿瘤位置及R.E.N.A.L.评分方面有显著差异(P<0.3,表1)。无阻断组ORT和EBL显著高于阻断组,术后7 d的eGFR变化率显著小于阻断组(P<0.05)。输血率、切缘阳性率、住院时间两组间无显著差异(P>0.05,表2)。无阻断组术后3个月eGFR变化率小于阻断组,但差异无统计学意义(P>0.05)。
经Logistic回归分析,年龄、术前eGFR、肿瘤直径、肿瘤位置以及R.E.N.A.L.评分是导致实施无阻断失败的独立危险因素(P<0.05,表3)。根据以上结果绘制出预测实施无阻断技术失败因素的ROC(图1),年龄的AUC为0.674(95%CI0.516~0.833,临界值56岁);eGFR 的AUC为0.725[95%CI0.564~0.885,临界值91.42 ml/(min·1.73 m2)];肿瘤直径的AUC为0.826(95%CI0.700~0.951, 临界值3.33 cm);R.E.N.A.L.评分的AUC为0.892(95%CI0.797~0.987, 临界值6.55)。肿瘤直径及R.E.N.A.L.评分在预测无阻断技术成功率方面的效力更高(AUC>0.8)。
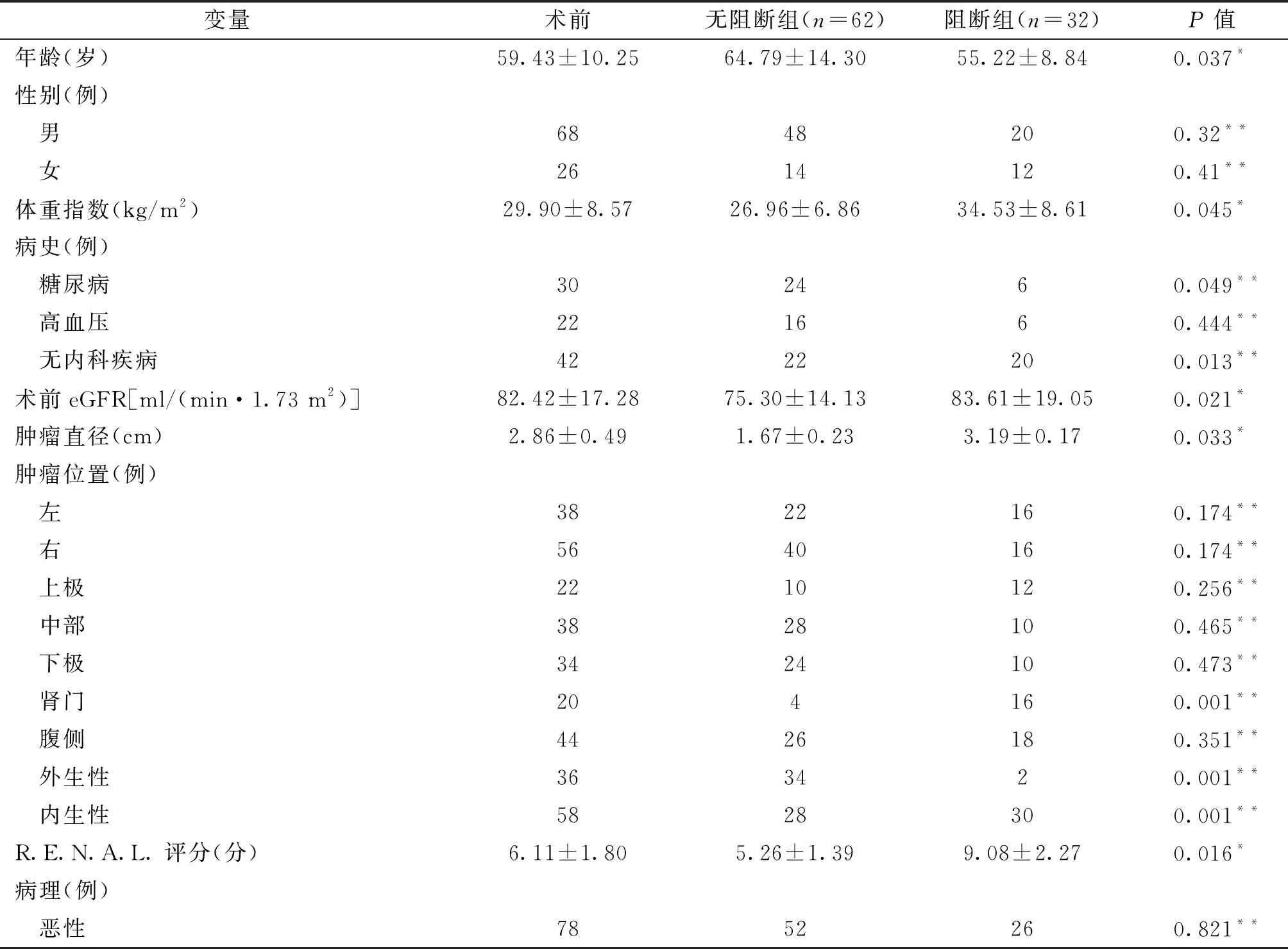
表1 阻断组与无阻断组的基线参数特性比较
注:*t检验;**χ2检验
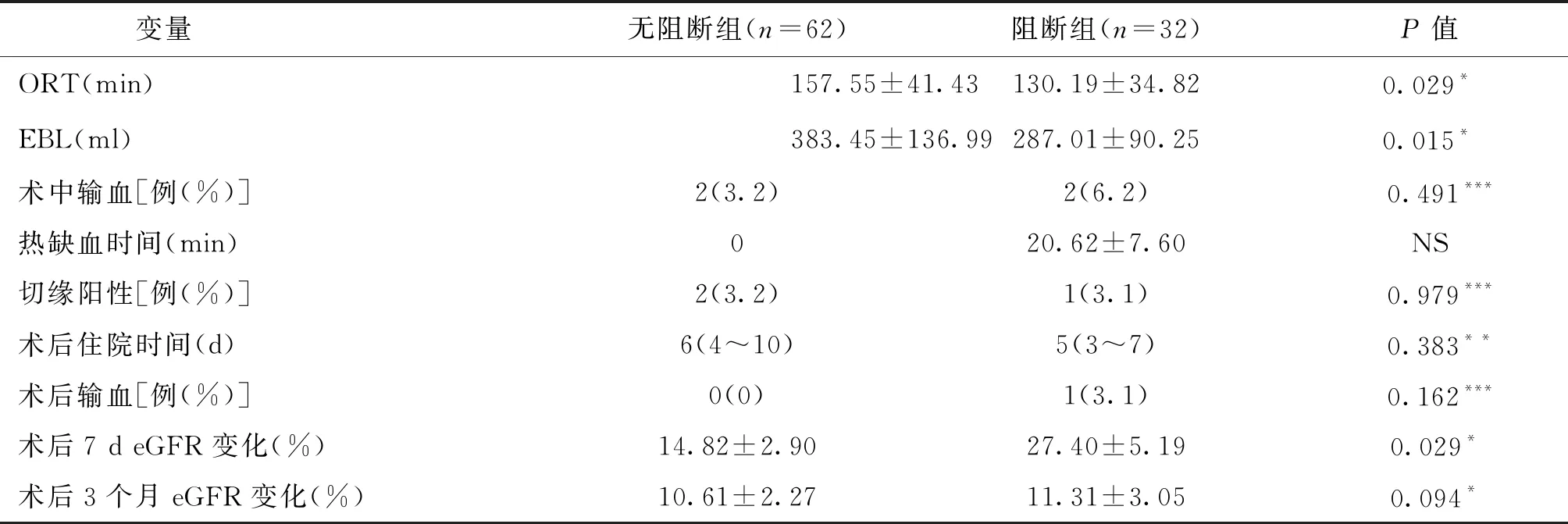
表2 无阻断组和阻断组围手术期及术后随访参数比较
注:*t检验;**Mann-Whitney U检验;***χ2检验;NS-无意义
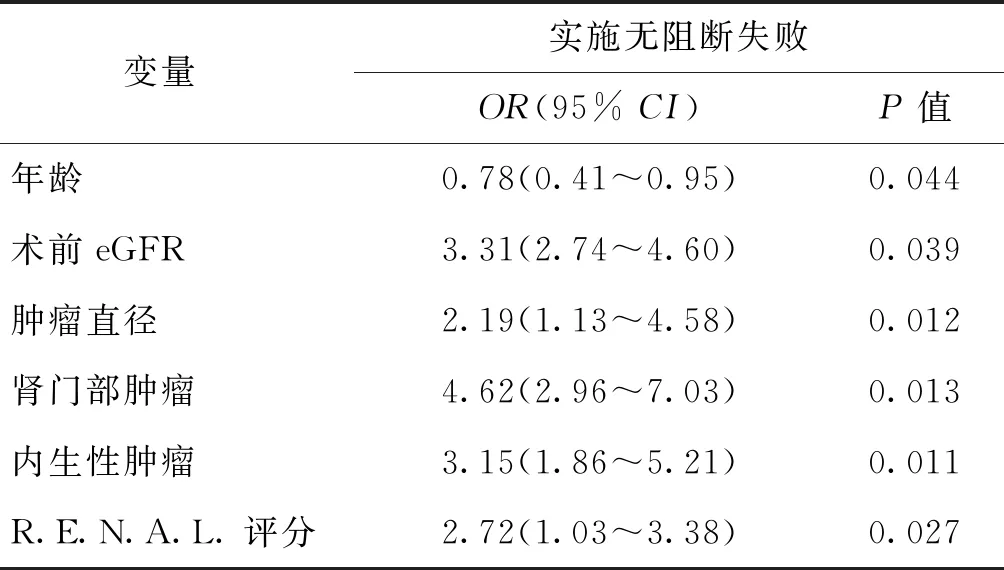
表3 无阻断技术应用的影响因素的Logistic多元回归分析
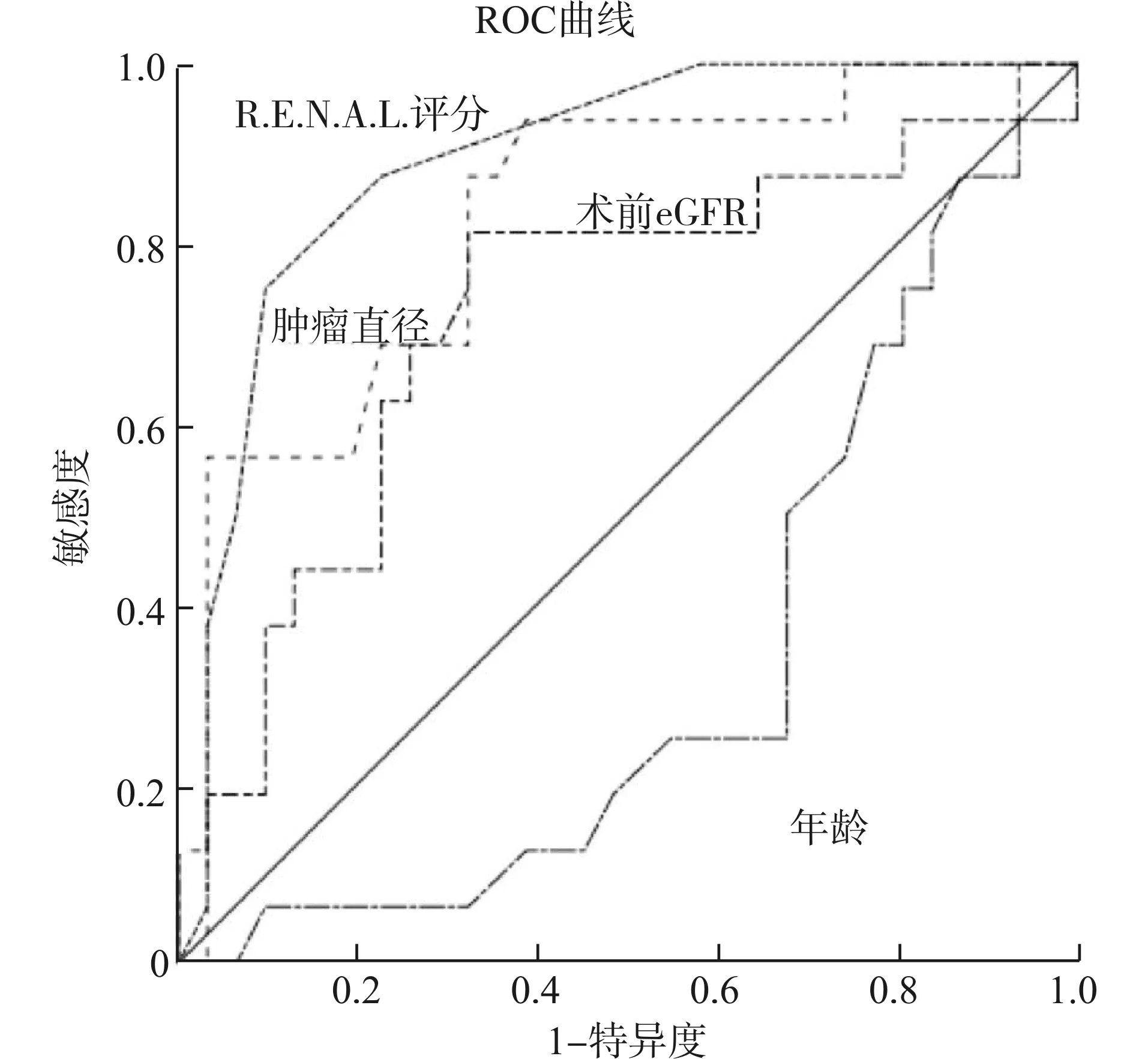
图1 年龄、术前eGFR、肿瘤直径及R.E.N.A.L.评分在预测实施术中无阻断失败方面价值比较
讨 论
随着超声、CT和MRI等现代影像学检查的应用,更多的肾脏肿瘤可以在早期发现[18]。这些肿瘤多为小的偶发肿块,无明显症状,且恶性潜能较低。PN是治疗T1a期肾肿瘤的金标准,其适应证已扩展至T1b和T2期肿瘤,即使对侧肾脏功能正常[19]。自1993年LPN被首次报道至今,该术式被广泛使用并逐渐改进[20]。肾蒂阻断技术被广泛应用于OPN、LPN和机器人辅助下PN中,目的是减少创面出血、保持术野清晰、确保精细切除肿瘤并对创面进行可靠缝合[2,21]。然而,肾蒂阻断将带来肾脏的缺血性损伤,并有可能影响远期肾脏功能。曾认为热缺血时间控制在30 min以内,仅会对肾功能造成短暂和可逆的损害。但Gill等[13]发现,即使短暂的缺血也会对肾功能造成不可逆损伤,特别是在高龄、合并基础疾病及隐性肾功能不全患者中。基于以上原因,零缺血技术得以问世,旨在消除热缺血对接受PN患肾功能的影响。零缺血技术包括:①选择性阻断肾动脉/静脉,即选择性阻断2、3级甚至4级血管分支;②完全无阻断,即在术中不阻断肾蒂血管[22-23]。
1篇包含10项回顾性研究(728例试验组和1 267例对照组)的Meta分析显示,在合适患者中运用无阻断技术具有良好的安全性,与常规阻断相比疗效相同,且能更好保护远期患肾功能[15]。Rais-Bahrami等[24]比较了无阻断(126例)和常规阻断(264例)下PN患者的术后肾功能,认为无阻断技术可作为治疗T1~2期肾癌的可选方法。在处理大体积、复杂肿瘤时,无阻断技术并不会影响手术时间、输血、住院时间、并发症及切缘阳性率。Boyarsky等[25]回顾性分析了89例瘤体中位直径3 cm(1.0~8.0 cm)无阻断LPN,认为LPN可以在无阻断情况下成功完成。George等[26]比较了289例常规阻断和150例无阻断LPN患者,发现无阻断技术安全可行,给患肾带来的损伤较小。Thompson等[27]比较了362例常规阻断和96例无阻断PN患者,发现相对于无阻断技术,常规阻断更易发生急性肾功能衰竭。王启飞等[28]回顾性分析了15例平均肿瘤直径2.5 cm,并接受无阻断LPN患者的临床资料,认为将无阻断技术应用于较小的局限性肿瘤是安全有效的,可以避免术中肾脏热缺血,减少肾脏组织的损伤范围,并最大程度保护肾功能。陈少豪等[29]回顾性分析了54例接受常规阻断和19例接受无阻断LPN患者的临床资料,发现阻断和无阻断肾动脉对短期肾功能的影响有差别,而对长期肾功能的影响无差别。
然而,无阻断的代价可能是巨大的,主要是无法控制的出血及相关的各种并发症。Rais-Bahrami等发现无阻断技术带来更多的EBL。George等的研究发现无阻断组的EBL较高,但组间输血率无显著差异。Liu等[15]发现无阻断LPN组的输血率显著高于常规阻断组(15.3% vs 6.3%,P=0.02)。Papalia等[12]认为零缺血技术是可行的,在直径大于4 cm的肿瘤中,EBL及术后并发症发生率显著高于体积较小的肿瘤。因此,选择合适的患者给予无阻断技术,才可以使无阻断技术的获益得到最大化。
PN术中出血主要来源于肿瘤和周围肾实质的血供,与肿瘤的大小和位置密切相关。R.E.N.A.L.评分从多方面描述肾肿瘤的复杂性,被证明具有良好的适用性。肿瘤大小(R)是影响手术计划的一个重要因素,和集合系统的关系(N)则是PN并发症一个很好的预测因素[30-31]。在751例射频消融治疗肾脏肿瘤患者中,发现R.E.N.A.L.评分的增高与治疗失败和并发症发生具有显著相关性[32]。在我们的研究中,R.E.N.A.L.评分具有最大AUC,说明其具有良好的预测能力。同样,肿瘤直径也具有良好的预测价值(AUC=0.826),R.E.N.A.L.评分的AUC大于肿瘤直径,预测价值优于肿瘤直径。因此,临床上我们更多推荐使用R.E.N.A.L.评分来替代简单依据肿瘤大小作为判断是否实施无阻断LPN的因素。即当患者肿瘤R.E.N.A.L.评分大于6分,且靠近肾蒂时,需谨慎给予无阻断LPN。
本研究发现高龄是无阻断技术失败的保护性因素。我们认为,随着年龄的增长,正常肾实质和肿瘤的血供都会相应减少,这或许可以减少LPN术中发生不可控出血的可能性。此外,术前eGFR也被发现是一个危险因素,或许由于术前eGFR与肾灌注呈正相关。也就是说,对于高龄或术前既存在肾功能不全的患者,可以考虑给予无阻断技术。
综上所述,本研究探讨了术前参数影响LPN术中无阻断技术实施的可能性。发现年龄是无阻断技术顺利实施的保护因素,而术前eGFR、肿瘤直径及R.E.N.A.L.评分为危险因素。这些参数有助于预测无阻断技术实施的风险,并提高其成功率。本研究在样本量和无阻断技术操作技巧方面仍存在局限性,需要进一步的大样本研究来验证。
