H4SiW12O40@MIL-100(Fe)的制备及催化正丁醛自缩合反应性能
2019-08-01史雅玫李步卫安华良赵新强王延吉
史雅玫,李步卫,安华良,赵新强,王延吉
(河北工业大学 化工学院 河北省绿色化工与高效节能重点实验室,天津 300130)
正丁醛自缩合合成辛烯醛(2-乙基-2-己烯醛)是工业生产辛醇(2-乙基己醇)的重要反应步骤之一。该反应属于典型的羟醛缩合反应,既可以被酸催化也可以被碱催化[1]。工业上通常采用强碱的水溶液催化该反应,虽然可以获得较高的辛烯醛收率,但存在生产成本高、含碱废水排放量大和环境污染严重等缺点[2-3]。所以,开发环境友好型固体催化剂成为研究者关注的焦点。杂多酸作为一种固体酸催化剂,具有腐蚀性小、对环境友好等优势,已被广泛应用到酸催化反应中。本课题组陈翠娜等[4]研究了负载型杂多酸对正丁醛自缩合反应的催化性能,发现H4SiW12O40/SiO2催化活性最高。在催化剂用量15%(质量分数)、反应温度120 ℃、反应时间6 h的条件下,正丁醛转化率为90.4%,辛烯醛选择性为89.2%。但活性组分H4SiW12O40易流失,导致催化剂失活。因此,解决活性组分流失问题是该类催化剂的研究重点。
MIL系列MOFs材料具有高比表面积和孔隙率,常被用来负载和封装分子催化剂[5]。Canioni等[6]以六水合氯化铁、1,3,5-苯三羧酸三甲酯、磷钼酸和水为原料,在无氟化氢条件下合成了H3PMo12O40@MIL-100(Fe)。对H3PMo12O40@MIL-100(Fe)的稳定性进行了分析,发现将H3PMo12O40@MIL-100(Fe)在水中存放两个月或者在含有四丁基高氯酸铵物种的有机相中存放,均没有造成客体分子磷钼酸的流失。Zhang等[7]以磷钨酸、硝酸铁和均苯三甲酸为原料,在常压、低温和无氟化氢存在的条件下制得H3PW12O40@MIL-100(Fe),并将其应用于正己醇与乙酸的酯化反应,催化剂重复使用4次,未出现活性组分磷钨酸溶脱现象,表明催化剂具有良好的稳定性。可见,将杂多酸封装在MIL-100(Fe)的孔笼中,可以有效抑制其在反应过程中流失。
鉴于此,为解决前期研究过程中H4SiW12O40/SiO2催化剂因H4SiW12O40溶于反应体系导致的活性组分流失及难以重复使用问题[4],本课题组拟采用原位合成法将H4SiW12O40封装在MIL-100(Fe)的孔笼中制备H4SiW12O40@MIL-100(Fe)催化剂,将其应用于正丁醛自缩合反应。研究H4SiW12O40负载量对其催化性能的影响,反应条件对正丁醛自缩合反应的影响;结合分析表征,探讨催化剂中H4SiW12O40的稳定性及H4SiW12O40@MIL-100(Fe)的重复使用情况;采用GC-MS对反应体系进行定性分析,建立正丁醛自缩合反应网络。
1 实验部分
1.1 原料和试剂
硅钨酸(H4SiW12O40·xH2O),分析纯,天津市科密欧化学试剂开发中心产品;硝酸铁(Fe(NO3)3·9H2O)、苯三甲酸(C6H3(CO2H)3)、正丁醛(CH3(CH2)2CHO),分析纯,天津大茂化学试剂厂产品;N,N-二甲基甲酰胺(DMF,C3H7NO)、乙醇(CH3CH2OH),分析纯,天津市风船化学试剂有限公司产品;邻二甲苯(C6H4(CH3)2),分析纯,天津市光复精细化工研究所产品。
1.2 催化剂制备[7-8]
采用原位合成法制备H4SiW12O40@MIL-100(Fe),通过改变H4SiW12O40的添加量制备了4种不同负载量的催化剂。以H4SiW12O40负载量为13.7%(质量分数)的H4SiW12O40@MIL-100(Fe)的制备为例:将1.0 g硅钨酸、8.08 g硝酸铁、2.8 g苯三甲酸和12 mL去离子水加入50 mL单口烧瓶中,磁力搅拌约30 min后升温至95 ℃,回流冷凝12 h。反应结束后,将样品在110 ℃下恒温干燥10 h。干燥后的样品首先在80 ℃水中恒温搅拌5 h,过滤分离后于80 ℃下真空干燥3 h;之后在DMF中搅拌2 h,过滤分离后于80 ℃下真空干燥3 h;最后于60 ℃乙醇中恒温搅拌3 h,过滤分离后于80 ℃下真空干燥3 h,即得到H4SiW12O40@MIL-100(Fe)催化剂样品。
1.3 催化剂表征
采用日本理学D/MAX-2500 型X射线衍射仪对催化剂样品进行物相分析。操作条件为:Cu靶,石墨单色滤光片,狭缝SS/DS=1°,RS=0.15 mm,工作电压为40 kV,电流100 mA,扫描范围3°~30°,扫描速率6°/min。
采用美国Micromeritics公司的ASAP2020型比表面积及孔隙度分析仪对催化剂的比表面积、孔体积和孔径进行分析。首先称取0.2 g左右的样品置于分析站,然后将样品在150 ℃下真空脱气4 h,在液氮冷肼中进行N2吸附-脱附测定。采用BET法计算催化剂的比表面积,采用BJH脱附法计算孔体积和孔径。
采用美国PerkinElmer公司的Optima 7300V型电感耦合等离子体原子发射光谱仪测定催化剂活性组分的含量。自激式射频发生器,频率40.68 MHz,功率1300 W。
采用德国Bruker公司的Vector 22型傅里叶红外光谱分析仪对催化剂的结构进行表征。分辨率为4 cm-1,扫描速率为0.2 cm/s,扫描波数范围为400~4000 cm-1。KBr压片法制备样品。
1.4 催化剂活性评价
正丁醛自缩合反应在100 mL的高压反应釜中进行。具体操作步骤如下:取30 mL的正丁醛(约24 g)和3.75 g催化剂置于高压反应釜中,密封后用N2置换釜内空气3次,在搅拌条件下升温至120 ℃,反应8 h后停止加热。待反应釜冷却至室温,将产品离心分离,液相用气相色谱分析其组成,同时回收催化剂。考察了3种不同处理方式对回收催化剂性能的影响:一是150 ℃下真空干燥6 h;二是经DMF和无水乙醇洗涤3次后,于150 ℃下干燥6 h;三是经无水乙醇回流条件下洗涤3次后,于150 ℃下干燥6 h。
在正丁醛自缩合反应中,正丁醛转化率x、辛烯醛收率y、辛烯醛选择性s分别按式(1)、(2)、(3)进行计算。
x=nBA/nBA0×100%
(1)
s=n2E2H/n2E2H0×100%
(2)
y=x×s
(3)
其中,nBA为已转化正丁醛的物质的量,mol;nBA0为反应前正丁醛的物质的量,mol;n2E2H为反应产物中辛烯醛的物质的量,mol;n2E2H0为反应后所有产物的总物质的量,mol。
1.5 产物分析
采用Thermo Finnigan TRACE DSQ型气-质联用仪对产物进行定性分析。载气为氦气,流量1 mL/min;分流体积比100/1;柱温:初温40 ℃,以升温速率10 ℃/min升温至250 ℃,保留5 min;气化室温度250 ℃,传输线温度250 ℃。质谱采用EI电离源:温度200 ℃,相对分子质量范围:40~500,进样量0.02 μL。
采用北京北分瑞利分析仪器(集团)有限责任公司的3420A型气相色谱仪对产物进行定量分析,以邻二甲苯为内标物。色谱分析条件:氢火焰检测器,检测器温度220 ℃,气化室温度220 ℃,进样量0.4 μL。KB-1毛细管柱,采用程序升温控制色谱柱温:初温100 ℃,保持2 min,以升温速率 10 ℃/min 升温至200 ℃,保持10 min。载气为N2,流速30 mL/min。
2 结果与讨论
2.1 催化剂H4SiW12O40@MIL-100(Fe)的表征结果
2.1.1 N2吸附-脱附表征
首先采用ICP-OES测定了制备的4种不同负载量样品中H4SiW12O40的实际负载量(质量分数,以下同),结果分别为8.4%、13.7%、18.7%和21.5%。然后表征了不同负载量H4SiW12O40@MIL-100(Fe)的比表面积和孔结构,结果如表1所示。从表1可以看出,随着 H4SiW12O40负载量增加,H4SiW12O40@MIL-100(Fe)的比表面积和孔体积均呈逐渐降低的趋势,这表明硅钨酸已进入到MIL-100(Fe)的介孔笼中[9-10]。而催化剂平均孔径随着H4SiW12O40负载量增加逐渐增大,则是硅钨酸优先进入MIL-100(Fe)的小孔造成的[11]。

表1 不同负载量的H4SiW12O40@MIL-100(Fe)催化剂的织构性质Table 1 Textural properties of H4SiW12O40@MIL-100(Fe) with different loadings of H4SiW12O40
1)Determined by ICP-OES
2.1.2 XRD表征
H4SiW12O40负载量为13.7%的H4SiW12O40@MIL-100(Fe)和MIL-100(Fe)的XRD谱图如图1所示。可以看出,MIL-100(Fe)的特征衍射峰与其单晶结构数据模拟的XRD谱峰位相吻合,表明在该制备条件下合成了MIL-100(Fe)[8]。H4SiW12O40@MIL-100(Fe)的特征衍射峰位置与MIL-100(Fe)相似,只是在小角部分其特征衍射峰位置及相对强度发生了轻微变化,这是由于小角X射线是同原子中的电子发生交互作用,所以对电子密度的不均匀性特别敏感。小角峰强度分布与周围介质电子云密度有关,负载H4SiW12O40后增大了MIL-100(Fe)孔中的电子密度,使得小角部分峰的相对位置及相对强度发生了改变。Canioni等[6]在表征MIL-100(Fe)和H3PMo12O40@MIL-100(Fe)时也发现了同样的现象。此外,在H4SiW12O40@MIL-100(Fe)的XRD谱图中没有检测到H4SiW12O40的特征衍射峰,说明H4SiW12O40高度分散在MIL-100(Fe)的孔笼中。

图1 MIL-100(Fe)和H4SiW12O40@MIL-100(Fe)的XRD谱图Fig.1 XRD patterns of MIL-100(Fe)andH4SiW12O40@MIL-100(Fe)(1)H4SiW12O40;(2)H4SiW12O40@MIL-100(Fe);(3)MIL-100(Fe);(4)MIL-100(Fe)simulated by crystal structure data
2.1.3 FT-IR表征
MIL-100(Fe)、H4SiW12O40和H4SiW12O40负载量为13.7%的H4SiW12O40@MIL-100(Fe)的红外光谱图如图2所示。在MIL-100(Fe)的红外光谱中,1385 和1625 cm-1处的吸收峰分别归属为1,3,5-苯三甲酸羧基基团的对称伸缩振动COO—和非对称伸缩振动COO—;712~762 cm-1处的吸收峰属于苯环的C—C峰。具有Keggin结构的H4SiW12O40的特征吸收峰出现在980、926、1028和779 cm-1处,其中980 cm-1是W=O的伸缩振动吸收峰,926 cm-1是Si—O的伸缩振动吸收峰,1028和779 cm-1对应W—O—W的伸缩振动吸收峰[12]。由图2可见,H4SiW12O40@MIL-100(Fe)在保持MIL-100(Fe)的红外特征吸收峰的同时,也包含H4SiW12O40的特征吸收峰,这表明H4SiW12O40以客体分子的形式进入MIL-100(Fe)的孔笼中,且固载在MIL-100(Fe)中的H4SiW12O40仍保持了Keggin结构。

图2 MIL-100(Fe)、H4SiW12O40和H4SiW12O40@MIL-100(Fe)的红外光谱图Fig.2 IR spectra of MIL-100(Fe),H4SiW12O40 and H4SiW12O40@MIL-100(Fe)(1)MIL-100(Fe);(2)H4SiW12O40@MIL-100(Fe);(3)H4SiW12O40
2.2 硅钨酸负载量对H4SiW12O40@MIL-100(Fe)催化性能的影响
考察了H4SiW12O40负载量对H4SiW12O40@MIL-100(Fe)催化性能的影响,结果见表2。可以看出,随着H4SiW12O40负载量增加,正丁醛的转化率和辛烯醛的收率均呈先升高后降低的趋势,辛烯醛的选择性则先保持基本稳定后降低。当未添加H4SiW12O40时,MIL-100(Fe)由于其本身的不饱和金属位点而显Lewis酸性,对正丁醛自缩合反应也有一定的催化活性。当H4SiW12O40负载量较低时,增加H4SiW12O40负载量,活性中心数目随之增多,催化活性提高,故正丁醛转化率和辛烯醛收率升高。当H4SiW12O40负载量增至13.7%时,H4SiW12O40@MIL-100(Fe)催化活性最好,正丁醛的转化率、辛烯醛的收率和选择性分别为72.9%、60.9%和83.5%。继续增加H4SiW12O40负载量,正丁醛的转化率、辛烯醛的收率和选择性均逐渐降低,说明H4SiW12O40负载量并非越大越好。H4SiW12O40负载量较高会导致H4SiW12O40在MIL-100(Fe)载体上团聚或分布不均,分散度较低,比表面积显著下降,降低其催化性能[13-14]。这与表1中H4SiW12O40@MIL-100(Fe)催化剂的比表面积随H4SiW12O4负载量的增加而逐渐降低的结论相符。故选择适宜的H4SiW12O40负载量为13.7%。
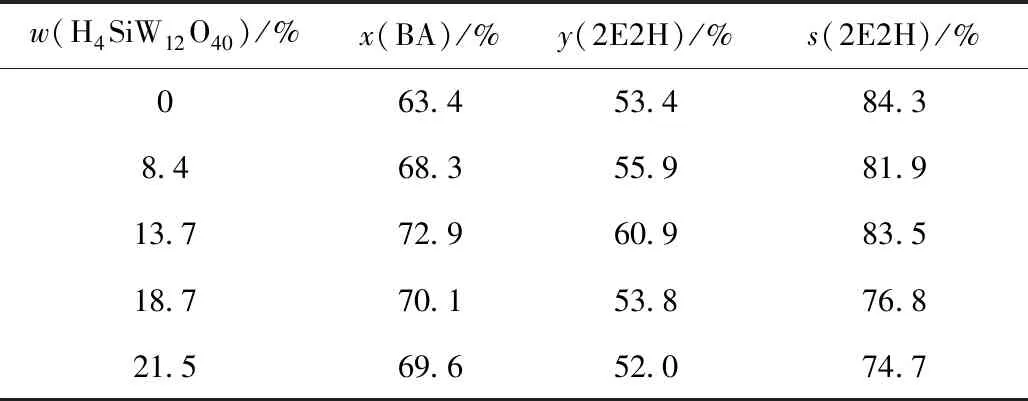
表2 H4SiW12O40负载量对H4SiW12O40@MIL-100(Fe)催化性能的影响Table 2 Effect of H4SiW12O40 loading on the catalytic performance of H4SiW12O40@MIL-100(Fe)
Reaction condition:w(H4SiW12O40@MIL-100(Fe))=15%;T=120 ℃;t=6 h
x—Conversion;y—Yield;s—Selectivity;BA—n-Butyraldehyde;2E2H—2-Ethyl-2-hexenal
2.3 反应条件对正丁醛自缩合反应的影响
2.3.1 催化剂用量的影响
考察了催化剂用量对正丁醛自缩合反应的影响,结果如图3所示。可以看出,随着催化剂用量的增加,正丁醛的转化率先升高后无明显变化,而辛烯醛的收率和选择性呈先升高后降低的趋势。当催化剂用量(质量分数,以下同)小于15%时,催化活性中心数目不够,增加催化剂用量相当于增加催化活性中心,有利于反应的进行;当催化剂用量等于15%时,辛烯醛的收率和选择性达到最大,分别为60.9%和83.5%;继续增加催化剂用量,辛烯醛的收率和选择性均有所下降。这可能是由于催化剂提供的活性中心过多,促进了反应体系中2-乙基-3-羟基己醛与正丁醛发生季先科反应生成丁酸-2-乙基-3-羟基己酯[15]、辛烯醛与正丁醛进一步缩合生成2,4-二乙基-2,4-辛二烯醛[4]等副反应,从而导致辛烯醛的选择性降低。所以,选择适宜的催化剂用量为15%。

图3 催化剂用量对正丁醛自缩合反应的影响Fig.3 Effect of catalyst amount on n-butyraldehyde self-condensation reactionReaction condition:w(H4SiW12O40)=13.7%;T=120 ℃;t=6 h
2.3.2 反应温度的影响
考察了反应温度对正丁醛自缩合反应的影响,结果如图4所示。可以看出,随着反应温度升高,正丁醛的转化率先升高后保持稳定,辛烯醛的收率和选择性均先升高后略有降低。采用ABWY法对正丁醛自缩合合成辛烯醛反应进行了热力学计算,该反应为放热反应。但开始时正丁醛转化率和辛烯醛收率随着反应温度升高明显上升,这主要是因为在较低反应温度时,在固定反应时间内反应尚未达到平衡,动力学影响为主要因素,提高反应温度可加快反应速率。当温度达到120 ℃时,辛烯醛收率达到最大为60.9%;继续升高温度,正丁醛转化率基本保持不变,说明在反应时间内该反应已达到平衡。由热力学计算可知,110 ℃以上热力学平衡常数随反应温度升高变化不明显,这应该是继续升高温度正丁醛转化率基本不变的原因。但反应温度过高会促进2-乙基-3-羟基己醛和正丁醛进行季先科反应生成丁酸-2-乙基-3-羟基己酯以及辛烯醛和正丁醛进一步缩合生成2,4-二乙基-2,4-辛二烯醛等副反应[16-17],从而导致辛烯醛的收率和选择性略有下降。所以,选择适宜的反应温度为120 ℃。

图4 反应温度对正丁醛自缩合反应的影响Fig.4 Effect of reaction temperature on n-butyraldehyde self-condensation reactionReaction condition:w(H4SiW12O40)=13.7%;w(H4SiW12O40@MIL-100(Fe))=15%;t=6 h
2.3.3 反应时间的影响
考察了反应时间对正丁醛自缩合反应的影响,结果如图5所示。可以看出,随着反应时间延长,正丁醛转化率先升高后保持稳定,而辛烯醛的收率和选择性均呈先升高后降低的趋势。当反应时间小于6 h时,随反应时间延长,反应进行的越充分,正丁醛转化率和辛烯醛收率均明显上升;当反应时间为6 h时,正丁醛转化率、辛烯醛收率和选择性均达到最高,分别为72.9%、60.9%和83.5%;当反应时间大于6 h时,正丁醛转化率基本保持不变,说明该反应已达到化学平衡。辛烯醛收率和选择性有所下降是反应时间大于6 h后反应体系中副反应开始增多所致。所以,选择适宜的反应时间为6 h。

图5 反应时间对正丁醛自缩合反应的影响Fig.5 Effect of reaction time on n-butyraldehyde self-condensation reactionReaction condition:w(H4SiW12O40)=13.7%;w(H4SiW12O40@MIL-100(Fe))=15%;T=120 ℃
2.4 H4SiW12O40@MIL-100(Fe)催化正丁醛自缩合反应体系分析
采用GC-MS技术对H4SiW12O40@MIL-100(Fe)催化正丁醛自缩合合成辛烯醛反应体系进行了定性分析。结果表明:反应液中除原料正丁醛(A)和目标产物辛烯醛(F)外,主要还有正丁醇(B)、3-庚烯(C)、正丁酸(D)、3-壬烯(E)、丁酸丁酯(G)、2,4-二乙基-2,4-辛二烯醛(H)和丁酸-2-乙基-3-羟基己酯(I)等。与La-Al2O3、Ce-Al2O3和[HSO3-b-N(Et)3]p-TSA催化正丁醛自缩合反应体系的副产物相比[18-20],3-壬烯(E)和2,4-二乙基-2,4-辛二烯醛(H)是在H4SiW12O40@MIL-100(Fe)催化正丁醛自缩合合成辛烯醛反应体系中产生的。一是辛烯醛(F)与正丁醛(A)发生二次缩合生成2,4-二乙基-2,4-辛二烯醛(H),这与Shen等[17]以碱土金属氧化物为催化剂催化正丁醛自缩合反应时发现辛烯醛会进一步与正丁醛深度缩合生成2,4-二乙基-2,4-辛二烯醛相符;二是辛烯醛(F)的C—C键断裂生成乙烷和正己醛(M),这也与Kim等[21]以负载金属Pd的金属氧化物为催化剂催化正丁醛合成汽油支链碳氢化合物时发现辛烯醛的C—C键会断裂生成乙烷和正己醛相一致。正己醛(M)与正丁酸(D)发生偶联反应生成4-壬酮(N),4-壬酮(N)进一步加氢、脱水生成3-壬烯(E)。
基于上述分析结果,对H4SiW12O40@MIL-100(Fe)催化正丁醛自缩合反应网络进行了推测,如图6所示。可以看出,反应体系中主要发生的是正丁醛(A)自缩合合成中间产物2-乙基-3-羟基己醛(L),然后中间产物脱水生成目的产物辛烯醛(F)的反应。除此之外,小部分正丁醛(A)可以发生季先科反应生成丁酸丁酯(G),丁酸丁酯(G)再水解生成正丁醇(B)和正丁酸(D)。丁酸丁酯(G)还可以经酮化、加氢及脱水过程生成3-庚烯(C)[22]。少量的2-乙基-3-羟基己醛(L)与正丁醛(A)发生季先科反应生成丁酸-2-乙基-3-羟基己酯(I)。辛烯醛(F)除与一分子正丁醛(A)发生二次缩合生成2,4-二乙基-2,4-辛二烯醛(H)外,其C—C键还可以发生断裂生成乙烷和正己醛(M)。正己醛(M)与正丁酸(D)偶联生成4-壬酮(N),4-壬酮(N)经加氢、脱水生成3-壬烯(E)。
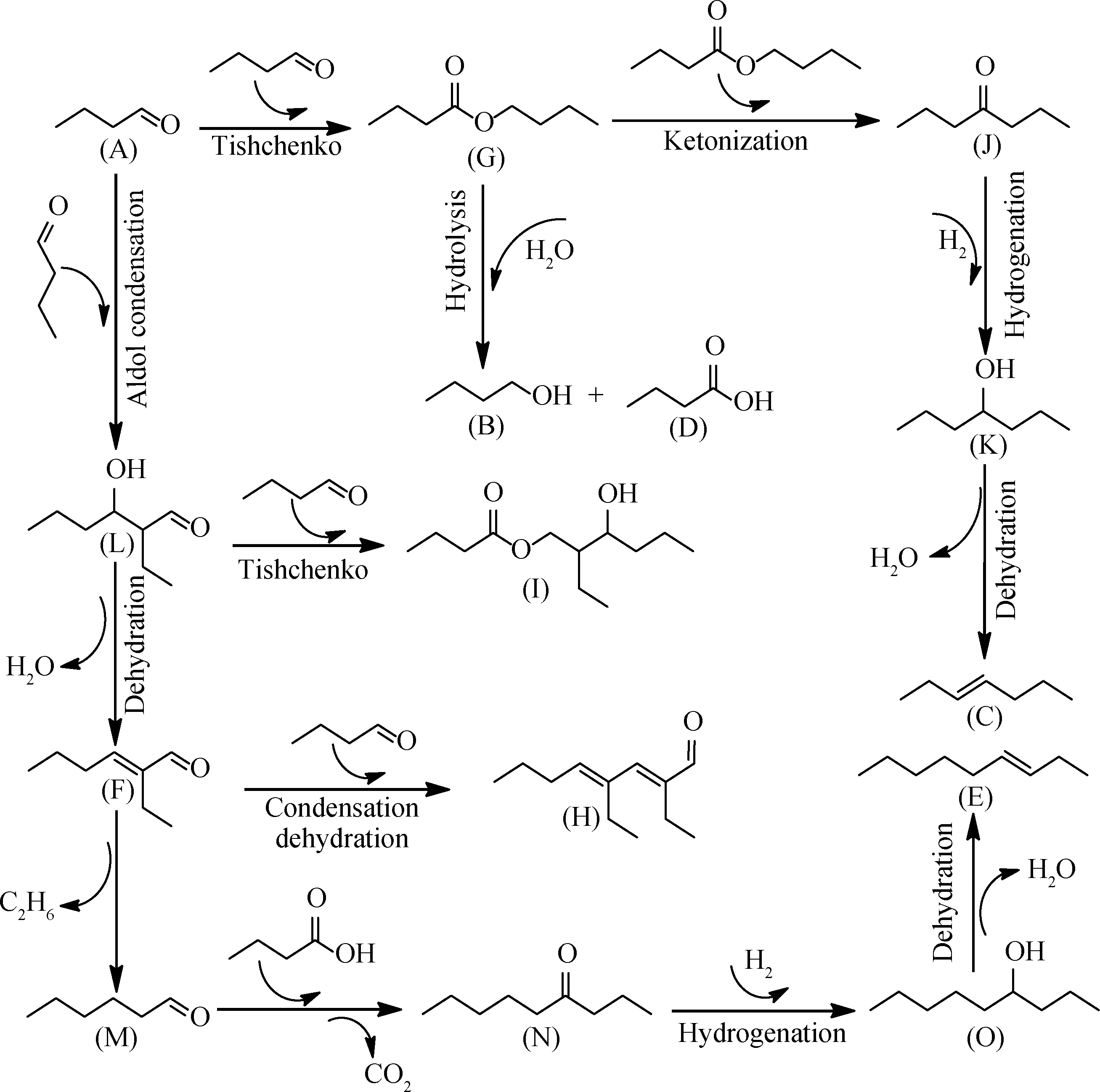
图6 H4SiW12O40@MIL-100(Fe)催化正丁醛自缩合反应网络Fig.6 Reaction network of n-butyraldehyde self-condensation catalyzed by H4SiW12O40@MIL-100(Fe)
2.5 H4SiW12O40@MIL-100(Fe)催化剂失活与再生
2.5.1 催化剂重复使用性能考察
将回收的H4SiW12O40@MIL-100(Fe)催化剂分别用3种不同方式处理后,直接用于正丁醛自缩合合成辛烯醛反应,结果见表3。可以看出,与新鲜催化剂相比,回收后的催化剂经过干燥处理,活性明显下降。由于催化剂在制备过程中已用去离子水、DMF和乙醇反复清洗纯化,所以催化剂失活原因不应该是由硅钨酸流失造成的。Guo等[23]以H3PW12O40/SiO2为催化剂催化苯酚和乙酰丙酸合成双酚酸反应时,发现在磷钨酸无流失的情况下,回收后催化剂催化活性仍下降较多,分析催化剂失活是双酚酸分子吸附在催化剂上造成的。由此推测,本研究中回收催化剂H4SiW12O40@MIL-100(Fe)可能吸附了有机物,造成催化剂的孔结构发生变化,从而致使催化剂失活。与干燥处理的回收催化剂相比,使用DMF和无水乙醇清洗回收催化剂,并未有效提高催化剂的催化活性;而经无水乙醇回流条件下洗涤回收的催化剂使得正丁醛的转化率由42.2%升至69.5%,辛烯醛的收率由40.2%升至59.0%,回收催化剂基本保持了原有的催化活性。因此,将使用后的催化剂在无水乙醇回流条件下清洗3遍,每次清洗3 h,再经150 ℃下真空干燥6 h作为回收催化剂的处理方式。
将使用过的H4SiW12O40@MIL-100(Fe)催化剂以上述方式处理并用于正丁醛自缩合反应。在适宜反应条件(催化剂用量15%,反应温度120 ℃,反应时间6 h)下考察催化剂的重复使用性能,结果如表4所示。可以看出,H4SiW12O40@MIL-100(Fe)催化剂重复使用4次后,正丁醛转化率和辛烯醛收率略有降低,辛烯醛选择性基本保持不变。这与本课题组陈翠娜等[4]以H4SiW12O40/SiO2催化正丁醛自缩合反应,催化剂重复使用3次后辛烯醛收率下降23.3%相比,催化剂重复使用性能得以明显改善。通过对正丁醛自缩合产液进行ICP-OES分析,未检测到有铁离子和钨离子存在,表明H4SiW12O40@MIL-100(Fe)催化剂在反应中未发生骨架坍塌等变质现象,且不存在H4SiW12O40流失问题,说明用MIL-100(Fe)包覆H4SiW12O40能够较好地解决活性组分流失问题。上述实验及表征结果表明,H4SiW12O40@MIL-100(Fe)催化剂具有良好的重复使用性能。
Reaction condition:w(H4SiW12O40@MIL-100(Fe))=15%;T=120 ℃;t=6 h

表4 H4SiW12O40@MIL-100(Fe)的重复使用性能Table 4 Reusability of H4SiW12O40@MIL-100(Fe)
Reaction condition:w(H4SiW12O40@MIL-100(Fe))=15%;T=120 ℃;t=6 h
2.5.2 催化剂失活原因分析
对使用前后的H4SiW12O40@MIL-100(Fe)催化剂及无水乙醇回流条件下处理的回收催化剂进行了比表面积及孔结构分析,结果如表5所示。可以看出,与新鲜催化剂相比,回收催化剂的比表面积和孔体积减小较多,平均孔径增大很多,这可能是回收催化剂吸附了有机物造成孔道堵塞所致。回收催化剂经无水乙醇回流条件下洗涤3次后,其织构性质得到改善。其中,比表面积和孔体积明显增大,与新鲜催化剂的测定结果相近,其平均孔径也由原来的2.88 nm降至2.28 nm。这说明用无水乙醇反复处理可以清除堵塞在催化剂孔道中的有机物,从而使催化剂活性恢复。

表5 H4SiW12O40@MIL-100(Fe)催化剂的织构性质Table 5 Textural properties of H4SiW12O40@MIL-100(Fe) catalyst
对使用前后的H4SiW12O40@MIL-100(Fe)催化剂及无水乙醇回流条件下处理的回收催化剂进行了红外分析,结果如图7所示。可以看出,H4SiW12O40@MIL-100(Fe)在使用前后均在1385、1625和712~762 cm-1处出峰,说明使用前后催化剂均保持了MIL-100(Fe)的红外特征吸收峰。另外,与新鲜催化剂相比,回收催化剂除在980、926、1028和779 cm-1处仍然保持H4SiW12O40的Keggin特征吸收峰外,在1054、1725和2968 cm-1等处还出现了新的特征吸收峰,分别归属于—CH2、C=O、—CH3的伸缩振动,表明回收催化剂吸附了有机物[24]。回收催化剂经无水乙醇回流条件下清洗后,1054和1725 cm-1处吸收峰大大减弱,2968 cm-1处吸收峰消失,而其他位置的主要特征峰与新鲜催化剂的主要特征峰基本保持一致,说明用无水乙醇反复清洗可以清除吸附在催化剂孔道中的有机物,这也与比表面积及孔结构表征所得到的结论相符。上述分析结果表明,回收催化剂孔道吸附有机物造成的孔道堵塞应该是致其失活的主要原因,用无水乙醇反复清洗即可清除大部分堵塞在催化剂孔道的有机物,使催化剂活性恢复。
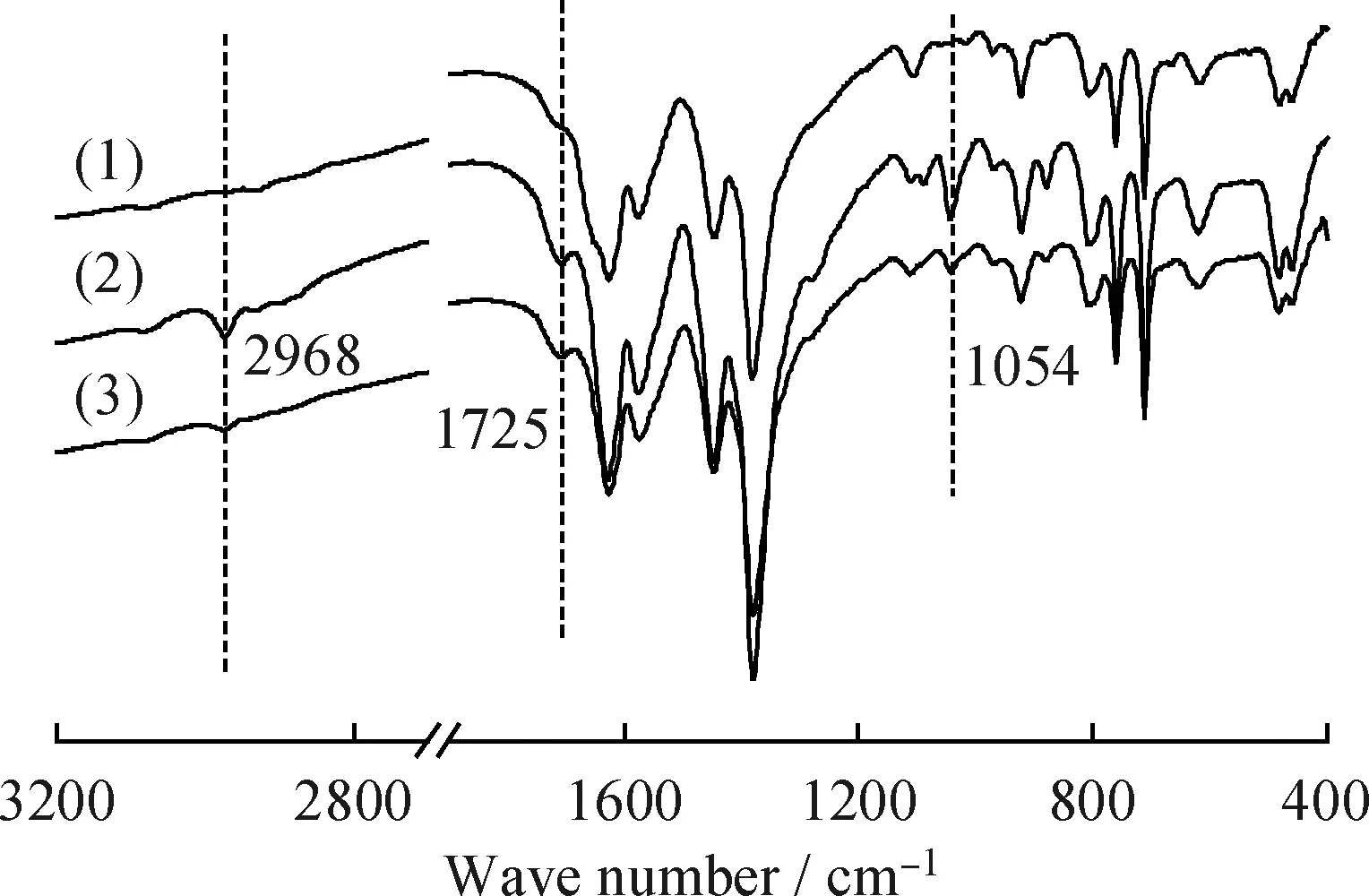
图7 不同H4SiW12O40@MIL-100(Fe)催化剂的红外光谱图Fig.7 FT-IR spectra of different H4SiW12O40@MIL-100(Fe)(1)Fresh H4SiW12O40@MIL-100(Fe);(2)Recovered H4SiW12O40@MIL-100(Fe);(3)Recovered H4SiW12O40@MIL-100(Fe)treated by ethanol under reflux conditions
3 结 论
(1)采用原位合成法制备了H4SiW12O40@MIL-100(Fe),XRD、FT-IR、N2吸附-脱附的表征结果证明H4SiW12O40成功固载在MIL-100(Fe)的介孔笼中且呈高度分散状态。
(2)H4SiW12O40@MIL-100(Fe)催化剂对正丁醛自缩合合成辛烯醛反应有较好的催化性能。硅钨酸适宜负载量为13.7%;适宜反应条件为催化剂用量15%、反应温度120 ℃、反应时间6 h。在此条件下,正丁醛转化率为72.9%,辛烯醛收率为60.9%。
(3)H4SiW12O40@MIL-100(Fe)催化剂的重复使用性较好,反应液中检测不到H4SiW12O40的存在,说明通过制备H4SiW12O40@MIL-100(Fe)可以避免活性组分H4SiW12O40的流失。催化剂失活原因主要是由于反应过程中吸附了有机物,采用无水乙醇回流条件下洗涤3次的方法处理,可以使催化剂活性基本恢复。
