低变质煤热解气体产物的析出特性*
2019-07-31张秋利李凤英惠相荣
张秋利 李凤英 惠相荣 罗 敏 周 军
0 引 言
在我国能源消费结构中,煤炭仍占主导地位[1-3]。我国煤资源煤种分布中低变质煤占主要组成部分,其中陕北地区煤炭资源丰富,煤种多为低变质长焰煤,含油率较高,无黏结性,具有低灰、低硫、低磷、高发热量的特点,是低温干馏的理想原料[4-5]。我国对煤炭资源的利用还存在许多问题,而低变质煤的中低温热解是煤热加工利用中必不可少的工艺环节,也是实现煤炭资源综合、洁净、高效利用的重要途径,更是一种高效、低污染的煤炭分级转化技术[6-7]。因此,研究中低温热解过程的物理化学机理对实现低变质煤安全高效清洁利用有着非常重要的理论和实际意义[8-9]。目前,对煤热解机理的研究主要有两种方法,一种是测热解过程中的产物及相应的失重量,通过推断产物的形成及反应的量来推测反应过程,研究装置为热重在线色谱或质谱。另一种是直接以模型化合物为热解物,可以比较准确推断煤的热解机理。为了获得低变质煤热解气体产物析出规律与演变特征,本研究采用第一种方法,通过改变反应终温,对热解过程产物及相应失重量的测量和热解后固体产物的官能团分析表征,推测不同温度段低变质煤的热解气体产物析出特性。
1 实验部分
1.1 原料
实验原料是来自陕西神木县的长焰煤,原煤经过破碎筛分处理后得到粒径小于0.3mm的粉煤样品以待用。
1.2 仪器及分析方法
1.2.1 工业分析与元素分析
Mad,Aad,Vdaf及 FCad检测依据《煤的工业分析方法》(GB/T 212-2008);C和 H 含量检测依据GB/T 476-2008,N含量检测依据 GB/T 19227-2008,S含量检测依据 GB/T 214-2007。Oad含量用差减法得到,其依据为Cad+Had+Nad+Sad+Oad+Mad+Aad=100%。煤样的工业分析与元素分析见表1。
由表1看出,煤样的挥发分(Vdaf)含量为38.39%,硫的含量为0.42%,是一种具有陕北煤特点的高挥发分、低硫含量的低变质煤,为特别适合热解的优质原料。
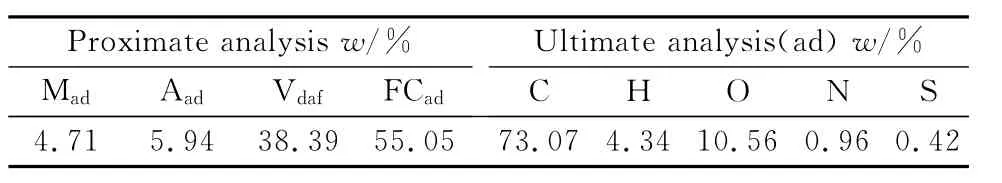
表1 煤样的工业分析与元素分析Table 1 Proximate and ultimate analysis of coal sample
1.2.2 气体组成分析
使用便捷式气体分析仪(Gasboard-3100)来测定主要气体组成,包括CO,CO2,CH4,H2和CnHm。在测定之前需用标准气体进行仪器标定,然后开机预热,将气袋与气体分析仪进口相连接进行测试,为提高结果准确性,记录三组数据,计算其平均值作为最终数据。
1.2.3 傅立叶红外光谱分析(FTIR)
用德国Bruker VERTEX70傅立叶变换红外光谱仪和KBr压片技术,在4 000cm-1~400cm-1的范围内记录样品的傅立叶变换红外光谱(FTIR)。扫描总数为16,光谱分辨率为4cm-1。使用标准KBr粒料程序制备样品来进行光谱分析。

图1 实验设备及流程Fig.1 Flow diagram for experimental equipment
1.3 热解过程
煤热解的实验流程如图1所示,热解过程实验装置依次为管式热解炉、石英管反应器、空气冷却装置、焦油收集装置、一级水冷装置、二级水冷装置、气体干燥装置、气体收集装置,各个装置连接处确保密封良好。
在装有石英反应管的电加热管式炉中进行热解实验。将100g未经预处理的原煤粉样品加入石英管反应器中,置于管式热解炉内,分别设定不同的目标温度,均以相同的升温速率10℃/min进行加热,升至目标终温后保温120min。气体产物用集气袋收集,液体产物用焦油收集装置进行收集,固体产物则残存于石英管中,待炉内温度冷却至室温后称重取样分析。
2 结果与讨论
2.1 气态产物分析
低变质煤分子普遍认为是由不同脂族基团连接的芳族和氢化芳族环的簇[12],一般来说,其热解包括键断裂反应和大分子网络分解成较小的碎片,这些碎片可能以焦油和气体的形式析出,气体产品的主要成分是甲烷(CH4)、一氧化碳(CO)、二氧化碳(CO2)、氢气(H2)和少量碳氢化合物(CnHm)。在不同热解温度下得到的气态产物总体积的拟合曲线见图2。

图2 不同热解温度下的气态产物体积Fig.2 Volume of gaseous product at different pyrolysis temperature
由图2可以看出,热解过程中在很宽的温度范围内有裂解气体释放。实验发现在150℃时开始有气体产生,达到350℃时,气体产生速率逐渐加快,在600℃以上迅速增加,并且温度越高气态产物产生速率越快。
为进一步清楚阐明各种气态产物的释放规律,对气体组分进行了分析,结果见表2。
由表2可以看出,随着温度的增加,CO含量持续增加,在800℃左右达到峰值,然后略微下降。CO2在700℃之前少量逸出,在700℃之后含量迅速增加。H2在700℃之前含量极少,在700℃之后大量增加。在热解过程中,CH4是随温度升高而逐渐增加的,在800℃含量达到最大。较大分子量的碳氢化合物(CnHm)的生成量比较小分子量的碳氢化合物(CH4)的量要少得多,其含量变化波动不大。
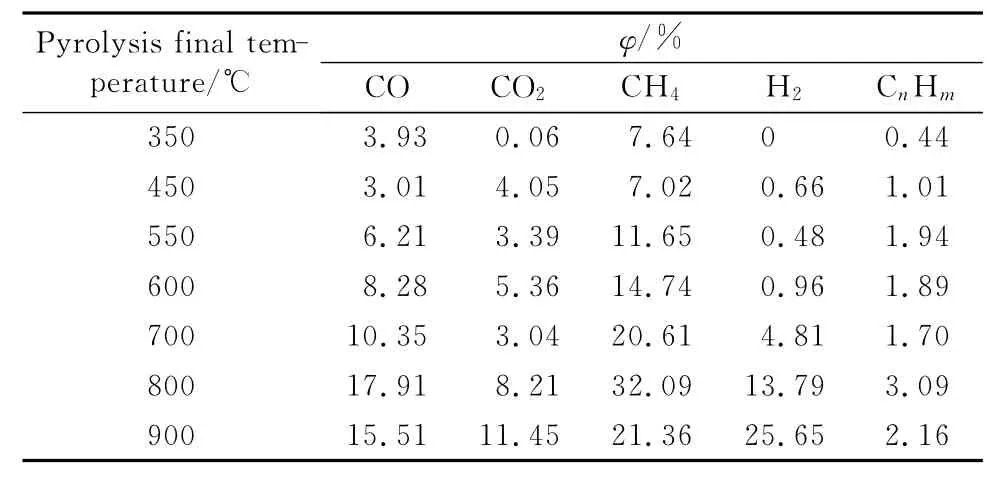
表2 不同热解温度时的气体成分变化Table 2 Gas composition change at different pyrolysis temperatures
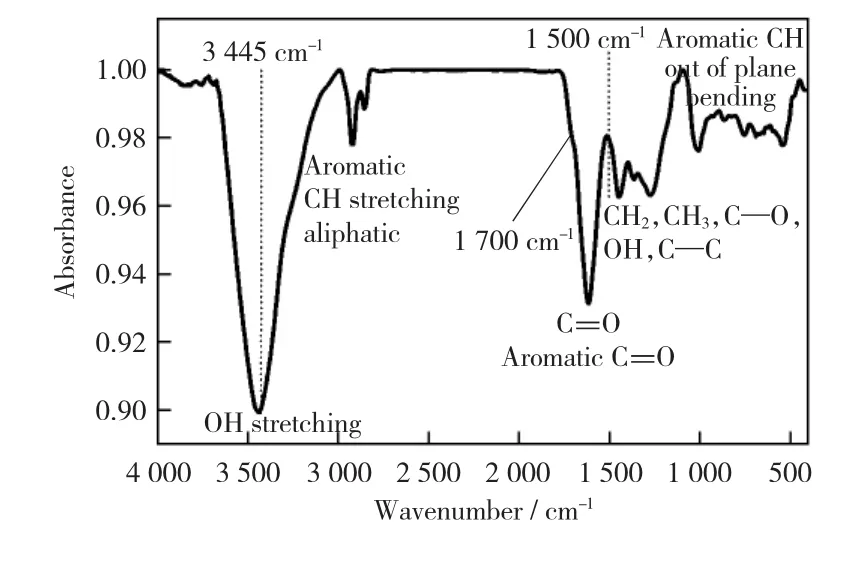
图3 煤样的红外光谱分析Fig.3 FTIR spectra of coal sample
2.2 固态产物的分析表征
图3为原煤的傅立叶变换红外光谱。由图3可知,在约3 445cm-1处有明显的吸收峰,其归属于羟基(—OH)基团。在3 000cm-1~2 700cm-1区域的吸收峰对应的是芳族氢、CH伸缩和脂族氢的吸收峰。在1 800cm-1~1 100cm-1和1 100cm-1区域中也可以分别观察到含氧官能团和C—O—R结构的显著吸收峰。芳香氢位于900cm-1~700 cm-1区域。此外,在1 500cm-1处存在明显的吸收峰,该峰与芳香单元的缩合和取代程度有关[10],并且也受苯环上取代基的性质和位置的影响[11]。
将不同温度下得到的固态产物进行红外表征,红外光谱分析如图4所示。由图4可以看出,在3 445cm-1,2 929cm-1,1 622cm-1,1 452cm-1以及1 269cm-1附近均出现了明显的吸收峰[13-14]。
图4中3 445cm-1处为羟基(—OH)的伸缩振动,说明原煤和不同终温下固体产物表面均有醇或酚结构存在。随着温度的升高,热解程度进一步加深,固态产物的羟基吸收峰与原煤相比明显减弱。2 929cm-1处是CH2反对称伸缩振动,表征着固体表面环烷和脂肪族类物质,峰值均较小,低温时随着温度的变化较小。热解温度对固态产物表面的脂肪结构影响不明显,热解温度升高到600℃~700℃时,吸收峰明显相对减小,在800℃~900℃逐渐增大。1 622cm-1处为 C O伸缩振动,说明固体表面结构中存在羧基、醛或酮类结构。从350℃起,固态产物的此吸收峰相对原煤明显变小,在较低温度的热解过程中变化较小,在较高温度下变化较明显。1 452cm-1处为CH3反对称变形振动,表征着甲基基团的特征吸收,随着热解温度的升高,吸收峰强度逐渐减小。1 269cm-1处为C—O—C伸缩振动,表明可能存在醚或环氧类物质,而且该峰为大分子环氧类物质的C—O振动,随着温度的升高呈现逐渐减弱趋势。
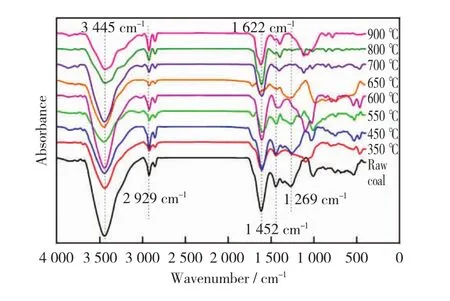
图4 不同温度下固态产物与原煤的红外光谱分析Fig.4 FTIR spectra of the solid products and raw coal at different temperature
2.3 气态产物的析出特性
将不同条件下的析出气体组分分布规律与固态产物结构变化进行对比分析,可以推测在不同温度段下气态产物的析出特性。原煤与不同温度下固态产物的红外光谱如图5所示。
由图5a可以看出,在350℃时固态产物吸收峰与原煤明显不同。3 445cm-1处羟基振动峰强度明显减弱,2 929cm-1处的CH2反对称伸缩振动峰略微减小,实验过程中发现有水生成。因此,水的形成与醇、酚结构中一些不稳定羟基的断裂以及环烷和脂肪族类物质发生断裂产生氢自由基有关,推测此阶段水的形成是由式(1)~式(3)的反应和原煤表面的吸附水解析所得。

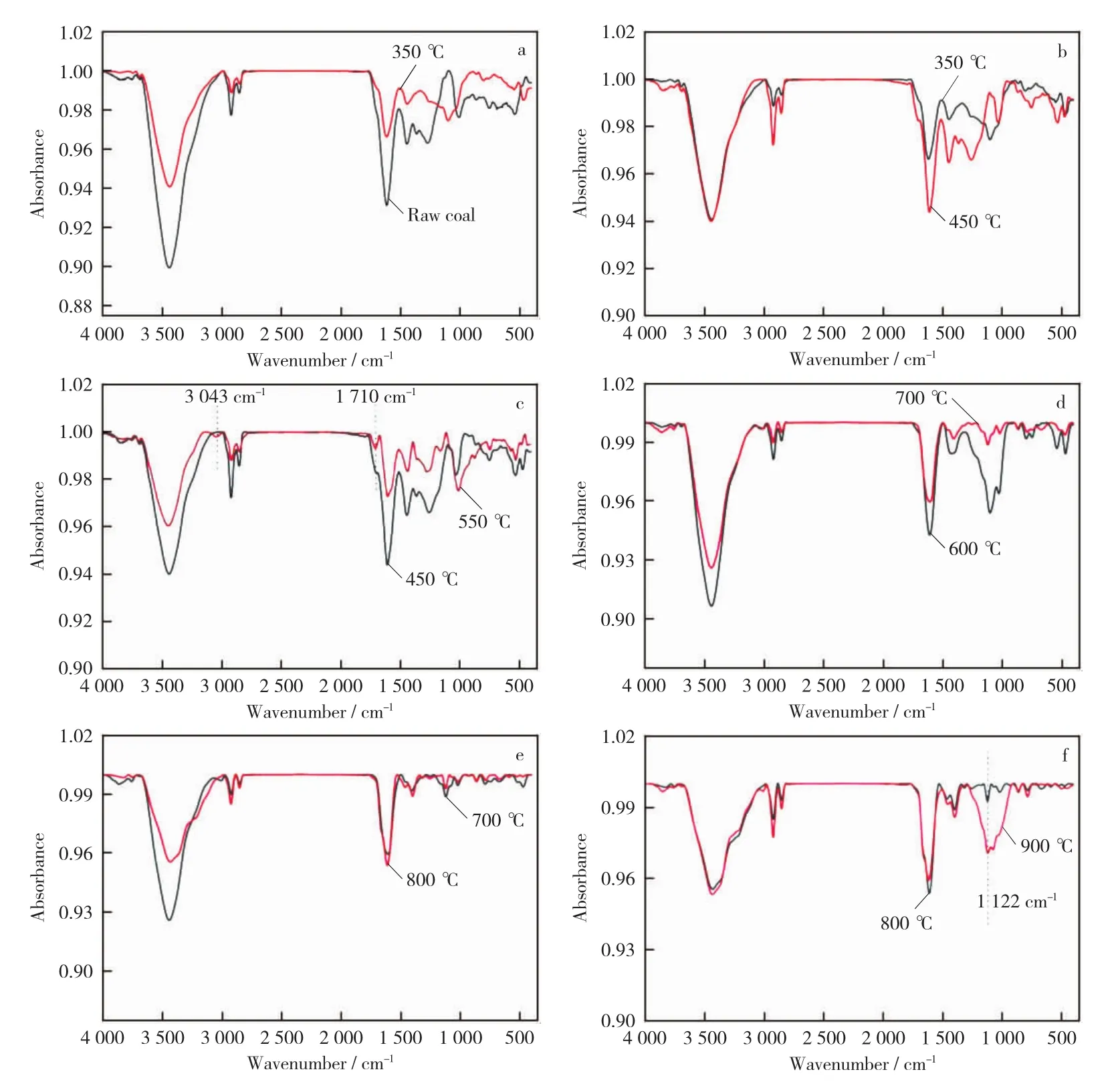
图5 原煤及不同温度下固态产物的红外光谱对比Fig.5 Comparison of FTIR spectra between raw coal and solid products at different temperature

图5a中1 622cm-1处的 C O伸缩振动峰明显减弱,1 269cm-1处的C—O—C伸缩振动峰略微减弱,此时实验测得CO含量为3.93%(见表2),说明煤表面结构中的羧基、醛或酮类结构中的弱键断裂分解以及小部分醚键和含氧杂环发生裂解,导致CO生成,其反应为式(4)~式(6)。由于此时CO2含量仅为0.06%(见表2),推测极少部分CO与氧原子生成CO2(见式(7)和式(8)),CO2还有可能是由于羧基裂解产生(见式(9))。

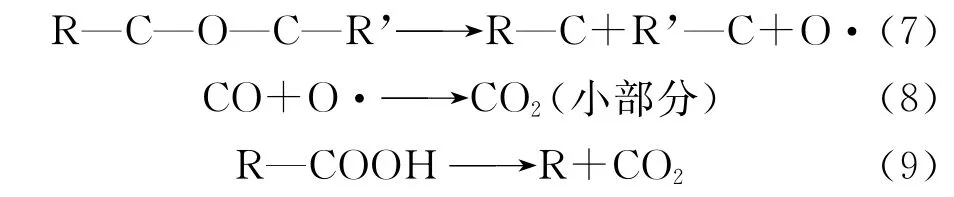
图5a中1 452cm-1处的CH3反对称变形振动峰也相应减弱,此时得到的CH4含量为7.64%(见表2),CnHm为0.44%,表明含量较高的CH4是由煤中含有甲基官能团的脂肪链和芳香侧链断键形成的,同时伴随少量碳氢化合物产生,其反应为式(10)和式(11)。

由图5b可以看出,在450℃与350℃时固态产物的羟基振动峰峰值几乎一致,说明不稳定的弱键羟基官能团已经在350℃之前断裂完全。CH2反对称伸缩振动峰则明显增强,说明此阶段自由基片段结合使得脂肪链与环烷结构有所增加以及部分次甲基转化为亚甲基,推测其反应为式(12)~式(14)。伸缩振动峰明显增强,C—O—C醚键略微增强,此时CO含量减少,而CO2含量为4.05%(见表2),增加明显,表明自由片段重新组合形成醌、醛或酮类结构以及醚键结构,并且部分以CO2形式释放,其反应为式(15)~式(17)(式(17)中Ph代表芳香基团,下同)。
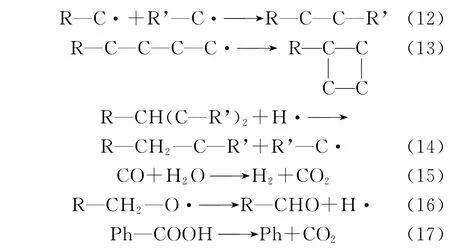
由图5c可以看出,在550℃时固态产物的羟基振动峰相对450℃减弱,表明此时H2O形成是由一些较强的羟基键断裂生成,反应可能为式(18)~式(21)。CH伸缩振动峰代表的芳香次甲基基团增加,是由于亚甲基的转化和叔碳上的羧基的分解(见式(22)和式(23))。 C O伸缩振动峰明显减弱,且此时CO含量为6.21%(见表2),增加一倍多,表明煤结构中一些较强的 C O结构分解以CO形式析出(见式(4)与式(24))。CH4含量大量增加,为11.65%(见表2),且CH3结构也相应减弱,表明CH4一部分是由与芳基/烷基醚键相连甲基的断裂形成(见式(10)与式(25))。此时 H2含量略微减少,表明部分H2参与了反应(见式(26))。此阶段的各明显吸收峰都相应减弱,说明了在此温度段的热解程度进一步增强,气体总产率显著增大,这与气体总体积变化趋势一致。
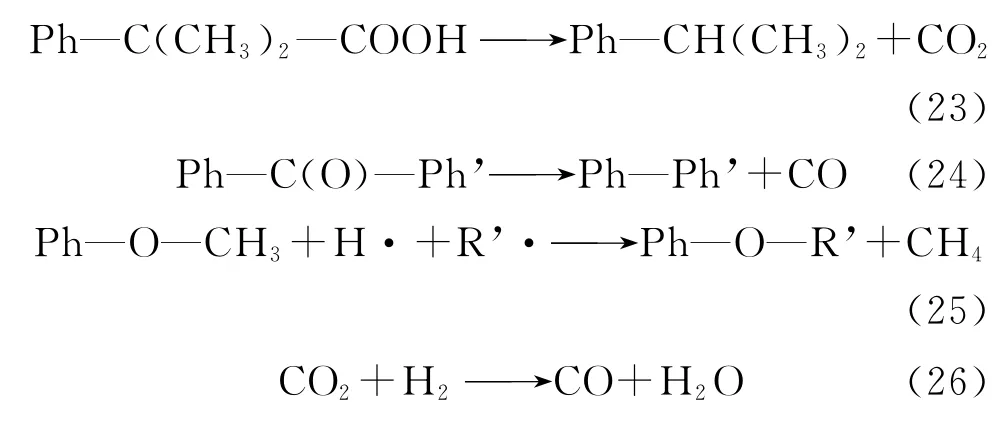
由图5d可以看出,各个官能团吸收峰进一步显著减弱,表明低变质煤的热解程度进一步加深,官能团裂解反应更为剧烈,自由基碎片大量增加,挥发分大量析出,这与热解产物析出率显著增加一致。从产物气体组成可以看出,CO为10.35%,CH4为20.61%(见表2),明显迅速增加,这归因于大量羟基、羰基、醚键裂解反应(见式(4)~式(6)、式(10)和式(27)),以及脂肪链、甲氧基等强键的断裂反应(见式(10)、式(11)、式(25)和式(28))。H2组分含量迅速增加,为4.81%(见表2),这是由一些自由基碎片重组发生缩聚脱氢以及环烷烃的芳构化导致的,其反应见式(29)~式(32)。此时CO2含量减少,由于此时的固态产物自身与CO2发生反应,同时与H2反应,其反应见式(33)和式(34)。
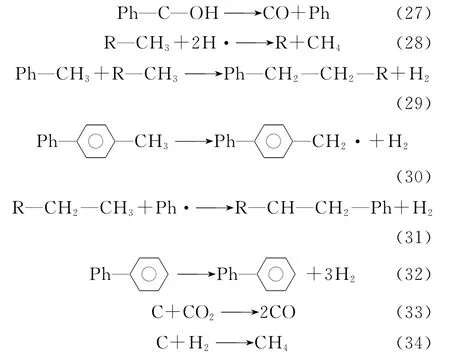
由图5e可以看出,羟基官能团吸收峰明显减弱,其他特征吸收峰变化较小,这表明此时煤中的挥发分组分绝大部分已析出完全,但此时各组分气体都大量增加,且实验分析发现此时气体产率显著增大,焦油产率明显减少,焦炭略微减少,由此得出此阶段气体增加是由于焦油的二次裂解(见式(35)和式(36))。H2含量呈加速增长趋势,表明温度越高,缩聚反应越剧烈(见式(37))。

由图5f看出,固态产物的红外光谱大致重合,在1 122cm-1处的醚键官能团吸收峰有所变化,此时CO含量减少,推测CO形成与醚键官能团有关,并且可能由于高温条件下参与二次化学反应,其反应见式(38)和式(39)。此时H2含量大幅增加,为25.65%(见表2),表明在此阶段以芳环结构脱氢缩聚为主,固态产物结构进一步芳构化,密度增加,体积收缩,形成具有一定强度的碎块,从而使得H2大量析出(见式(32)和式(40))。CH4与CnHm烃类含量相对减少,这是由于在高温下发生了裂解与缩合反应(见式(41)~式(43))。

由以上分析得出,CO析出规律分为三个阶段:在低温区开始析出,随温度升高含量缓慢增加,这是由于羧基、醛或酮类结构当中的弱键断裂分解和小部分醚键、含氧杂环发生裂解,以及部分CO2与固态产物或H2发生反应;在700℃~800℃为迅速增加阶段,大量羧基、甲氧基、酚羟基、醚键以及含氧杂环等含氧结构裂解,并且液态产物焦油发生二次裂解,此时热解程度最大,CO大量析出;在800℃之后,CO析出减少,这是由于在高温条件下CO参与二次化学反应。
CO2析出规律分为两个阶段:在700℃之前析出量较少,波动大,此阶段主要是醌、醛或酮类结构以及醚键结构发生裂解,部分以CO2形式释放,同时也会与固态产物或者H2反应;在700℃之后,CO2含量呈大幅上升趋势,这是由焦油二次裂解其中含氧杂环或羰基官能团断裂而形成的,CO与CO2部分之间伴随着相互转换。
CH4析出规律分为三个阶段:450℃之前CH4是由一些弱甲基键的断裂形成的;450℃~800℃之间为线性增长阶段,随温度的升高,CH4产率增加,此阶段CH4主要是由甲氧基和侧链甲基以及焦油中烷烃类物质的裂解而形成,同时固态产物与氢气发生二次反应也会产生CH4;在800℃之后CH4含量呈下降趋势,这是由于部分CH4发生裂解。CnHm碳氢化合物变化差异不大且含量相对较少。
H2析出规律分为两个阶段:在600℃之前只有少量H2逸出,这是由极少部分游离氢自由基的自由组合形成;在600℃之后H2析出量开始迅速增加,并且温度越高,释放速率越大,这主要是由于脱氢缩聚、固态产物结构芳构化以及气体分子间的聚合反应和小分子裂解。
2.4 热解产物收率
煤在热解过程中生成气态产物、液态产物和固态产物。实验得到的低变质煤热解产物的产率见表3。

表3 在不同温度下的各热解产物产率Table 3 Yield of pyrolysis products at different temperature
由表3可以看出,随热解温度的升高,固态产物产率因挥发分的析出而降低,结合前述气态产物析出特性分析,得出热解过程分为四个阶段。第一阶段室温至450℃之间,气液态产物产率缓慢增加,主要是由于煤表面吸附物质的释放以及一些不稳定弱键开始断裂析出少量气体,同时自由基碎片自由重组。煤热解的液态产物包含焦油和水,水的产生是由于煤本身含有的吸附水分与羟基官能团热解断裂产生的。第二阶段在450℃~700℃之间,气体释放量显著增大并且气体各组分浓度都相应增加,焦油产率明显增加,特征官能团振动峰都相应减弱,说明在此温度段的热解程度进一步增强,各个官能团裂解反应更为剧烈,自由基碎片大量增加并以挥发分形式析出。在700℃到达最大值,此时液态产物焦油的产率最大。第三阶段700℃~800℃,液态产物产率呈现下降趋势,主要是由于液态焦油发生二次裂解,这与气态产物大量增加、固态产物略微减少是一致的。第四阶段800℃~900℃之间,气态产物持续增加,主要原因为固态产物结构芳构化脱氢和焦油二次裂解。
3 结 论
1)随着热解温度的升高,热解程度加深,各个官能团自由基脱落或者发生缩合反应以挥发分的形式释放,因此,固态产物的特征吸收峰与原煤相比明显发生变化。
2)CO在低温区是由含氧结构中的弱键断裂以及部分CO2与固态产物或H2发生反应转化而成,在高温时是由于大量含氧结构裂解和焦油二次裂解。CO2产生主要是由于醌、醛或酮类结构、醚键结构发生裂解,以及焦油中含氧杂环或羰基官能团的断裂。CH4在低温区是由弱甲基键的断裂形成的,中高温时是由于甲氧基、侧链甲基、焦油中烷烃类物质的裂解,以及固态产物与氢气的二次反应。H2是由部分游离氢自由组合形成的,高温时由于脱氢缩聚、固态产物结构芳构化以及气体分子间的聚合反应和小分子裂解形成了H2。
3)各温度段产物的析出规律为:第一阶段,煤表面吸附物质释放以及一些不稳定的弱键开始断裂析出少量气体,并伴随着自由基碎片发生重组;第二阶段,气体和焦油释放量显著增大,热解程度增强,官能团裂解反应剧烈,自由基碎片大量增加;第三阶段,焦油发生二次裂解;第四阶段,固态产物结构芳构化脱氢。
