自体心包在主动脉瓣重建中的临床应用▲
2019-07-22刘永春郑晓宇叶仕高石俊杰
刘永春 郑晓宇 陈 文 叶仕高 石俊杰
(广西医科大学第五附属医院暨南宁市第一人民医院心胸血管外科,南宁市 530021)
主动脉瓣膜及根部疾病的治疗绝大部分需要行机械瓣或生物瓣置换。机械瓣的主要远期并发症为抗凝相关并发症和瓣下内膜增生导致瓣膜急性失功;生物瓣的主要远期并发症为瓣膜毁损,且发生率较高。鉴于瓣膜置换远期并发症较多,很多学者一直致力于主动脉瓣修复手术。国内有关主动脉瓣修复手术的报道比较少,而且报道仅限于主动脉瓣关闭不全。Ozaki等[1]报道了一种适用范围更广的主动脉瓣重建手术(AVneo手术),Valdis等[2]报道综合性的主动脉瓣膜及根部成形技术,不仅适用于主动脉瓣关闭不全,而且适用于主动脉瓣狭窄、感染性心内膜炎、人工瓣膜心内膜炎以及主动脉瓣环扩张患者,而且对儿童的主动脉瓣膜病变也同样适用。我院近期开展了3例主动脉瓣重建手术,现将结果报告如下。
1 资料与方法
1.1 例1病例资料和手术方法
1.1.1 病例资料 男,72岁,体重44.5 kg,因“反复胸闷、气喘2个月,再发加重2 d”入院,诊断为主动脉瓣狭窄并关闭不全;慢性肾功能不全;心功能(NYHA)Ⅲ级。冠脉造影未见明显狭窄;升主动脉+左心室造影显示主动脉瓣狭窄并关闭不全;心脏彩超显示主动脉瓣环直径20 mm,主动脉窦部直径32 mm,升主动脉内径30 mm,左室舒张末期内径58 mm,射血分数(EF)64%,主动脉瓣呈三叶式结构,瓣膜增厚并局部不规则钙化,于左冠瓣与无冠瓣交界处可见一大小约1.0 cm×0.7 cm之钙化斑回声,瓣膜开幅受限,开幅9~10 mm,瓣口前向血流速度增快,速度360 cm/s,跨瓣压差52 mmHg。
1.1.2 手术方法 予全身麻醉,正中开胸,取大小7 cm×7 cm自体心包,并剔除心包表面脂肪组织,用0.6%戊二醛溶液浸泡心包10 min,重复漂洗10 min,主动脉根部及上下腔静脉插管建立体外循环,横向切开主动脉管壁,经左右冠状动脉开口灌注HTK溶液,探查病变情况。无冠瓣、右无交界及左无交界钙化固定,剪除主动脉瓣叶,测量窦管交界直径25 mm,主动脉瓣环直径19 mm,标记各瓣叶中点及瓣叶交界点,根据窦管交界直径,将固定的心包根据窦管交界长度制作三个新的瓣叶,光滑面向左室面,从瓣环的最底部开始缝合,用5/0号Prolene线连续缝合(图1),分别将三个新的瓣叶缝合至瓣叶交界顶端,调整并固定于主动脉壁(图2),复温,缝合主动脉切口,排气,心脏复跳辅助循环,血流动力学稳定后常规停机拔除插管及关胸,术中食管超声检查见重建主动脉瓣叶开闭良好。
1.2 例2病例资料和手术方法
1.2.1 病例资料 男,68岁,体重70.5 kg,因“反复胸闷、气喘2年余,再发加重2 h”入院,冠脉造影后突发气喘、大汗淋漓、烦躁、胸闷、呼吸困难、半卧位、呼吸急促、急性左心衰,予气管插管呼吸机辅助呼吸,冠脉造影未见异常。诊断:主动脉瓣重度狭窄;心功能Ⅳ级;急性左心衰竭;肺部感染;脑梗死后遗症。心脏彩超显示主动脉瓣环直径22 mm,主动脉窦部直径32 mm,升主动脉内径40 mm,左室舒张末期内径51 mm,左室收缩末期内径36 mm,室间隔厚15 mm,左室后壁厚15 mm,EF 57%,主动脉瓣明显增粗钙化,受钙化影响瓣叶结构显示不清,似呈斜裂式二叶瓣,开瓣活动明显受限,瓣口前向血流速度增快,流速425 cm/s,跨瓣压差72 mmHg;轻度反流,二尖瓣前瓣轻微脱垂并轻度关闭不全,左室壁增厚,左室舒张功能减退。
1.2.2 手术方法 心包处理同前,探查病变情况:主动脉瓣二瓣化,呈前后瓣叶,后瓣全部钙化固定,并波及主动脉瓣环。剪除主动脉瓣叶,测量窦管交界直径25 mm,将12点交界作为标记,三等分标记另两个新的交界点(图3),根据窦管交界直径,将固定的心包根据窦管交界长度制作三个新的瓣叶,光滑面向左室面,从交界最底部中点开始,用5/0号Prolene线连续缝合,分别将三个新的瓣叶缝合至瓣叶交界顶端,调整并固定于主动脉壁,复温,缝合主动脉切口,排气,辅助循环,术中食管超声检查见重建主动脉瓣叶开闭良好。停机,左房压力大于30 mmHg,考虑左心肥厚导致左心功能不全,行左心辅助,待血流动力学稳定后,常规停机并拔除插管及关胸,但需要大量血管活性药物维持,即行体外膜肺氧合辅助。
1.3 例3病例资料和手术方法
1.3.1 病例资料 男,80岁,因“反复气喘1年余,再发加重3 d”入院。诊断:主动脉瓣狭窄并关闭不全;心功能Ⅲ级;冠脉造影冠脉未见明显狭窄。心脏彩超显示主动脉瓣环直径19 mm,主动脉窦部直径32 mm,升主动脉内径37 mm,左室舒张末期内径68 mm,EF 36%,主动脉瓣叶数目显示不清,瓣叶明显增厚、钙化、粘连、开放明显受限,最大开幅约6.2 mm,瓣口前向血流速度增快,速度468 cm/s,跨瓣压差88 mmHg。
1.3.2 手术方法 手术方法过程同例1,术中探查:主动脉瓣三个瓣叶全部钙化,窦管交界直径27 mm。

图1 Prolone线连续缝合
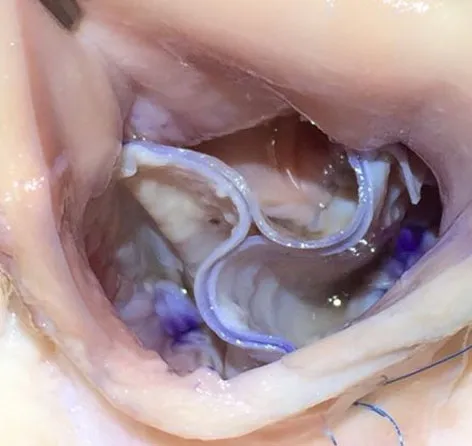
图2 缝合瓣叶固定

图3 瓣角交界标记点
2 结 果
3例患者手术前后结果显示,主动脉瓣瓣环明显扩大,瓣叶活动良好,瓣叶关闭良好,无明显反流,瓣叶的血流速度减慢,跨瓣压差减小,患者症状消失,均顺利出院。与常规更换瓣膜手术对比,自体心包主动脉瓣重建术后患者的瓣环仍保留收缩性,患者未服用抗凝药,减少到医院复查凝血功能次数,无排异反应,减少医疗费用,提高了生活质量,延长寿命,此手术后具备重复性,也可以再次介入下行生物瓣置换术。手术前后经胸超声检查结果对比如下,效果良好。见表1。
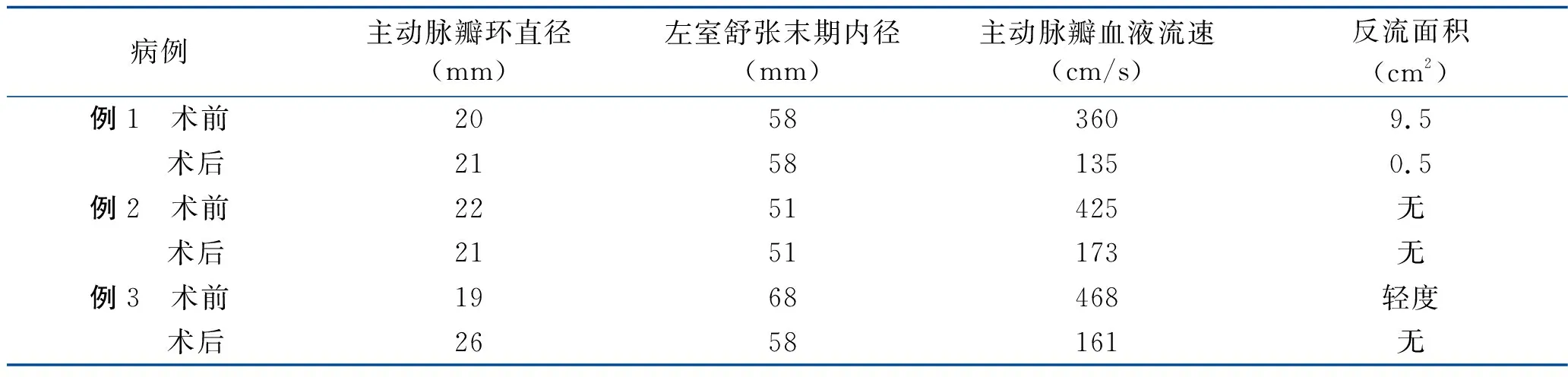
表1 3例患者手术前后经胸超声检查结果
3 讨 论
主动脉瓣由于特殊的结构及位置,承受的压力大,而主动脉瓣成形手术的技术要求较高,难度大,所以目前临床治疗主要是人工主动脉瓣置换术为主。但在整个心动周期中,包括主动脉瓣叶、瓣环在内的根部结构都是活动的[3],主动脉根部结构随心动周期扩张和收缩是左心室机械性射血和充盈机制的重要组成部分,在收缩期瓣环扩张以降低压力梯度,在舒张期瓣环收缩血流往瓣膜回流分布至窦部与瓣叶。机械瓣和生物瓣由于存在相对固定的瓣架结构,使主动脉根部丧失了这种动态活动的功能。自体心包主动脉瓣重建术有效地保护了主动脉根部的功能。
以自体心包作为材料,没有人工材料替换产生的血栓和排异问题,而且保留了主动脉瓣三维结构和良好的血流动力学效果,可以较好地维持心脏的解剖生理功能。自体心包主动脉瓣重建,不仅取材容易,无组织抗原性,组织学上有间皮层、弹力纤维及胶原纤维,具有较好的弹性和组织相容性[4],重建的主动脉瓣有效开口面积大,跨瓣压差小,从而使得患者术后左心室构型和功能恢复较快。
美国心脏学会(AHA)指出,主动脉瓣成形术只能在具备相关手术技巧并保证与主动脉瓣置换取得同等效果的心脏中心施行。可行主动脉瓣置换的患者原则上都可行主动脉瓣成形术,但目前主动脉瓣成形术主要适用于部分主动脉瓣关闭不全患者,少部分适用于主动脉瓣狭窄患者。主动脉瓣关闭不全患者能否施行主动脉瓣成形术,取决于主动脉瓣关闭不全的病因、主动脉瓣及相关结构的病理变化[5]。因此自体心包作为主动脉瓣重建材料,可用于风湿性主动脉瓣病变、感染性心内膜炎、先天性主动脉瓣狭窄或关闭不全、退行性主动脉瓣关闭不全,此类主动脉瓣成形患者术后不需要华法林抗凝治疗,仅需短期使用阿司匹林即可,避免了人工瓣膜置换后华法林抗凝的定期复查和出现出血/血栓形成的风险,大大提高了患者的生活质量,自体心包主动脉瓣重建不仅适用于主动脉瓣关闭不全,还适用于主动脉瓣狭窄、感染性心内膜炎、人工瓣膜心内膜炎以及主动脉瓣环扩张患者。由于儿童的生理特点,华法林剂量可能会随生长发育而不断变化,加之儿童依从性较差,长期治疗可能出现漏服或停药,导致相关并发症的发生[6]。自体心包主动脉瓣重建不需要抗凝,因此不仅适用于成年人,对儿童也同样适用。
自体心包主动脉瓣重建不改变患者的瓣环大小,术后不会导致瓣口面积减少。传统的瓣膜置换手术,对小的主动脉瓣环需要扩大瓣环技术,才能从解剖上改变瓣环大小。传统采用Nicks法(经无冠窦部切开瓣环并补片加宽)、Manouguian法(经左无交界切开瓣环并补片加宽)等各种瓣环扩大技术,手术过程较为复杂,易出现吻合口撕裂、出血、瓣周漏、严重低心排、传导束受损、冠状动脉血运受阻等手术并发症,因此在瓣环扩大的实施上心脏外科医生多持慎重态度[7]。人工瓣膜的不匹配现象会影响术后患者血流动力学改变,可导致术后心衰的发生,同时使患者的早期死亡率及心血管不良事件发生率增加[8]。
综上所述,自体心包主动脉瓣重建术属于自体组织,无排异,术后不需要抗凝治疗,跨瓣压低,相比于常规主动脉瓣置换的可重复性更好,比Ross手术更简单,无瓣环大小限制,更具抗感染性。因此,自体心包主动脉瓣重建手术是一种全新的主动脉瓣叶重建手术,有着诸多临床优势,具有良好的推广和应用前景。
