抗HU抗体阳性副肿瘤性小脑变性1例及文献复习
2019-06-21高晓宇郑雪姣狄政莉薛秀云刘志勤
高晓宇 郑雪姣 狄政莉 薛秀云 刘志勤
西安市中心医院,陕西 西安 710003
1 病例资料
患者 男,54岁。以“行走不稳17 d”之主诉于2017-09-18入院,患者17 d前出现呕吐,呈间断性反复呕吐,呕吐物为胃内容物,曾就诊于当地医院,给予静脉药物治疗(具体治疗不详),治疗期间患者出现双下肢乏力感,行走欠稳,但日常生活不受影响,查头颅、颈椎及腰椎MRI示,头颅、颈椎未见明显异常,轻度腰椎间盘突出。住院治疗期间上述症状进行性加重,出现行走费力,双下肢发软,言语混乱,间断性呕吐,无头痛、头晕、肢体的抽搐及意识不清,就诊于西安市中心医院门诊,门诊以“行走不稳待查”收入我科。既往糖尿病病史6 a余,未规律治疗。
1.1体格检查体温36.2 ℃,脉搏75次/min,呼吸20次/min,血压103/62 mmHg(1 mmHg=0.133 kPa),发育正常,皮肤黏膜无黄染,双瞳孔等大等圆,直径约2.5 mm,对光反应灵敏,双眼向各方向运动充分,心、肺、腹检查(-)。躯干及四肢肌力V级,肌张力正常。未见不自主运动,双侧指鼻试验、轮替试验、跟膝胫试验均欠稳准,闭目难立征阴性,躯干及四肢浅感觉未见异常,双侧深反射及跟腱反射均(+),腹壁反射、提睾反射正常存在,双侧病理征均(+),颈软,无抵抗,脑膜刺激征阴性。
1.2辅助检查入院后查甲状腺功能:游离甲状腺素25.24 pmol/L;贫血系列正常;肝肾功、生化、心肌酶谱、血、尿、粪常规未见明显异常;追问病史患者1个月前无明显诱因出现反复呕吐,查肿瘤系列示胃癌抗原(CA199)40.15 U/mL,正常值<37 U/mL,胃泌素释放肽前体(Pro-GRP)248.7 U/mL,>300 U/mL对小细胞肺癌的诊断可能性大,细胞角蛋白19片段测定(CYFRA21)5.09 U/mL,>2.13为阳性,神经元特异性烯醇化酶测定(NSE)22.30 U/mL,男性正常值3.4~11.7 U/mL,因此不除外消化道肿瘤的可能。行胃镜示胃角黏膜病变,慢性萎缩性胃炎伴急性炎症;腹部CT示纵膈淋巴结肿大;胃镜病理回报示,胃角小块黏膜重度慢性炎,因此排除消化道肿瘤,治疗期间患者行走困难未改善。行胸部CT示,右肺中叶、下叶及左肺上叶纤维条索;结合腹部CT示纵膈淋巴结肿大,目前仍不排除呼吸道肿瘤的可能,建议患者进一步行脑脊液及血液肿瘤相关抗体检查,继续给予改善循环等对症治疗。脑脊液生化示,葡萄糖4.73 mmol/L,微量总蛋白548.00 mg/L;脑脊液抗酸、墨汁染色阴性。脑脊液常规示,红细胞数0,白细胞26个/mm3;副肿瘤相关抗体抗Hu抗体阳性。肌电图检查考虑患者为糖尿病神经病变,目前患者复查肿瘤系列示,胃泌素释放肽前体(Pro-GRP)174.3 U/mL,细胞角蛋白19片段测定(CYFRA21)6.06 U/mL,神经元特异性烯醇化酶测定(NSE)22.58 U/mL,仍考虑可能存在呼吸道肿瘤。行胸部增强CT示,左肺上叶前段占位病变,考虑新生物(图1);左肺上叶尖后段纤维条灶索;纵隔内及左肺门区多发淋巴结肿大(图2)。结合患者临床表现和辅助检查,临床诊断为副肿瘤性小脑变性。
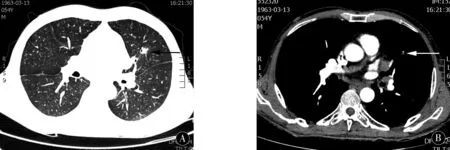
图1 左肺上叶前段占位病变,考虑新生物 图2 纵隔窗可见小结节,密度不均,内可见高密度影,边界不清
2 讨论
神经系统副肿瘤综合征(paraneoplastic neurologicalsyndromes,PNS)是指由肿瘤引发的“远隔”神经系统损害的症候群。而副肿瘤性小脑变性(paraneoplastic cerebellardegeneration,PCD)是累及中枢神经危害最大也最易鉴别的 PNS[1]。神经系统副肿瘤综合征(PNS)是一种罕见的副肿瘤综合征,并不是由肿瘤转移或直接浸润到神经系统引起,是由免疫反应的改变引起[2]。PNS多为中年以上起病,呈亚急性进展病程[3]。其中最常见的是亚急性小脑变性、边缘叶脑炎、感觉神经元病[4]。25%以上的患者不同的PNS可叠加在一起[5]。PNS以小脑损害的症状和体征为主,与其他类型的亚急性小脑性共济失调很难鉴别,仅少数可自行行走,约40%的患者以不对称性共济失调起病,很快进展为对称性。脑干症状,如构音障碍、复视等常见,也可见认知障碍及精神障碍,使该病难以诊治[6]。目前对 PCD 的亚型分类尚有争议[7-8]。PCD是一种罕见的非转移性神经并发症,是癌症的一种远程效应[9]。该患者即以双下肢行走不稳收入院,表现为小脑受损的症状与体征,脑干受损症状与体征未表现。有文献报道PCD常与肺癌、乳腺癌、卵巢癌和霍奇金淋巴瘤有关[10],也有文献报道PNS主要见于肺癌,尤其小细胞肺癌。本例患者是单独以副肿瘤性小脑变性为首发的肺癌。PNS可于恶性肿瘤发生之前、之后或同时发生,约80%的患者在发现肿瘤前出现神经系统症状[11],本例患者符合这一点。PCD 与自身免疫关系密切,目前累计报道有近30 种不同的自身抗体与 PCD 有关,包括抗 Yo 抗体,抗 Tr抗体、抗 Hu 抗体和抗 Ma 抗体等[12]。抗Hu抗体被认为是最常见的抗体[13]。还有文献报道抗Hu抗体阳性的PNS患者中75%为男性[14],该患者即中老年男性,亚急性小脑变性。患者头颅MRI未见明显异常,可排除原发颅内肿瘤或转移瘤,CSF检查有蛋白升高,国外研究发现,7例副肿瘤性小脑变性的患者行脑脊液检查,4例蛋白含量略增高,1例蛋白含量、细胞数轻度增高,2例完全正常[11]。
本例患者为中老年男性,亚急性起病,首发症状双侧行走不稳,且症状在几周内进行性加重,伴双眼眼震,但无构音障碍、恶心、眩晕、呕吐等,通过贫血系列检查排除脊髓亚急性联合变性,肌电图明确了糖尿病周围神经病变,头颅MRI排除了颅内原发肿瘤及转移瘤,脑脊液副肿瘤相关抗Hu抗体阳性,结合病史、体检及辅助检查结果,临床诊断为副肿瘤性小脑变性。通过对副肿瘤性小脑变性为首发表现的肺癌患者的临床特征进行分析发现,肺癌相关PNS以神经系统相关表现为主,且神经系统表现早于肺癌诊断时间,对副肿瘤性小脑变性的诊断应提高认识,结合病史及临床表现,对影像资料进行综合分析,选择合适的影像学检查手段提高肿瘤的检出率,及时治疗,以提高患者生存率。该病的治疗包括肿瘤治疗和免疫治疗,虽然患者有时对肿瘤治疗有反应,但免疫疗法很少成功,而且神经系统预后普遍较差[15],也有文献报道免疫抑制治疗目前尚有争议,有报道认为在症状开始之处给予免疫抑制治疗可明显控制病情的发展[16]。可使用免疫球蛋白、血浆置换、激素和免疫调节剂治疗。尽早治疗对于改善神经系统状有一定的帮助。但不同类型的PNS对于这些治疗的反应是不同的。抗Hu阳性的患者对于免疫抑制治疗的反应较差,快速进展且无抗神经抗体的患者经免疫抑制治疗可能会改善[17]。
临床如遇中老年男性、亚急性起病、具有进展较快的小脑症状和体征、无颅内压增高表现、不符合原发神经病病变规律,排除小脑卒中、小脑肿瘤、感染、中毒性小脑病变、应考虑到副肿瘤性小脑变性,需行全身详细的体检及影像学检查,避免原发灶的遗漏。早期诊断副肿瘤性小脑变性对于及时发现和根除宿主体内的肿瘤至关重要,尤其小细胞肺癌、乳腺癌、卵巢癌等。有条件可在血液和脑脊液中检测特定的抗神经元抗体,目前发现许多抗神经元抗体与PCD有关,并且对特定的肿瘤类型的早期诊断提供依据,如抗Hu抗体提示小细胞肺癌,抗Yo抗体提示乳腺、卵巢等肿瘤。研究表明,>10%的抗神经元抗体阳性患者,即使进行全面细致的检查仍可能找不到原发肿瘤,所以需要随访[6,18]。该病总体预后不良,有文献报道,抗Yo抗体阳性PCD患者保留行走能力者仅占21%,患者的中位数生存期为13~22个月,主要死因为神经科或者肿瘤病情加重[19-20]。 尽管如此,仍应积极采取综合治疗手段,控制肿瘤的转移及复发,以提高患者生存质量,延长生存时间,改善生存率。
