铜绿假单胞注射液和顺铂治疗结直肠癌恶性腹腔积液的疗效对比
2019-06-21王光林王飞飞孟泽松王贵英
王光林 王飞飞 孟泽松 王贵英
结直肠癌是消化道常见肿瘤,近年来我国人民饮食结构发生了很大变化,脂肪摄入过多导致结直肠癌的发病率呈增高趋势。我国结直肠癌发病率居世界第三位[1]。结直肠癌治疗方式是以手术为主,放化疗为辅的综合治疗。尽管针对结直肠癌的治疗技术有了很大的进步,但是Ⅳ期结直肠癌患者的生存率并未见明显的提升[2]。尤其是存在恶性腹腔积液的结直肠癌患者。目前,针对这类患者的有效的治疗方式尚不明确。结直肠癌恶性腹腔积液为结直肠癌患者晚期的临床表现,严重影响患者的生活质量及生存期。因此,探索一种有效的治疗结直肠癌恶性腹腔积液的方案,已经成为结直肠癌恶性腹腔积液患者亟待解决的问题。
免疫治疗目前已经成为肿瘤治疗的方法之一。铜绿假单胞菌注射液-甘露糖敏感性血凝菌毛的铜绿假单胞菌-铜绿假单胞注射液(pseudomonas aeruginosa-mannose sensitive hemagglutinin,PAMSHA)为生物免疫制剂,能够通过引起自身免疫反应,达到治疗腹腔积液的目的[3]。目前本品已经在癌恶性胸腔积液,胃癌恶性腹腔积液,卵巢癌恶性腹腔积液等治疗中取得可喜的疗效[4-5],但铜绿假单胞注射液在结直肠癌的恶性腹腔积液中的疗效尚未可知。本实验主要是通过回顾性分析铜绿假单胞注射液和顺铂在结直肠癌恶性腹腔积液的治疗中近期疗效和安全性。
资料与方法
一、一般资料
收集2016年1月至2017年12月期间就诊于河北医科大学第四医院,符合入组标准的结直肠癌恶性腹腔积液的患者49例。其中男性20例,女性29例;年龄25~77岁,17例小于或等于60岁,32例大于60岁。见表1。

表1 铜绿组与顺铂组临床资料对比情况(例)
二、纳入与排除标准
1.纳入标准:(1)结直肠原发癌有明确的病理诊断;(2)初诊时腹部B超证实存在腹腔积液为中-大量腹腔积液,且腹腔积液找到癌细胞,血清白蛋白水平≥35 g/L;(3)有完整的临床及随访资料;(4)血常规及肝肾功能结果正常,无化疗禁忌;(5)自愿加入本次临床实验,并签署相关知情同意书。
2.病例排除标准:(1)一般情况差,不能耐受本次治疗;(2)精神疾患等不能配合本次治疗者;(3)预期生存期<3个月者;(4)排除合并其他原发肿瘤。
三、腹腔积液的诊断和评价
超声是主要的诊断和评价方法。腹腔积液量的评价标准为:少量积液局限于肠间隙或盆腔,前后径2~4 cm;中量积液分布于中、下腹部,前后径5~7 cm;大量积液分布全腹腔脏器周围,最深处前后径 8~10 cm[4]。
四、研究方法
本临床试验为回顾性研究,回顾性分析了2016年1月至2017年12月就诊于本院确诊为结直肠癌伴恶性腹腔积液的患者,所有入组患者均经B超定位后行腹腔穿刺置单腔中心静脉导管,在置管后1~3天内尽可能引流腹腔积液,然后给予常规腹腔内给药。铜绿组:给予铜绿假单胞注射液1 mL×10支+100 mL生理盐水(40~42 ℃)腹腔灌注,第1、3、5天给药,7天1个周期,共2个周期,同期给予mFOLFOX6全身化疗。顺铂组:顺铂50 mg/m2+100 mL生理盐水(40~42 ℃)腹腔给药,第一天给药,7天为一个周期,共2个周期,同期给予mFOLFOX6全身化疗。4周后再次行B超检查,测量腹腔积液最大深度。
五、治疗疗效评价标准
治疗疗效评价标准参照WHO(1981)制定的标准进行疗效判定:(1)完全缓解:腹腔积液完全消失,持续4周以上;(2)部分缓解:腹腔积液较治疗前减少50%以上(以B超检查所见积液最大深径为准),持续4周;(3)疾病稳定:腹腔积液较治疗前较少不足50%或增加不超过25%(以B超检查所见积液最大深径为准);(4)疾病进展:腹腔积液较治疗前增加超过25%以上。本实验治疗有效定义为完全缓解和部分缓解总和,治疗无效定义为疾病稳定和疾病进展的总和。
生活质量(QOL)的评估参考KPS评分的变化。以治疗后KPS增加大于等于10分为生活质量有改善,增加小于10或减少的为生活质量未改善。
记录并统计两组治疗过程中出现的不良反应。
六、统计学分析
使用SPSS 22.0软件对数据进行统计,铜绿组和顺铂组的入组患者的临床基本情况,组间比较采用卡方检验,铜绿组与顺铂组两组疗效及生活质量的对比及治疗过程中不良反应的发生率对比采用卡方检验,以P<0.05为差异有统计学意义。
结 果
一、铜绿组和顺铂组的治疗疗效及生活质量的改善情况
1.治疗疗效:铜绿组19例患者有效,12例患者无效,顺铂组5例患者治疗有效,13例患者无效(χ2=5.118,P=0.024),差异具有统计学意义。结果表明铜绿假单胞注射液能有效控制结直肠癌恶性腹腔积液,有效率显著高于顺铂。见表2。
2.生活质量的改善情况:铜绿组22例患者生活质量发生改善,9例患者生活质量未发生改善。顺铂组7例患者生活质量发生明显改善,11例患者生活质量无明显改善,铜绿组生活改善情况显著高于顺铂组(χ2=6.586,P=0.028),差异具有统计学意义。
二、铜绿组与顺铂组治疗过程中不良反应
在结直肠癌恶性腹腔积液治疗过程中发生的不良反应,铜绿组有12例患者出现发热,顺铂组中2例患者出现发热,铜绿组在治疗过程中出现发热的概率显著高于顺铂组(χ2=4.250,P=0.035),差异具有统计学意义。铜绿组1例患者出现腹痛,顺铂组6例患者出现腹痛,铜绿组发生腹痛的几率显著低于顺铂组(χ2=8.430,P=0.004),差异具有统计学意义。铜绿组无腹腔感染的情况出现,而顺铂组有2例,铜绿组发生腹腔感染的几率与顺铂组差异无统计学意义(χ2=3.591,P=0.058)。铜绿组及顺铂组在治疗过程中均未出现骨髓抑制现象。见表3。
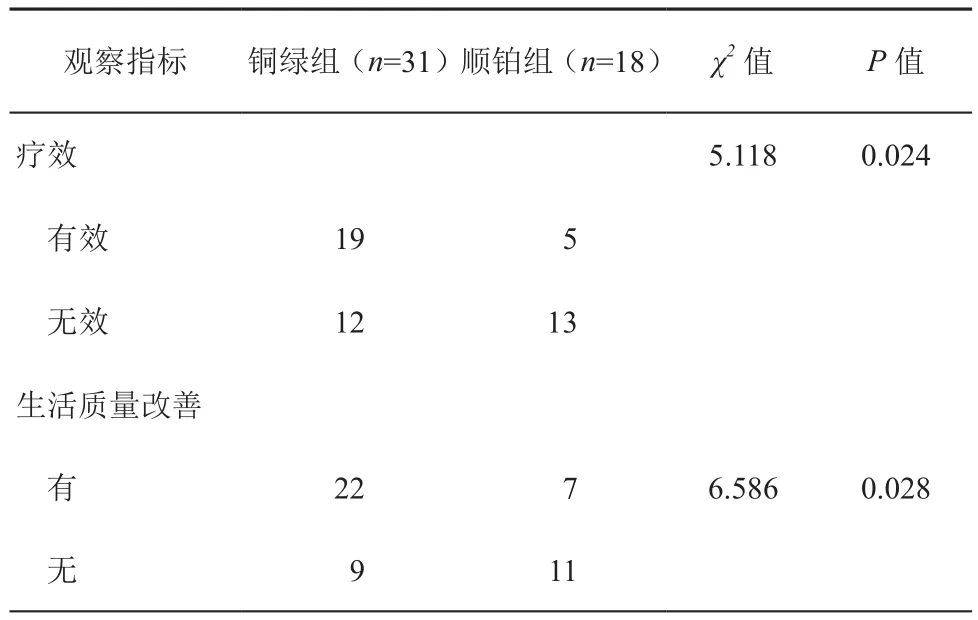
表2 铜绿组与顺铂组疗效与生活质量的改善情况(例)

表3 铜绿组与顺铂组不良反应的情况(例)
讨 论
晚期结直肠癌侵犯腹膜可出现恶性腹腔积液[6],机制大致有如下几点:①肿瘤浸润引起周围炎性反应,导致毛细血管通透性增加,组织液外渗;②癌栓阻塞血管,组织液回流受阻;③肿瘤消耗大量营养,导致机体低蛋白血症,影响组织液回流。恶性腹腔积液患者预后较差,有效控制恶性腹腔积液有利于提高患者生存质量。目前恶性腹腔积液的处理手段主要有:反复抽液[7]、浓缩腹腔积液回输[8]、利尿治疗、抗菌肽[9]、腹腔热灌注[10]等,但疗效不是很理想,给患者心理及生理造成严重影响,患者常因此失去治疗信心,临床处理比较棘手,因此探索能有效治疗结直肠癌恶性腹腔积液的方法,成为治疗结直肠癌恶性腹腔积液亟待解决的问题。
免疫疗法在肿瘤治疗中挥着越来越重要的作用[11-12],成为肿瘤治疗的一个新的选择,而且在恶性腹腔积液的治疗中也表现出明显疗效[13]。铜绿假单胞注射液具有免疫调节功能,广泛应用于抗炎、抗感染甚至抗肿瘤的治疗中[14-15]。研究表明,铜绿假单胞杆菌注射液-铜绿假单胞菌甘露糖敏感血凝素PA-MSHA可通过激活树突状细胞(DCs)、抗原提呈细胞(APCs)和自然杀伤细胞(NKs),刺激细胞增殖和分化,增加抗原呈递功能[16],PA-MSHA通过Toll样受体通路,来激活机体固有免疫,增强机体免疫力[17]。
研究表明,铜绿假单胞注射液已成功应用于多种恶性肿瘤的治疗中,通过固有免疫如Toll样受体通路及其他通路,发挥抗肿瘤的作用。Liu等[18]采用PA-MSHA与人乳腺癌细胞系共培养,其研究结果表明不同浓度的PA-MSHA均可诱导乳腺癌细胞凋亡,影响细胞周期调控机制,使细胞停滞于G0-G1期,促进肿瘤细胞凋亡蛋白:Caspase 3,8,9和Fas蛋白表达。Xu等[19]研究发现,PA-MSHA疫苗可通过IRE1信号通路诱导乳腺癌细胞内质网发生应激反应,导致细胞自噬。通过抑制细胞自噬作用可增强PA-MSHA对乳腺癌细胞株的杀伤作用。在IRE1基因敲除小鼠异种移植动物模型中,PA-MSHA表现出更强的肿瘤抑制作用。表明PA-MSHA联合抑制自噬药物可能是治疗乳腺癌的一种很有前景的治疗策略。研究人员发现,铜绿假单胞菌制剂可通过Nrf2/p62通路抑制对阿霉素耐药的乳腺癌细胞的生长[20]。研究发现PA-MSHA可应用于膀胱癌的治疗[21],PA-MSHA可通过与肿瘤相关的巨噬细胞相互作用,抑制膀胱癌细胞转移,促进癌细胞凋亡。铜绿假单胞注射液有望成为肝细胞性肝癌的治疗新方案[22]。PA-MSHA与肝细胞、肝癌细胞共培养,可通过EGFR/Akt/IκBβ/NF-κB信号通路,下调癌细胞cyclins D1,cyclins E蛋白的表达,使得细胞周期停滞,明显降低癌细胞的活性、侵袭性和远处转移的能力;同时采用铜绿假单胞注射液处理肝细胞肝癌荷瘤小鼠,能够抑制肿瘤组织的上皮间质转化,降低癌细胞的远处转移。Li等[23]研究了PA-MSHA在肺癌和恶性淋巴瘤中的安全性及有效性,共招募88例恶性淋巴瘤患者和89例肺癌患者。实验组均接受化疗+PA-MSHA疫苗,对照组只给予化疗。结果显示,铜绿假单胞注射液在恶性淋巴瘤患者综合免疫的有效率为77.78%,肺癌患者综合免疫的有效率为84.09%。不良反应5例,其中1例给予内科治疗,另1例自动恢复。表明PA-MSHA疫苗作为一种新型的免疫调节剂,可提高肿瘤的治疗效果,且不良反应发生率低。
目前铜绿假单胞注射液已经应用恶性胸腔积液,胃癌恶性腹腔积液,卵巢癌恶性腹腔积液等恶性胸腹腔积液的治疗中,研究表明其能有效的抑制恶性胸腹腔积液的产生,显现出良好的应用前景[24]。但铜绿假单胞注射液在结直肠癌恶性腹腔积液中的安全性及有效性尚未可知。
本临床试验主要是通过对照分析铜绿假单胞注射液和顺铂在结直肠癌恶性腹腔积液的治疗中近期疗效和安全性。本研究结果显示,铜绿假单胞注射液能有效控制结直肠癌恶性腹腔积液,31例采用铜绿假单胞菌注射液治疗的患者中,19例患者的腹腔积液症状得到明显改善,有效率达61.29%,显著高于顺铂组(P=0.024);铜绿组患者生活质量得到明显改善,31例采用铜绿假单胞菌注射液治疗的患者中,22例患者的生活质量得到明显改善,显著高于顺铂组(P=0.028)。在治疗过程中出现的不良反应,如发热、腹痛及腹腔感染,都在可控范围,无因不良反应而致死病例和中途放弃治疗的病例。铜绿组因其调节机体免疫功能的特性,常在治疗过程中出现发热症状,31例患者中有12例患者(38.7%)出现发热症状,显著高于顺铂组(11.11%;P=0.039)。但发热症状均在可控范围,给予物理降温、非甾体类药物后,体温均可恢复正常,无恶性高热病例。铜绿假单胞注射液属于生物制剂,在激发机体免疫的过程中,机体通过升高体温,提高机体免疫力,从而发挥治疗作用,因此铜绿组的患者通常出现发热症状。腹痛和腹腔感染的发生率在治疗过程中发生率低,且无恶性不良事件发生。铜绿组腹痛发生率仅为3.2%,顺铂组为33.33%,铜绿组未出现腹腔感染和骨髓抑制的病例。验证了铜绿假单胞杆菌注射液在治疗结直肠癌恶性腹腔积液过程中的安全性。
本研究结果显示,铜绿假单胞菌注射液对于结直肠癌恶性腹腔积液患者近期疗效确切,能明显改善患者近期生活质量,且不良反应都在可控范围,在疗效方面优于顺铂。研究表明,铜绿假单胞注射液是治疗结直肠癌合并恶性腹腔积液安全、有效的治疗手段。铜绿假单胞菌制剂联合同期mFOLFOX6方案化疗有望成为结直肠癌恶性腹腔积液治疗的新手段,为恶性腹腔积液的全身治疗提供了新的思路。由于本试验纳入的病例数量有限,需大规模临床试验研究进一步验证铜绿假单胞菌在结直肠癌恶性腹腔积液中的疗效。
