光合作用中光反应的机制和由来(2)
2019-06-15朱钦士美国南加州大学医学院
朱钦士 (美国南加州大学医学院)
2 醌分子在能量转化和能量储存上的核心作用
原核生物并不直接催化氢气与硝酸盐反应,因为这种直接反应只能以热的形式释放能量,生物无法加以利用。 要利用该氧化还原反应释放的能量,原核生物采取的办法是,先用氢酶(hydrogenase)将氢气(H2)中的氢原子转移到一种叫做“醌”(quinone)的分子上,使其变为“氢醌”,再通过硝酸盐还原酶(nitrate reductase)将氢醌分子上的氢原子转移给硝酸盐分子,将硝酸盐(NO3-)变为亚硝酸盐(NO2-),同时生成水。 硝酸盐失去了1个氧原子,因此是被部分“还原”了。
之所以该反应要经过醌分子, 是因为醌分子有一种能力,可利用氧化还原反应释放的能量,将氢离子(H+)从细胞膜的一侧转移至另一侧,使氢离子在膜一侧的浓度极大超过另一侧。 氢离子在膜两侧浓度不一样的状况称为“跨膜氢离子梯度”。它就像水库大坝两侧的水位不一样高, 是储存能量的一种方式。水库里面的高水位具有势能,在通过大坝时势能被释放, 驱动水轮机进而带动发电机发电。同样,氢离子从浓度高的一侧通过膜流至另一侧时, 也会带着位于膜上的ATP 合成酶转动,转动的力量可使酶的形状改变,将ADP(二磷酸腺苷)和磷酸分子“捏合”到一起,形成ATP 分子。 ATP(adenosine triphosphate,即三磷酸腺苷)是腺苷分子上再连上3 个磷酸根而成。 由于磷酸根是带负电的,彼此排斥,将3 个磷酸根强行“捏”在一起,就像是将弹簧压缩,一旦有机会(即释放出磷酸根时)就会释放能量。 因此ATP 是细胞中的“高能分子”,能为细胞中各种需要能量的生命过程提供能量。 原核生物利用氧化还原反应释放能量的方式, 就是先将这些能量以跨膜氢离子梯度的形式储存起来, 再将跨膜氢离子梯度储存的能量转化为ATP 分子中的能量。
醌分子是如何将氧化还原反应释放的能量转化为跨膜氢离子梯度的? 这与醌分子的化学结构和性质有关。醌分子的化学结构较为简单,即一个能进行氧化还原反应的“头部”连上一条长“尾巴”(图1)。这条“尾巴”只含有碳原子和氢原子,是高度亲脂的,它使醌分子能“溶解”在细胞膜的油性内层中并在膜内“游动”,使其“头部”可接近细胞膜的任何一侧。
醌分子的“头部”是一个环状结构(化学名称叫“苯环”),上面连有2 个“羟基”(-OH,“羟”是化学家造的字,就是“氢加氧”组成的基团的意思)而成。 这2 个羟基可以各失去1 个氢原子,变成2个“羰基”(C=O,“羰”也是化学家造的字,读音“汤”,意思是“碳加氧”形成的基团,这里的C 表示环上的碳原子)。 羰基得到氢原子, 又可以变回羟基, 因此醌分子可反复得到和失去2 个氢原子,可作为氢原子的“转运站”。醌分子中的氧原子以羰基形式存在时,是失去氢原子的,处于被“氧化”的状态,叫做醌(quinone,简称为Q);醌分子中的氧原子以羟基的形式存在时,是得到氢原子的,处于被“还原”的状态,叫做氢醌(quinol,简称QH2)。
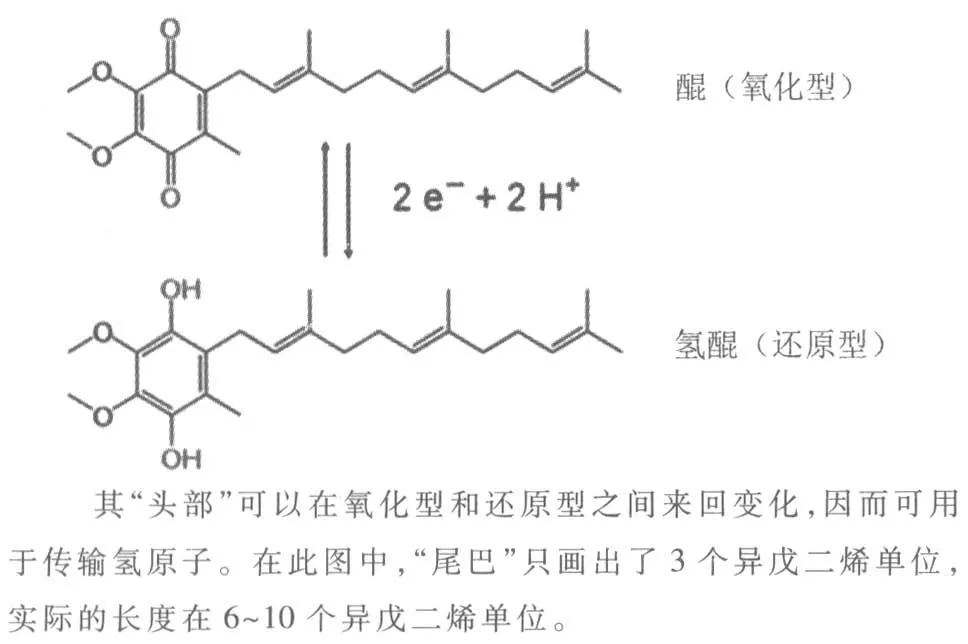
图1 醌分子的结构
要建立跨膜氢离子梯度, 首先需要一种氢离子无法直接通过的膜,就像水库的坝。这应该不是问题,因为最初的生命就是以细胞的形式出现的,细胞膜将细胞的内容物与环境分开, 以免组成生命的化学系统被水稀释。 细胞膜是磷脂组成的双层膜,中间有约2.5 nm 厚的“油”层,主要由磷脂分子上脂肪酸的碳氢链“尾巴”组成。 这个油质层对于各种带电的离子,包括氢离子、钠离子、氯离子,都是不通透的。这些离子要通过细胞膜必须通过膜上由蛋白质组成的通道, 而通道的开关是受控制的,就像水坝的出水口是可以关闭的,所以细胞膜就可以起到“水坝”的作用。 有了不透氢离子的细胞膜,再有了“溶解”在膜中且能进行氧化还原反应的醌分子,转化能量即可进行。
如果氢醌分子是将其上的氢原子以原子的形式直接转移给硝酸盐, 则跨膜氢离子梯度无法建立。 但巧妙的是,氢醌被氧化时,其上面的氢原子是分为电子和氢离子这2 个部分而“分开走”的。硝酸盐还原酶先脱去醌分子中氢原子上的电子,将电子传递给硝酸盐, 失去电子的氢原子以氢离子的形式被释放至溶液中。 得到电子的硝酸盐再从溶液中得到与电子数相同的氢离子, 让电子变回氢原子,与硝酸盐中的1 个氧原子结合成为水,硝酸盐变为亚硝酸盐, 总的结果就好像是氢原子被直接转移一样。 但实际上,原核生物就“钻”了电子和氢离子分开走这个“空子”,将氢离子的释放和结合安排在膜的两侧, 就可实现能量转化和氢离子的跨膜转移(图2 右)。
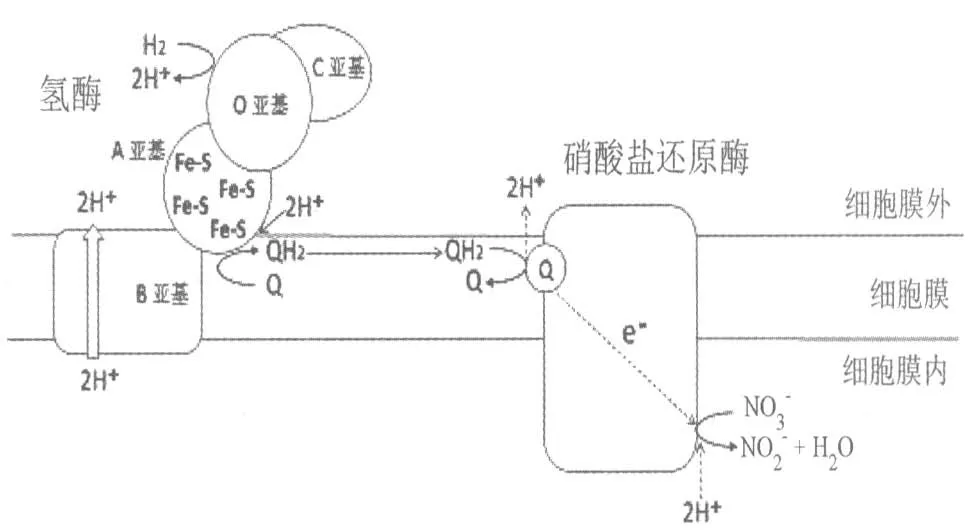
图2 氢气被硝酸盐氧化时释放的能量被用于建立跨膜氢离子梯度
氢醌在被硝酸盐氧化时, 硝酸盐还原酶上氧化氢醌的地方接近细胞膜的外表面, 因而氢离子也被释放至细胞膜外。 细胞膜外本来就有高浓度的氢离子,由于氢离子是带正电的,细胞膜外的溶液也因此带有正电, 所以在细胞膜外侧释放带正电的氢离子在能量上是不利的, 因为带正电的氢离子会被细胞膜外的正电所排斥。 但是电子从氢醌进入硝酸盐还原酶上的氧化还原中心, 能量是降低的。 这个释放的能量就可“拉动”氢醌在细胞膜的外侧释放氢离子,这就是能量转化的过程。
硝酸盐分子从硝酸盐还原酶得到电子后,还需要同样数量的氢离子才能将电子变回氢原子。由于该反应是在酶伸到细胞质内进行的, 氢离子也是从细胞质内取得。 该反应在能量上也是不利的, 因为要从带负电的环境中再拿走带正电的氢离子。 但硝酸盐被还原时释放的能量也足以驱动该反应。这样,氢醌被氧化时在细胞膜外释放2 个氢离子, 硝酸盐被还原时在细胞膜内拿走2 个氢离子, 总的效果就相当于2 个氢离子被转移到细胞膜外, 氢醌被氧化时释放的能量就以跨膜氢离子梯度的形式被储存。
利用醌分子的氧化还原反应中电子和氢离子分开走的特点,建立跨膜氢离子梯度,实现氧化还原反应释放的能量的转化和储存, 为细胞的生理活动所用,这是原核生物的伟大发明。自从几十亿年前由原核生物发明以来,所有生物,包括人类,都仍然在使用这种方法建立跨膜氢离子梯度以储存能量。 由于原核生物中的细菌(Bacteria)和古菌(Archaea)都含有醌,也都使用这种方式建立跨膜氢离子梯度, 醌分子的合成及在能量转化和储存中的使用, 一定出现在原核生物分化为细菌和古菌之前,也就是在原核生物的共同祖先中,那就是最早的细胞生命。
也许在醌分子出现之前, 原核生物就开始将跨膜氢离子梯度作为能量的一种来源。 一种生命起源的学说就认为, 最初的生命是在海底热泉处产生的。 热泉喷出的带碱性的水和带酸性的海水之间如果有膜状结构相隔, 就会形成跨膜氢离子梯度,可以为最初的生命所利用。一旦这种储存能量的方式被建立,就一直为细胞所使用,而醌分子的出现使得细胞能主动将氧化还原反应释放的能量以跨膜氢离子梯度的形式储存起来。
正是由于醌分子有转化能量的能力, 所以氧化还原反应中的电子传递链都是以醌分子为核心枢纽的: 醌分子从各种能提供氢原子的分子收集氢原子,变为氢醌,氢醌再将氢原子“分配”给各种氧化物。从各种分子中脱下氢原子,并将氢原子交给醌分子的酶称为“脱氢酶”(dehydrogenase);氧化氢醌,将氢原子交给氧化物的酶就称为“氧化酶”(oxidase,如果最终氢原子受体是氧,例如氢醌氧化酶),或者某分子的“还原酶”(reductase,如果最终氢原子受体不是氧,例如硝酸盐还原酶)。 原核生物要适应环境,往往利用多种还原物,也利用多种氧化物,以增加自己生存的机会。例如大肠杆菌(Escherichia coli)的电子传递链就使用了15 种脱氢酶、10 种氧化酶或还原酶。 人也有类似的电子传递链,也以醌分子为电子传递链的核心枢纽。
不仅如此, 醌分子在能量转化和储存中的巧妙机制还被光合作用所利用, 成为光合作用中转化太阳光能量的关键机制(见下文)。 因此,醌分子在转化和利用氧化还原反应释放能量的过程中,以及转化储存太阳光能量的过程中,都起到关键作用,是所有细胞生物,包括细菌、古菌、真菌、动物和植物都使用的重要分子。市面上卖的“辅酶Q”或者“Q10”,其实就是醌分子,使人们可通过口服的方式补充细胞中的醌分子。相反,降低血液中胆固醇水平的“他汀”(statin)类的药物,在抑制胆固醇合成的同时也抑制醌分子的合成, 使细胞中能量转化的过程受到影响,降低肌肉的功能,甚至造成肌肉疼痛,要靠服用Q10缓解。
醌分子在能量转化和储存上的作用也有局限性,即氢离子的释放和接收必须在膜的两侧。如果释放和接收氢离子的过程发生在膜的同一侧,这种机制就不起作用(见图2 左)。 例如氢酶将氢分子中的氢原子转移到醌分子上时, 氢原子也是分为电子和氢离子分别走的。氢酶从氢气分子(外来分子)获得电子的位置在细胞膜外,因此氢离子也被释放在细胞膜外。 虽然看上去会增加细胞膜外侧氢离子的浓度, 但由于醌分子从氢酶得到电子的地方靠近细胞膜的外侧, 得到电子的醌分子也从细胞膜外的溶液中获得氢离子变为氢醌, 所以开始时释放到细胞膜外的氢离子后来又被用掉了,没有净的氢离子跨膜运输。这是一种能量上的浪费, 因为氢原子的氧化还原电位是-0.42 V,而醌的氧化还原电位在0V 左右, 氢分子上的氢原子转移到醌分子上也是要释放能量的, 但是在这里不能加以利用。 许多脱氢酶由于氧化还原性分子的位置在细胞膜外, 还原醌分子的位置也靠近细胞膜的外侧,所以也有同样的问题。 为此,原核生物还发展出了另一种转化和储存这些能量的方法,即利用电子传递所引起的蛋白质形状的变化,直接将氢离子从膜的一侧“泵”到另一侧,即用电子流动驱动氢离子。
3 用电子流动引起的蛋白形状变化“泵”氢离子
用电子传递过程中蛋白分子形状的变化,将氢离子从细胞膜的内侧“泵”到外侧,是原核生物的另一大发明。 例如大肠杆菌就有一种氢酶叫Hyd-2,它含有4 个蛋白亚基,其中O 亚基和C 亚基彼此结合位于膜外,与氢分子反应。A 亚基连接OC 和位于膜内的B 亚基(图2 左)。A 亚基含有4个转移电子的铁硫中心, 负责将电子传递到醌分子上,而B 亚基不含有任何电子转移中心。 实验表明,位于膜内且不含电子转移中心的B 亚基具有“泵”氢离子的功能。 电子通过A 亚基时引起的蛋白形状变化带动B 亚基的形状变化,该形状变化改变了蛋白质分子中不同氨基酸侧链结合氢离子的强度, 使得B 亚基可将氢离子从膜的一侧“泵”到另一侧。 许多(不是所有)脱氢酶都有此功能, 使各种还原性分子在还原醌分子时释放的能量也能被生物所利用。
同样, 氢醌被外来氧气氧化时放出的能量很多,也需要将其尽量储存。 氧的氧化还原电位为+0.82 V, 比硝酸盐的+0.42 V 高近一倍, 用同样的醌机制转移氢离子,会造成很大的能量浪费。为避免这种浪费, 生物将氢醌氧化的过程分为两大步,由膜上的2 个蛋白复合物分别催化。第1 步,用“细胞色素bc1复合物”(cytochrome bc1complex)氧化氢醌,将电子传递给“细胞色素c”。 这一步能量转化的机制仍然是氢醌氧化时转移氢离子。 第2步,用细胞色素c 还原氧分子,能量转化过程就不是通过醌分子(这里也没有醌分子的参与),而是通过蛋白复合物形状的变化“泵”氢离子。 催化该反应的蛋白复合物称为“细胞色素c 氧化酶”(cytochrome c oxidase)。 这样, 氢醌被外来氧气氧化时所释放的能量,由2 个蛋白复合物分段转化,用不同的机制建立跨膜氢离子梯度, 效率比单一的酶提高很多。
更重要的是,细胞色素bc1复合物,还与醌分子一起,成为光合作用电子传递链中的重要组成部分。但至此,只介绍了醌分子的构造和作用,还没有介绍还原和氧化醌的蛋白质分子的结构,在光合作用中,光驱动电子还原醌分子的蛋白质也有类似的结构。 为了更好地了解光合作用的分子机制,有必要先介绍传递电子的蛋白复合物的结构。
(待续)
