青白通痹方药半仿生提取工艺条件优选研究*
2019-06-14王卫锋张小丽张军茹任得志
李 凡,王卫锋,张小丽,张军茹 ,任得志 ,李 芳△
1.陕西省中医药研究院(西安 710003);2.陕西省中医医院(西安 710003)
青白通痹方由青风藤、白芍和炙甘草组成,为陕西省中医医院米烈汉名老中医和学科带头人胡筱娟主任医师的临床经验方,具有消肿通痹止痛,舒筋活络之功效。临床上主治风湿、类风湿、痛风、骨关节病等所致的关节肿胀、僵硬、疼痛、屈伸不利。目前该方已被开发成院内制剂,效果显著。为了进一步发挥青白通痹方的临床功效,对其进行深入研究,我们拟采用半仿生提取(Semi-bionic extraction,SBE)、半仿生-生物酶法提取(Semi-bionic-enzyme extractio,SBEE)、醇提取(Alcohol extraction,AE)三种提取法对其药效物质进行提取研究,并与原水提取工艺进行对比实验,从而确定青白通痹方药效物质的最佳提取工艺及参数。半仿生提取法通过模拟药物在胃肠道中的作用过程,充分发挥混合物成分的综合作用特点,并且有利于以单体成分来控制提取物质量,同时也符合药物在体内代谢、发挥药效的过程。尤其是对于作用物质基础不明确而又疗效确切的药物,半仿生提取法更能确切反应药物真正的药效物质基础。本文参考相关文献[1-7],对青白通痹方药用SBE的工艺条件进行优选,为进一步的研究奠定基础。
材料与方法
1 材 料
1.1 仪器:Waters Acquity H-CLASS型超高效液相色谱仪(UPLC)(EmpowerTM3色谱工作站、PDA检测器);ACQUITY UPLC BEH C18色谱柱(2.1 mm×50 mm,1.7μm);电子分析天平(型号:BT25S,d=0.01 mg;BS210S,d=0.1 mg,北京赛多利斯天平有限公司)、DELIS超声波清洗机(深圳市洁盟清洗设备有限公司)、四孔水浴锅(北京科伟永兴仪器有限公司)、WS70-1型红外快速干燥箱(上海市吴淞五金厂制造)、101型电热鼓风干燥箱(北京市永光明医疗仪器厂)、HCTP11B10托盘药物天平(北京市宣武区天平厂)。SartoriusPB-10型精密pH计(赛多利斯科学仪器北京有限公司)、TGL18型台式高速冷冻离心机(长沙英泰仪器有限公司)、U-2910 型紫外可见分光光度计(HITACHI)、血清超滤器(上海德宏生物医学科技发展有限公司)。
1.2 试药:青风藤为防己科植物和毛青藤 Sinomenium acutum(Thunb.)Rehd.et Wils.var.cinereum Rehd.et Wils .的干燥藤茎;白芍为毛莨科植物芍药Paeonia lactiflora PalL.的干燥根;炙甘草为豆科植物甘草Glycyrrhiza uralensis Fisch.的根及根茎的炮制加工品,以上药材经陕西省中医药研究院王卫锋主任药师鉴定后应用于本实验。青藤碱对照品(批号:110774-200507),芍药苷对照品(批号:110736-201539),甘草次酸对照品(批号:110723-201514),以上对照品均购自中国药品生物制品检定院。液相用甲醇、乙腈试剂均为HPLC级(瑞典欧普森);其它试剂均为AR级(天津市富宇精细化工有限公司)。
2 研究方法
2.1 实验设计 本次实验是在饮片规格、煎煮温度、用水量、滤过、浓缩等基本提取条件相同的情况下进行,对第一煎水pH(A)、第二煎水pH(B)、第三煎水pH(C)和煎煮时间h(D)4个主要因素各3个水平进行考察,因素及水平见表1。按表2 L9(34)表安排实验。

表1 因素与水平

表2 L9(34)实验设计表
注:D因素括号内数字依次为第1,2,3次的提取时间。
2.2 样品溶液的制备 将清风藤、白芍和炙甘草分别粉碎,过筛(10~20目之间),按处方比例称取三者粗粉80 g并混合均匀,按表2中所列的实验参数,常压下加热回流提取3次(第1次加水量为10倍、第2次加水量8倍、第3次加水量8倍),用4层纱布加100目药筛过滤实验的提取液,合并3次提取的滤液,分别定容至2000 ml,即得青白痛痹方药半仿生提取的正交实验样品液。
2.3 供试溶液的制备
2.3.1 供试液A的制备:分别精密吸取2.2项下青白痛痹方药半仿生提取的正交实验样品液各100 ml,离心(3500 r/min,20 min),取上清液各10 ml,加甲醇定容至25 ml,用0.22 μm微孔滤膜滤过,即得供试液A1-9,用于测定青藤碱和芍药苷的含量。
2.3.2 供试液B的制备:分别精密吸取2.2项下青白痛痹方药半仿生提取的正交实验样品溶液各100 ml,参考文献甘草次酸供试液制备方法[8],最后用甲醇转移至10 ml量瓶中并定容,再用0.22 μm的微孔滤膜滤过,得到的溶液为正交实验供试液B1-9。用于测定甘草次酸的含量。
2.3.3 供试液C的制备:精密吸取2.2项下青白痛痹方药半仿生提取的正交实验样品溶液各15 ml,蒸至近干,加入硅藻土1 g拌匀,烘干,研匀后转移至锥形瓶中,加甲醇25 ml,称重,超声提取(250W,40K Hz) 30 min,放冷,补足减失的重量,滤除硅藻土,即得供试液C1-9。用于测定总生物碱含量。
2.3.4 供试液D的制备:取2.2项下青白痛痹方药半仿生提取的正交实验样品溶液各500 ml,离心,先经过0.45 μm微孔滤膜过滤,再经由中空纤维膜(截留量为1000Da)滤过,过滤至500 ml容量瓶并用蒸馏水定容至刻度,得到供试液D1-9。用于测定分子量≤1000Da的提取物。
2.4 青藤碱的含量测定[9-11]
2.4.1 色谱条件 色谱柱:ACQUITY C18色谱柱(2.1 mm×50 mm,1.7μm);流动相:乙腈-0.1%磷酸(10:90);检测波长:262 nm;柱温室温;流速:0.3 ml/min;进样量4.0μl。
2.4.2 对照品溶液的制备:取青藤碱对照品,精密称定(5.21 mg),置10 ml容量瓶中,用70%的乙醇溶解并稀释至刻度,摇匀,即得青藤碱对照品溶液(0.521 mg/ml),置于4℃冰箱中保存。
2.4.3 青藤碱线性关系考察:取2.4.2项下青藤碱对照品溶液 (0.521 mg/ml),分别自动进样0.4 μl、0.8 μl、1.0 μl、2.0 μl、4.0 μl及8.0 μl,测定色谱峰面积。以青藤碱对照品溶液的进样量为横坐标,以色谱峰面积为纵坐标,即得到标准曲线。其回归方程为:Y=1719463.26x-52291.966,R=0.9999。结果表明,在进样量为0.2084~4.1680 μg范围内,青藤碱线性关系良好。
2.4.4 精密度试验:取2.4.2项下青藤碱对照品溶液 (0.521 mg/ml),色谱条件同2.4.1项下,分别连续进样6次,记录色谱峰面积及计算RSD。结果表明,仪器精密度良好(RSD=0.99%)。
2.4.5 稳定性试验:精密吸取2.3.1项下的供试品溶液A1,按2.4.1项下色谱条件分别于0、2、4、6、8、10 h重复进样6次,青藤碱色谱峰面积的RSD=1.05%,表明供试品溶液在10 h内稳定性良好。
2.4.6 重复性试验:按2.3.1项下方法平行制备正交1号样品的供试液,共6份,按2.4.1项下色谱条件进样,记录色谱峰面积及计算RSD。结果表明,青藤碱平均含量=9.33 mg/g,RSD=0.99%,表明重复性良好。
2.4.7 加样回收试验:精密吸2.3.1项下正交1号样品上清液5 ml(含青藤碱9.33 mg/g)6份,分别加入青藤碱对照品溶液 (0.8360 mg/ml)2.2 ml、2.2 ml、2.2 ml、2.2 ml、2.2 ml、2.2 ml,按照2.3.1项下的方法制备供试品液,按照2.4.1项下的条件进行含量测定,计算加样回收率。青藤碱平均加样回收率为97.89%,RSD=1.52%。
2.4.8 青藤碱的含量测定:取2.3.1项下供试品溶液A1-9,进行进样分析,色谱条件同2.4.1项下,测定供试品溶液中青藤碱的含量,结果见表3。
2.5 芍药苷的含量测定[12-14]
2.5.1 色谱条件:色谱柱:ACQUITY C18色谱柱(2.1 mm×50 mm,1.7μm);流动相:乙腈-0.1%磷酸(12:88);检测波长:230 nm;柱温为室温;流速:0.3 ml/min;进样量2.0μl。
2.5.2 对照品溶液的制备:取芍药苷对照品,精密称取1.55 mg,加甲醇溶解于25 ml量瓶中,并稀释至刻度,摇匀,即得浓度为0.062 mg/ml芍药苷对照品溶液。
2.5.3 芍药苷线性关系考察:按2.5.1项的色谱条件,取2.5.2项下浓度为0.062 mg/ml的芍药苷对照品溶液分别进样0.5 μl、1.0 μl、2.0 μl、4.0 μl、6.0 μl、8.0 μl。以芍药苷的进样量为横坐标,以色谱峰面积为纵坐标,绘制标准曲线。芍药苷的回归方程为:Y=3343254.57x+7878.94,R=1.0。结果表明,芍药苷在0.0310~0.4960μg范围内线性关系良好。
2.5.4 精密度试验:取2.5.2项下浓度为0.062 mg/ml的芍药苷对照品溶液,按2.5.1项下色谱条件连续进样6次,记录色谱峰面积及计算RSD。结果表明,RSD=0.89%,表明所用实验仪器精密度良好。
2.5.5 稳定性试验:精密吸取2.3.1项下供试品溶液A1,按2.5.1项下色谱条件分别于0、2、4、6、8、10 h进样,记录色谱峰面积及计算RSD。结果表明,RSD=1.48%,供试品溶液在10 h内稳定性良好。
2.5.6 重复性试验:按2.3.1项下供试液A的制备方法制备正交1号样品的供试液,平行6份,按2.5.1项下色谱条件,记录色谱峰面积及计算RSD。结果表明,芍药苷平均含量=7.25 mg/g,RSD=1.03%,表明重复性良好。
2.5.7 加样回收试验:精密吸取已知含量(含芍药苷7.25 mg/g)的正交1号样品上清液5 ml,共6份,分别加入浓度为1.4520 mg/ml的芍药对照品溶液1 ml、1 ml、1 ml、1 ml、1 ml、1 ml,按2.3.1项下方法制备供试液,按2.5.1项下液相色谱条件依法测定含量并计算加样回收率。芍药苷平均加样回收率为97.35%,RSD=1.06%。
2.5.8 芍药苷的含量测定:取2.3.1项下供试品溶液A1-9,按2.5.1项色谱条件进样分析,测定并计算芍药苷的含量,见表3。
2.6 甘草次酸的含量测定
2.6.1 色谱条件 色谱柱:ACQUITY C18色谱柱(2.1 mm×50 mm,1.7μm);流动相:乙腈-0.05%磷酸(80:20);检测波长:250 nm;柱温设为室温;流速:0.3 ml/min;进样量2.0μl。
2.6.2 对照品溶液的制备:取甘草次酸对照品,精密称取10.28 mg,加甲醇使溶解于50 ml量瓶中,并稀释至刻度,摇匀,即得浓度为0.2056 mg/ml的甘草次酸对照品溶液,置于4℃冰箱中保存。
2.6.3 甘草次酸线性关系考察:在2.6.1项的色谱条件下,取2.6.2项下浓度为0.2056 mg/ml的甘草酸对照品溶液,分别进样0.4 μl、0.8 μl、1.0 μl、2.0 μl、4.0 μl、8.0 μl,测定色谱峰面积。以甘草次酸的进样量为横坐标,以峰面积为纵坐标,绘制标准曲线。甘草次酸回归方程为:Y=7332322.3x-108956.6,R=0.9999。结果表明,甘草次酸在0.0822~1.6448μg范围内线性关系良好。
2.6.4 精密度试验:取2.6.2项下浓度为0.2056 mg/ml的甘草次酸对照品溶液,连续进样6次,色谱条件同2.6.1项下。记录色谱峰面积及计算RSD。结果表明,RSD=0.83%,仪器精密度良好。
2.6.5 稳定性试验:精密吸取2.3.2项下甘草次酸供试品溶液B1,按2.6.1项下色谱条件分别于0、2、4、6、8、10 h进样,记录色谱峰面积及计算RSD。结果表明,RSD=1.40%,表明用于甘草次酸含量测定的供试品溶液在10 h内稳定性良好。
2.6.6 重复性试验:按2.3.2项下甘草次酸供试液的制备方法,制备正交1号样品供试液,平行6份,进样并记录色谱峰面积及计算RSD,色谱条件同2.6.1项下,结果表明,甘草次酸平均含量=0.7047 mg/g,RSD=1.18%,表明重复性良好。
2.6.7 加样回收试验:精密吸2.2项下正交1号样品液50 ml(含甘草次酸0.7047 mg/g)6份,分别加入甘草次酸对照品溶液 (1.4220 mg/ml)1 ml、1 ml、1 ml、1 ml、1 ml、1 ml,按2.3.2项下方法制备供试液,按2.6.1项下液相色谱条件依法测定含量并计算加样回收率。结果为甘草次酸平均加样回收率96.17%,RSD=1.45%。
2.6.8 甘草次酸的含量测定:取2.3.2项下供试品溶液B1-9,在2.4.1项色谱条件下进样分析,测定甘草次酸的含量,结果见表3。
2.7 分子量≤1000Da提取物的测定 取2.3.4项下供试液D1-9各100 ml,置蒸发皿中,水浴蒸至近干,于烘箱中105℃烘至恒重,计算分子量≤1000Da提取物的得率。结果见表3。
2.8 总生物碱的含量测定
2.8.1 青藤碱对照品溶液的制备:精密称取青藤碱对照品5.25 mg,置10 ml量瓶中,加PH7.0的缓冲溶液溶解稀释至刻度,摇匀,得青藤碱对照液 (0.5250 mg/ml)。
2.8.2 标准曲线的绘制:精密量取青藤碱对照品溶液0.4、0.6、0.8、1.0、1.2、1.5 ml,分别置干燥具塞试管中,加PH7.0的缓冲液稀释至2.0 ml。加入0.007%溴麝香草酚蓝8.0 ml,摇匀,加入三氯甲烷10.0 ml,振摇,静置2 min至分层。分取三氯甲烷层,用干燥滤纸滤过,相应试剂为空白,在413 nm波长处测定,以浓度为横坐标,吸光度为纵坐标,回归方程:Y=0.083X+0.1577,r=0.9991,线性范围为:2.10~7.875 μg/ml。
2.8.3 总生物碱的含量测定:精密量取2.3.3项下供试液C1-9各0.5 ml,按2.8.2 标准曲线的绘制项下方法,测定吸光度,计算总生物碱的量,结果见表3。
2.9 干浸膏量的测定 量取2.2项下样品液各50 ml,置蒸发皿中,水浴蒸至近干,置于105℃烘干至恒重,称量并计算干浸膏量。见表3。
2.10 多指标综合评判优选SBE法工艺条件 青白痛痹方药的半仿生提取工艺条件优选的评价指标选取青藤碱、芍药苷、甘草次酸、分子量≤1000Da提取物、总生物碱和干浸膏量。这6个指标的原始数据参考文献[15]进行标准化处理,并根据6个指标在工艺优选方法中的主次地位,给予加权后求和确定综合评价指标Y值。本次实验的Y=(芍药苷+青藤碱+甘草次酸)/3×7+(总生物碱+干浸膏+分子量≤1000Da提取物)/3×3,结果见表3。

表3 各指标成分含量及标准化处理结果
注:表中各成分量单位中的“g”是已经折算到方中中药的质量;括号内的数值已经经过了标准化处理
根据上述实验中收集到的实验数据,进行正交实验分析。从表4的试验结果直观分析来看,实验设计中的影响因素主次为D>A>C>B。进一步对收据到的数据进行方差分析,由表5的方差分析结果来看,影响因素A、C、D均有统计学的差异,根据上述情况来确定提取工艺条件为A1B2C3D3。即青白痛痹方药用SBE法提取的工艺条件为:3煎用水的pH依次为2.0、7.0、9.0;本试验对药物的提取时间依次为2.0 h、1.5 h、1.5 h。
2.11 工艺验证实验:严格按照实验操作方法取中药饮片粗粉,并按照上述处方比例对药物进行称取,称量80 g,平行3份,依照优选出的工艺条件进行提取并制备出样品溶液以及对各评价指标进行测定,平行3份。从实验得到的数据结果来看,工艺验证实验提取液的综合评价值是接近于其预测值的,具体的数据情况见表6。
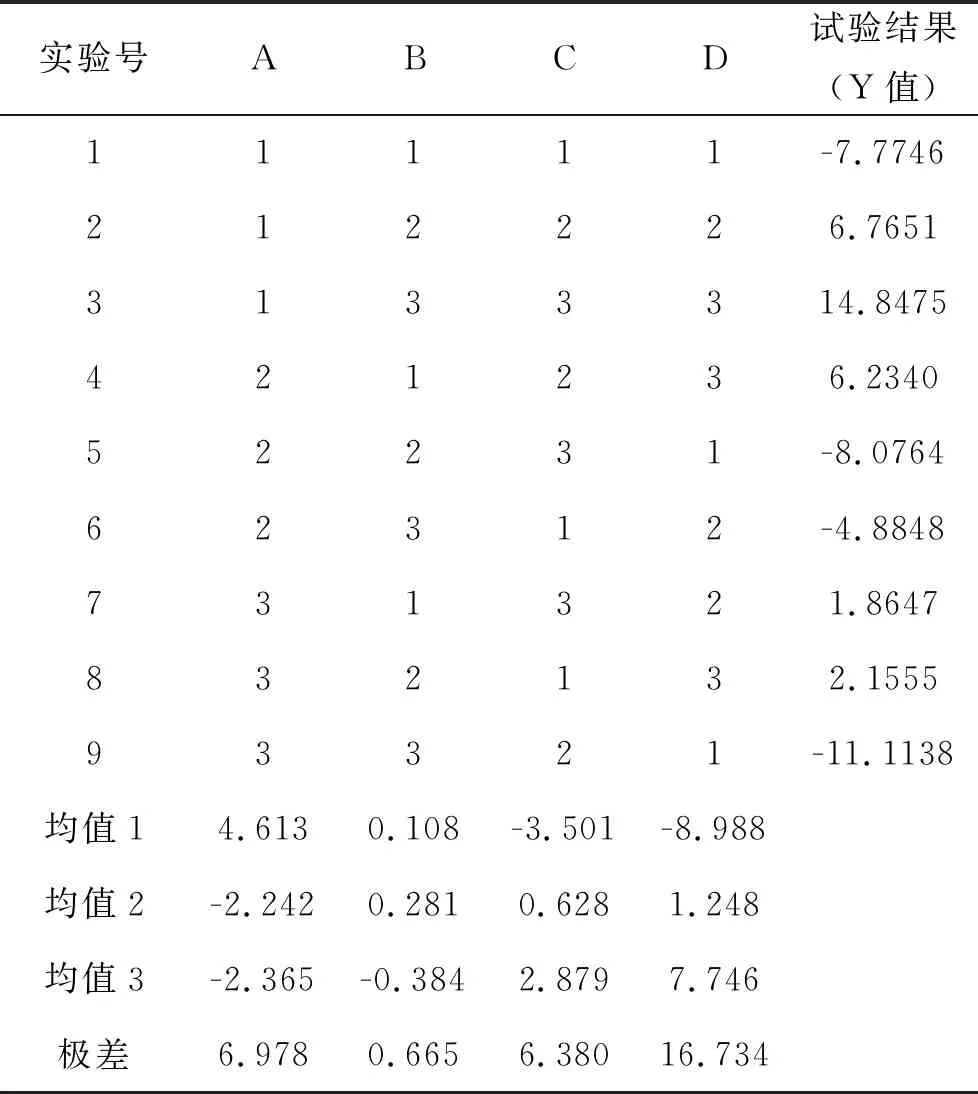
表4 正交实验结果

表5 方差分析
讨 论
青白痛痹方临床上主治风湿、类风湿、痛风、骨关节病等所致的关节肿胀、僵硬、疼痛、屈伸不利。青风藤中青藤碱具有抗炎、镇痛、免疫抑制的药理活性;白芍中含有的活性成分芍药苷,具有抗自由基损伤,抑制细胞内钙超载和抗神经毒性等活性,体内实验证明其有降低血液黏度、抗血小板聚集、扩张血管、改善微循环、抗氧化等多种生物学效应;甘草中甘草次酸具有抗炎及增强免疫、抗氧化、抑菌、肾上腺皮质激素样作用等药理作用,这些与该方的功能与主治相一致,故选择这三个单体成分为提取工艺的评价指标。
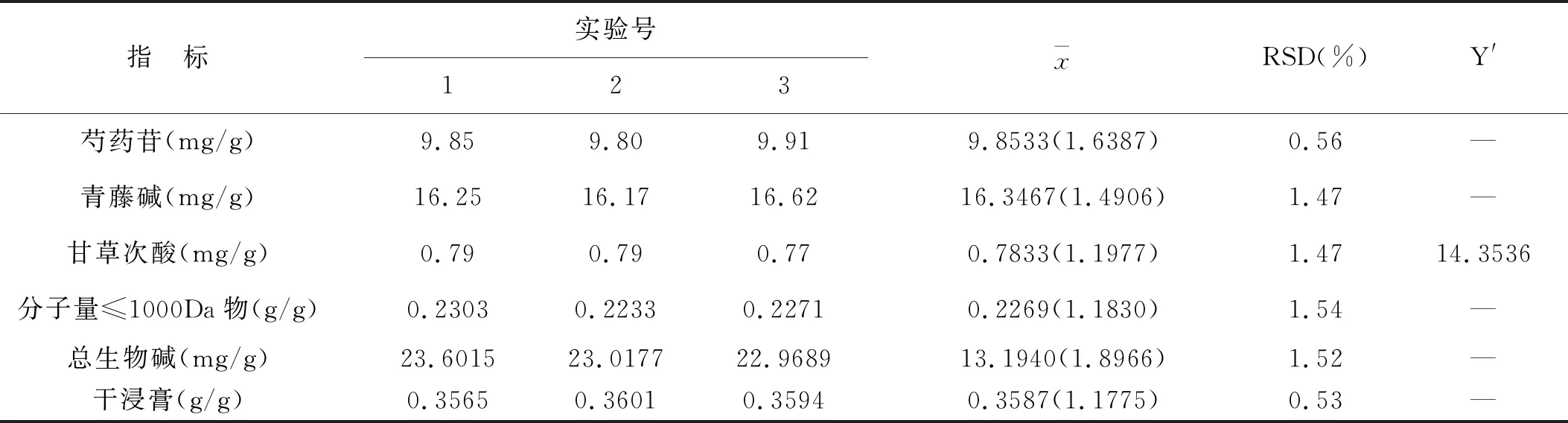
表6 3批验证性试验结果
注:括号内为标准化处理后数值。
中药中,已知单体活性化合物绝大多数为小分子物质,故本次提取工艺评价引入分子量≤1000Da的提取物这个评价指标,能体现中药整体、综合、客观、模糊的特点。本实验的工艺评价采用了多指标综合评判,为了消除各指标的单位和量纲的不同,以及各指标变量范围相差悬殊所造成的影响,对原始实验数据进行了标准化处理,并根据各指标在工艺选择中的主次地位,给予不同的加权系数,这样,优选出的SBE法工艺条件更科学、合理。本次实验优选出的青白通痹方药的半仿生提取的工艺条件为3次提取用水的pH值依次为2.0、7.0、9.0;提取时间依次为2.0 h、1.50 h、1.50 h。后续我们在此基础上再优选青白通痹方药半仿生-生物酶法提取(SBEE)、青白通痹方药醇提取(AE)的工艺条件,以期对青白通痹方药药效物质的提取进行系统研究。
