超小氧化钆点缀的介孔二氧化硅作为磁共振T1造影剂的实验研究
2019-06-12司元纯张桂龙吴正岩邹多宏陈乔尔
司元纯,张桂龙,王 丹,吴正岩,邹多宏,陈乔尔
磁共振成像(magnetic resonance imaging,MRI)造影剂是一类能够增强局部软组织图像对比度的物质,T1造影剂主要通过改变水质子的自旋-晶格驰豫时间,使病灶组织图像变的更亮,增强微小病灶与正常组织间的信号差异,为图像诊断提供有力的影像信息[1-2]。临床上应用的主要是T1造影剂,如二乙三胺五乙酸钆(gadolinium-diethylenetriaminepentaacetic acid,Gd-DTPA)。Gd-DTPA是一种小分子造影剂,其在体内代谢时间较短,难以获得病灶组织的高分辨影像,且纵向弛豫率仅有4~5 mmol-1·s-1,远远未达到钆(gadolinium,Gd)离子的理论弛豫率,这为研究人员对高性能钆基纳米造影剂的开发提供了巨大的提升空间[3-5]。该研究将具有顺磁性的氧化钆(gadolinium oxide,Gd2O3)整合到比表面积大、生物兼容性好的介孔二氧化硅(silicon dioxide,SiO2)的表面,保证Gd与水分子的有效接触,来产生更强的造影效果。
1 材料与方法
1.1 试剂和材料十六烷基三甲基溴化胺(cetyltrimethyl ammonium bromide,CTAB)、三乙醇胺(triethanolamine,TEA)、正硅酸四乙酯(tetraethyl orthosilicate,TEOS)购自上海阿拉丁公司;六水合氯化钆 (hexahydrated gadolinium chloride,GdCl3·6H2O)购自美国Sigma-Aldrich公司;细胞技术试剂盒(CCK-8)购自日本Dojindo公司。
1.2 仪器使用透射电子显微镜(TEM,JEM-2100F,日本JEOL公司)观测样品的形态;通过动态光散射粒度分析仪(DLS,Nanotrac Wave Ⅱ,美国Microtrac公司)检测粒径;孔隙率分仪(BET, Tristar Ⅱ,3020M,美国Micromeritics公司)测量样品的氮吸附-脱附等温曲线;采用X射线衍射仪(XRD,TTR-Ⅲ,日本Rigaku公司)分析晶体结构;使用傅里叶变换红外光谱仪(FTIR,iS10,美国Nicolet公司)检测有机共价键;热重分析仪(TGA, Q5000IR, 美国TA 公司)进行材料的热重分析;通过电感耦合等离子体光学发射光谱法(inductively coupled plasma optical emission spectrometer, ICP-OES,ICAP7200,美国Thermo Fisher Scientific公司)测定Gd离子浓度。
1.3 材料合成
1.3.1合成SiO2取50 ml锥形瓶,加入 2 g CTAB、20 μl TEA和20 ml超纯水,在磁力搅拌下,升温到80 ℃,保持此温度20 min后,逐滴加入1.5 ml TEOS,反应4 h。12 000 r/min离心10 min收集,60 ℃鼓风干燥箱内烘干,玛瑙研钵磨成粉,置于陶瓷坩埚中,在马弗炉中600 ℃煅烧6 h,得到SiO2。
1.3.2合成不同梯度Gd2O3镶嵌的SiO2另取5组50 ml锥形瓶,分别编号为②、③、④、⑤、⑥,分别加入2 g CTAB,20 μl TEA和20 ml超纯水,在磁力搅拌下,升温到80 ℃,保持此温度20 min后,逐滴加入1.5 ml TEOS,反应4 h。然后,编号②、③、④、⑤、⑥的锥形瓶中,分别加入1 ml不同浓度(0 、0.001、0.01、0.1、0.5 g/ml)的GdCl3·6H2O溶液,继续反应2 h,然后分别逐滴加入1 ml TEOS, 4 h后,12 000 r/min离心10 min收集。将上述6组离心产物分别收集至洁净容器中,置于60 ℃鼓风干燥箱内烘干,使用玛瑙研钵磨成粉,分别置于陶瓷坩埚中,在马弗炉中600 ℃煅烧6 h,编号为②、③、④、⑤、⑥煅烧后得到的产物,分别命名为SG0、SG0.001、SG0.01、SG0.1、SG0.1和SG0.5。
1.4 SG0.1的结构表征将适量SG0.1超声分散至无水乙醇中,再将混合溶液滴加到含有无定形碳膜的铜网上,烘干后放入到高分辨率投射电子显微镜中进行观察,观察SG0.1的形貌、尺寸和表面结构,X-射线能谱仪测量纳米材料中Gd的相对含量。
1.5 SG0.1的驰豫率测定制备不同Gd浓度(0、4.375、8.75、17.5、35、70 μmol/L)SG0.1的琼脂糖溶液封装于2.0 ml离心管中,使用临床磁共振扫描器(Sigma HDxt 3.0 Tesla MRI 系统),通过饱和恢复法自旋回波序列(回波时间=10 ms,脉冲时间=4 000、2 000、1 000、600、300、150 ms)获取T1加权的磁共振图像,并测得不同核磁管的纵向弛豫时间T1。使用ICP测定Gd离子浓度。通过纵向驰豫值的倒数/Gd离子浓度的线性拟合,来计算纵向弛豫率(longitudinal relaxation rate,r1)。
1.6 Gd离子泄露研究取SG0.1(5 mg)分别分散于含有pH为7.4、6.5、5.5、4.5和2.0 的4 ml的磷酸盐缓冲液(PBS)离心管中,另取SG0.1(5 mg)于10 ml试管中,加入2 ml浓硝酸和2 ml去离子水,在37 ℃水浴中静置72 h,用高速离心机12 000 r/min离心10 min,随后用电感耦合等离子体原子发射光谱仪(ICP)检测上清液中Gd离子的浓度。
1.7 细胞培养和细胞毒性测定将牙髓干细胞(dental pulp stem cell,DPSC)接种在96孔板中,应用含10 %胎牛血清的高糖DMEM培养液培养DPSC,置于37 ℃、5% CO2恒温恒湿培养箱内培养。当细胞增殖融合达培养皿80%时,使用0.25%胰蛋白酶消化细胞,然后将两组DPSCs用不同浓度SG0.1分别处理24 h和48 h,除去培养基,并用PBS洗涤细胞。使用CCK-8试验测定细胞存活量。
2 结果
2.1 结构表征SiO2具有最高的比表面积,在加入TEOS后,比表面积降低了50%,随着GdCl3·6H2O的添加量逐渐增大,比表面积逐渐增大,加入0.1 g时,比表面积最大,为661 cm3/g,继续提高添加量,比表面积开始减小。见图1A、1C。不同梯度的纳米粒子,均具有明显的介孔孔道结构,SiO2孔容积最大,随着加入的GdCl3·6H2O剂量逐渐增大,纳米粒子的介孔孔径逐渐减小,直径均小于4 nm,且孔容积逐渐降低。在添加不同GdCl3·6H2O浓度梯度中,SG0.1具有最高的比表面积,且在孔直径为1.6 nm时,孔容积最大。见图1B、1D 。
透射电子显微镜结果:合成后的纳米粒子呈球形,粒度分布窄,尺寸均一,粒径大小约50 nm, 具有明显的孔道结构,SG0.1在50、20、5 nm尺度下,均可明显看到Gd2O3纳米点,白色圈标记的为超小Gd2O3,不具有晶格结构,为无定形形态。见图 2。
X射线能谱图,X射线能谱分析仪(energy dispersive spectrometer,EDS)展现出纳米复合材料中存在明显的Gd元素,直接说明了纳米Gd2O3被成功整合在介孔硅中。见图3A。材料中硅元素与Gd元素的相对含量见图3B,Gd的相对质量占比为0.44%,原子百分比为0.08%。通过电感耦合等离子体原子发射光谱仪测得纳米复合材料(SG0.1)中Gd元素的质量百分比为1.6%(5 mg SG0.1经50%硝酸消解72 h后,ICP测得的Gd离子含量为80 μg)。
动态光散射粒度分析仪检测结果表明,SG0.1具有较窄的粒径分布,水合粒径约为200 nm,见图4A,这些结果说明SG0.1在溶液中具有较好的稳定性。X射线衍射结果显示SG0.1中SiO2的吸收峰变弱,且没有新的吸收峰出现,见图4B,这说明整合在SiO2中的Gd2O3为无定形形态。傅里叶红外结果显示,SiO2和SG0.1在1 100 cm-1明显的吸收峰和在1 150 cm-1~1 250 cm-1较弱的吸收带归属于Si-O非对称伸缩峰;在800 cm-1的吸收峰,属于Si-O-Si对称伸缩振动,在465 cm-1属于Si-O弯曲振动;此外,2 850 cm-1和2 925 cm-1为C-H伸缩振动,1 470 cm-1为C-H键的弯曲振动,见图4 C,说明SG0.1煅烧前含有有机物CTAB,而相应的峰位在煅烧后消失,表明CTAB被完全去除。热重分析仪(thermal gravimetric analyzer, TGA)检测结果见图4D,通过TGA检测SG0.1的水分和有机含量,测试温度从室温(20 ℃)开始,以20 ℃/min的升温速率,升到820 ℃。SG0.1(煅烧前)热重数据显示,温度小于200 ℃的重量损失主要由于水分子的损失(包含自由水和结合水),失重量为2.28%,温度在200~600 ℃之间的重量损失,主要是由于有机物模板剂(CTAB)煅烧分解产生的,失重量为43.17%,由此可知,煅烧前的产物中,有机物质量比为43.17%。600 ℃以后趋于平稳。SG0.1(煅烧后)在小于100 ℃区段内,失重量为5.68%;200 ℃以后基本趋于平稳,说明有机物在煅烧后已经完全去除。
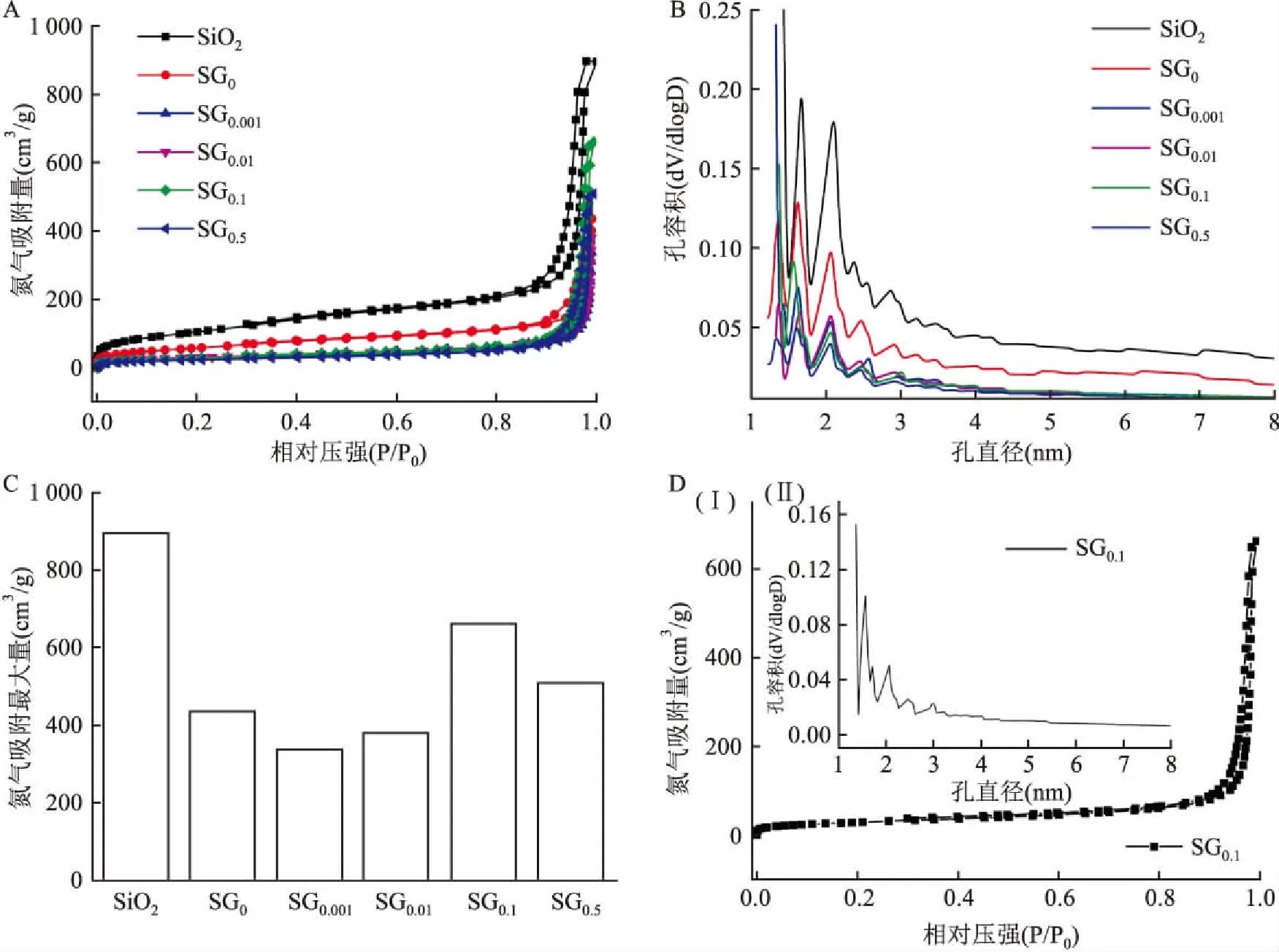
图1 不同氧化钆含量点缀的二氧化硅的比表面积及孔径分布图
A、B:分别为不同组份(SiO2、SG0、SG0.001、SG0.01、SG0.1及SG0.5)组合的氮气吸附-脱附曲线图和孔径分布图;C:上述各组份的比表面积柱状图;D:SG0.1的氮气吸附-脱附曲线图(Ⅰ)和孔径分布图(Ⅱ)

图2 SG0.1在不同放大倍数下的透射电镜图

图3 X射线能谱分析

图4 SG0.1的材料表征
A:SG0.1的水合粒径分布图;B:SiO2和SG0.1的X射线衍射图;C:SG0、SG0.1煅烧前和SG0.1煅烧后的红外图谱;D:SG0.1煅烧前和SG0.1煅烧后的热重分析
2.2 SG0.1的驰豫率在场强为3.0 T的磁共振扫描器中,测得SG0.1纵向驰豫率r1为45.1 mmol-1·s-1,是Gd-DTPA的10倍(r1=4.2 mmol-1·s-1),线性度高(R2= 0.99,R2是决定系数),SG0.1的明暗图表明随着Gd离子浓度逐渐增加,T1加权图像逐渐变亮,见图5。这些数据均表明制备的SG0.1具有较高的磁共振造影性能。
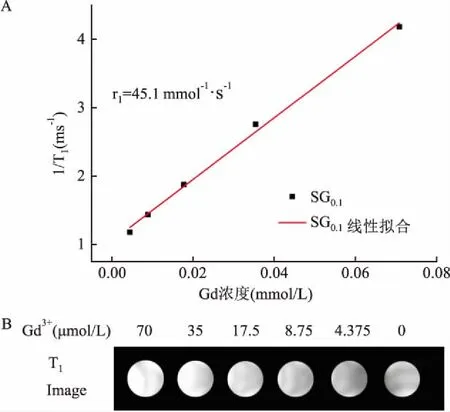
图5 SG0.1的磁共振性能表征
A: 1/T1-Gd浓度线性图,计算SG0.1的纵向弛豫率;B:不同Gd离子浓度的明暗图(场强3.0T)
2.3 SG0.1体外稳定性研究溶酶体和核内体是细胞内酸性最强的细胞器,pH通常在4.5~6.5之间。SG0.1在pH≥4.5的磷酸盐溶液中,Gd离子几乎不泄露,即使pH 2.0磷酸盐溶液中处理72 h,也仅有不到1%的泄漏,表明SG0.1具有极佳的酸稳定性能。见图6。
2.4 SG0.1的生物兼容性研究为了研究SG0.1的生物兼容性,通过CCK-8来评价其对细胞的毒性。
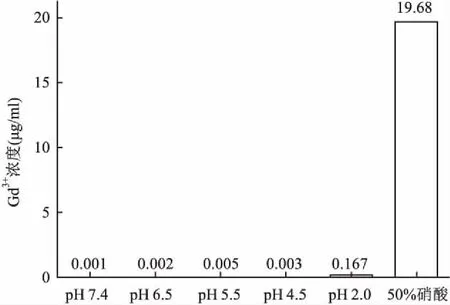
图6 不同pH的磷酸盐缓冲液中SG0.1的Gd3+释放量
在培养时间为24 h及48 h时,不同浓度SG0.1与对照组(0 μg/ml)比较,进行单因素方差分析。24 h的数据中,细胞存活率较低的几组数据(浓度为5 、10 、20 、40 μg/ml)与0 μg/ml单因素比较,细胞存活率差异无统计学意义(F=2.640,P>0.05)。其他浓度组与对应0 μg/ml比较,细胞存活率差异有统计学意义 (24 h:F=12.77,P<0.05; 48 h:F=12.07,P<0.05),但细胞存活率增加而未降低。见表1、图7。这些结果说明SG0.1纳米造影剂具有很好的生物安全性。

表1 24 h和48 h细胞存活率

图7 梯度浓度SG0.1与牙髓干细胞共培养24、48 h的细胞存活率
3 讨论
磁共振成像技术具有无电离辐射、高空间分辨率、穿透深度不受限制等特点,已广泛用于临床诊断[6]。目前MRI检查中,约有30%的检查需要用到MRI造影剂来增强局部造影能力,而目前临床使用的造影剂主要是Gd的螯合物(如Gd-DTPA、钆特酸葡胺),由于这类Gd螯合物为小分子物质,在机体中代谢很快,为了达到肉眼可辨识的成像效果,需要加大造影剂的使用剂量,从而增加Gd离子泄露导致的风险(如肾纤维化),特别是对于肾功能不全的患者更要慎用。研究[7-8]表明,相比于传统小分子造影剂,纳米造影剂在机体滞留时间较长,可以降低造影剂的使用剂量,易于功能化修饰,提高磁共振成像效果,因此众多研究人员大力开发纳米尺度(1~100 nm)造影剂。
造影剂本身不能产生造影信号,而是借助本身的磁学性质,通过与水分子的相互作用,间接改变病变部位与正常部位的氢质子的弛豫时间,使两者差别化更为明显,改变其信号强度,从而增强病变部位的图像对比度。Gd3+最外层有七个单电子,具有最强的偶磁矩,因而成为MRI造影剂的主要研究对象[9-10]。
介孔SiO2具有较高的比表面积、稳定介孔孔道、可调节的纳米尺度、较高的药物负载能力、易于表面修饰和良好生物兼容性等特点,氧化硅纳米材料的商用产品已广泛应用于临床,因而,介孔SiO2被广泛用于生物医药的研究[11-12]。Taylor et al[13]将Gd组装到介孔SiO2介孔晶体材料(mesoporous crystalline material,MCM)MCM-41的孔道当中,利用介孔SiO2多孔的结构特点,使钆离子与孔道内的水分子充分接触,改变周围水质子的翻转时间,提高纵向弛豫率。
本研究参考相关文献,选择相对尺寸适中,合成稳定的介孔SiO2合成方法[14],先合成出直径大小为30 nm左右,具有2 nm左右的孔道结构,以此介孔SiO2纳米粒子为内核,在反应混合溶液中,先加入GdCl3·6H2O,在碱性条件下(混合溶液的pH为9.0),先形成氢氧化钆包覆于介孔SiO2的表面,再加入TEOS,将Gd2O3束缚于SiO2表层,烘干后又经过高温煅烧,除去有机模板,氢氧化钆脱水变成Gd2O3,形成Gd2O3镶嵌在介孔SiO2的表面。通过SiO2的多孔结构束缚水分子,延长水分子的滞留时间,增加Gd2O3与水分子的接触时间,提高造影效果,本实验合成和机制诠释图见图8。

图8 SG0.1的合成及机制诠释
介孔SiO2的比表面积越大,其所能束缚水分子的能力越强,自由通过孔道进入的水分子也就越多,因而,表面Gd2O3接触的水分子数量和时间也就越长[10]。通过探讨5个梯度的GdCl3·6H2O添加量,显示在添加量为0.1 g时,获得的产物比表面积最大,孔道结构明显。以SG0.1作为研究对象,并进一步对SG0.1的结构进行表征,检测其MRI造影性能、稳定性以及生物相容性。
本研究表明,SG0.1作为新型MRI造影剂,具有稳定均一的纳米结构,优良的对酸稳定性能,极佳的造影性能和生物兼容性,为未来潜在的临床应用提供坚实依据。
