光合作用中光反应的机制和由来(4)
2019-05-23朱钦士美国南加州大学医学院
朱钦士 (美国南加州大学医学院)
(上接2019年第4期第12页)
6 色素分子吸收可见光的原理
细胞中常见的分子,例如氨基酸、核苷酸、脂肪酸、葡萄糖,以及由它们组成的蛋白质、核酸、脂肪和淀粉都无法吸收可见光, 因为这些分子的吸收峰都在紫外区。 这个事实也可以从这些分子都没有颜色这一现象中辨别。 如果一种分子能吸收可见光, 由于它通常不可能吸收可见光中所有波长的光,而只能吸收某些波长的光,没有被吸收的光就会显现出颜色。例如某个分子吸收蓝绿光,没有被吸收的可见光在人们眼中就显现为橙红色。 因此,如果一种分子有颜色,则说明它能吸收可见光。人们将这些能吸收可见光,因而也有颜色的分子称为“色素”(pigment)。 生物所使用的色素主要是视黄醛(retinal)和叶绿素(chlorophyll),其中视黄醛是橙黄色的,叶绿素的颜色是绿色的,它们都可以将太阳光的能量转化为跨膜氢离子梯度。在进一步介绍其生理功能前,先介绍为什么色素分子能吸收可见光。
一个分子要吸收可见光, 必须要有电子能吸收可见光波长范围内的光子的能量, 而跃迁到更高的能级轨道上, 这与分子中电子所在的化学键有关。 色素分子和其他主要的生物分子(葡萄糖、脂肪酸、氨基酸、核苷酸等)一样,也是以碳原子彼此相连形成的线状(分支或不分支)或环状的结构为骨架的。色素分子之所以能吸收可见光,与它含有由许多双键,特别是碳原子之间的双键,所组成的巨大“共轭系统”(conjugated system)有关。
碳原子以4 条共价键与其他原子(包括碳原子)相连。 如果这4 条键都是单键,碳原子外层的4 个电子(1 个s 电子和3 个p 电子)的轨道彼此混合,形成4 个相同的轨道,称为sp3杂化轨道。这4 个轨道再与其他原子以单键相连。 单键对电子的束缚较大, 吸收光能实现电子跃迁需要的能量较多, 因此吸收的光波长都较短。 例如甲烷(1个碳原子与4 个氢原子以单键相连)的吸收峰在125 nm,其他饱和烷烃(即由碳原子以单键连成的链或环,上面再连上氢原子)的吸收峰在150 nm 左右,都在紫外区,饱和脂肪酸的长“尾巴”部分就相当于饱和烷烃。葡萄糖和氨基酸分子的骨架也由碳原子以单键相连组成,这些单键中的电子跃迁吸收的光都在紫外区,在可见光区都没有吸收。
碳原子之间以双键相连时,就不形成sp3杂化轨道,而是2 个p 电子和1 个s 电子的轨道混合,形成3 个sp2杂化轨道, 剩下的1 个p 电子的轨道不变,仍为纺锤形。 在碳-碳双键中,一条键是通过sp2杂化轨道形成的,另一条链是未改变的p轨道彼此重叠形成的。 这种重叠的p 轨道叫做π轨道,π 轨道中的电子叫做π 电子。 由于碳原子之间是通过2 条共价键相连,它们之间的距离(即双键的长度)为0.134 nm,明显短于碳-碳单键的0.154 nm。双键中电子的运动范围比单键大,跃迁所需要的能量也比单键少, 例如乙烯的吸收峰就在162 nm,长于乙烷的135 nm。
如果有2 个碳-碳双键,彼此被一条单键隔开,这2 个双键的π 轨道又可以彼此部分重叠, 形成一个共同的大π 轨道, 使得隔开2 个双键的那条单键变短,从0.154 nm 变为0.148 nm,成为部分双键,相当于2 个双键和它们之间的1 个弱一些的双键融合在一起,使电子活动的范围更大,跃迁需要的能量更低,例如1,3-丁二烯的吸收峰就在217 nm,长于乙烯。 这种π 轨道可彼此重叠的双键就称为“共轭双键”(conjugated double bonds)。
除了2 个双键可形成共轭双键, 多个被单键隔开的双键还可形成更大的共轭系统, 即更大的π 轨道,因为它们的π 轨道也可以像丁二烯分子内的2 个π 轨道那样彼此重叠。 参与共轭双键体系的双键数量越多,π 轨道的范围越大,电子的活动范围就越大,跃迁需要的能量则越少。例如1,3,5-己三烯(3 个双键共轭)的吸收峰移到285 nm,葵5 烯(5 个双键共轭)的吸收峰在335 nm。 组成蛋白质的氨基残基中,酪氨酸、色氨酸和苯丙氨酸的侧链含有由3~4 个双键组成的环状共轭系统,所以蛋白质在280 nm 有一个吸收峰, 可用于测定蛋白质的浓度。 DNA 中的碱基(嘌呤和嘧啶)也是环状的共轭系统,在260 nm 有吸收峰,可用于测定DNA 的浓度。 尽管如此,这些光吸收仍然在紫外光的范围内,要有效地捕获光能,需要更大的共轭系统,将吸收区域转移到可见光的范围内,这就只有色素分子办得到。上面说的视黄醛和叶绿素就是具有这种功能的分子,下文分别加以介绍。
7 结合于膜蛋白上的视黄醛分子在受到光照时可建立跨膜质子梯度
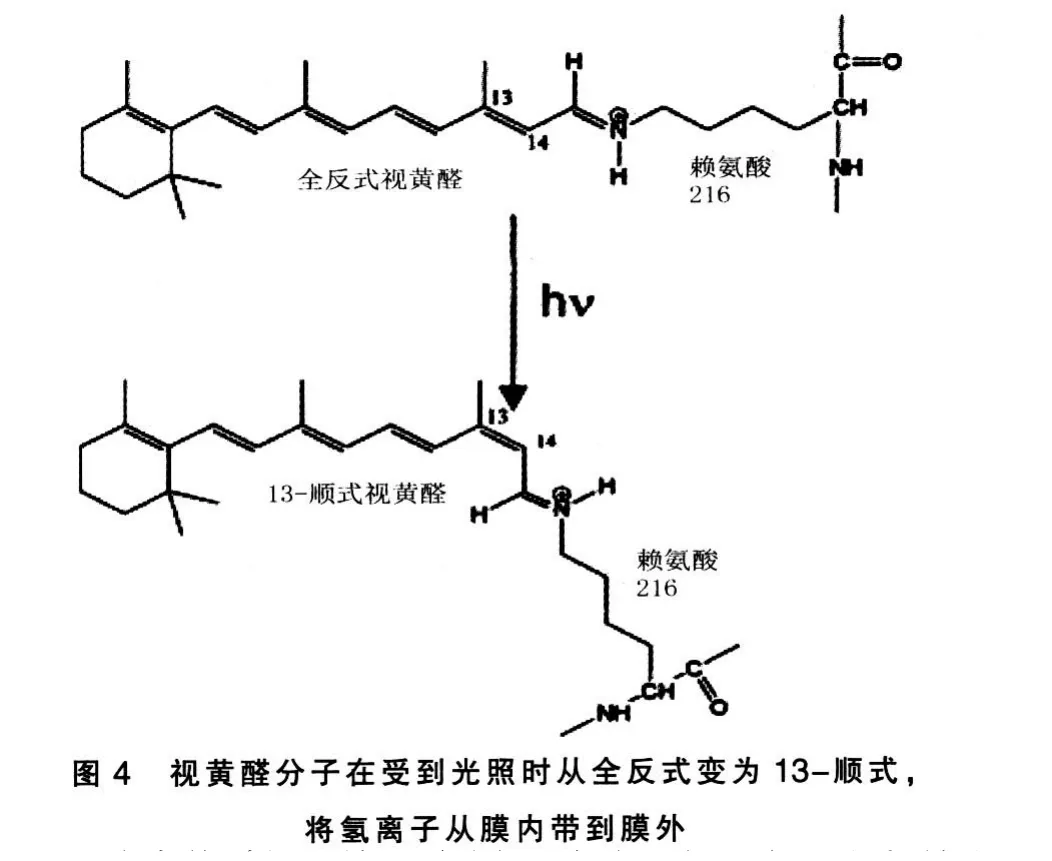
视黄醛(retinal)的分子构造有点像醌分子,也含有一个由6 个碳原子连成的环状“头部”和一条亲脂的“尾巴”(图4)。 视黄醛的“头部”并不像醌分子那样含有2 个羟基, 所以没有传递氢原子的功能,但它“尾巴”的结构却使它有另一种奇特的功能,就是在受到光照时可改变形状。轭系统,包括6 碳环中的1 个双键和“尾巴”中的4个双键。 仅凭这5 个双键组成的共轭系统,视黄醛的吸收峰仍然在紫外区域,峰值大约在380 nm。之所以视黄醛能吸收可见光, 和视黄醛与蛋白质的结合有关。
视黄醛分子“尾巴”末端的醛基可以和蛋白质分子中的一个赖氨酸残基上的氨基以共价键结合,形成一个称为“席夫碱”(Schiff base,由氨基NH2和羰基C=O 缩合而成的C=N 键)的结构,这样视黄醛就可以与蛋白质分子以共价键相连了。不仅如此,席夫碱上的氮原子还能与蛋白质中带羧基的氨基酸(例如谷氨酸和天冬氨酸)侧链上的氢离子结合,称为席夫碱的“质子化”(protonated)。 席夫碱及其质子化都会增大视黄醛分子共轭系统中电子的自由度, 使其吸收峰从原来的380 nm 移到可见光的范围内(500 nm 或更长)。 由视黄醛和视蛋白(opsin)共价相连组成的分子叫视紫质(rhodopsin),是转化太阳光能量的分子。
视紫质之所以能转化太阳光中的能量, 除了能吸收可见光外,还与“尾巴”的性质有关。 视黄醛的“尾巴”含有由双键组成的大共轭系统,而双键是不能转动的,这样的结构就具有“刚性”,像一根不易弯曲的“棍子”。 但奇特的是,它在受光照射时可改变形状,从“全反式”(与双键相连的2个碳原子在双键的异侧)变为“13-顺式”(在第13位碳原子处的双键, 与其相连的2 个碳原子在双键的同侧),也就是“直棍”在中间拐个弯,变成“弯棍”。 此性质就可用于跨膜移动氢离子。
例如有些古菌就利用视黄醛建立跨膜氢离子梯度。 这些古菌是“嗜盐菌”(Halophiles),可在高浓度的盐溶液中生活。 其中的盐杆菌(Halobacteria)的细胞膜呈紫色, 因为膜上含有大量的视紫质蛋白。 它有7 个跨膜区段,在细胞膜内围成筒状,视黄醛分子就位于筒的中央,与第216 位的赖氨酸形成席夫碱共价连接。 这个席夫碱上的氮原子能与第96 位上的天冬氨酸残基上的1 个氢离子结合,即质子化,使视紫质蛋白中视黄醛能吸收500 ~650 nm 的 光(绿 色 和 黄 色),其 吸 收 峰 在568 nm,呈现紫红色。 在受到光照时,视黄醛分子形状变化,从“直棍”变为“弯棍”。 这个形状的改变就将氢离子从位于膜内侧的第96 位的天冬氨酸残基上,转移到位于膜外侧第85 位的天冬氨酸残基上,再释放至细胞膜的外面,产生跨膜氢离子梯度(图4)。 这是盐杆菌利用光能的巧妙机制,也属于广义的“光合作用”的范畴。
这种利用光能的方法虽简单直接,但它只能形成跨膜氢离子梯度,而不是像基于叶绿素的光合作用那样还可以产生具有还原作用的高能电子用于有机合成,所以只有少数微生物使用它。虽然如此,视黄醛在受到光照时改变形状这一宝贵的特性,还被生物用于执行别的功能,包括开启离子通道。 例如一些嗜盐菌所含的盐菌紫质(Halorhodopsin),在受橙色光照射时可打开膜上的离子通道,让带负电的氯离子通过细胞膜。 真核生物莱氏衣藻(Chlamydomonas reinhardtii)在细胞膜上含有光敏离子通道(channelrhodopsin),它在受到光照时开启,让各种正离子,例如氢离子、钠离子、钾离子和钙离子通过细胞膜。
视黄醛最重要的生理功能,是形成动物(包括人)的视觉。光照时动物的视紫质不是产生跨膜氢离子梯度,而是通过视黄醛受光照时的形状改变,使与之结合的蛋白形状改变, 在视觉细胞中将光能转化为神经信号,使动物产生视觉。由于视紫质在视觉中的作用在1876年就被发现,因而其中的辅基后来也被称为“视”黄醛(retinal),来自“视网膜”(retina)这个名称,而视黄醛在建立跨膜氢离子通道的作用直至20 世纪80年代才被发现,其名称也因此仍然称为视黄醛, 尽管在此其功能与视觉无关。利用光照建立跨膜氢离子梯度的任务,主要是依靠叶绿素分子执行的。
(待续)
