抗VEGF靶向药物联合化疗对NSCLC患者脑转移发生率、生存时间及实验室指标的影响
2019-04-03宋春青高正兴卢桂龙任建鸿
宋春青,高正兴,卢桂龙,韩 磊*,任建鸿
0 引言
肺癌对人类的生命健康威胁极大,大多数患者确诊时已为晚期,其中非小细胞肺癌(NSCLC)占肺癌发病率的80%以上[1]。目前,晚期肺癌的标准治疗方案是铂类联合其他细胞毒性药物,但疗效仍欠佳[2]。贝伐单抗属于新型靶向治疗药物,可以抑制血管内皮细胞生长因子(VEGF),是NSCLC治疗的研究热点[3]。本文研究贝伐单抗联合培美曲塞和顺铂化疗对NSCLC患者脑转移发生率、生存时间及VEGF蛋白的影响,现报道如下。
1 资料与方法
1.1 研究对象 选择2013年1月至2014年12月在我院接受治疗的晚期NSCLC患者60例。纳入标准:①经病理学检查均确诊为NSCLC;②TNM分期为Ⅲ~Ⅳ期;③预计生存期>3个月;④KPS评分>70分,ECOG评分0~2分,符合化疗指征;⑤均有可测量的肿瘤病灶且未发生脑转移;⑥患者家属知情同意。排除标准:①合并严重原发性心、肝、肾、血液疾病;②患出血性疾病或存在凝血机制障碍;③妊娠期、哺乳期妇女或精神疾病。经医院伦理委员会批准,共纳入符合标准的患者60例,用随机数表法分为2组,每组30例。两组患者的一般资料比较差异无统计学意义(P>0.05),见表1。
1.2 方法 对照组患者给予培美曲塞和顺铂治疗,培美曲塞(规格:500 mg,批准文号:国药准字H20090135,生产企业:南京先声东元制药有限公司)500 mg/m2,静脉滴注,d1;顺铂(规格:20 mg,批准文号:国药准字H37021358,生产企业:齐鲁制药有限公司) 75 mg/m2,静脉滴注,d1。患者用药前1周口服叶酸片0.4 mg/d,持续到治疗结束;用药前1周给予维生素B121 mg肌注,每3个疗程再补充1次维生素B12,用药前1 d、当天和次日口服地塞米松片4 mg,2次/d。
观察组患者在对照组的基础上加用贝伐单抗,贝伐单抗(规格:100 mg∶4 ml,批准文号:注册证号S20120068,生产企业:瑞士罗氏制药公司)7.5 mg/kg,静脉滴注,d1。21 d为1个周期,化疗2个周期后进行疗效评价。
1.3 观察指标 ①根据《实体瘤的疗效评价标准》评价患者的近期疗效,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD),客观有效率(ORR)=(CR+PR)/总例数,疾病控制率(DCR)=(CR+PR+SD)/总例数。②统计两组患者的1年、2年和3年生存率。③采用酶联免疫吸附法检测患者的VEGFA、VEGFB和VEGFC蛋白水平。④根据WHO标准的抗肿瘤药物不良反应分级,统计Ⅲ+Ⅳ级不良反应的患者例数。⑤统计两组患者的脑转移例数。

2 结果
2.1 两组患者的近期疗效比较 观察组患者的ORR为53.33%,DCR为86.67%,明显高于对照组,见表2。
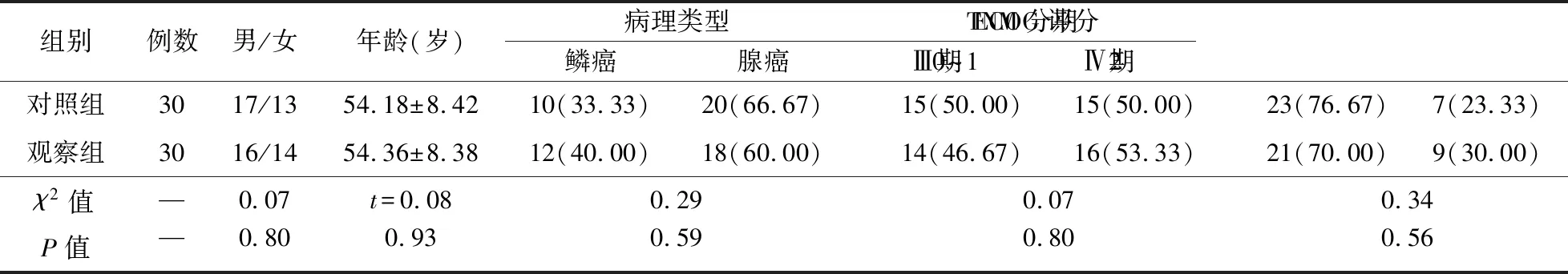
表1 两组患者一般资料比较(例,%)

表2 两组患者的近期疗效比较(例,%)
2.2 两组患者的生存率比较 观察组患者1年生存率为66.67%,2年生存率为40.00%,3年生存率为26.67%,均明显高于对照组(P<0.05),见表3。
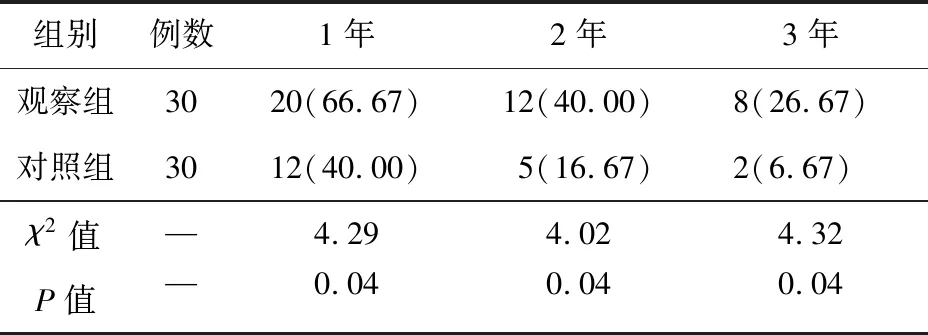
表3 两组患者的生存率比较(例,%)
2.3 两组患者的VEGF蛋白水平比较 观察组患者的VEGFA蛋白水平为(87.51±10.36) pg/ml,VEGFB蛋白水平为(78.42±9.48) pg/ml,VEGFC蛋白水平为(50.17±7.34) pg/ml,均明显低于对照组(P<0.05),见表4。

表4 两组患者的VEGF蛋白水平比较(pg/ml)
2.4 两组患者的不良反应比较 观察组患者高血压的发生率高于对照组(P<0.05),两组患者恶心呕吐、血小板减少、白细胞减少、贫血、蛋白尿、出血的发生率比较差异无统计学意义(P>0.05),见表5。
2.5 两组患者的脑转移发生率比较 治疗1年后,观察组脑转移2例(6.67%),对照组5例(16.67%),两组比较差异无统计学意义(χ2=1.46,P>0.05);治疗2年后,观察组脑转移3例(10.00%),对照组10例(33.33%),观察组脑转移发生率低于对照组(χ2=4.82,P<0.05)。
3 讨论
肺癌的恶性程度较高,导致死亡率较高,虽然目前社会的禁烟力度逐渐加大,但肺癌的发病率仍不容小觑。肺癌死亡例数占恶性肿瘤死亡例数的20%左右,居恶性肿瘤死亡率首位。NSCLC早期缺乏特异性的临床特征,早期诊断率较低,大多数患者确诊时已为晚期[4]。NSCLC具有生长速度快、危害程度高、治愈率低等特点,及时有效的治疗是延长患者生存时间的根本方法。NSCLC化疗的主要目的是缩小肿瘤体积、降低肿瘤分期,但是NSCLC的恶性程度较高,肿瘤内血管的新生能力较强且转移快,因此,常规的化疗方案难以有效控制肿瘤的生长和转移[5]。
本文研究结果显示,观察组患者的ORR为53.33%,DCR为86.67%,明显高于对照组,近期疗效较好,与邱水晶等[6]的研究结果基本一致。但张玉梅等[7]研究发现,NSCLC患者采用贝伐单抗联合培美曲塞化疗与单用培美曲塞化疗的临床缓解率相近,这可能与病例数较少有关。观察组患者1年生存率为66.67%,2年生存率为40.00%,3年生存率为26.67%,明显高于对照组。培美曲塞是对肺癌有效的第3代细胞毒性化疗药物,可以抑制嘌呤和胸腺嘧啶核苷的合成,从而抑制肿瘤细胞基因的复制和转录,使肿瘤增殖停滞于S期,有效抑制肿瘤细胞的生长[8-10]。贝伐单抗是针对VEGF的重组人源化单克隆IgG抗体,能够与VEGF特异性结合,从而抑制VEGF的生物学效应,降低内皮细胞的增殖,抑制新生血管形成,从而阻断氧气和营养物质的供应,抑制肿瘤生长和转移[3,11-12]。
肿瘤的发生、发展与新生血管的形成关系密切,而VEGF是促进血管形成的重要因素。本研究中,观察组患者的VEGFA、VEGFB、VEGFC蛋白水平分别为(87.51±10.36)、(78.42±9.48)、(50.17±7.34) pg/ml,明显低于对照组。血管生成在实体肿瘤的发生及发展中起着重要作用,肿瘤直径超过2 cm就需要产生新的血管支持肿瘤进行增殖和侵袭,而VEGF是肿瘤血管生成的重要参与物质,因此,抑制VEGF的作用可以抑制肿瘤的发展[13-14]。贝伐单抗可以与VEGF特异性结合,抑制VEGF的促血管形成作用,从而抑制肿瘤新生血管的形成,提高患者的临床疗效[15]。

表5 两组患者的不良反应比较(例,%)
本研究显示,观察组患者高血压的发生率高于对照组,两组患者恶心呕吐、血小板减少、白细胞减少、贫血、蛋白尿、出血的发生率比较差异无统计学意义。VEGF可以作用于内皮细胞,促进血管舒张剂的分泌,从而稳定血压。贝伐单抗抑制VEGF的活性,影响患者血压的正常调节[16]。陈瑞琳等[16]研究结果显示,晚期非鳞癌NSCLC患者采用贝伐单抗联合培美曲塞+铂类化疗方案,除高血压外,其不良反应与采用培美曲塞联合铂类化疗的患者无明显区别,与本文研究结果一致。
本研究显示,治疗1年后,两组脑转移例数比较差异无统计学意义;治疗2年后,观察组脑转移例数少于对照组。肺癌是恶性肿瘤脑转移瘤的常见原因,在肺癌发展的过程中,脑转移的发生率甚至达到了40%~50%[17]。肺癌患者出现脑转移会严重降低生存质量和认知功能,中位生存期仅3~6个月[18]。脑转移的发生是一个多阶段、多步骤的过程,新血管的生成在脑转移的发展过程中起到了非常重要的作用[19]。VEGF信号通路是血管生成有关的许多路径中最重要的信号通路,肺癌脑转移的发生、发展与VEGF作用密切相关,因此,采用贝伐单抗化疗抑制VEGF的生物效应可以在一定程度上降低NSCLC患者的脑转移发生率。
综上所述,贝伐单抗联合培美曲塞和顺铂化疗可以提高NSCLC患者的近期疗效,降低脑转移发生率,抑制血管内皮细胞生长因子,且患者耐受性较好,值得在临床推广应用。
