温经汤中6种水溶性活性成分的含量测定*
2019-04-02路娟柴瑞平陈曦
路娟,柴瑞平,陈曦
(中国医学科学院药用植物研究所,北京 100193)
温经汤出自《金匮要略·妇人杂病脉证并治第二十二》,全方由12味中药组成,分别为吴茱萸、桂枝、当归、川芎、牡丹皮、阿胶、麦门冬、芍药、人参、甘草、半夏、生姜和甘草[1]。临床使用历史悠久,疗效明显,主治妇科原发性痛经等病[2-3]。目前,温经汤的化学成分分析及质量标准制定笔者还未见报道,仅有方中部分单味药材的质控研究,这对于中药复方新药的开发是远远不够的。寻找快速、准确、简便的分析方法对复方制剂的质量控制至关重要,不仅要提升复方质量标准,还要符合企业生产实际,本次研究拟对涵盖12味中药的中药复方温经汤的含量测定方法进行探索,以期对后续进入实际生产发挥指导与参考意义。关于古方温经汤,桂皮醛、丹皮酚、甘草酸、吴茱萸碱为2015年版《中华人民人民共和国药典》中规定的桂枝、牡丹皮、甘草、吴茱萸指标性成分[4-7],绿原酸及隐绿原酸则是具有多种药理活性作用的酚酸类化合物[8-10]。本课题组前期已成功建立温经汤高效液相指纹图谱,基本反映了其整体化学特征,并对绿原酸等6个化学成分进行了指认,方法简单易行,数据清晰可信。本研究结合前期基础,采用高效液相色谱法同时测定温经汤中绿原酸、隐绿原酸、甘草酸、桂皮醛、丹皮酚和吴茱萸碱等6种水溶性活性成分的含量,涉及本方多种关键药味,为其临床使用的安全性及有效性提供参考。
1 仪器与试药
1.1仪器 Waters UPLC H-Class系统(含四元溶剂泵,自动进样装置,在线真空脱气装置,PDA检测器,Empower2色谱工作站)、AB265-S型分析天平(十万分之一,瑞士METTLER公司)、2-16R台式高速微量冷冻离心机(上海托莫斯科学仪器有限公司)。
1.2药品与试剂 人参饮片购于吉林敖东健康科技有限公司,生姜购于北京物美超市,其余药材饮片均购于北京市同仁堂药店(马连洼店),经中国医学科学院药用植物研究所云南分所李海涛教授鉴定均为正品,符合2015版《中国药典》标准。 绿原酸(批号:170903)、隐绿原酸(批号:171016)、甘草酸铵(批号:170603),桂皮醛(批号:170328),丹皮酚(批号:170421)及吴茱萸碱(批号:170524)均购自于上海融禾医药科技有限公司。乙腈(Merck公司,色谱纯)、甲酸(汕头市西陇化工厂有限公司,分析纯)、屈臣氏双蒸水,其他试剂为分析纯。
2 方法与结果
2.1温经汤水煎液及供试品溶液的制备 参考《名方配伍分析及应用》(人民卫生出版社)收录,按一两=3 g计算,取吴茱萸9 g,当归6 g,川芎6 g,人参6 g,桂枝6 g,阿胶6 g,生姜6 g,牡丹皮6 g,甘草6 g,半夏6 g,麦冬9 g,加水10倍量,浸泡30 min,加热回流提取2次,每次1 h,合并两次滤液,摇匀后水浴浓缩至750 mL,取适量滤液,4 ℃,12 000 r·min-1离心(r=6 cm)10 min,经孔径0.22 μm微孔滤膜滤过,取续滤液即得供试品溶液,置于进样小瓶中待测,剩余样品密封后保存于-20 ℃环境中[11]。同法平行制备温经汤水煎液10批,编号S 1~S 10,供测试用,同时留样保存于实验室冰箱。
2.2对照品溶液的制备 精密称取绿原酸、隐绿原酸、甘草酸铵、桂皮醛、丹皮酚、吴茱萸碱对照品分别置于5 mL量瓶中,加入纯甲醇制备单一对照品母液;精密吸取单一对照品母液适量,置于同一量瓶中,加入纯甲醇定容摇匀,配制得到含有绿原酸、隐绿原酸、甘草酸铵、桂皮醛、丹皮酚、吴茱萸碱浓度分别为150.08,150.36,344.08,16.83,51.06,40.74 μg·mL-1的混合对照品溶液(其中:甘草酸质量=甘草酸铵质量/1.0207)。
2.3阴性对照溶液的制备 按照“2.1”项下供试品溶液制备方法分别制备缺吴茱萸、缺甘草、缺桂枝、缺牡丹皮的阴性样品及缺吴茱萸、甘草、桂枝、牡丹皮的阴性样品溶液,处理方法不变。
2.4色谱条件 Waters Xselect HSS T3色谱柱(4.6 mm×250 mm,5 μm),流动相为乙腈(A)-0.1%甲酸水溶液(B),梯度洗脱(0~25 min,5%~22% A,25~35 min,22%~30% A,35~45 min,30%~60% A,45~60 min,60%~80% A),平衡色谱柱15 min,流速0.8 mL·min-1,柱温25 ℃,进样量10 μL,检测波长分别为:绿原酸327 nm、隐绿原酸327 nm、甘草酸(铵)237 nm、桂皮醛290 nm、丹皮酚274 nm、吴茱萸碱225 nm。分别精密吸取混合对照品溶液、供试品和阴性对照溶液各10 μL,进液相色谱仪进行分析,记录色谱图。样品中绿原酸等6种水溶性成分的色谱峰达到较为理想的分离效果,且阴性对照无干扰。对照品、样品及阴性样品色谱图见图1。
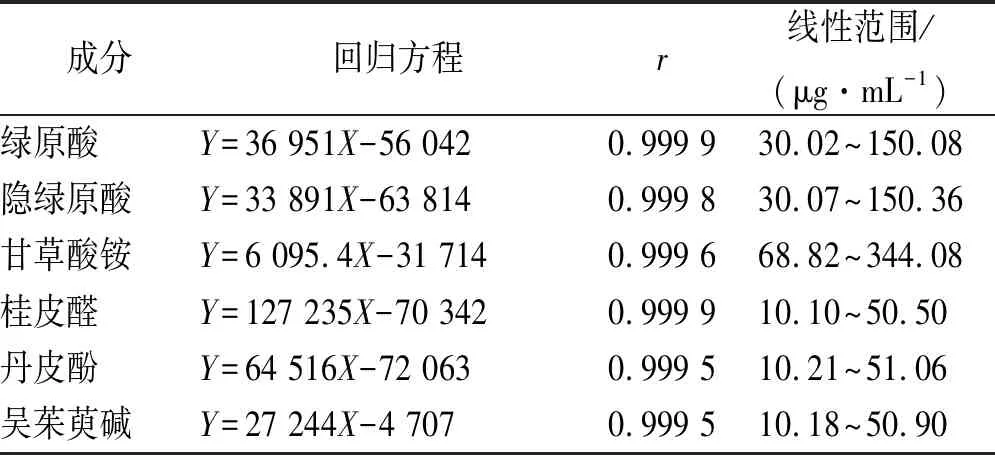
2.5线性关系考察 将“2.2”项得到的混合对照品溶液梯度稀释为一系列不同浓度的混合对照品溶液,按照“2.4”项下色谱条件进样测定。以进样浓度为横坐标(X),峰面积(Y)为纵坐标,绘制标准曲线,计算回归方程。绿原酸、隐绿原酸、甘草酸铵、桂皮醛、丹皮酚、吴茱萸碱对照品回归方程、峰面积与浓度相关系数(r)及线性浓度范围见表1。结果显示,各个成分在各自范围内呈良好的线性关系。
2.6重复性实验 精密吸取S1批温经汤样品 5份,按“2.4”项色谱条件进行测定,测得绿原酸、隐绿原酸、甘草酸、桂皮醛、丹皮酚和吴茱萸碱各成分峰面积的RSD分别为0.44%,0.56%,0.32%,0.51%,1.02%,0.88%,表明该方法重复性良好。
2.7精密度实验 精密吸取混合对照品溶液,按“2.4”项色谱条件连续进样5次进行测定,测得绿原酸、隐绿原酸、甘草酸、桂皮醛、丹皮酚和吴茱萸碱各成分峰面积的RSD分别为0.31%,0.15%,0.22%,0.60%,0.18%,0.77%,表明仪器精密度良好,符合要求。
2.8稳定性实验 精密吸取同一温经汤样品溶液,在室温下放置,分别于0,2,4,8,12,24 h按“2.4”项色谱条件进行测定,测得绿原酸、隐绿原酸、甘草酸、桂皮醛、丹皮酚和吴茱萸碱各成分峰面积的RSD分别为0.35%,0.29%,0.30%,0.48%,0.35%,1.11%,表明样品溶液中6种水溶性成分在24 h内稳定性良好。
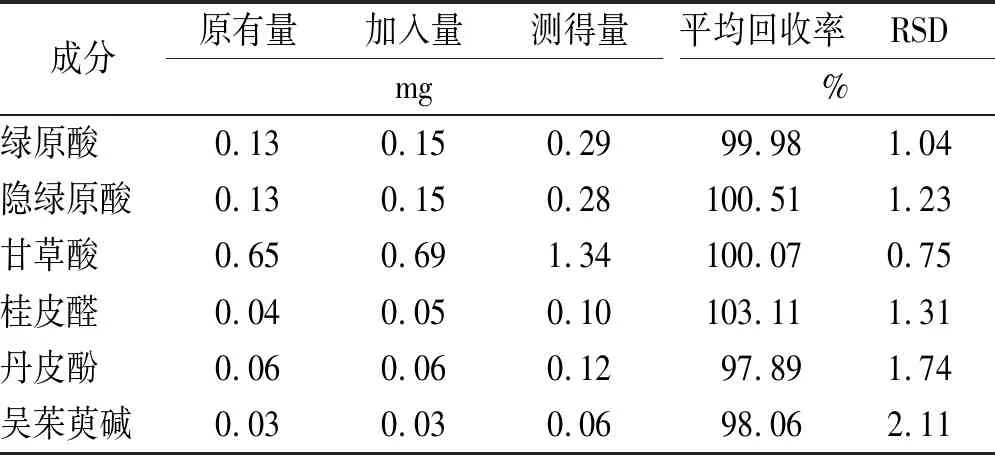
2.9加样回收率实验 取已知绿原酸、隐绿原酸、甘草酸、桂皮醛、丹皮酚、吴茱萸碱含量的温经汤样品6份,每份2.5 mL,精密加入绿原酸、隐绿原酸、甘草酸铵(其中:甘草酸质量=甘草酸铵重量/1.0207)、桂皮醛、丹皮酚、吴茱萸碱对照品适量,制得供试品溶液,按“2.4”项色谱条件进行测定并计算加样回收率,结果见表2,表明该方法准确度良好,符合技术要求。
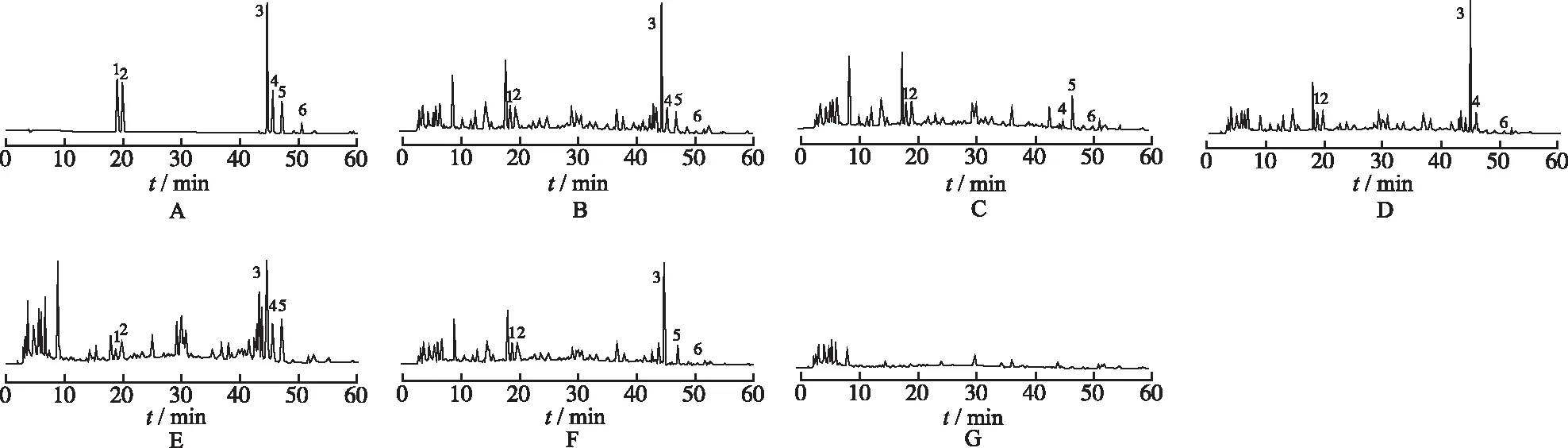
A.混合对照品; B.温经汤水煎液;C.缺甘草阴性样品溶液;D.缺牡丹皮阴性样品溶液;E.缺吴茱萸阴性样品溶液;F.缺桂枝阴性样品溶液;G.同时缺以上4味药材的阴性样品溶液;1.绿原酸;2.隐绿原酸;3.甘草酸铵;4.桂皮醛;5.丹皮酚;6.吴茱萸碱
图1254nm波长下温经汤HPLC色谱图
A.mixed reference substances; B.Wenjingdecoction; C.negative sample withoutGlycyrrhizaeRadix;D.negative sample withoutMoutanCortex; E.negative sample withoutEvodiaeFructus;F.negative sample withoutCinnamomiRamulus;G. Negative sample withoutGlycyrrhizaeRadix,MoutanCortex,EvodiaeFructusandCinnamomiRamulus;1.chlorogenic acid;2.cryptochlorogenic acid;3.glycyrrhizic acid;4.cinnamaldehyde;5.paeonol;6.evodiamine
Fig.1HPLCchromatogramofWenjingdecoctionat254nm
表1温经汤6种水溶性成分回归方程、峰面积与浓度相关系数及线性范围
Tab.1Regressionequation,correlationcoefficientofpeakareaandconcentration,andlinearrangeofsixwater-solubleactiveingredientsfromWenjingdecoction
成分回归方程r线性范围/(μg·mL-1)绿原酸Y=36 951X-56 0420.999 930.02~150.08隐绿原酸Y=33 891X-63 8140.999 830.07~150.36甘草酸铵Y=6 095.4X-31 7140.999 668.82~344.08桂皮醛Y=127 235X-70 3420.999 910.10~50.50丹皮酚Y=64 516X-72 0630.999 510.21~51.06吴茱萸碱Y=27 244X-4 7070.999 510.18~50.90
表2温经汤6种水溶性成分加样回收率实验
Tab.2Recoveryofsixwater-solubleactiveingredientsfromWenjingdecoctionn=6
成分原有量加入量测得量mg平均回收率RSD%绿原酸0.130.150.2999.981.04隐绿原酸0.130.150.28100.511.23甘草酸0.650.691.34100.070.75桂皮醛0.040.050.10103.111.31丹皮酚0.060.060.1297.891.74吴茱萸碱0.030.030.0698.062.11
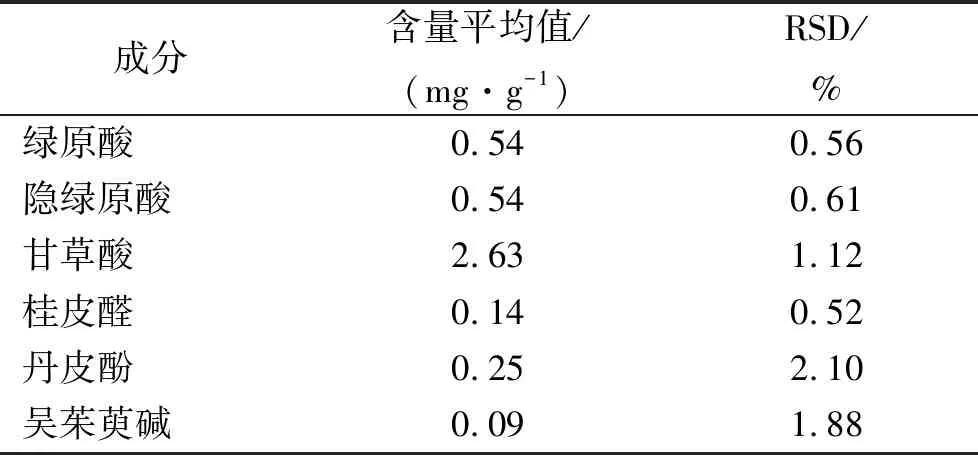
2.10样品含量测定 取温经汤样品溶液平行5份,按“2.4”项色谱条件进行测定,将测得的峰面积分别代入“2.5”项下的回归方程,计算样品中绿原酸、隐绿原酸、甘草酸、桂皮醛、丹皮酚和吴茱萸碱的含量,(其中:甘草酸重量=甘草酸铵重量/1.0207)。见表3。
表3温经汤6种水溶性成分的含量
Tab.3Contentsofsixwater-solubleactiveingredientsfromWenjingdecoctionn=5
成分含量平均值/(mg·g-1)RSD/%绿原酸0.540.56隐绿原酸0.540.61甘草酸2.631.12桂皮醛0.140.52丹皮酚0.252.10吴茱萸碱0.091.88
3 讨论
本研究根据课题组前期建立的温经汤高效液相指纹图谱为参考,采用全波长扫描的方法对样品及对照品在210~400 nm下进行光谱扫描,发现绿原酸、隐绿原酸在327 nm处有最大吸收,甘草酸铵在237 nm处有最大吸收,桂皮醛在290 nm处有最大吸收,丹皮酚在274 nm处有最大吸收,吴茱萸碱在225 nm处有最大吸收,因此分别在各个成分最大吸收波长下进行含量测定。
笔者考察了不同规格的色谱柱对成分分离的影响,分别为Waters XBridge Shield RP18(4.6 mm×250 mm,5 μm)、Waters XBridge BEH Amide(4.6 mm×250 mm,5 μm)和Waters Xselect HSS T3色谱柱(4.6 mm×250 mm,5 μm),结果发现采用Waters Xselect HSS T3色谱柱(4.6 mm×250 mm,5 μm)时峰形对称,分离度符合要求[12];通过考察常用流动相甲醇-水、乙腈-水、甲醇-0.1%磷酸溶液、乙腈-0.1%甲酸溶液等条件[13-14],其中乙腈-0.1%甲酸溶液作为流动相时供试品溶液色谱峰分离度等指标均优于其他,最终确定其为流动相,采用梯度洗脱的方法对供试品进行分析。古代经典名方是中药新药开发重要宝库,挖掘前人宝贵经验,全面开发中药新药,提升质量与疗效的工作刻不容缓。本研究建立了HPLC法同时测定温经汤中6种水溶性成分含量测定的方法,该方法简单易行、准确真实,稳定可靠,为古代经典名方开发及质量标准的建立提供了参考[15-17]。
