敌草快二氯盐制备工艺
2019-03-27岳瑞宽王福军陈洪龙王文魁
岳瑞宽,王福军,陈洪龙,王文魁
(南京红太阳生物化学有限责任公司,江苏南京210047)
敌草快是IMPERIAL CHEMIAL INDUSTRIES LIMITED(ICI,后为先正达)公司于1958 年开发的接触性干燥剂或具有某些内吸性的除草剂,作用机理是通过产生超氧化物破坏植物细胞[1]。敌草快(CAS:2764-72-9)是指阳离子部分,最终是以敌草快二溴盐(CAS:85-00-7)的形式商品化,但其除草活性只与阳离子有关,与阳离子的反荷离子无关[2-4],其生物毒性也与阴离子无关[5]。敌草快与百草枯同为联吡啶类除草剂,它们的除草效果相仿,但中毒机理则有很大不同,百草枯对哺乳类动物的中毒机制主要是在I 型、Ⅱ型肺泡上皮细胞和Clara 细胞膜上存在能够主动摄取百草枯阳离子的多胺摄取系统,百草枯阳离子的分子大小与多胺类分子大小类似,多胺摄取系统将百草枯误认为多胺分子,摄取的百草枯阳离子在肺器官中累积,对其产生严重损伤,最终导致了肺的纤维化[6-10],最后动物体因呼吸衰竭而亡。然而敌草快不存在肺中毒现象,敌草快阳离子不会在肺中累积[11-13],所以,敌草快的毒性远远小于百草枯。
随着2016 年7 月百草枯水剂在国内被禁止销售[14],其空缺出来的市场份额急需相关产品补位。草铵膦是备选替代产品之一,其除草性能较好,正在被各企业重点开发,但草铵膦的工艺路线较长,对工程化要求很高[15]。敌草快是一个更具潜力的百草枯替代品,其除草效果与百草枯相仿,而毒性较低,在作物催枯、种子处理等方面更具优势。成本较高是制约敌草快推广使用的一个重要原因,若能适当降本,从而降低农民的用药成本,敌草快的市场潜力是完全可以释放出来的。降本的关键是开发新工艺路线,思路有二:一是开发吡啶直接偶联制备2,2'-联吡啶工艺路线;二是开发敌草快二氯盐工艺,节约昂贵的溴素。两方面结合可以达到大幅降低敌草快成本之目的。
商品化的敌草快都是以敌草快二溴盐为有效成分的载体化合物,其合成方法是以2,2'-联吡啶与1,2-二溴乙烷经环合得到[16]。
1 敌草快二氯盐的合成工艺简介及不能产业化原因分析
敌草快二溴盐工艺较为简单,用2,2'-联吡啶与二溴乙烷进行环合反应即可制得敌草快二溴盐。但敌草快其他反荷离子盐的制备则较为困难,从原子经济性上来讲,敌草快的二氯盐最为经济,但因二氯乙烷的低活性,用类似于敌草快二溴盐的制备方法制备敌草快二氯盐,需要很高的压力及温度,对设备造成严重腐蚀[17],不能实现工业化生产。ICI 公司的一系列专利文献[18-21]中关于敌草快二氯盐的制备最终都没有工业化。
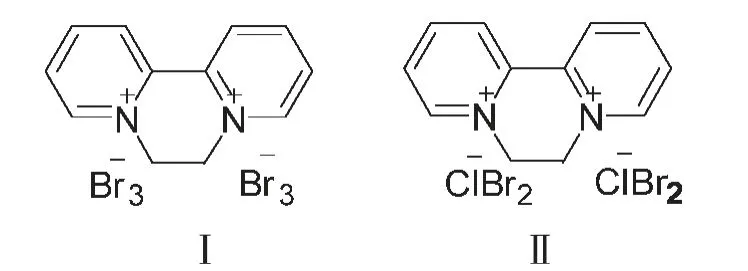
盐中卤素阴离子的交换,常用方法有利用其银盐溶解度的不同实现离子交换,如溴化钠溶液中加入氯化银,充分搅拌反应,可实现氯离子与溴离子的交换。ICI公司当年关于敌草快的专利中对敌草快二氯盐的制备也有对此方法的说明[16]。再者利用氧化还原反应来实现卤离子的交换,溴素的工业化制备即是利用此方法,向卤水或者海水中充分通氯气氧化,将溴离子氧化成单质溴,然后通过浓缩、精馏、分离得到溴素。诚然,敌草快二氯盐也可以参考此方法进行制备,本公司的科研人员也对此工艺进行了考查[22],发现此方法存在较多问题,不适合工业化生产。敌草快二溴盐溶液进行通氯反应时,产生大量的棕色固体,经过分析,该固体是敌草快二溴盐或者敌草快二氯盐的加合物(式Ⅰ,Ⅱ),该加合物在水中溶解度较小,粘度较大,不易过滤。美国大湖化学公司对此加合物的制备和应用进行过研究[23-25],之后就没有后续报道。通过加热蒸馏可以实现单质溴与敌草快盐的分离,但在此过程中,溴在水中生成的次溴酸能将敌草快氧化[26],敌草快的损失较大,且其损失成本远远高于溴的回收成本。
所以,通过上述卤素交换的方法来实现敌草快二氯盐的制备还是不能做到工业化生产,必须寻找到合适的工艺方法,在敌草快二氯盐的生成时,既能实现溴的回收利用,又不能使敌草快有较大的损失。
2 敌草快二氯盐的制备原理
吡啶的鎓盐(溴离子)能继续与溴反应生成三溴化物,该三溴化物可以作为一种很好的溴化剂,此类溴化剂在双键的加成反应,与酚类的取代反应等反应中都表现出很好的反应特性,如常见的吡啶三溴盐(式Ⅲ),同样有文章对DMAP.HBr3(式Ⅳ)[27],1,2-Dipyridiniumditribromide-ethane (DPTBE) (式Ⅴ)[28], 1,10- (ethane-1,2-diyl) phenanthrolinedinium bistribromide (EPDBT) (式Ⅵ)[29]等此类溴化剂做过研究,在其参与的相关反应中,在选择性和产率等方面都能得到较好的结果。

本课题是以敌草快二溴盐为原料,经过氧化、溴化等一系列操作,实现了敌草快二氯盐的高收率,并将溴素转化为更为重要的化工中间体(三溴苯酚),同样实现了溴素的再利用。
敌草快二氯盐制备方法的化学反应式:

3 实验部分
3.1 试剂与仪器
敌草快二溴盐母液(41% ),华洲药业有限公司;双氧水 (29.5% ) ,南京试剂有限公司;盐酸(36% ),南京试剂有限公司;苯酚(99% ),国药集团化学试剂有限公司。
ZK-82B 型电热真空干燥箱,上海实验仪器厂有限公司;SZCL-2A 型数显控温磁力搅拌器,巩义予华仪器有限责任公司;旋转蒸发仪;GC-14C 气相色谱仪,岛津公司;CTO-10AS 高效液相色谱仪,岛津公司。
3.2 合成方法
将150.5 g 敌草快二溴盐水溶液(40.5% ,0.177 mol)与36.3 g 盐酸(36% ,0.358 mol)混合,滴加到30.3 g 双氧水(46% ,0.410 mol)、150.1 g 正丁醇、11.2 g 苯酚(0.119 mol)三者混合液中,维持体系温度于60℃,控制滴加速度,约40 min 滴加完毕,升温至70℃~80℃下保温搅拌,使两相液体充分混合,反应1.5 h,反应结束后分液得水相和反应油相,水相先用100 g 正丁醇萃取,分得萃取水相和萃取油相,萃取水相再加入0.5 g 碳酸氢铵,充分搅拌,调节水相pH 至3.5,浓缩出部分水后配制成108.9 g 含量为40.9% 的敌草快二氯盐母液(阳离子含量为29.5% ),收率为98.5% 。
合并反应油相和萃取油相,浓缩结晶得三溴苯酚粗品,重结晶得38.4 g 三溴苯酚纯品,气谱纯度99.5% ,溴回收率97.7% 。
4 结果与讨论
阳离子的收率主要与双氧水的用量及反应时间相关,苯酚及盐酸的用量不影响阳离子的收率。溴的回收率则与反应时间、反应温度、盐酸用量、苯酚用量、双氧水用量都相关。
4.1 保温时间对阳离子收率及溴回收率的影响
固定敌草快二溴盐150.5 g(40.5% ),正丁醇150.1 g,n(盐酸): n(双氧水): n(苯酚)=3.0: 3.5: 1.0,滴加温度维持在(60±2)℃,滴加时间40 min,保温(75±2)℃,考查保温时间对阳离子收率及溴回收率的影响。结果如表1 所示。

表1 保温时间对阳离子收率及溴回收率的影响
由表1 可以看出,随着反应时间的增加,阳离子收率逐渐降低,双氧水对敌草快阳离子有一定的氧化能力,但随着双氧水逐渐消耗,其对敌草快阳离子的作用也减小了;溴回收率随着时间的增加而增加,时间超过1.5 h后,无明显变化。
4.2 保温温度对阳离子收率及溴回收率的影响
固定敌草快二溴盐150.5 g(40.5% ),正丁醇150.1 g,n(盐酸): n(双氧水): n(苯酚)=3.0: 3.5: 1.0,滴加温度维持在(60±2)℃,滴加时间40 min,保温时间1.5 h,考查反应温度对阳离子收率及溴回收率的影响。结果如表2 所示。

表2 温度对阳离子收率及溴回收率的影响
由表2 可以看出,随着温度的升高,阳离子的损失会逐渐增大。因温度升高,加剧了双氧水对阳离子的氧化反应;溴的回收率开始变化不大,温度超过75℃后,收率开始降低,双氧水随着温度的升高分解率也变大,从而使溴离子的氧化反应变慢。
4.3 苯酚用量对溴回收率的影响
固定敌草快二溴盐150.5 g(40.5% ),正丁醇150.1 g,n(盐酸): n(双氧水)=3.0: 3.5,滴加温度维持在(60±2)℃,滴加时间40 min,保温温度控制在(75±2)℃,保温时间在1.5 h,考查苯酚用量对溴回收率的影响。结果如表3 所示。

表3 苯酚用量对溴回收率的影响
由表3 可以看出,苯酚的量在11 g 左右,溴的回收率最高;小于11 g,溴回收率明显降低;大于11g,则溴回收率变化不大。
4.4 双氧水用量对阳离子收率及溴回收率的影响
固定敌草快二溴盐150.5 g(40.5% ),正丁醇150.1 g,n(盐酸): n(苯酚)=3.0: 1.0,滴加温度(60±2)℃,滴加时间40 min,保温(75±2)℃,保温时间1.5 h,考查双氧水用量对阳离子收率及溴回收率的影响。结果如表4 所示。

表4 双氧水用量对阳离子收率及溴回收率的影响
由表4 可以看出,双氧水的用量增加,阳离子损失会变大,反应液未消耗的双氧水会持续氧化阳离子;溴回收率升高后保持不变;双氧水量少,不能将溴离子完全氧化,双氧水过量后,不影响溴与苯酚的反应,溴的回收率变化不大。
4.5 盐酸用量对溴回收率的影响
固定敌草快二溴盐150.5 g(40.5% ),正丁醇150.1 g,n(双氧水): n(苯酚)=3.5: 1,滴加温度维持在(60±2)℃,滴加时间40 min,保温(75±2)℃,保温时间1.5 h,考查盐酸用量对溴回收率的影响。结果如表5 所示。

表5 盐酸用量对溴回收率的影响
由表5 可以看出,盐酸的用量增加,溴回收率升高后保持不变。盐酸用量不足,其参与的双氧水对溴离子的氧化反应不能进行完全;盐酸过量,则对苯酚的溴化反应没有影响。
5 结论
(1)以双氧水为氧化剂,苯酚为溴素吸收剂,确定了最佳反应条件:n(敌草快二溴盐): n(盐酸): n(H2O2): n(苯酚)=1.5: 3.0: 3.5: 1.0,萃取剂正丁醇的用量与敌草快二溴盐母液相同,滴加温度60℃,保温75℃,保温时间1.5 h。在此条件下,敌草快阳离子损失率≤1.5% ,溴回收率≥97.0% 。
(2)该工艺操作简便,克服了直接合成敌草快二氯盐工艺的缺陷,适合工业化生产。回收的三溴苯酚为重要的阻燃剂原料,用途广泛。
