杀虫剂Oxazosulfyl 合成方法综述
2019-03-27许新华
许新华
(宁波浙铁江宁化工有限公司,浙江宁波315207)
Oxazosulfyl 是日本住友化学株式会社开发的新型杀虫剂,开发代号S-1587,商品名为ALLESTM。该品种是含乙磺酰基吡啶结构的新型苯并噁唑类杀虫剂,主要应用于防控水稻病虫害,是住友化学株式会社研发管道新农化项目B2020 的产品之一。该项目有望2020 年面世,具有接近9 亿美元的市场价值潜力。
1 Oxazosulfyl 的基本性质
Oxazosulfyl 分子式:C15H11F3N2O9S2,相对分子质量:420.38,CAS 号:1616678-32-0,化学名称:2-[3- (乙基磺酰基) -2-吡啶基]-5-[ (三氟甲基) 磺酰基]苯并噁唑,英文名:{2-[3- (ethylsulfonyl) -2-pyridinyl]-5-[ (trifluoromethyl) sulfonyl]benzoxazole}[2,4]。属于苯并噁唑类杀虫剂,分子中含有磺酰基吡啶片段[1,5]。首次的专利申请是日本住友化学株式会社在2013-12-26 日申请的[8],专利号是WO2014104407AI,目前暂没有中国专利。
Oxazosulfyl 化学结构式如图1。
2 工艺路线
文献报道Oxazosulfyl 的合成路线[6-16]主要有以下三种:
路线1:以3-乙硫基吡啶-2-甲酸为原料,直接与2-氨基-4-三氟甲硫基苯酚进行缩合反应,得到酰胺中间体,该中间体在DMEAD 和三苯基膦作用下环合,得到苯并噁唑环,再经过两步氧化,得到目标产物,见图2。

图2 路线1
路线2:以3-乙磺酰基吡啶-2-甲酸为原料,经过氯化亚砜氯化得到其酰氯中间体,然后与中间体2-氨基-4-三氟甲磺酰基苯酚酰化反应获得酰化产物,再在对甲苯磺酸的作用下环合,得到目标产物,见图3。
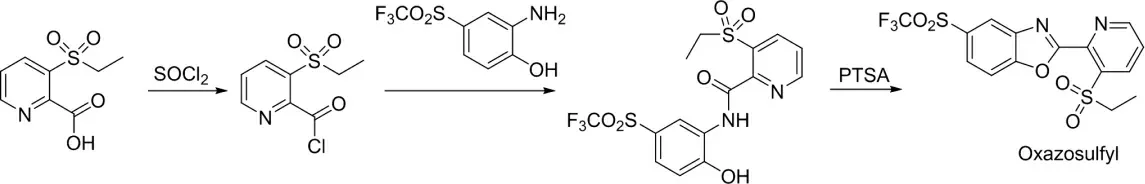
图3 路线2

图4 路线3

图5 中间体2-氨基-4-三氟甲硫基/三氟甲磺酰基苯酚的合成

图6 中间体3-乙硫基/乙磺酰基吡啶-2-甲酸的合成
路线3:以3-氯吡啶-2-甲醛为原料,经乙磺酰基化反应得到3-乙磺酰基吡啶-2-甲醛中间体,再与2-氨基-4-三氟甲磺酰基苯酚中间体直接环合得到目标产物,见图4。
由于路线3 中3-氯吡啶-2-甲醛原料价格贵,不易获得且较难合成,并且环合条件苛刻,污染较严重,因而更倾向于路线1 和路线2,虽然步骤较多,但原料简单易得,整个反应也便于操作,收率较高,其中路线1 和路线2 涉及到的关键中间体的合成路线如图5、图6。
3 合成方法
3.1 中间体2-氨基-4-三氟甲磺酰基苯酚的合成
将4-三氟甲硫基苯酚10.0 g、钨酸钠0.86 g、35% 过氧化氢水溶液4.99 g 混合物升温到70℃搅拌30 min;之后补加35% 过氧化氢水溶液5.0 g,升温到80℃反应1 h;继续补加35% 过氧化氢水溶液2.0 g,在80℃下反应3 h;最后再补加35% 过氧化氢水溶液1.0 g,继续80℃下反应3 h。冷却到室温,加入亚硫酸钠水溶液,析出固体并过滤。固体在减压干燥下得到4-三氟甲磺酰基苯酚10.81 g。
1H-NMR (CDCl3) δ: 7.95-7.91 (2H, m) , 7.08-7.04 (2H,m) ,6.31 (1H,s) .
将4-三氟甲磺酰基苯酚5.0 g 溶于20 mL 醋酸溶液中,升温到50℃,在50℃下缓慢滴加65% 的硝酸1.9 mL,保温反应9 h,再升温到60℃反应2 h。然后在60℃左右缓慢滴加65% 硝酸1.26 mL,保持60℃反应1 h,再升温到70℃反应8 h。冷却到室温,缓慢向体系中加入冰水,析出固体,过滤收集固体。用水淋洗固体,减压干燥,得到2-硝基-4-三氟甲磺酰基苯酚4.98 g。
1H-NMR (CDCl3) δ: 11.22 (1H, s) , 8.85 (1H, d) , 8.18 (1H,dd) ,7.47 (1H,d) .
将2-硝基-4-三氟甲磺酰基苯酚4.5g、5% 的Pd/C 1.37 g、醋酸0.05 mL 溶于45.6 mL 的乙醇溶剂中,在氢气条件下,加热到40℃反应9 h。反应结束,冷却到室温,过滤收集滤液。滤液减压蒸除溶剂后,用甲苯溶剂洗涤固体,固体干燥后得到2-氨基-4-三氟甲磺酰基苯酚3.78 g。
1H-NMR (DMSO-d6) δ:11.11 (1H,brs) ,7.25-7.14 (2H,m) ,6.98-6.93 (1H,m) ,5.38 (2H,brs) .
3.2 中间体3-乙磺酰基吡啶-2-甲酸的合成
将3-氯-2-氰基吡啶1.39 g、乙硫醇0.9 mL 溶于10 mL DMF 溶剂中,用冰水浴冷却,然后缓慢加入60% 的氢化钠0.52 g,恢复到室温搅拌反应1 h。反应结束,加入水猝灭反应,用乙酸乙酯萃取混合物。有机相用饱和碳酸氢钠水溶液、饱和食盐水洗涤,无水硫酸钠干燥。减压浓缩后柱层析得到3-乙硫基-2-氰基吡啶1.52 g。
1H-NMR (CDCl3) δ:8.49 (1H,dd) ,7.75 (1H,dd) ,7.43 (1H,dd) ,3.06 (2H,q) ,1.38 (3H,t) .
将15 mL 浓硫酸和5 mL 水混合,然后加入3-乙硫基-2-氰基吡啶1.4 g,混合物升温到130℃反应2 h。反应结束,冷却到室温,加入KOH 水溶液至碱性,并用乙酸乙酯萃取。向水相中加入浓盐酸,调pH 到酸性,并用氯仿溶剂萃取,收集有机相,用无水硫酸钠干燥,减压浓缩后得到3-乙硫基吡啶-2-甲酸1.15 g。
1H-NMR (CDCl3) δ:8.31 (1H,d) , 7.75 (1H, dd) , 7.49 (1H,dd) ,2.97 (2H,q) ,1.44 (3H,t) .
将3-乙硫基吡啶-2-甲酸1.0 g 溶于30 mL 氯仿溶剂中,冰水浴冷却,然后缓慢加入m-CPBA(含量65% 以上)2.7 g,恢复室温搅拌反应6 h,然后加入10% 的亚硫酸钠水溶液猝灭反应,混合物用氯仿萃取。有机相用饱和碳酸氢钠溶液洗涤,无水硫酸镁干燥,减压浓缩后柱层析得到3-乙磺酰基吡啶-2-甲酸0.88 g。
1H-NMR (CDCl3) δ:8.31 (1H,d) , 7.75 (1H, dd) , 7.49 (1H,dd) ,2.97 (2H,q) ,1.44 (3H,t) .
3.3 路线1 的合成方法
将3-乙硫基吡啶-2-甲酸0.87 g、2-氨基-4-三氟甲硫基苯酚1.0 g、EDCI(碳二亚胺盐酸盐)1.10 g 溶于10 mL 氯仿溶剂中,混合均匀,在常温下搅拌30 min,然后向反应体系中加入水,用乙酸乙酯萃取。有机相用饱和碳酸氢钠、饱和食盐水洗涤,无水硫酸镁干燥,减压浓缩后柱层析得到3-乙硫基-N- (2-羟基-5-三氟甲硫基苯基) -2-吡啶酰胺1.32 g。
1H-NMR (CDCl3) δ: 10.40 (1H, brs) , 9.63 (1H, s) ,8.36 (1H,dd) ,7.75 (1H,dd) ,7.53 (1H,d) ,7.45 (1H,dd) ,7.41 (1H,dd) ,7.08 (1H,d) ,2.97 (2H,q) ,1.44 (3H,t) .
将3-乙硫基-N- (2-羟基-5-三氟甲硫基苯基) -2- 吡啶酰胺1.23 g、DMEAD(2- 甲氧基偶氮二羧酸酯)1.28 g、三苯基膦1.39 g 溶于30 mL THF 溶剂中,在常温下搅拌反应1 h,再升温到50℃反应1 h。冷却到室温后,减压浓缩出溶剂后,加入水,并用乙酸乙酯萃取。有机相用饱和碳酸氢钠、盐水洗涤,无水硫酸镁干燥。减压浓缩后柱层析得到2- [3-乙硫基-2-吡啶基]-5-三氟甲硫基苯并噁唑1.21 g。
1H-NMR (CDCl3) δ: 8.59 (1H, dd) , 8.27 (1H, s) , 7.78 (1H, dd) , 7.75-7.69 (2H, m) , 7.42 (1H, dd) , 3.07 (2H, q) ,1.47 (3H,t) .
将2- [3-乙硫基-2-吡啶基]-5-三氟甲硫基苯并噁唑1.06 g 溶于30 mL 氯仿溶剂中,冰水浴冷却,然后缓慢加入m-CPBA(含量65% 以上)1.47 g,然后恢复室温搅拌反应6 h,再加入10% 的亚硫酸钠水溶液猝灭反应,混合物用氯仿萃取。有机相用饱和碳酸氢钠溶液洗涤,无水硫酸镁干燥,减压浓缩后柱层析得到2-[3- (乙基磺酰基) -2-吡啶基]-5-三氟甲硫基苯并噁唑0.87 g。
1H-NMR (CDCl3) δ: 9.03 (1H, dd) , 8.60 (1H, dd) ,8.19 (1H,dd) ,7.80-7.71 (3H,m) ,4.02 (2H,q) ,1.43 (3H,t) .
2-[3- (乙基磺酰基) -2-吡啶基]-5-三氟甲硫基苯并噁唑0.35 g 溶于8 mL 氯仿溶剂中,冰水浴冷却,缓慢加入m-CPBA(含量65% 以上)0.43 g,然后升温到40℃搅拌反应6 h,加入10% 的亚硫酸钠水溶液猝灭反应,混合物用氯仿萃取。有机相用饱和碳酸氢钠溶液洗涤,无水硫酸镁干燥,减压浓缩除去溶剂。向残余物中加入4 mL 乙腈、30 mg 钨酸钠、30% 的过氧化氢溶液4 mL,混合物升温到80℃反应6 h。冷却到室温后,向体系中加入水,析出沉淀,过滤收集固体。固体用10% 亚硫酸钠溶液溶解,并用乙酸乙酯萃取,有机相用饱和碳酸氢钠溶液和盐水洗涤,无水硫酸镁干燥。减压浓缩后柱层析得到2-[3- (乙基磺酰基) -2-吡啶基]-5-[ (三氟甲基) 磺酰基]苯并噁唑0.35 g。
1H-NMR (CDCl3) δ: 9.05 (1H, dd) , 8.61 (1H, dd) ,8.59 (1H, dd) , 8.17 (1H, dd) , 7.96 (1H, d) , 7.80 (1H, dd) ,3.98 (2H,q) ,1.45 (3H,t) .
3.4 路线2 的合成方法
将3-乙磺酰基吡啶-2-甲酸1.0 g、甲苯12 mL、DMF 0.1 mL 混合后升温到60℃,缓慢逐滴滴加氯化亚砜0.8 mL,然后在60℃下反应4 h,然后冷却到室温,减压浓缩后加入5 mL THF 溶解,然后将2-氨基-4-三氟甲磺酰基苯酚0.6 g 溶解在5 mL THF 溶剂中。将后者溶液缓慢滴加到前者溶液中,保持温度在20℃~25℃之间。滴加结束,常温下搅拌2 h,然后减压除去溶剂,抽滤得到固体,干燥后得到3-乙磺酰基-N- (2-羟基-5-三氟甲磺酰基苯基) -2-吡啶酰胺1.09 g。
1H-NMR (DMSO-d6) δ: 12.35 (1H, brs) , 10.44 (1H,s) ,8.96 (1H,dd) ,8.85 (1H,d) ,8.44 (1H,dd) ,7.87 (1H,dd) ,7.81 (1H,dd) ,7.31 (1H,d) ,3.68 (2H,q) ,1.19 (3H,t) .
将3-乙磺酰基-N- (2-羟基-5-三氟甲磺酰基苯基) -2-吡啶酰胺0.6 g、一水的对甲苯磺酸0.52 g、氯苯溶剂7.23 g 混合后升温回流17 h,反应结束冷却到室温,加水猝灭,用40 mL 乙酸乙酯萃取。有机相用水洗2次,再用饱和碳酸氢钠和盐水洗涤,无水硫酸镁干燥。减压浓缩后柱层析得到2- [3- (乙基磺酰基) -2-吡啶基]-5-[ (三氟甲基) 磺酰基]苯并噁唑0.35 g。
4 小结
本文总结了杀虫剂Oxazosulfyl 经文献报道的主要合成路线,其中路线3 因为原料价格贵,不易得,环合步骤污染较大,不适宜工业化生产。路线1 和路线2 虽然合成步骤偏多,但因原料简单易得,合成上操作相对简单,收率较高,是比较合适的工业化路线。
