前循环症状性颅内动脉狭窄患者支架成形术联合药物治疗的有效性与安全性
2019-03-25陈渊钟维章李吕力陈娟带韦俊杰李燕华范秉林何国永
陈渊,钟维章,李吕力,陈娟带,韦俊杰,李燕华,范秉林,何国永
症状性颅内外动脉粥样硬化性狭窄是导致缺血性脑卒中的重要原因之一,中国国家脑卒中中心统计的数据显示大动脉粥样硬化约占所有缺血性卒中的45%[1]。目前,颅外段动脉狭窄通过颈动脉剥脱术或支架治疗已形成共识[2],对于症状性颅内动脉狭窄的治疗,根据SAMMPRIS研究及其长期随访结果[3-4],在美国主流医学界仍建议首选药物治疗。然而颅内动脉支架技术在近年发展较快,同时国内不少学者进行了相应的研究[5],新近的研究提示支架植入术可能优于药物治疗[6]。结合SAMMPRIS及相关研究,为进一步评估前循环系统颅内动脉支架成形术的优劣,本研究对广西脑卒中中心统计的前循环症状性颅内动脉狭窄患者的治疗疗效进行回顾性分析,报道如下。
1 资料与方法
1.1 临床资料 选取2012年4月—2016年4月广西壮族自治区人民医院神经内科/广西脑卒中中心统计的前循环症状性颅内动脉狭窄患者108例作为研究对象,患者有不同程度的神经功能缺损症状,如肢体无力、肢体麻木、头晕等,且均行全脑血管造影术(DSA)明确诊断。根据治疗方法分为支架成形术联合药物治疗组(观察组)51例,单纯药物治疗组(对照组)57例。
1.2 选择标准 (1)纳入标准: ①造影证实前循环血管狭窄(70%~99%);②近3个月内首次发生的缺血性卒中事件(为便于评估,TIA患者不纳入),狭窄血管为缺血事件责任血管;③患者年龄>18岁,且<80岁。(2)排除标准: ①脑梗死导致的严重神经功能障碍;②非动脉粥样硬化性血管狭窄者;③合并心源性卒中的患者;④对肝素、阿司匹林或其他抗血小板聚集类药物禁忌者;⑤对造影剂过敏者;⑥伴有颅内动脉瘤,且不能提前或同时处理者。
1.3 治疗方法 所有患者术前先完善头颅CT或头颅MR、DSA等检查。观察组:术前5 d开始口服阿司匹林(100 mg/d)及氯吡格雷(75 mg/d),阿托伐他汀钙片(20 mg/d)。手术时机确定为卒中发生2周后。手术采用局部浸润麻醉,在C型臂X线机下将指引导管通过股动脉进入动脉系统,到位后根据患者血管情况选择植入Apollo支架或Wingspan支架,再次造影显示支架到位且血管狭窄改善后结束操作。术后1个月改为氯吡格雷(75 mg/d)、阿托伐他汀钙片(20 mg/d),9个月后改阿司匹林(100 mg/d)长期服用。根据危险因素药物调整患者的血压、血糖、血脂等指标。对照组:急性期口服阿司匹林(100 mg/d)及氯吡格雷(75 mg/d),阿托伐他汀钙片(20 mg/d),1个月后改为氯吡格雷(75 mg/d)、阿托伐他汀钙片(20 mg/d),9个月后改阿司匹林(100 mg/d)长期服用。根据危险因素药物调整患者的血压、血糖等指标。若2组患者颈部血管超声等检查提示有不稳定斑块,则予以阿托伐他汀钙片(40 mg/d)治疗。
1.4 疗效观察 所有患者由神经内科医师通过门诊、电话或住院复查等方式进行随访,记录2组患者入组后到12月内任何形式的卒中发作以及死亡事件,采用NIHSS评分、改良 Rankin量表(mRS)评分[7]评估患者术前、治疗后1、6、12个月的神经缺损功能及生活质量。NIHSS评分是临床上衡量神经功能缺损情况的量表评分,分值范围在1~42,分值越高提示神经功能缺损越严重;改良 Rankin评分常用于评估脑卒中患者在日常活动中的残疾程度,分值范围在0~6,分值越高说明残疾程度越严重。

2 结 果
2.1 基本情况比较 2组患者性别、年龄、患高血压、糖尿病、高脂血症、高同型半胱氨酸血症等基本资料比较,差异均无统计学意义,具有可比性(P>0.05),见表1。
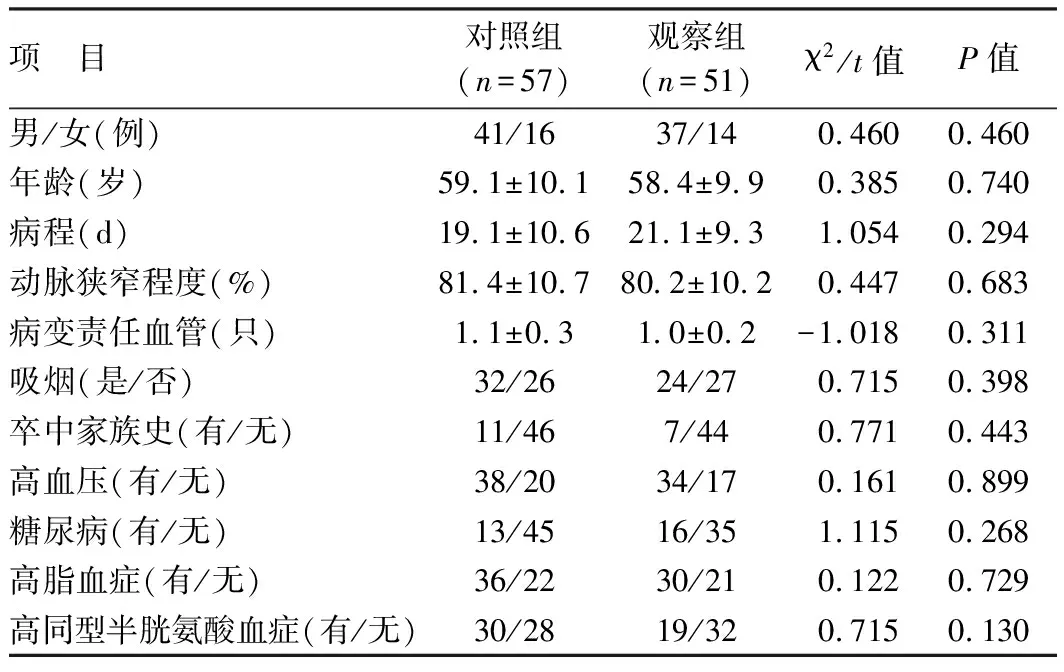
表1 2组患者基线资料比较
2.2 NIHSS评分比较 2组患者NIHSS评分手术前及术后1个月比较差异无统计学意义(P>0.05),术后6、12个月观察组患者低于治疗前,且观察组低于对照组,差异有统计学意义(P<0.01),见表2。
2.3 改良Rankin评分 2组患者手术前、术后1、6个月时改良Rankin评分比较差异无统计学意义(P>0.05),术后12个月观察组患者低于对照组,差异有统计学意义(t=-2.091,P=0.039),见表3。
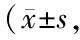
表2 2组患者治疗前后NIHSS评分比较分)
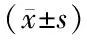
表3 2组患者治疗前后改良Rankin评分比较
2.4 终点事件发生率比较 术后6、12月终点事件发生率观察组患者为4例(7.84%)、6例(11.76%),低于对照组的6例(10.53%)和8例(14.04%),但差异无统计学意义(χ2/P=0.231/0.746,0.455/0.565)。
2.5 生存分析比较 2组患者进行Kaplan-Meier生存分析,治疗12个月、18个月、24个月后生存率观察组高于对照组,但Log-lank假设检验表明,2组患者生存率比较差异无统计学意义(χ2=1.167,P=0.280),见图1。

图1 2组患者生存率比较
3 讨 论
本研究纳入前循环系统症状性颅内动脉狭窄患者,药物治疗原则遵循国内最新指南[8],而在观察组的患者选择、术者经验、术前处理等均有相应的设计,与部分国内外的部分研究有一定的差别。
本研究只纳入前循环症状性颅内动脉狭窄患者,未将后循环患者囊括在内,目的在于减少研究误差;神经功能缺损相对缓和的前循环脑卒中患者,其症状通常较单一,往往临床表现较轻,基本不影响患者呼吸、吞咽功能等,一方面便于对此类患者进行神经功能评分,且更利于观察疾病的复发(支架植入后部分医院拒绝行MR检查,而对头晕等不典型症状的发生,CT上未观察到梗死灶时难以判断是否卒中复发),使随访更简便准确,研究数据更为可靠。其次,本研究中手术者具有丰富的手术经验,累积手术量均大于50例,有学者回顾相关国外研究时认为,手术经验很可能是影响血管内治疗预后的一个重要因素[9]。第三,早在2008年即有研究提示缺血事件发生2周之内行血管内治疗,与梗死2周后再进行治疗的患者比较,30 天内卒中或死亡风险显著升高[10],对颈动脉狭窄患者,目前认为患者延迟至脑梗死急性期之后再行血管内治疗并不会对神经功能恢复产生负面影响[11-12]。鉴于此,本研究纳入手术患者均未处于缺血性卒中急性期,所有血管内治疗的患者从发病到接受治疗时间均超过2周,避免了卒中急性期血流动力学以及血管斑块的不稳定等因素可能造成的不良影响。最后,全部患者均按照当时国内最新指南的药物进行治疗。对于颈部血管超声或头颅MRA提示有不稳定斑块者,则予以强化阿托伐他汀钙片(40 mg/d)治疗[13-14],以尽量避免术中出现斑块脱落等情况。
本研究使用NIHSS评分及mRS评分对患者神经功能进行评估。NIHSS评分通常被用于评估缺血性卒中患者的神经功能缺损[15],而mRS评分则常被用于评估卒中的预后[16]。本研究结果提示,从远期来看,前循环症状性颅内动脉狭窄患者行支架成形术甚至更有利于神经功能的恢复。根据2014年发布的SAMMPRIS[3]研究结果显示, 30 d内支架组不良终点事件发生率明显高于药物观察组(14.7% vs. 5.8%),因此试验被提前终止。虽然试验被提前终止,但是SAMMPRIS随访研究[4]仍继续进行,研究结果显示在平均随访32.4个月期间,227例药物观察组患者中有52例(22.91%),224例支架组患者中有34例(15.18%)达到主要终点事件(脑卒中或死亡),但如果除去早期(术后30 d)发生的终点事件,两者的差异无统计学意义。本研究将卒中再发及死亡作为终点事件,尽管数据上观察组患者术后6个月、12个月终点事件发生率低于对照组,而且观察组生存率在12个月后高于对照组,但上述数据的差异并无统计学意义,因此认为在本研究中,对于前循环症状性颅内动脉狭窄患者,支架成形术与单纯药物治疗在卒中复发、长期生存方面无明显差异。
当前学界关于症状性颅内动脉狭窄是否应进行血管内治疗仍无定论,而本研究从病例选择、术者选择、术前处理等方面进行了一定的设计,研究结果则提示,相比于单纯药物治疗,前循环系统的症状性颅内动脉狭窄更倾向于实施支架成形术。但本研究也存在不少有待改进之处。包括本试验为单中心研究,缺乏多中心数据的说服力;药物治疗时未进行血栓弹力图的试验,小部分患者未能针对性地进行抗血小板药物治疗;在随访过程中未能对所有患者复查DSA或相关血管检查,缺乏狭窄血管术后的影像学动态对比等。而症状性颅内动脉狭窄的治疗恰恰需要多中心、大样本、更优药物/支架选择、更具体随访的研究及相关结果,给临床工作提供更全面的帮助,有待下一步深入开展研究。
利益冲突:无
作者贡献声明
陈渊、钟维章:设计研究方案,实施研究过程,分析试验数据;李吕力:论文审核;陈娟带:提出研究思路;李燕华、范秉林:实施研究过程,资料搜集整理;韦俊杰、何国永:论文撰写,进行统计学分析
