硬脑膜修复材料的临床使用评价和质控标准建立的研究
2019-03-15吴敏黄亚萍黄丹李婷婷汪长岭
吴敏,黄亚萍,黄丹,李婷婷,汪长岭
1. 东部战区总医院 a. 医学工程科;b. 神经外科,江苏 南京 210002;2. 南通市第一人民医院 设备处,江苏 南通 226001
引言
伴随生物医学材料的应用取得极大成功,医用耗材的使用在现代医院诊疗中发挥的作用不可或缺,占医疗器械市场份额已超40%。临床医学工程技术人员通过对医用耗材流通各个环节的深入分析研究,实现对医用耗材的透明管理、溯源管理、全过程管理,确保临床诊疗工作和应急救援的器材供应[1]。重视医用耗材采购后的跟踪管理和质量控制,包括采购人员和库管人员定期到临床科室的巡访,临床和管理科室对植入性材料(如心脏起搏器、人工脑膜材料)的追踪回访,以及发生医用耗材不良事件后的报告等。本文以神经外科常用医用耗材——硬脑膜修复材料为例,探讨临床工程技术人员的工作进展。
1 充分了解硬脑膜修复材料使用适应症
硬脑膜是脑组织表面一层重要的组织结构,是保护脑组织的一道重要屏障[2]。硬脑膜缺损是神经外科临床上经常面临的问题,开放性颅脑损伤、炎症、脑肿胀、肿瘤侵犯脑膜、过分电灼脑膜等因素均可能导致术中硬膜无法关闭,形成缺损。在神经外科中,硬脑膜的完整性对于颅脑手术患者十分重要[3]。在神经外科手术中,修补缺损的硬脑膜对于维持解剖学的完整和保护脑组织,防止脑脊液漏、颅内感染、脑膨出、癫痫等并发症是十分必要的。
目前,在国内主要是应用自体膜及人工硬脑膜材料来修补缺损的硬脑膜[4]。在硬膜缺损修补方面,过去多采用自身组织修复,如颞肌筋膜、颅骨骨膜、帽状腱膜等,因为这些材料组织相容性好,不会产生免疫反应,而且现取现用,不需要消毒,不会传染疾病,因此目前仍还应用。但是自体膜取材来源局限,给患者新增创伤,增加痛苦。对于小的缺损,可以采用自体组织如肌筋膜等进行修复,而对于大面积硬膜缺损的修补较为困难,往往需要采用人工硬膜替代材料。
2 在用人工硬脑膜修复材料临床使用评价
目前在临床上主要应用的硬脑膜替代材料有:① 患者自身的筋膜、骨膜等组织;② 同种异型组织;③ 异种生物材料;④ 人工合成材料等[5]。课题组对在用的多种硬脑膜修复材料的成分、化学固定、消毒方式、抗拉强度、降解、组织相容性、免疫原性、缝合方式、特点等多参数进行对比研究[6],建立动态使用评价体系。此批参与评价的有如下几种。
2.1 生物型(异种)-动物源性
因文章篇幅问题,仅将材料资质列出,具体评价课题组按比较模板逐一实验并评价,详见相关文章。
(1)海奥生物膜。2009年上市,国食药监械(准)字2013第3461708号,牛的皮肤组织经一系列处理后制备的异种(牛)脱细胞真皮基质,主要成分为胶原蛋白,保留了胶原蛋白特有的三维空间结构。化学固定方式为未交联固定,γ射线辐照灭菌(灭菌彻底),抗拉强度好,可完全降解(6个月),组织相容性较好,有利于新生脑膜组织有序修复,免疫原性弱,缝合使用。特点:纯天然三维空间结构、引导脑膜组织再生重建修复、降解时间合适、使新生脑膜组织有序再生修复。
(2)冠昊生物型硬脑(脊)膜补片。商品名冠昊脑膜建,异种(猪)脱细胞膜材(猪源心包膜)制成,2004年12月上市,广东冠昊生物科技股份有限公司,国食药监械准(字)2014第3460539号。
(3)冠昊B型硬脑(脊)膜补片。商品名冠朗,是将牛的膜材组织(为心包膜)经环氧交联固定处理和生化技术改造后制成的硬脑(脊)膜外科修补材料,基本成分是胶原蛋白,国食药监械(准)字2013第3460949号。
(4)佰仁脑膜补片。商品名佰仁思,牛心包经化学改性处理制成,2007年4月上市,国食药监械(准)字2013第3461592号。
(5)Cook Biotech Incorporated生物硬脑膜修补片。商品名BiodesignSurgisis,猪的小肠黏膜下层组织(被命名为SIS材料)制成,为可吸收得细胞外基质,无孔型多层结构。2010年6月上市,国食药监械(进)字2010第3461684号。
(6)美国Integra生物硬脑膜修补片。商品名来之瑞(DuraGen),牛跟腱I型胶原,2007年2月上市,国食药监械(进)字2015第3462914号。
(7)北京天新福生物膜。商品名天义福(DuraMax),牛肌腱I型胶原制成,2003年1月上市,国食药监械(准)字2013第3460505号。
(8)天新福生物膜。天义福的替代品,硬膜修复材料,商品名愈强,牛跟腱提取的胶原制成,是具有三维孔隙结构的材料,2015年4月上市,国械注准2015第3460562号。
2.2 生物型-植物源性
迈普可吸收硬脑(脊)膜补片,商品名睿膜,是聚乳酸为原材料通过静电纺丝技术制成的膜片,可降解的生物材料,结合生物3D打印加工工艺,具有高度模拟人体微观结构特点,可直接贴合在患者的脑膜破损处,实现伤口缝合的效果。特点是以合成高分子可吸收材料构成仿生ECM结构,利于细胞在网状结构中爬行、生长,促进缺损脑膜的修复、再生。2014年4月上市,国食药监械(准)字2014第3460521号。
2.3 高分子材料
(1)日本グンゼ株式会社可吸收性硬脑膜修补材料。商品名赛膜SEAMDURA,2013年7月上市,国食药监械(进)字2013第3462695号(更),由可吸收性高分子合成材料聚乙醇酸(PGA)、L-乳酸和ε-己内酯的共聚物经加工制成,为三层的三明治式复合结构,中间为聚乙醇酸无纺布层,其两侧面为L-乳酸和ε-己内酯的共聚物膜,环氧乙烷消毒(微量残留毒气可能)。特点:① 具有良好的生物相容性;② 半透明可以观察正下面有无出血情况;③ 可吸收;④ 粘连和包裹可能;⑤ 脑脊液渗漏可能;⑥与脑表面的适应性稍差。
(2)比利时Ethisorb Dura Patch硬膜修补片。商品名Ethisorb,由乙交酯丙交酯共聚物和聚二氧环己酮PDS制成的未染色羊毛状织物,以及2号紫色PDS涂膜组成。国食药监械(进)字2013第3461291号。
(3)美国戈尔硬脑膜修补材料。商品名PRECLUDE,采用膨体聚四氟乙烯材料(ePTFE)构成。2010年1月上市,国食药监械(进)字2012第3462004号。
(4)德国蛇牌神经补片。商品名蛇牌Neuro-Patch,由聚氨基甲酸乙酯制成,为多微孔、绒状非编织材料。2006年3月上市,国食药监械(进)字2013第3464036号。
(5)膨体聚四氟乙烯外科隔离膜。商品名Membthes,由聚四氟乙烯分散树脂加工而成的膨体聚四氟乙烯膜,分人造硬脑膜与人造硬脊膜两种型号。2013年10月上市,国食药监械(准)字2013第3461580号。
(6)深圳市沃尔德硬脑膜修复补片,商品名生物桥,由聚四氟乙烯树脂经拉伸等特殊加工方法制成, 具有微细纤维连接而形成的网状结构。2015年6月上市,国械注准2015第3461058号。
另术中偶用自体材料(同种)自体组织取材修补,如自体筋膜组织;或异体材料(同种),源于人类尸体或活体,异体筋膜组织制成。特点有降解缓慢,需缝合,安全、无排异反应,但取材尺寸受限、手术繁杂、延长手术时间、增加出血量、增加创伤等,易引起脑组织粘连、诱发癫痫[4]。
目前工作小结,见图1。因本文讨论相关耗材临床使用和质控标准评价内容和依据,仍处院内小样本实验对比阶段,避免对产品定性,故表中对具体品牌型号暂时隐去。上述耗材在临床使用原则为[7-8]:① 应用优缺点互补,结合具体情况,选择适当使用;② 产品是否能长久性市场生存是多种因素互相作用的结果;③ 产品优缺点经过临床应用检验,有时亦需术者按指引正确应用。
3 生物膜检测质控标准研究
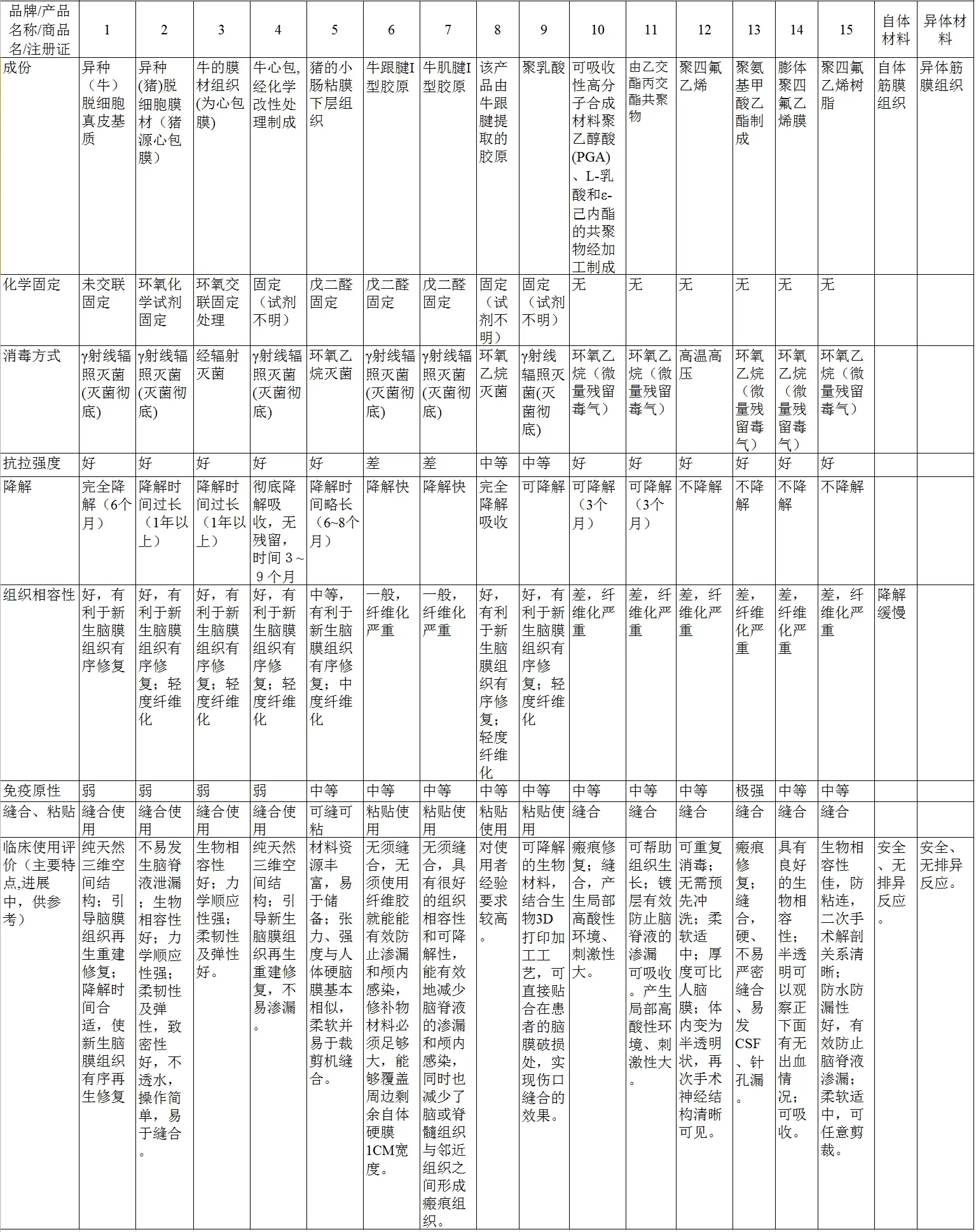
图1 在用人工硬脑膜修复材料临床使用评价情况表
对医用耗材的质控标准的研究也是临床工程师的工作重点,依据现行的国家和行业法规及标准,即《中华人民共和国药典》2015版、GB/T 1040.3-2006、GB/T 16886.12-2017、YY 0954-2015、YY/T 1453-2016、YY/T 1511-2017、QB 2732-2005等[9-15],硬脑膜修复材料主要检测参数有外观、规格型号、抗拉强度、热变性温度、缝合线撕裂力、pH值、重金属、炽灼残渣、含水量、蛋白总量、羟脯氨酸含量、无菌检查、内毒素检查[16-19]。上述指标也是常规植入性生物医用材料的质控标准,具有一定的通用性。以海奥生物膜为例,项目设置、检测方法和性能指标依据及参数,见表 1~3。

表1 在用人工硬脑膜修复材料物理项目检测表

表2 在用人工硬脑膜修复材料化学项目检测表
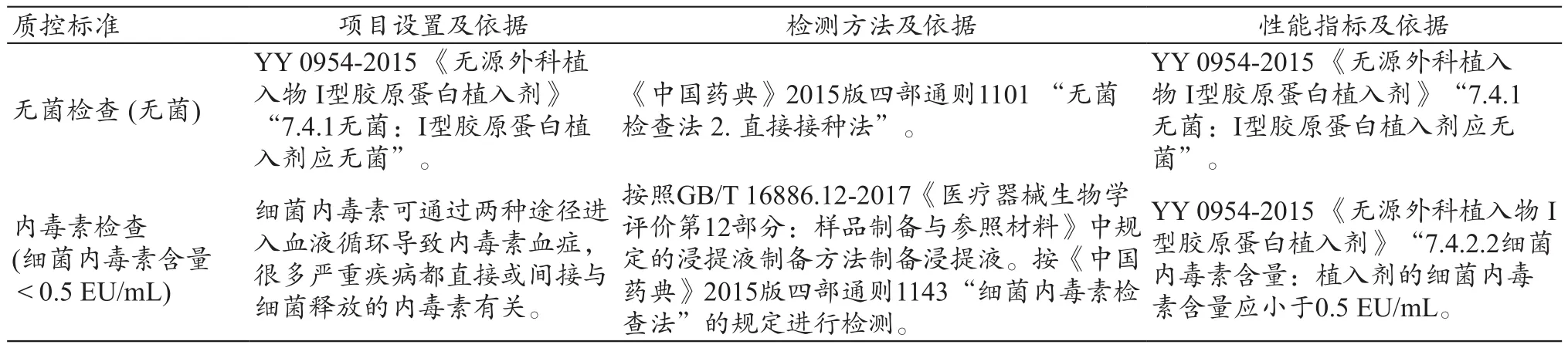
表3 在用人工硬脑膜修复材料生物学项目检测表
3.1 物理项目
硬脑膜修复材料质控的物理项目主要有5项,分别是外观、规格型号、抗拉强度、缝合线撕裂力、热变性温度的设定,结合产品物理性能指标和各级标准[16],达标才能够保证产品的有效性,通过动物实验、临床试验验证,各项指标符合规定,植入缺损部位,移植成活率高,临床修复效果好。
3.2 化学项目
硬脑膜修复材料质控的化学项目主要有6项,其中pH值、重金属、炽灼残渣是植入类耗材共性的技术参数,是对产品的安全性指标的控制[17]。含水量、蛋白总量、羟脯氨酸含量是规定产品主要成分含量,是对产品有效性指标进行控制[18]。
3.3 生物学项目
硬脑膜修复材料质控的生物学项目主要为无菌性和内毒素含量检测,其达标与否直接对应产品的安全性是否合格[19]。
4 讨论
在医院临床医学工程技术人员完成医用耗材的计划、论证、引进、采购、发放、流通、使用的管理和质量控制。大部分医院仅注重或能做到采购和发放,常规进行的入库验收只是一个初步的程序[20],主要着眼于外观和资格文件的验收,基本未涉及产品内在质量及其使用情况和长期效果,因此,入库后的跟踪管理显得非常重要。课题组基于医疗器械国家标准、行业标准、地方标准、企业标准的各级法规标准的学习融汇,通过对临床具体使用的深入了解和检测,可针对性的解决医用耗材功能、免疫性、服役寿命等不能很好地满足临床应用要求的问题,也是医院临床工程技术人员的重要研究和工作方向。
