基于磁锚定技术的磁性水凝胶辅助内镜黏膜下剥离术
2019-03-15刘豪赵广宾张勇韩珍珍史爱华吕毅1a严小鹏1a
刘豪,赵广宾,张勇,韩珍珍,史爱华,吕毅1a,,严小鹏1a,
1. 西安交通大学第一附属医院 a. 肝胆外科;b. 精准外科与再生医学国家地方联合工程研究中心;c. 胸外科,陕西 西安 710061;2. 西安交通大学 a. 启德书院;b. 机械制造系统工程国家重点实验室,陕西 西安 710061
引言
我国是消化道疾病高发国家,其中消化道肿瘤在消化道疾病中占比大,是重要的医疗负担。早年因消化道内镜技术检查率低,大部分食管癌、胃癌、结直肠癌发现时已到中晚期,外科手术成为消化道肿瘤的主要治疗手段。目前,内镜技术普及率明显升高,内镜检查率也大大提高,因此更多的消化道早癌实现了早发现、早诊断、早治疗的目标。内镜黏膜下剥离术(Endoscopic Submucosal Dissection,ESD)以确切的疗效和微创化治疗使其成了消化道早癌及癌前病变的首选治疗方案[1]。
黏膜创面的暴露是影响ESD术中操作的关键因素。常规做法是标记病灶后于标记点外侧多点行黏膜下注射药物,以达到抬高病灶,利于切除的目的。目前常用的黏膜下注射药物有肾上腺素生理盐水混合液[2]、甘油果糖[3]、水凝胶[4]、玻璃酸钠[5]以及多种液体的混合液[6-7]等。通过药物注射抬高病灶的方法简单易行,但当病灶面积较大时,此法对黏膜创面的暴露效果有限。为此,有研究者提出了通过悬吊牵引增加黏膜创面的显露的方法[8],也有将特殊设计的机器人增强内镜外科系统MASTER[9]用于切除过程中帮助暴露黏膜创面。
磁锚定技术(Magnetic Anchor Technique,MAT)是磁外科(Magnetic Surgery,MS)的临床核心技术之一,它利用磁体与磁体、或磁体与顺磁性物质之间的磁场吸引力,使锚定磁体(Anchor Magnet,AM)对靶磁体(Target Magnet,TM)进行非接触性空间锚定的技术,磁锚定系统中的主动施力部分为AM,被动受力部分为TM[10]。MAT通过在病变黏膜边缘的钳夹结构上附着微小靶磁体,然后通过体外的AM对体内的TM进行锚定牵拉,从而更好地显露黏膜创面。MAT辅助ESD术具有定位精准、黏膜锚定方向可灵活掌控、锚定力可控等诸多优势,在ESD术中应用前景良好[11-12]。该方法目前尚不能广泛用于食管病变切除,原因在于腔内TM锚定需要一定的空间,而食管管腔较小,不能为TM提供足够牵拉锚定的空间。为此,本团队首次提出了基于MAT的磁性水凝胶辅助ESD术,现介绍如下。
1 工作原理
ESD术操作的关键是要充分暴露黏膜剥离面,基于MAT的胃黏膜剥离面暴露技术已经成熟,AM能够与TM之间建立锚定力,并可灵活掌控锚定方向,大大方便了ESD术,目前MAT辅助ESD术适用于胃黏膜切除,针对空间较小的食管,我们提出了利用磁性水凝胶黏膜注射法来替代TM的思路,通过磁性水凝胶给病变黏膜内赋磁性,这样体外的AM可直接与病变黏膜产生磁性吸引力,从而实现基于MAT的ESD术黏膜创面充分显露的目的。
2 设计方法
2.1 磁性水凝胶的制备
参照翟羽等[13]介绍的化学共沉淀法合成纳米铁氧体粒子,反应方程式为:Fe2++2Fe3++8OH-=Fe3O4+4H2O,具体过程为以2:1.2的摩尔比将FeCl3×6H2O和FeSO4×7H2O溶于100 mL去离子水中,200 r/min搅拌,缓慢滴加30 mL 12.5%的氨水,持续搅拌30 min,去离子水洗涤至中性,即可获得纳米铁氧体粒子。向纳米铁氧体粒子中加入适量50%葡聚糖水溶液,超声振荡10 min,70℃水浴,300 r/min搅拌30 min,盐酸滴定使pH=6,即可得到葡聚糖磁流体。
将磁流体、质量浓度为1%~3%的海藻酸钠人溶液、质量浓度为1%~3%的氯化钙溶液按照(1~3)g:(3~6)mL:(1~3)mL比例快速混匀注射至病变部位,数秒后即可成凝胶状。
2.2 AM
AM有两种解决方案。方案一:采用高性能永磁材料。AM为圆柱状,直径8 cm,高度14 cm,边缘倒角,采用N48烧结型钕铁硼永磁材料精加工而成,表面镍铜镍镀层,轴向饱和充磁。方案二:采用电磁装置。其优点是AM的磁力可控性好,与永磁体相比缺点是使用时需要外接电源和电流调控装置。
3 动物实验
3.1 实验方法
基于MAT的磁性水凝胶辅助ESD术操作过程如下(图1):① 以食管ESD术为例,术前行内镜检查明确病变位置、病变性质、病变范围、超声内镜确定黏膜病变深度,做好术前准备,经口下胃镜至病变组织处,再次明确病变范围,并用氩气刀标记病变黏膜切除范围;② 利用胃镜活检孔将适量磁性水凝胶注射到待切除的病变黏膜内;③ 在病变黏膜食管对侧体外放置AM,可见在AM的磁力吸引下含有磁性水凝胶的病变组织被吸起,并能维持一定的组织张力;④ 内镜下,IT刀沿预先设定的黏膜切除范围边缘开始逐步切除病变组织,在病变切除过程中,可通过改变体外AM的位置,从而调节锚定力方向,可灵活满足黏膜创面暴露的需要,直至病变黏膜组织被完成切除。

图1 基于MAT的磁性水凝胶辅助ESD术
3.2 磁力测试
该项创新技术临床应用的关键问题在于AM对病变黏膜的锚定力是否能达到充分显露黏膜创面的效果。大鼠模拟实验中,我们将1 mL磁性水凝胶注射到大鼠腹部皮下,然后观察并测量AM对含有磁性水凝胶的皮肤的吸引情况。体外模拟结果显示,AM能够对大鼠腹部皮肤起到明显的吸引牵拉。万能材料试验机测试结果显示磁性吸引力在0距离时为1.3 N,随着距离增大,磁性吸力迅速下降,至间距为40 mm时,吸力为0.2 N(图2)。
4 讨论
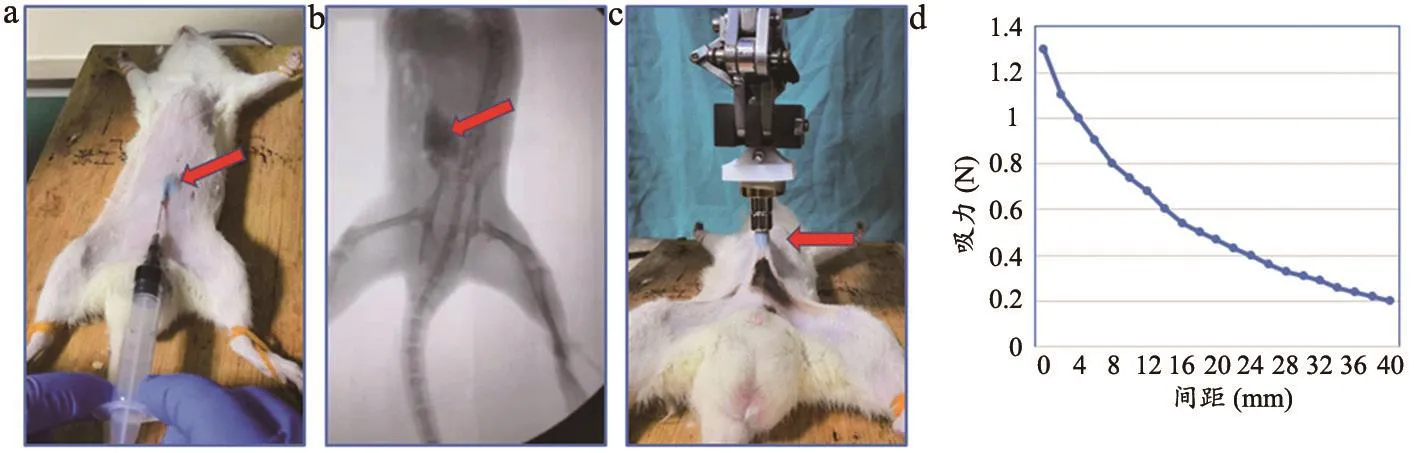
图2 模拟实验
ESD作为先进的内镜下治疗技术,对内镜操作技术要求很高,学习曲线长,人才培养时间成本高,在我国仅为数不多的三甲医院的消化内镜中心开展,可以说,在一定程度上ESD的开展代表着一个医院消化内镜水平的高低。据临床统计报道,ESD术后出血率在胃、食管、结直肠分别为 0.6%~15.2%[14]、0[15]、0.5%~9.5%[16];穿孔率在胃、食管、结直肠分别为 1.2%~9.7%[14]、0~6%[15]和 1.4%~8.2%[16]。ESD并发症除了与患者病情有关之外还与操作者的经验技术、医疗设备条件的有关。分析ESD手术操作的关键难点在于:缺乏能够提供组织反向牵拉力的装置,不能给予解剖平面足够的组织张力。在ESD术中,整个操作只通过一个内镜完成,不能像外科手术那样拥有“第二只手”辅助暴露,这样既限制了视野,又增加了手术操作难度,最终增加了术后并发症发生率。
MAG-ESD通过在待切除的病变组织上钳夹尾端固定有永磁体的组织夹,然后在体外放置AM,体外AM可吸引组织夹尾端的永磁体,并能调整牵引方向,从而给待切除病变组织提供反向的组织张力进而清晰地显露手术切除部位,极大地降低手术操作难度,也能有效避免因术野不清导致切除过深、误切血管等,减少了术中及术后出血风险。MAG-ESD所需的辅助装置简单易获取,操作便捷,效果显著,目前主要用于胃和结直肠黏膜的病变切除。少见将MAG-ESD用于食管早癌,其根本原因在于:食管相对于胃而言,可供术者操作的空间太过狭小,食管虽然是一个肌性器官,但通常直径不超过50 mm,且存在三处狭窄,如果病变恰好位于狭窄处,会更加限制ESD术者的操作。有限的食管内空间和TM的结构本身限制了MAG-ESD在食管黏膜病变切除中的应用。
磁流体作为一种新型智能材料,兼具磁性物质的磁学性能和液体的流动性[17]。水凝胶是一种以水为分散介质的凝胶,具有网状交联结构的水溶性高分子中引入一部分疏水基团和亲水残基,亲水残基与水分子结合,将水分子连接在网状内部,而疏水残基遇水膨胀的交联聚合物,是一种高分子网络体系,性质柔软,能保持一定的形状,能吸收大量的水[18]。磁性水凝胶融合磁流体的特性,又使其具备凝胶特性,使其被注射到机体病变组织中后具备很好的稳定性,减少弥散。
现有MS技术体系中,用于压榨吻合和磁性医疗器械研发的磁性材料大多为永磁材料[19-20]。本项目立足腔内MAT,首次提出将磁性水凝胶作为TM的设计,而目前的实验结果已初步证实,磁性水凝胶组织内注射后能够与AM产生足够的锚定力,使黏膜创面充分暴露,利于ESD术的实施。通过进一步研究磁性水凝胶的生物相容性、优化其加工工艺和磁学参数,基于MAT的磁性水凝胶辅助ESD术必将在临床中发挥重大作用。
