经皮肝穿刺胆囊引流术后二期LC在中度急性胆囊炎中的应用价值
2019-02-26周程严白莉龚昭杨光耀夏辉曾志武朱鹏
周程,严白莉,龚昭,杨光耀,夏辉,曾志武,朱鹏
(武汉市第一医院,1.肝胆外科,2.疼痛科,湖北 武汉 430022)
胆囊结石是常见的肝胆外科疾病,并在20%的病人中表现为急性胆囊炎(acute cholecystitis, AC)合并系统性疾病,且炎症程度差异很大[1]。在胆囊疾病的病人中,胆绞痛发生率每年约为1%~4%[2]。虽然,腹腔镜胆囊切除术(laparoscopic cholecystectomy, LC)已经成为治疗AC的金标准[3],但对于严重的AC病人,并发症如胆漏、胆总管损伤、肠管损伤等的发生率在LC术后更高[4],说明胆囊炎症的严重程度与LC困难程度之间存在相关性。
2013版东京指南(Tokyo Guideline 2013,TG13)[5]将AC分为3个等级:轻度(1级)、中度(2级)和重度(3级),2018版东京指南(TG18)沿用了TG13关于AC的诊断标准和严重程度分级。对于3级胆囊炎病人因合并严重的系统性疾病,TG13强烈推荐经皮肝穿刺胆囊引流术(percutaneous trans-hepatic gallbladder drainage, PTGBD),循证依据充分。而对以局部炎症反应为主的中度胆囊炎病人,则既可选择急诊LC,也可考虑PTGBD。PTGBD由Radder医生[6]首次报道于1980年,在外科条件并不发达的当时,得以普及运用,然而随着腹腔镜技术的出现与成熟,PTGBD的运用范围日渐缩窄,尤其是针对以局部重度炎症为主要表现的2级胆囊炎,PTGBD是否能使病人获益,目前尚未见文献报告,是一个值得探讨的问题。本文拟通过回顾性分析我院接受PTGBD和急诊LC的TG13中度AC人群,以探索PTGBD在当前外科环境下的临床价值。
资料与方法
一、病例收集
回顾性采集我院肝胆外科2017年1月至2018年6月中度胆囊炎病例164例。胆囊炎的诊断及分级基于TG13的标准,病人因接受的治疗方法不同被分成两组:PTGBD+LC组和急诊LC组。PTGBD+LC组病人在接受PTGBD术后,出院4~6周复诊入院行择期LC,而急诊LC组则在急性胆囊炎发作期内完成LC。
按TG13标准中度胆囊炎的纳入标准为:①白细胞计数(WBC)>18.0×109/L;②右上腹可扪及触痛包块;③症状持续时间>72 h;④显著的局部炎症(坏死性胆囊炎、胆囊周围积脓、肝脓肿、胆汁性腹膜炎以及产气性胆囊炎),以上条件符合其中之一即视为中度胆囊炎。排除标准为急性胆囊炎伴系统功能障碍符合以下任何项者:①心血管功能障碍(低血压需要治疗,多巴胺>5 μg·kg-1·min-1或任何剂量的去甲肾上腺素);②神经功能障碍(意识下降);③呼吸功能障碍(PaO2/FiO2<300);④肾功能障碍(无尿或肌酐>176.8 μmol/L);⑤肝功能障碍(PT-INR>1.5倍正常值);⑥凝血功能障碍(血小板计数<100×109/L);⑦既往有上腹部手术史者;⑧因胆管结石接受经内镜逆行胰胆管造影(ERCP)术后病例。
此项研究受华中科技大学同济医学院第四临床医院伦理委员会批准。
二、B超X线双重引导的经皮肝穿刺胆囊引流术(BX-PTGBD)
病人取平卧位,右上臂屈曲并置于头顶以充分显露右侧肋间隙。先以超声定位选择合适肋间隙,通常为右侧腋中线7~10肋间。1%利多卡因作肋间隙局部浸润后,超声同轴引导下以PTCD套件(Cook公司,美国),行一步法穿刺胆囊,穿刺成功后留置8.5~10.2F猪尾导管,透视下碘海醇造影以确认造影剂无外溢,并判断胆囊管通畅程度(图1)。常规留取胆汁行细菌培养及药敏实验。保留导管直至病人第2次复诊入院时(BX-PTGBD术后4~6周),于择期LC术前再次造影以评估胆道状况(图2),并于LC术中腔镜明视下拔除导管(图3、图4)。
三、LC
病人取平卧位,于全身麻醉下行LC,手术均由超过2 000例LC经验的高年资医生实施,大部分病例以4孔法由一助配合完成。术中胆囊三角重度粘连水肿者,则行逆行切除;胆囊壁重度水肿或坏疽与肝床界限不清者,则行保留胆囊底的胆囊次全切除并黏膜消融;胆囊壶腹或胆囊管结构明显扩张,则以胆道镜检查确认无残石后,予以镜下Endo-loop套扎或4-0 Vicryl缝扎胆囊管内口处理;若术中术者判断腹腔镜无法安全地实施手术则中转开腹胆囊切除。
四、“困难胆囊”的定义
“困难胆囊”的判断标准为术中发现存在下列情况之一者[7]:①腔镜手术中转开放手术;②次全胆囊切除和(或)黏膜毁损术;③坏死性胆囊炎或胆囊周围脓肿形成;④胆囊颈周围致密粘连。
五、变量分析
针对术前基线特征,我们对两组病人的年龄、性别、体质量指数(body mass index,BMI)、体温、术前症状持续时间、术前黄疸、右上腹压痛性包块、美国麻醉医师协会(American Society of Anesthesiologists,ASA)麻醉风险分级、WBC、C反应蛋白(C reaction protein,CRP)水平以及胆囊壁厚度进行统计分析;而关于预后的评判,我们则从中转开腹率、是否复杂胆囊、手术时间、切口感染率、并发症等级(Dindo-Clavien分级)、住院时间以及医疗费用7个方面进行评估。
六、统计学方法
独立样本Student-t检验及χ2检验用以分析两组间基线人群分布、临床和生化特征。为减少潜在的选择性偏倚所致的混杂因素,倾向性评分采用二分类Logistic回归分析以估计病人接受急诊LC而非PTGBD+LC的可能性。进入倾向模型的独立变量包括年龄、性别、BMI、体温、术前症状持续时间、术前黄疸、右上腹压痛性包块、ASA麻醉风险分级、WBC、CRP水平以及胆囊壁厚度。采用最邻近匹配法进行两组间的1∶1匹配,卡钳值取0.1。倾向评分的分布被用于评估组间重叠的充分性以确认两组间的可比性。我们从164例病人中移除了非重叠倾向评分分布的70例(PTGBD+LC组9例;LC组61例);因而,基于倾向性评分的调整后的资料为每臂47例。所有单因素分析中变量均进入多因素分析以评估其作为独立风险因素的显著性。风险比(hazard ratio,HR)及其95%的置信区间(CI)均在组间予以比较。
结 果
经回顾性分析资料并收集,共纳入病例164例,其中PTGBD+LC组56例,急诊LC组108例。术前两组病人的基线特征详见表1。
倾向性评分匹配前,两组病人的11项基线特征中BMI值、术前症状持续时间以及CRP水平,PTGBD+LC组均显著高于急诊LC组,提示两组基线特征存在不均衡。
经倾向性评分匹配处理后,两组共保留病例94例,其中PTGBD+LC与急诊LC组各47例,再次将两组的基线特征进行对比,详见表2。
原基线特征中差异显著的BMI、症状持续时间及CRP水平在匹配后,P值分别为0.559、0.424和0.497,两组间的混杂因素被良好的匹配消除。所有11项基线指标在两组间差异均无统计学意义,两组的基线特征保持均衡。
对倾向性评分匹配后的两组病人就中转开腹率、是否复杂胆囊、手术时间、切口感染率、并发症等级(Dindo-Clavien分级)、住院时间以及医疗费用7个预后指标进行对比,详见表3。

图1 PTGBD术中造影图 急诊胆囊炎PTGBD术后造影显示胆囊管因结石嵌顿及水肿原因未显影 图2 二期LC术前经PTGBD导管再次造影图 PTGBD术后5周再次造影,胆囊管、肝总管、胆总管显影良好,提示胆囊炎局部条件改善 图3 二期腔镜胆囊切除术中PTGBD窦道情况 PTGBD术后5周,腔镜探查术中见PTGBD穿刺窦道形成良好 图4 二期腔镜胆囊切除术中PTGBD导管情况 PTGBD术后5周,腔镜探查术中见良好固定于胆囊腔内的PTGBD导管
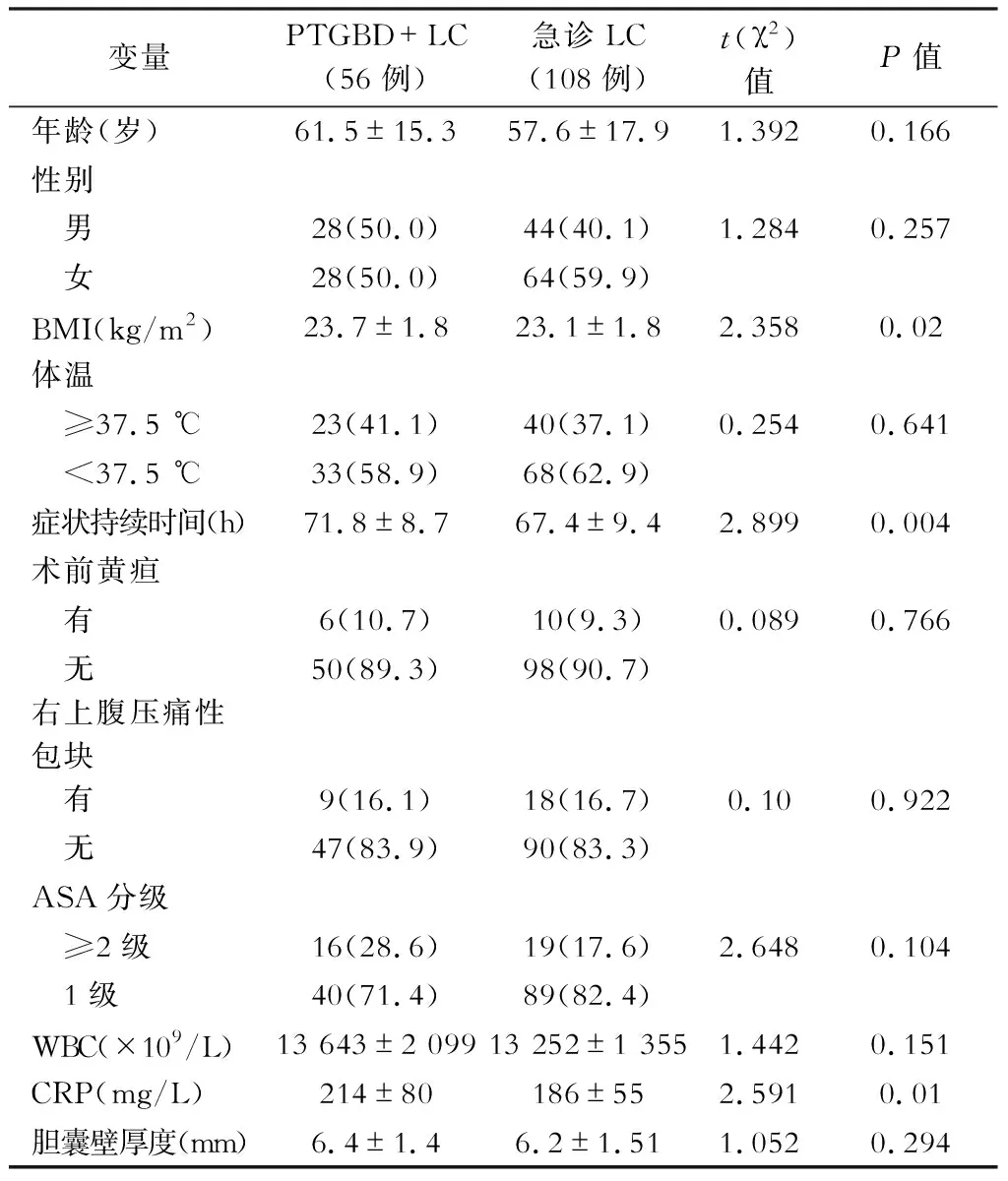
表1 倾向性评分匹配前PTGBD+LC与急诊LC术前基线特征对比
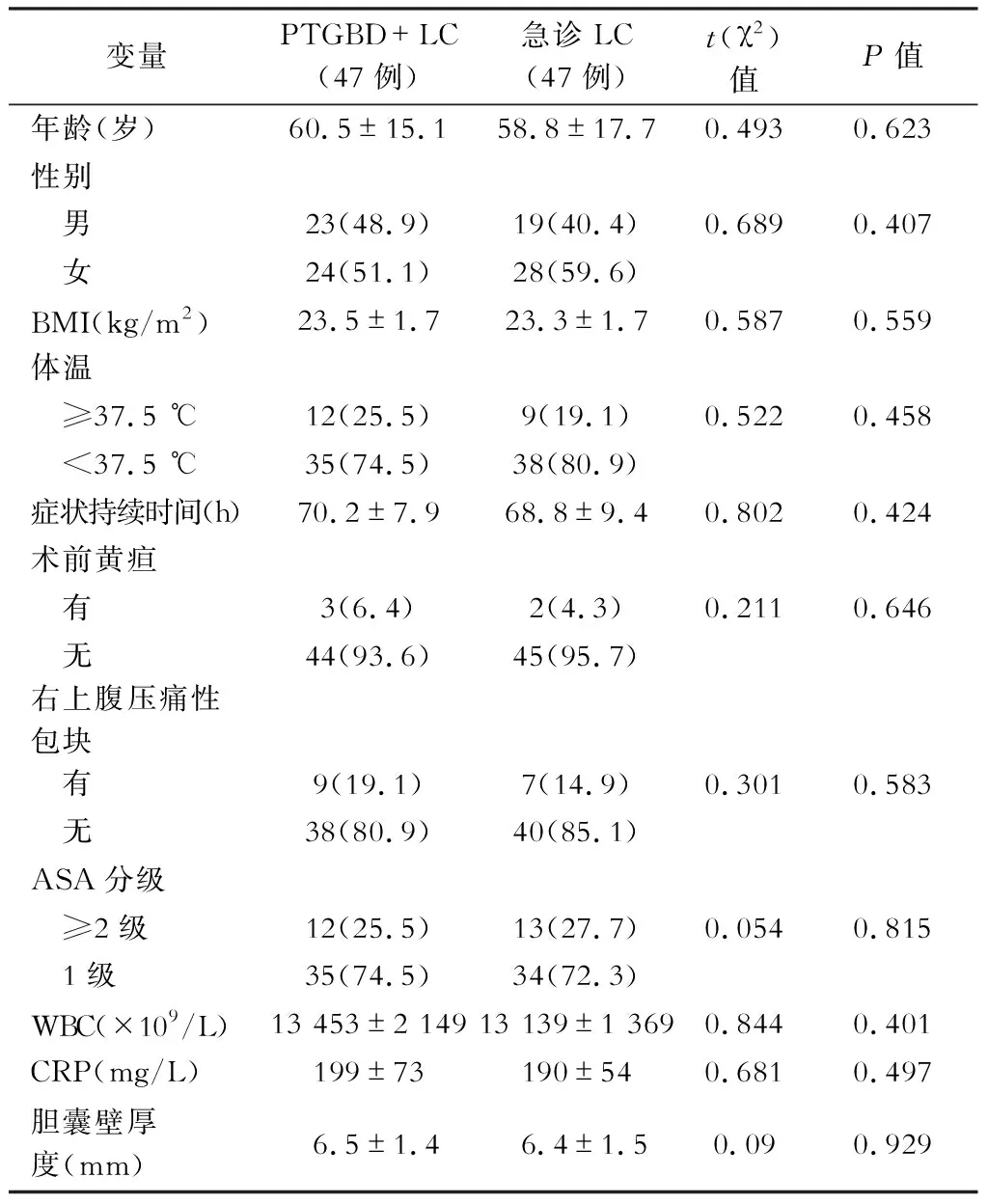
表2 倾向性评分匹配后PTGBD+LC与急诊LC术前
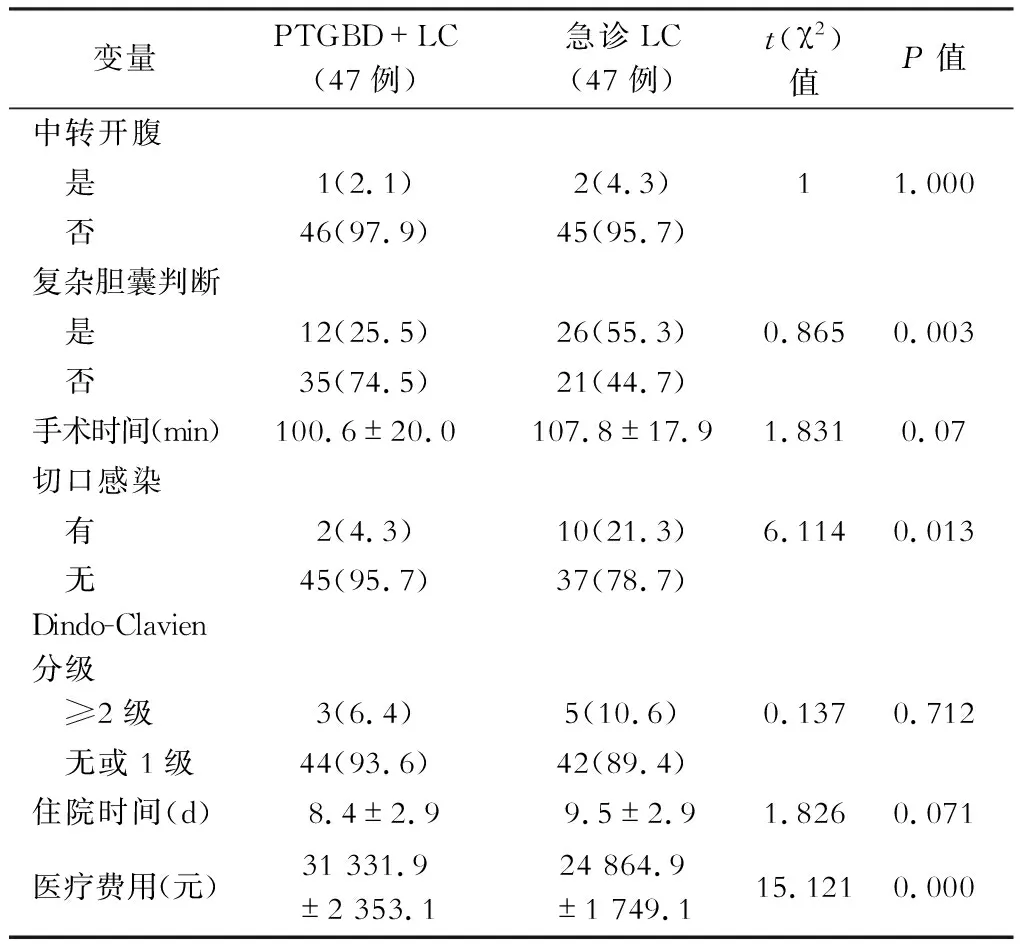
表3 倾向性评分匹配后两组病人临床预后比较
统计分析发现在由术者判断的复杂胆囊率方面PTGBD+LC组(25.5%)明显低于急诊LC组(55.3%),P值为0.003;而在手术切口的感染率上,PTGBD+LC组也显著低于急诊LC组(4.3%比21.3%,P=0.013);然而住院费用方面,PTGBD+LC组却是显著高于急诊LC组(P<0.01)。
将包含手术方式(PTCD+LC或急诊LC)在内的12项因素是否为构成“困难胆囊”的风险因素进行统计评估,详见表4。
统计分析发现,治疗方式选择PTGBD后接LC或急诊LC是构成“困难胆囊”的独立风险因素,B值为1.641,其他因素还有胆囊壁厚以及体温≥37.5 ℃同样是导致“困难胆囊”的独立风险因素,B值分别为0.421和1.254。
讨 论
急性胆囊炎症由水肿性发展形成坏死性,再到亚急性胆囊炎约需10 d左右时间。水肿期是致密粘连形成的前期,通常在症状开始后持续72 h[8]。PTGBD因可确切地减除胆囊内压力,理论上可以减轻胆囊壁的炎症水肿程度,但过久的PTGBD导管留置和等待本身也可能会导致胆囊周围纤维化和致密粘连的形成,从而影响腹腔镜胆囊手术的困难程度,因此就这个问题一直存在争议。我们的研究发现,由倾向性评分匹配后的结果来看,急诊LC组“困难胆囊”率为53.3%(26/47),显著高于PTGBD+LC组的25.5%(12/47);从多因素回归分析结果可以看出,治疗方案的选择即未经PTGBD而急诊LC是构成困难腹腔镜胆囊切除的独立风险因素,两者相符合。对于PTGBD到择期LC的间隔时间,尚无规范性意见,Chikamori等[9]认为PTGBD术后早期LC安全有效,而Kim等[10]则主张延迟LC。Inoue等[7]通过ROC曲线分析后,认为至少应该等待216 h,才能有效降低胆囊手术难度。就本院的实际情况来看,PTGBD至LC平均间隔时间为34.5 d,大于Inoue提出的Cut-off时间,可能是有效降低LC困难程度的主要原因。
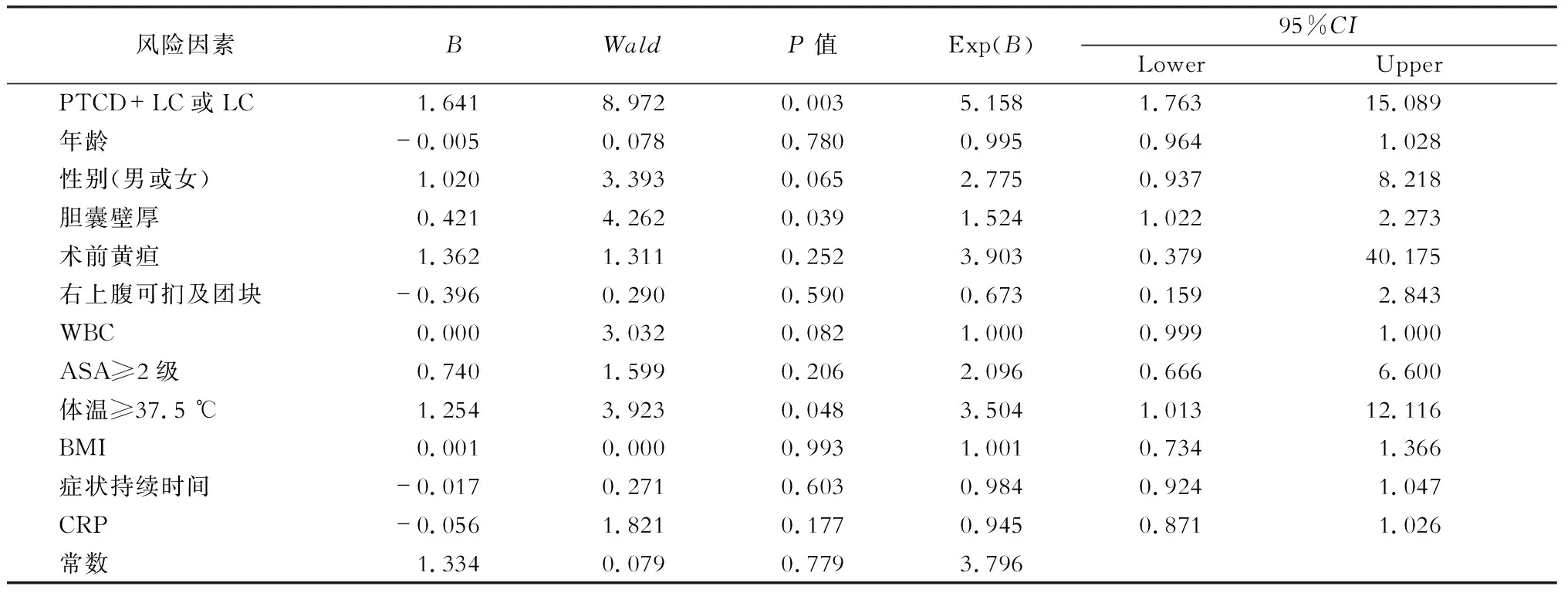
表4 多因素回归分析筛查“困难胆囊”的风险因素
Jackson等[11]以延时手术(即手术时间>90 min)来定义胆囊切除的困难程度,而我们则是按照术中5项客观指标[7]来判断是否归属于“困难胆囊”切除。虽然定义方式不同,我们的观察也发现:PTGBD组手术时间为(100.6±20.0) min,急诊LC为(107.8±17.94 ) min,两者差异也非常接近显著性水平(P=0.07)。Lee等[12]的报道中PTGBD+LC组手术时间为(73.4±28.7) min,而急诊LC组为(91.4±35.6) min,均低于我们数据,但其纳入的研究对象中包括了TG13重度病例。我们认为,由于其他合并的系统疾病而行PTGBD引流,与单纯因为重度胆囊炎症而需行穿刺减压,在胆囊局部的条件上是存在差异的,这可能是两组手术时间相异的原因。
虽然Bickel等[13]的研究结论认为早期PTGBD可以中断胆囊炎的进展,从而降低后期LC的中转率,但实际上关于PTGBD后LC的中转率,不同文献差异甚远,较低者仅5.0%~13.4%[7,12],而高者如Sanjay等[14]的报道可达67%。然而,我们的数据显示,PTGBD+LC组与急诊LC组均远低于其他文献报道,分别为2.1%(1/47)和4.3%(2/47),且两者差异无统计学意义。我们认为,这与术者大于2 000例的LC经验密不可分,合理的运用次全切除法、胆囊黏膜消融法,不仅能有效降低中转率,也可以大大降低并发症的发生率。
我们所观察到的Dindo-Clavien 2级以上并发症发生率,PTGBD+LC组仅为6.4%(3/47),而急诊LC组也只有10.6%(5/47)。虽然略高于Pucher等[15]所报道的总体并发症率(1.6%~5.3%),但由于Meta分析原因,Pucher无法对其纳入的505 292例 LC病例就其胆囊炎症的程度进行分层,是造成本文并发症率略高于总体水平的原因。Giger等[16]认为急性胆囊炎症与LC术后局部和全身并发症相关,而在本研究中两组间并无显著性差异,PTGBD似未能表现出降低并发症率的效应,我们认为这与纳入病例数量相对少以及手术经验相关。Schwaitzberg等[17]和Harrison等[18]的研究均证明,外科医生的经验以及外科机构的LC体量,在降低并发症、死亡率和再手术率方面有明显的正性效应。本单位年LC例数大于1 000例、主刀医生均经验丰富,以致两组并发症水平均处于低位,且相对较少的病例纳入量,是导致差异非著性的可能原因。
预后指标中存在显著性差异的还有切口感染率,在PTGBD+LC组仅为4.3%(2/47),而急诊LC组高达21.3%(10/47)。Warren等[19]对65 566例胆囊切除进行回顾,发现LC术后的总体切口感染率为0.64%,由于本文以TG13中度胆囊炎病例为观察对象,因此手术切口感染的发生率偏高。Warren等[19]的统计分析还发现腔镜处理急性胆囊炎/嵌顿是切口感染的独立风险因素,这与我们推论一致,由于PTGBD解除了胆囊结石的嵌顿、缓解了急性胆囊炎症,从而使后继LC的切口感染远低于急诊LC。
术后住院时间和治疗费用也被列为疗效评价指标。就住院时间而言,本研究PTGBD+LC组[(8.4±2.9) d]略短于急诊LC组[(9.5±2.9)d],差异虽无显著性,但侧面反应了实际临床管理中医生对急诊LC术后延迟性并发症的顾虑。由于本文以评价PTGBD对LC的影响为主要目的,文中仅比较了两组病人LC术后的住院时间,而未将PTGDB术后的留院时间也计算在内,而这一数据,与Inoue等[7]报道的PTGBD后长间隔组(>216 h)的LC术后住院时间[(8.6±0.81) d]非常接近,具有很强的可比性。由于PTGBD+LC组的治疗分成两个阶段,涉及到两种外科干预措施,因此治疗费用显著高于急诊LC组(P<0.001)。
我们的研究也存在一些局限性。首先,我们的研究是回顾性分析以及非随机化分组设计,虽然应用了倾向性评分匹配的方法,理论上具备前瞻性研究的证据水平,但仍不能避免所有的选择性偏倚。其次,较少的样本量可能会影响某些指标显著性的判断。
综上所述,我们的研究发现采用PTGBD术后二期LC处理TG13中度急性胆囊炎可以有效降低困难腔镜胆囊手术风险,减少术后切口感染,同时具备可接受的手术时间、中转开腹和并发症率,却存在医疗费用较高的不足。
