胰岛结合bFGF生物胶经肾被膜下移植逆转小鼠糖尿病
2019-02-14朱群燕蒋煊郑雅文黄志伟徐福远耿武军傅红兴赵应征
朱群燕,蒋煊,郑雅文,黄志伟,徐福远,耿武军,傅红兴,赵应征
(1.温州医科大学 药学院,浙江 温州 325035;2.温州医科大学附属第一医院 麻醉科,浙江 温州325035)
胰岛移植是目前临床糖尿病治疗领域中一种具有较大潜力的治疗手段,尽管埃德蒙顿方案公布后,胰岛移植取得了可观的进展,但胰岛需要量大、移植后微血管重建慢、胰岛功能低下等问题仍然阻碍着胰岛移植的大规模应用[1-4]。碱性成纤维细胞生长因子(basic fi broblast growth factor,bFGF)具有刺激血管新生、创伤愈合和组织再生等功能[5]。本实验室前期已证明bFGF能够促进胰岛内部微血管重建,提高胰岛体内活性和功能[6],但bFGF在体内半衰期短,单纯bFGF培养液与胰岛共移植的效果不理想。
重组人胶原蛋白(recombinant human collagen,RHC)是利用基因工程改性所得的一种III型胶原,该胶原能增强血管强度,为细胞提供养分,从而促进新血管的形成[7-8]。为提高胰岛移植后疗效、减少胰岛用量,本研究基于实验室前期基础,选用bFGF结合不同浓度RHC与胰岛共移植至同系糖尿病小鼠肾被膜下,并对术后胰岛功能和组织学进行评价,为进一步研究降低胰岛移植用量和提高移植效果奠定基础。
1 材料和方法
1.1 材料
1.1.1 实验动物:雄性Balb/C小鼠40只,6~8周龄,购自上海斯莱克实验动物有限责任公司。
1.1.2 实验试剂和器材:异氟烷(Baxter公司,美国);链脲佐菌素(STZ)、胶原酶V(sigma,USA);Ficoll-1077、Ficoll-1119、CMRL-1066、Hanks液(温州市怡康细胞移植技术开发有限公司);胎牛血清(Gibco,Thermo Fisher Scientific);重组人胶原蛋白(江苏江山聚源生物技术有限公司);碱性成纤维细胞生长因子(浙江格鲁特生物科技有限公司);血糖仪(博士医生,北京);恒温水槽(DKZ-450B,上海森信实验仪器有限公司);离心机(L500,上海利鑫坚离心机有限公司);体式显微镜(SDT-TL2,上海光泉科仪器有限公司)。
1.2 方法
1.2.1 糖尿病模型的建立:Balb/C小鼠造模前禁食12 h,不禁水,测定空腹血糖值和体重,腹腔注射STZ(55 mg/kg)。造模后第1、3、7天测定血糖值,血糖值≥22.2 mmol/L 视为糖尿病造模成功,可用于移植实验。
1.2.2 小鼠胰岛的分离:参考前期的实验基础[6,9-10],简述如下:取Balb/C小鼠吸入过量异氟烷致死后,胆总管逆行灌注胶原酶V溶液2.5 mL(浓度为1 mg/mL),摘取胰腺至50 mL离心管中,(37±0.5)℃恒温水消化至乳糜状,冷Hanks液终止消化,并用Ficoll-1077和Ficoll-1119进行非连续密度梯度纯化,在体视显微镜下进一步手工挑选。胰岛用CMRL-1066培养基(含10% FBS和1%青霉素-链霉素)于37 ℃、5%CO2培养箱中培养6 h后进行移植。
1.2.3 胰岛鉴定、活性测定和当量计算:采用常规的DTZ染色方法鉴定胰岛,并用FD/PI染色液染色测定胰岛活性[6]。参照Lembert等[11]方法,在倒置显微镜下记录每个胰岛的直径,按照胰岛当量表换算成相应直径150 μm的胰岛当量。
1.2.4 实验分组及体外培养:将造模成功的小鼠随机分成三组,分别为:(1)Free组(单纯胰岛移植组);(2)1 mg/mL RHC+60 ng/mL bFGF组(胰岛移植液中含1 mg/mL RHC和60 ng/mL bFGF);(3)16 mg/mL RHC+60 ng/mL bFGF组(胰岛移植液中含16 mg/mL RHC和60 ng/mL bFGF)。胰岛基础移植液与培养液一致,每只小鼠移植胰岛当量为(200±50)IEQ。以正常Balb/C组(NOR组)、糖尿病小鼠未移植胰岛组(DM组)为对照组。
1.2.5 小鼠肾被膜下移植:参照Zumda等[12]的研究。糖尿病小鼠持续吸入异氟烷麻醉后,剃去右侧背部毛发并消毒,暴露肾脏。在体式显微镜下用注射器将含(200±50)IEQ胰岛的混悬液推注至肾被膜下,棉签压迫止血,缝合伤口。皮下注射1 mL生理盐水补液。每日早晚给予头孢唑林钠皮下注射50 μL(浓度50 mg/mL),持续1周。
1.2.6 移植后胰岛功能和疗效评价
(1)血糖和体重监测:每日观察小鼠饮食、饮水和精神状况,测量和记录小鼠血糖和体重变化。连续两次血糖超过16.7 mmol/L预示着小鼠重回高血糖状态[13]。
(2)口服糖耐量试验(OGTT):移植后第30天,将移植组、正常组(NOR组)和糖尿病未移植组(DM组)小鼠禁食过夜,不禁水。用超纯水配制浓度为200 mg/mL的葡萄糖溶液,灌胃剂量为2 mg/g,测定各组小鼠灌胃前(0 min)和灌胃后20、40、60、90、120 min的血糖值。
(3)移植部位胰岛的组织学评价:移植后第30天,取各移植组小鼠,持续异氟烷吸入麻醉,经心脏灌注生理盐水后,取移植部位肾脏组织并固定于4%多聚甲醛中,进行HE、Insulin免疫组化染色和CD31免疫组化染色,观察移植部位胰岛的形态和新血管生成结果。
1.3 统计学分析
数据采用Graft pad 5统计学软件进行处理,所有数据用(±s)表示,并采用成对样品t检验进行统计学分析。P<0.05表示具有统计学意义。
2 实验结果
2.1 小鼠胰岛的分离和培养结果
经纯化和手工挑选后的小鼠胰岛纯度为(96.4±2.6)%。培养6 h后,胰岛外形完整、边缘清晰,经FD/PI染色显示,平均活性(90.1±3.5)%。
2.2 移植术后小鼠血糖和体重变化
16 mg/mL RHC+60 ng/mL bFGF组的小鼠胰岛移植后血糖下降最快,与1 mg/mL RHC+60 ng/mL bFGF组均能维持正常血糖超过30 d;Free组胰岛移植后血糖未能降至正常水平(见图1A)。胰岛移植治疗结束后,Free组体重明显降低[降低(-2.10±2.60)g],1 mg/mL RHC+60 ng/mL bFGF组[增加(3.36±0.78)g,P<0.05]和16 mg/mL RHC+60 ng/mL bFGF组[增加(3.04±1.01)g,P<0.05]小鼠体重则增加明显(见图1B)。
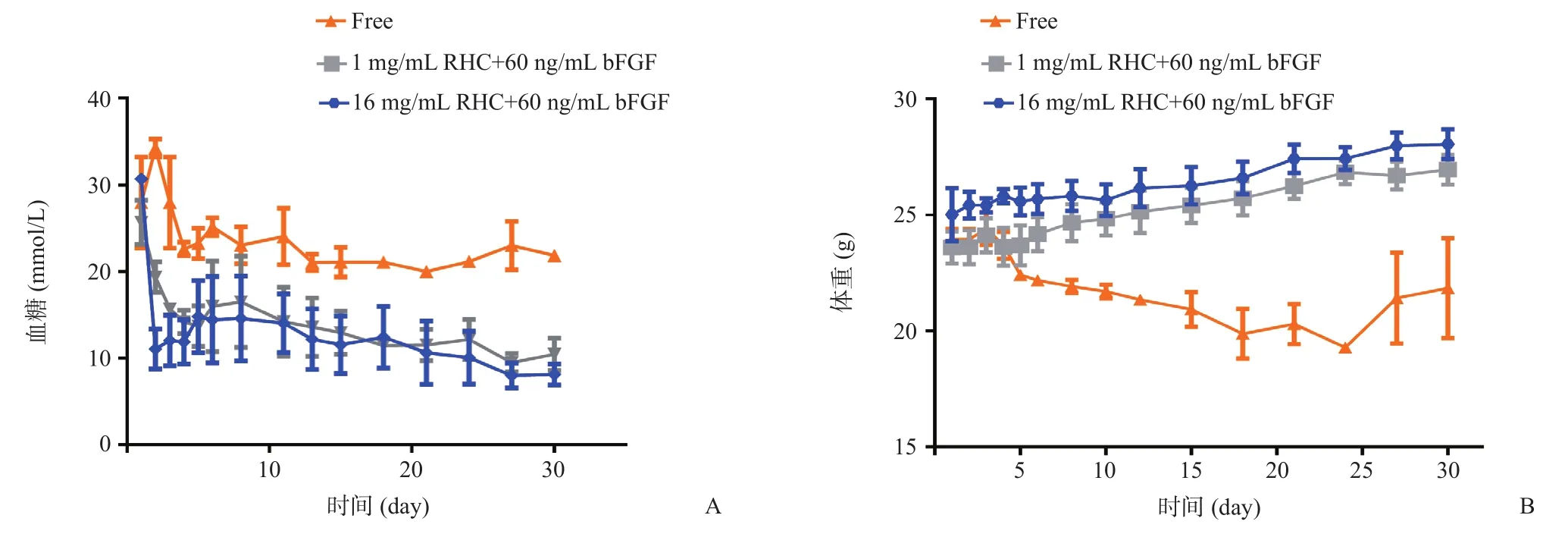
图1 胰岛移植后各组小鼠血糖(A)和体重(B)的变化结果
2.3 口服糖耐量试验(OGTT)
如图2所示,16 mg/mL RHC+60 ng/mL bFGF组小鼠的糖耐量曲线和NOR组相似,且120 min时血糖均恢复到基线水平;Free组和1 mg/mL RHC+60 ng/mL bFGF组小鼠在120 min时血糖均未能恢复到基线水平。

图2 小鼠胰岛移植后第30天糖耐量结果
2.4 移植后肾被膜下胰岛的组织学评价
取胰岛移植30 d后的小鼠肾组织进行HE、insulin素和CD31免疫组化染色,结果如图3所示。
由移植部位含胰岛组织的HE和insulin免疫荧光染色结果可见,各移植组肾被膜下的胰岛组织形态完整,且能分泌胰岛素(图3A)。由移植部位胰岛组织的CD31染色结果显示,1 mg/mL RHC+60 ng/mL bFGF组和16 mg/mL RHC+60 ng/mL bFGF组CD31蛋白表达较多,说明新血管生成较多,而Free组CD31阳性表达较少,说明新生血管较少(图3B)。
3 讨论
目前,可供胰岛移植用胰腺供体不足和胰岛分离纯化过程中造成的胰岛内部微血管系统的破坏均制约着临床胰岛移植在糖尿病治疗中的应用[6,14]。为了解决这些问题,国内外研究者进行了大量的探索,如构建三维多孔支架为胰岛提供生存的空间[14]、添加生长因子类药物促进受损微血管重建[6]、应用产氧微粒减少胰岛中心坏死[15]等。本课题小组初步研究表明,全量胰岛移植(400 IEQ)能有效控制糖尿病小鼠的血糖水平。本研究采用胰岛联合RHC和bFGF共移植,血糖监测结果显示(200±50) IEQ的胰岛亦能显著降低血糖至正常水平,且与单纯同当量胰岛移植的小鼠降低水平的能力有明显差异(P<0.01)。本研究亦发现,RHC-bFGF和胰岛共移植组的新生血管数量明显增加。

图3 移植部位肾脏组织HE染色、Insulin免疫荧光染色和CD31免疫组化染色
本研究通过联合应用RHC和bFGF,为胰岛提供一个富含bFGF的类细胞外基质的微环境,能够促进移植后胰岛的微血管重建和提高胰岛功能、降低维持正常血糖所需的胰岛移植量,有助于缓解胰岛移植中供体不足的难题。
