泸型酒蒸馏过程中基酒挥发性物质变化分析
2019-02-14蒲秀鑫郎召伟张晓娟王松涛沈才洪陆震鸣许正宏
徐 勇,蒲秀鑫,郎召伟,张晓娟,王松涛,沈才洪,陆震鸣*,许正宏,
(1.国家固态酿造工程技术研究中心,四川 泸州 646000;2.江南大学粮食发酵工艺与技术国家工程实验室,江苏 无锡 214122;3.江南大学 工业生物技术教育部重点实验室 生物工程学院,江苏 无锡 214122)
中国白酒因其悠久的历史、独特的工艺,而成为我国具有民族特色的蒸馏酒,并与威士忌、伏特加、白兰地、朗姆酒和金酒并称为世界六大蒸馏酒[1]。浓香型白酒是中国白酒的典型代表之一,具有独特的酒体风格。
白酒中最主要的物质是乙醇,但除了乙醇外还存在种类极其丰富的其他风味物质,尽管这些风味物质在酒中的含量很低,但是它们却对白酒风味和酒质起重要的作用[2]。蒸馏是白酒生产过程的重要工序之一,可将酒醅中乙醇和其他多种微量挥发性风味物质浓缩至基酒中[4-6]。蒸馏过程中的物质的馏出顺序是基于不同风味化合物的沸点差异和水溶性不同,进而导致了不同蒸馏时间的酒的风味的不同。因此,研究白酒蒸馏过程中不同时间段对应的风味化合物的变化情况,对于明确风味物质在蒸馏过程中各阶段基酒中的变化情况以及对后续监控基酒品质有重要意义。
本研究采用顶空固相微萃取(headspace solid-phase micro-extraction,HS-SPME)方法萃取泸型酒蒸馏过程中基酒的挥发性物质。并结合气相色谱质谱联用(gas chromatography-mass spectrometry,GC-MS)等检测手段来研究基酒在蒸馏过程中的挥发性风味物质的变化情况,监测了蒸馏过程中酒精度的变化情况,同时通过多元统计方法确定和分析了不同蒸馏时间对应的基酒风味特征物质。以其为后续深入研究白酒风味的变化机理奠定基础。
1 材料与方法
1.1 材料与试剂
取发酵成熟的酒醅并进行蒸馏,得到基酒样品。从蒸馏开始的第0 min开始取样,直至蒸馏结束,其间每隔1 min取样一次。在蒸馏过程中共取得20个样品,分别编号为0~19号。
氯化钠、无水乙醇、甲醇、浓硫酸、重铬酸钾(均为分析纯):国药集团化学试剂有限公司;2-辛醇(色谱纯):美国Sigma-Aldrich公司。
1.2 仪器与设备
Bruker SCIONSQ456气相色谱-质谱联用仪:德国Bruker公司;0/30μm DVB/CAR/PDMS顶空固相萃取头:美国Supelco公司。
1.3 方法
1.3.1 基酒酒精度的测定[7]
分别准确吸取0、0.02 mL、0.04 mL、0.06 mL、0.08 mL、0.10 mL、0.12 mL的乙醇标准溶液(40%)加入具塞比色管中,分别加入2 mL重铬酸钾溶液(8%)和1 mL浓硫酸,摇匀,静置反应10 min,用蒸馏水定容。反应后的溶液用蒸馏水稀释8倍后于波长585 nm处测量其吸光度值。以吸光度值为纵坐标,乙醇浓度为横坐标绘制标准曲线。吸取0.03 mL基酒至5 mL具塞比色管中,加2 mL重铬酸钾溶液(8%),再缓慢加入1 mL浓硫酸,摇匀,静置反应10 min,用蒸馏水定容,反应后的溶液先用蒸馏水稀释8倍后于波长585 nm处测定吸光度值。样品中的酒精含量根据乙醇标准曲线回归方程计算。
1.3.2 酒醅和基酒中挥发性风味物质的测定[8]
样品处理方法:称取2 g酒醅或8 mL基酒至20 mL顶空固相微萃取瓶中,加8 mL蒸馏水、3 g氯化钠和10μL 2-辛醇,振荡均匀。将萃取头插入萃取瓶上部空气,在50℃条件下吸附40 min,在GC进样口250℃解吸5 min。
分析条件:DB-Wax色谱柱(30 m×0.32 mm×0.25μm)。氦气(He)为载气,1.0 mL/min,气化室温度250℃,色谱柱起始温度40℃,维持3 min,再以5℃/min速率升温至60℃,最后以10℃/min速率升至230℃,维持8 min,共计32 min。电子电离(electron ionization,EI)源,电子倍增器电压为350 V,电子能量为70 eV,发射电流200μA,接口温度250℃,离子源温度200℃,扫描范围控制在33~450 u。
1.3.3 多元统计分析
(1)聚类分析
选取参与聚类分析的风味物质作为变量,对变量进行标准化处理。根据要求选择合适的聚类类型,本实验进行Q型聚类时选用欧氏距离(Euclidean distance)法,进行R型聚类时选用相关系数距离(Pearson correlation)法[9]。
(2)主成分分析
选取参与主成分分析的风味物质作为变量,对变量进行标准化处理。本实验主要选用巴特利特球形检验(Bartlett Test of Sphericity)和KMO(Kaiser-Meyer-Olkin)检验来确认原有变量是否适合主成分分析。并通过计算变量的协方差矩阵,根据结果选取特征值大于1,累计方差贡献率大于80%作为后续分析的主成分。通过分析结果找出每个样本与原变量之间的关系[9]。
2 结果与分析
2.1 蒸馏过程中基酒酒精度变化
泸型酒蒸酒过程是在边上汽边装料的条件下进行的。蒸馏完成后可将4%vol~6%vol左右的乙醇经汽化、冷凝、汽化等步骤浓缩为70%vol左右酒精度的大曲酒基酒[5]。从图1可以看出,随着蒸馏时间的延长,基酒中酒精度逐渐下降,第0~1 min为第一段酒头,此时酒精度较高为75.6%vol;第2~14 min为第二段,此时酒精度下降较为缓慢;第15~19 min为第三段酒尾,此时酒精度开始迅速下降至13.9%vol。
2.2 蒸馏过程中基酒挥发性风味物质变化
蒸馏过程中,在蒸汽的不断加热下,温度会不断升高,随着酒精的蒸出,酒醅中的多种微量风味物质在蒸馏过程中也会和蒸汽一同进入酒体。由于不同化合物具有不同的理化性质,因此不同蒸馏时间段的基酒具有不同的变化规律,从而造成了不同时间段的基酒具有不同的风味特点。本次通过GC-MS在蒸馏过程的20个基酒样品中共检测出105种挥发性风味化合物,其中64种酯类物质、12种醇类物质、5种酸类物质、8种醛类物质、3种酚类物质和13种其他化合物。
2.2.1 酯类物质
蒸馏过程中酯类物质总含量变化见图2,四大酯类化合物的变化见图3。酯类物质共检测出64种,是检测到的挥发性风味物质中种类最多、含量最高的。从图2可以看出,随着蒸馏时间的延长,酯类物质含量呈下降的趋势,从蒸馏开始时的1 700.9 mg/L下降至蒸馏结束时的320.5 mg/L。酯类物质大量集中在酒头,即0~1 min阶段,且呈现快速下降的趋势,其中含量较高的四大酯类化合物,如乙酸乙酯、丁酸乙酯、己酸乙酯在第0~1 min也呈现迅速下降。此外,通过图3可以看出,乳酸乙酯在蒸馏过程中表现为逐渐上升趋势,这可能是由于其具有沸点和极性相对较高的原因。
乙酸乙酯、丁酸乙酯、己酸乙酯、乳酸乙酯在浓香型白酒中含量较高且是白酒风味的主要贡献者,因此被称为是浓香型白酒的四大酯,其中己酸乙酯是浓香型白酒主体香气成分[10]。从图3可以看出,己酸乙酯在整个蒸馏过程中平均占挥发性风味物质总量的47.4%,并且含量呈下降趋势,从823.9 mg/L下降至169.3 mg/L。乙酸乙酯从开始时的155.8 mg/L下降至结束时的2.5 mg/L,丁酸乙酯从153.9 mg/L下降至7.3 mg/L。乳酸乙酯在蒸馏过程中间(10 min)才被检测到,这与张鹏等[11]报道的浓香型白酒的四大酯的变化规律一致。
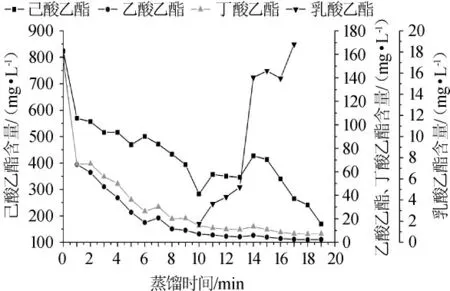
图3 蒸馏过程中四大酯类化合物的变化Fig.3 Changes of four main ester contents during distillation
2.2.2 醇类物质
醇类物质在白酒中对酯类物质具有助香、衬托作用,使香气更浓郁醇厚[12-14]。本实验共检测到包括丁醇、己醇、庚醇、辛醇、壬醇、葵醇、异丁醇、异戊醇、苯乙醇、6-十一烷醇、1-十六烷醇、烯丙基正戊基甲醇在内的12种醇类物质。从图4可以总结出,醇类物质在蒸馏过程中总体呈下降趋势,从22.1 mg/L下降至11.9 mg/L。且醇类物质在蒸馏第0~14 min时呈不规律的下降趋势,在第15 min以后开始急剧下降,造成这种变化规律的主要原因可能是由于在0~14 min基酒中含有较多的异戊醇和己醇,这两种物质对醇类物质的变化干扰较大,因此呈现不规律的变化结果,在14 min以后由于异戊醇含量迅速降低,导致醇类物质总量急剧下降,这与酒精度的变化趋势一致。
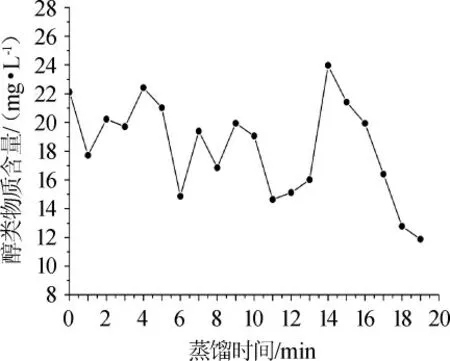
图4 蒸馏过程醇类物质的变化Fig.4 Changes of alcohol contents during distillation
2.2.3 酸类物质
酸类物质作为白酒中的重要呈味物质,在白酒中可以起到缓冲酒体、协调口感的作用[15-16]。在蒸馏过程中检测到的酸类物质主要有亚麻酸、戊酸、己酸、庚酸和辛酸这5种酸类物质,己酸是检测出来的酸类物质中含量最高的,在整个蒸馏过程都能检测到。从图5可以总结出,酸类物质的含量总体变化是呈上升趋势的,从2.1 mg/L上升至23.8 mg/L。在蒸馏过程的前半段即第0~13 min时酸类物质的含量上升趋势较为平缓,在第14分钟后才开始呈现较为急剧的上升趋势,尤其是第16分钟后变化更为明显。
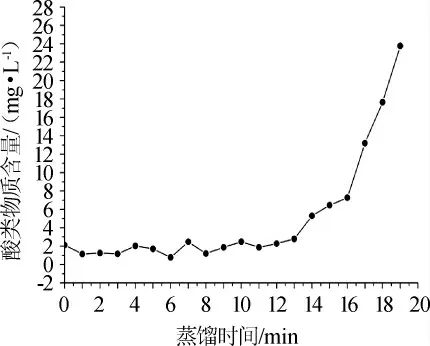
图5 蒸馏过程中酸类物质的变化Fig.5 Changes of acid contents during distillation
2.2.4 醛类物质
醛类物质在酒中可以起到很强的呈香作用[17-18],尽管其在酒中的含量低且种类少[19-20]。本次实验共检查到的醛类物质主要有壬醛、糠醛、苯甲醛、6-壬烯醛、反式-2-壬烯醛、苯乙醛二乙缩醛、反式-2,4-癸二烯醛、异丁醛二乙缩醛这8种醛类物质。从图6可知,醛类物质的变化趋势为刚开始蒸馏时上升较为缓慢,蒸馏进行到10 min后开始迅速上升,然后又在17 min后下降。醛类物质的含量从开始时的3.69 mg/L上升至18.9 mg/L,随后又下降至14.67 mg/L。
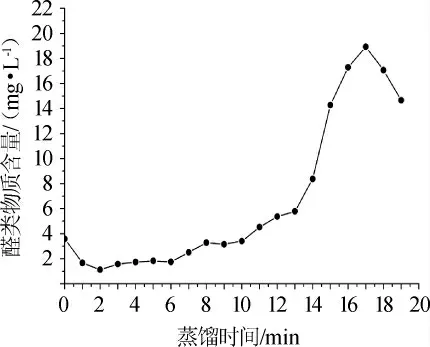
图6 蒸馏过程中醛类物质的变化Fig.6 Changes of aldehyde contents during distillation
2.3 泸型酒基酒蒸馏过程中挥发性成分的多元统计分析
多元统计分析的变量选择为在蒸馏过程中通过GC-MS检测到的检出率>80%的33种挥发性风味化合物,依次编号为V1~V33,结果见表1。
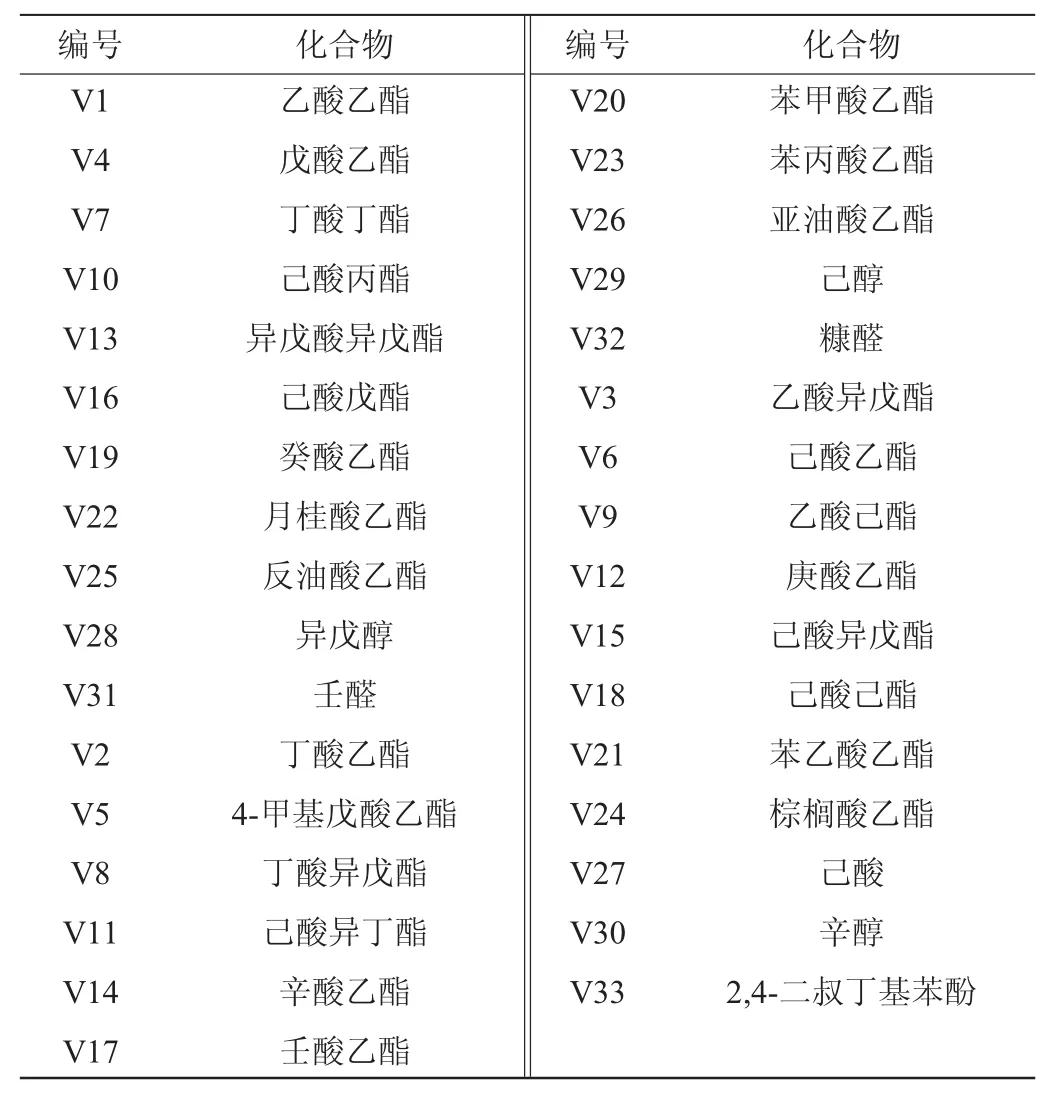
表1 参与多元统计分析的33种挥发性风味物质Table 1 Thirty-three volatile compounds used for multivariate statistical analysis
2.3.1 聚类分析
本实验对20个基酒样品进行聚类分析,结果如图7所示。
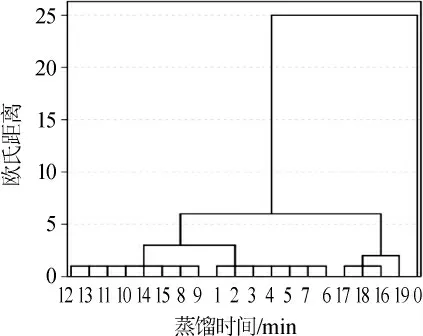
图7 基于风味物质的蒸馏过程中20个基酒样品聚类分析Fig.7 Cluster analysis of 20 base liquor samples based on the volatile compounds during distillation
根据聚类分析的结果可以将蒸馏过程分为四段,第一段是0~1 min,第二段是2~7 min,第三段是8~15 min,第四段是16~19 min。生产企业将蒸馏过程中基酒样品分为三段,分别是0~1 min为第一段酒头,2~14 min为第二段,15~19 min为第三段酒尾,这一分类与本实验的聚类结果相似。
2.3.2 主成分分析
通过对在蒸馏过程中检测到的检出率>80%的33种挥发性风味化合物和20个基酒样品作为变量分别进行主成分分析,结果如图8所示。
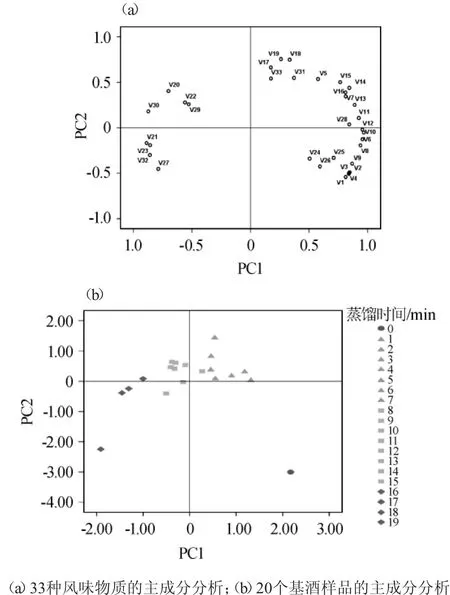
图8 蒸馏过程基酒中挥发性风味物质主成分分析Fig.8 Principal component analysis based on the volatile compounds in base liquor during distillation
结合图8(a)和(b)可以发现,在蒸馏开始时主要为大量的酯类化合物,分别是乙酸乙酯、乙酸异戊酯、乙酸己酯、丁酸乙酯、丁酸异戊酯、戊酸乙酯、己酸乙酯、己酸丙酯、庚酸乙酯、棕榈酸乙酯、反油酸乙酯、亚油酸乙酯。这12种酯类化合物赋予酒头丰富的香气,可以与其他蒸馏时间的基酒很好的分开;在蒸馏第1~7分钟主要对应的风味化合物为4-甲基戊酸乙酯、丁酸丁酯、己酸异丁酯、己酸异戊酯、己酸戊酯、己酸己酯、异戊酸异戊酯、辛酸乙酯、壬酸乙酯、癸酸乙酯、异戊醇、壬醛、2,4-二叔丁基苯酚,这13种风味化合物在这个蒸馏阶段含量较高,赋予该阶段基酒独特的香气,可以将其与其他阶段基酒区分开;在蒸馏第8~15分钟对应的风味物质主要为苯甲酸乙酯、月桂酸乙酯、己醇、辛醇这四种风味化合物,这些物质赋予此阶段基酒醇甜浓郁的香气,与其他阶段的基酒可以加以区分;在蒸馏第16~19分钟对应的风味物质主要为苯乙酸乙酯、苯丙酸乙酯、己酸、糠醛这四种风味化合物,这些化合物使蒸馏第16~19分钟的酒尾表现出酸涩苦闷的风味,与其他阶段基酒风味形成鲜明对比。
3 结论
本实验采用HS-SPME结合GC-MS等检测手段研究了泸型酒基酒蒸馏过程中的挥发性物质的变化规律。泸型酒基酒的酒精度从蒸馏刚开始的75.6%vol下降至结束时的13.9%vol。采用聚类分析方法对挥发性物质组成进行了分析,结果表明整个蒸馏过程可分为4个阶段:0~1 min,1~7 min,8~15 min,16~19 min。通过主成分分析发现,0~1 min基酒中的主要特征化合物为乙酸乙酯、乙酸异戊酯、乙酸己酯等各种酯类化合物,赋予了酒头丰富的香气成分;1~7 min基酒中主要特征化合物为丁酸丁酯等酯类,以及异戊醇、壬醛等;8~15 min基酒中主要特征化合物为苯甲酸乙酯、月桂酸乙酯等酯类,以及己醇、辛醇等醇类,赋予基酒醇甜浓郁的香气;16~19 min基酒中主要特征化合物为苯乙酸乙酯、苯丙酸乙酯、己酸、糠醛,可能使该阶段的酒体呈现酸涩苦闷的风味。本研究对于泸型酒蒸馏工艺的解释提供了数据支持和参考依据。
