一期前后路联合手术治疗对老年脊髓性颈椎病患者的临床研究
2019-02-10安永博侯文根
安永博 侯文根 路 坦 郭 鑫
新乡医学院第一附属医院骨外科二病区,河南 新乡 453100
脊髓性颈椎病(cervical spondylotic myelopathy,CSM)是颈椎病中危害最为严重的一种类型,可引起脊髓功能障碍与不同程度的四肢瘫痪,极大危害患者生命健康[1-3]。目前CSM治疗目的是解除颈脊髓压迫,最大程度恢复颈脊髓功能,阻止病情进一步进展,并重建或恢复颈椎管空间、颈椎的稳定性。保守治疗是CSM首选方法,但无法有效阻止病情进展[4-5]。前入路、后入路及前后路联合外科手术是治疗CSM常用入路方法,适用于保守治疗无效或未获满意效果患者,其中前路手术包括前路椎体减压植骨融合术、人工椎间盘置换术等,后路手术包括椎管扩大术等。有观点显示,单纯前路或后路手术无法实现彻底减压,而行一期前后路联合效果更好[6-7]。但有研究指出,一期前后路联合手术创伤与风险较大,因此关于联合手术的价值尚存在争议[8]。本研究选取96例老年CSM患者,探讨一期前后路联合手术的应用价值。
1 资料和方法
1.1一般资料选取2016-01—2019-02新乡医学院第一附属医院收治的96例老年CSM患者,简单随机化分为前路组、后路组、一期前后路联合手术3组,各32例。3组年龄、病程、体质量指数、性别、发病情况、病变节段、术前日本骨科协会(JOA)评分、合并疾病等资料均衡可比(P>0.05),见表1。
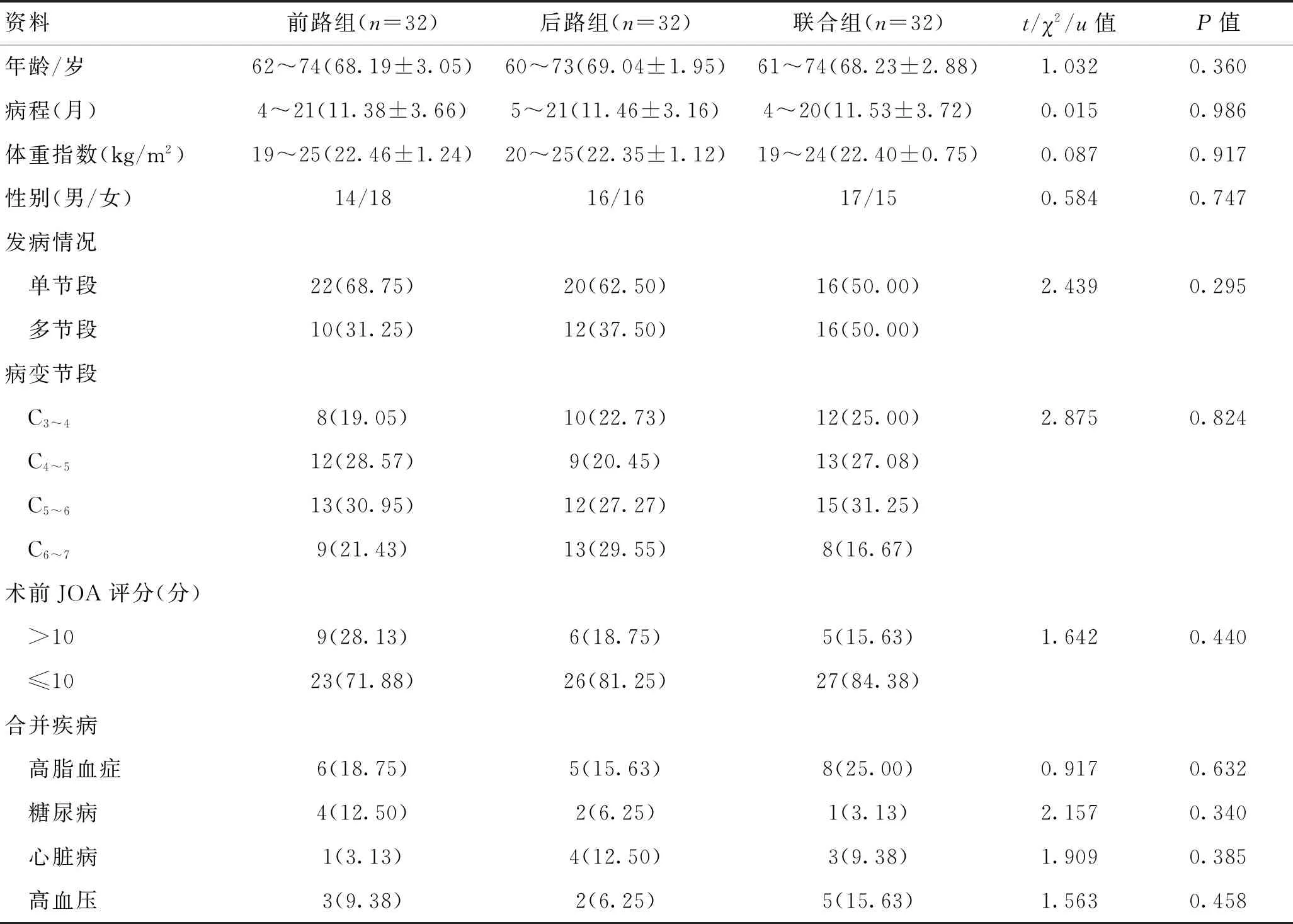
表1 3组临床资料对比
1.2纳入、排除标准(1)纳入标准:符合CSM诊断标准[9],保守治疗>3个月无效或未取得满意效果;年龄≥60岁;自愿签署知情同意书;既往无颈部手术史。(2)排除标准:术前骨密度检查t值<-2.5S者;病程较长,四肢有广泛性肌萎缩者;肝肾、心血管系统疾病不能承受手术者;凝血功能异常者;外伤导致脊髓损伤患者;合并精神疾病者。
1.3方法
1.3.1 主要工具、材料、术前准备:1 mm与2 mm枪状咬骨钳、导丝、吸引器、Caspar撑开器、刮匙、高速磨钻、电刀、髓核钳、咬骨钳、剥离子、定位针头、苏州优贝特钛板、钛钉,厦门大博零切迹融合器。颈后路微型钛板、螺钉:由北京春立正达公司生产,钛板长、宽分别为27.7、7 mm,孔距12 mm,厚2 mm;螺钉长度6~8 mm,直径2.5~3 mm。术前3组均完善血常规、凝血功能、电解质等相关检查,行颈椎CT、MRI、颈椎正侧位与动力位片等影像学检查,进行术前访视,指导患者禁食禁水12 h,按照正常颈椎生理弧度进行头颈胸支具的取模与制作,常规备皮。
1.3.2 联合组:全麻,俯卧位,C臂机透视进行体表定位。常规消毒术区,经颈椎后正中做直行纵切口,逐层切开皮肤、皮下组织等,显露项韧带,由上至下纵行切开项韧带,保留棘间韧带,紧贴棘突、椎板进行剥离,显露颈椎后方棘突、椎板、双侧关节突关节,自动拉钩牵开。根据术前影像学检查,选取需行神经根加压的一侧或颈脊髓受压较重一侧为开门侧,对侧为铰链侧,沿铰链侧关节突内侧缘小心磨除颈椎椎板外层骨皮质,形成槽状,继续磨除开门侧椎板至神经剥离器探查仅剩薄层椎板内侧骨皮质。用薄型枪钳仔细咬除开门侧内层骨皮质,未开门节段与开门节段棘突之间的棘间韧带切断,小心掀起开门侧椎板,使颈椎后方椎板呈开门状。操作过程中,应用明胶海绵压迫椎管内静脉丛出血,视野清晰后,去除增生的黄韧带、骨赘等后方致压物,并咬除需减压的神经根管周围骨质,完成单侧神经根减压。置入铰链侧侧块螺钉,棘突上钻孔,经孔穿线缝合打结至侧块铆钉。或通过微型椎板钛板固定开门侧椎板、关节突,保持椎板稳定的开门状态。冲洗切口,确认无活动性出血,置管引流,关闭切口。
转换为平卧位,保持颈部后伸,消毒,做颈前右中横切口,依次切开皮肤与皮下组织,分离颈阔肌,沿颈阔肌深层向上、下锐性、钝性分离,保护颈内动静脉、气管、食管等,深筋膜显露后切开,达椎体。切开颈前疏松筋膜,C臂透视下插入定位针头,上下软骨终板、退变椎间盘刮除,切除椎体后缘骨赘与钙化椎间盘,充分减压后,放入融合器试模,合适后在减压间隙置入融合器,C臂透视确认位置满意。冲洗术野,止血,置管引流,逐层关闭切口。
1.3.3 前路组:给予前路手术治疗。仰卧位,取颈前横切口,经气管食管鞘与血管神经鞘间隙暴露椎体前方,C臂透视下,插入定位针头,若为单节段病变者,行单节段病变部位椎间盘切除手术;多节段病变者,则行多节段病变部位椎间盘切除术。伴有纵韧带骨化者,病变部位切除后,置入融合器行椎间融合,通过钛板固定。冲洗术野,止血,置管引流,逐层关闭切口。
1.3.4 后路组:给予后路手术治疗。俯卧位,颈后正中做切口,显露棘突,行后路单开门术,方法同联合组的后路方案,完成后冲洗术野,止血,置管引流,逐层关闭切口。
1.3.5 术后处理:3组术后均注意保持引流管通畅,并予以脱水、营养神经等对症治疗,术后48 h内予以抗生素预防感染,密切注意患者四肢活动情况,术后第2天指导患者在颈托保护下进行适当活动,当引流管量<20 mL时拔除,颈托固定时间为2~4周,嘱患定期复查。
1.4观察指标(1)比较3组手术一般情况。(2)比较3组术后1个月临床疗效:以神经功能改善情况评估疗效:优、良、中、差判断标准依次为术后JOA评分较术前降低>75%、50%~75%、25%~49%、<25%,优良率取优、良、中之和。(3)比较3组术前、术后1个月神经功能、颈椎功能障碍情况:依次通过JOA、颈椎功能障碍指数(NDI)评估,其中JOA总分17分,分值越高,神经功能越好;NDI指数取值范围0~100%,指数越高,颈椎功能障碍越严重。(4)比较3组术前、术后1个月颈椎稳定性指标:颈曲指数(CCI)、颈椎活动度(ROM)。CCI=(a1+a2+a3+a4)/A×100%,A线为C2、C7椎体后下缘连线,a1、a2、a3、a4分别为C3~6各椎体后下缘至A线的垂线;ROM=b1+b2,颈椎动力位片上C2、C7椎体后缘连线夹角,屈曲位夹角为b1,过伸位夹角为b2。(5)统计入组患者手术切除的椎间盘组织中白介素-1β(IL-1β)、肿瘤坏死因子-α(TNF-α)水平:术中切除标本用无菌生理盐水冲洗干净,吸干水分,每1 g组织中加10 mL磷酸盐缓冲液,匀浆机匀浆,3 000 r/min离心10 min,采用固相分离放射免疫分析法检测上清IL-1β、TNF-α表达,分析IL-1β、TNF-α与疗效相关性。
2 结果
2.1手术3组手术均顺利实施,术中未发生颈脊髓及神经根或血管损伤等并发症。3组手术时间、术中出血量、卧床时间、住院时间比较,差异具有统计学意义(P<0.05);联合组手术时间、术中出血量、卧床时间、住院时间较前路组、后路组高(P<0.05);前路组、后路组手术时间、术中出血量比较,差异无统计学意义(P>0.05);后路组卧床时间、住院时间长于前路组(P<0.05)。见表2。
表2 3组手术一般情况比较±s)
注:与前路组、后路组相比,*P<0.05
2.2疗效3组优良率比较,差异具有统计学意义(P<0.05);联合组优良率高于前路组、后路组(P<0.05);前路组、后路组优良率比较,差异无统计学意义(P>0.05)。见表3。

表3 3组疗效比较 [n(%)]
注:与前路组、后路组相比,*P<0.05
2.3神经功能、颈椎功能障碍情况3组术前JOA评分、NDI指数比较,差异无统计学意义(P>0.05);3组术后1个月JOA评分、NDI指数比较,差异具有统计学意义(P<0.05);联合组术后1个月JOA评分高于前路组、后路组,NDI指数低于前路组、后路组(P<0.05);前路组、后路组术后1个月JOA评分、NDI指数比较,差异无统计学意义(P>0.05)。见图2。

图1 患者男,62岁,前后手术,颈椎前后路-后路单开门前路零切迹 A、B:术前X线片;C、D:术后颈椎X线片Figure 1 Patient male,62 years old,before and after surgery,anterior and posterior approach to the cervical spine with a single open anterior approach with zero notch.A,B:Preoperative X-rays;C,D:Postoperative cervical X-rays
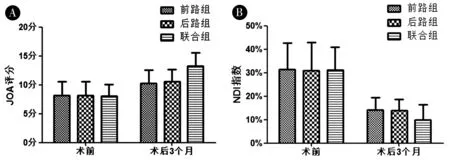
图2 A:3组JOA评分比较;B:3组NDI指数比较Figure 2 A:3 Comparison of JOA scores;B:Comparison of three groups of NDI indices
2.4CCI、ROM3组术前CCI、ROM比较,差异无统计学意义(P>0.05);3组术后1个月CCI、ROM比较,差异具有统计学意义(P<0.05);联合组、后路组术后1个月CCI、ROM与术前相比,差异无统计学意义(P>0.05);前路组术后1个月CCI、ROM较术前低(P<0.05);联合组、后路组术后1个月CCI、ROM高于前路组(P<0.05);联合组、后路组术后1个月CCI、ROM比较,差异无统计学意义(P>0.05)。见表5。
2.5IL-1β、TNF-α入组96例患者椎间盘组织中IL-1β表达量为(14.44±4.51)pg/mL,TNF-α表达量为(18.19±5.03)pg/mL。采用Pearson进行相关性分析发现,椎间盘组织中IL-1β、TNF-α与疗效呈负相关关系(r1=-0.314,P1=0.002;r2=-0.334,P2=0.001)。见图3。
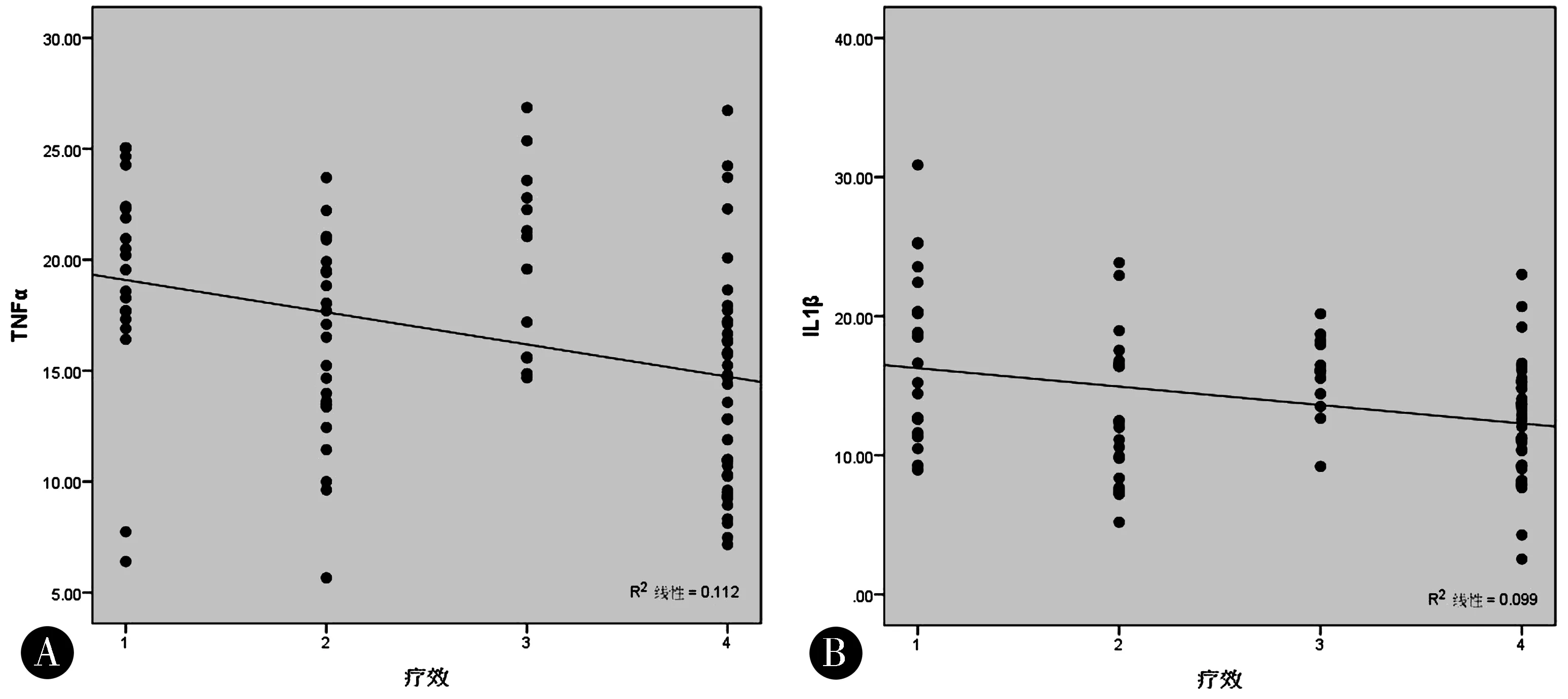
图3 椎间盘组织中IL-1β、TNF-α与疗效的相关性Figure 3 Correlation between IL-1β,TNF-α and efficacy in intervertebral disc tissue
3 讨论
CSM约占全部颈椎病的9%,髓核向后突出,压迫脊髓,可影响四肢感觉、活动、大小便等,且在病程中,由于椎间隙降低,突出的髓核刺激后方变得松弛的韧带,可造成韧带增生、变厚、失去弹性,并突入椎管,加重对脊髓的压迫,一旦出现严重的临床症状,则难以逆转病情进展,因此对符合手术指征患者给予及时、恰当手术治疗意义重大[10-11]。
前路手术适用于病变累及1~2个节段,脊髓压迫来自增厚或出现骨化的后纵韧带、前方退变的椎间盘组织等,能直接清除致压物,消除脊髓的动态压迫,并可于椎间隙植骨融合,通过恢复椎间高度,解除前后方致压物对颈脊髓的压迫,稳定椎体[12-13]。LI等[14]报道指出,CSM采用前路手术治疗,患者JOA评分可得到改善。但由于前路手术操作空间狭小,当病例发生硬脊膜囊与致压物黏连,可增加脑脊液漏、术后双下肢肌力降低的概率[15-16]。而后路手术适应于病变累及多个节段、伴有椎管狭窄患者,能直接显露神经组织,允许术中直接松解神经根周围的黏连、压迫,并扩大椎间孔[17-18]。ZHOU 等[19]报道显示,后路手术治疗CSM可改善患者神经功能。但后路手术减压不彻底[20]。因此本研究联合应用前后路一期手术,结果显示联合组术中出血量、住院时间、卧床时间、手术时间较前路组、后路组高,与BADHIWALA 等[21]研究相符,考虑与一期前后路联合手术同时行前路、后路手术增加了创伤与操作难度有关。同时联合组优良率、术后1个月JOA评分高于前路组、后路组,NDI指数低于前路组、后路组(P<0.05),表明一期前后路联合手术治疗CSM,可改善患者神经功能,提高患者颈椎功能,疗效显著。ZAVERI 等[22]研究显示,前后路联合手术时间、失血量较单纯前路、后路手术高,但神经功能改善率为83.37%,高于单纯前路的64.13%、后路的76.6%,支持本研究结论,但具体数据存在异质性,可能与纳入病例数及其病情不同有关。
表5 3组CCI、ROM比较±s)
一期行前后路联合手术有以下优点:(1)对不稳定的颈椎节段前后方能同时实施治疗,避免了单纯后方或前方无法同时重建后结构、前柱稳定的不足[23];(2)能同时对颈脊髓彻底减压,最大程度减少脊髓神经功能损害[24];(3)能避免分期手术病程较长的缺点,亦能减少脊髓继发性损伤的风险[25]。但前后路联合手术实施时,由于颈椎管狭窄,术中可能造成脊髓损伤,可先行后路手术,利用脊髓向后方的漂移效应减轻来自前方的压迫,再同期行前路手术,由于椎管扩大,为脊髓向后漂浮提供了空间,使手术危险性大大降低,因此具有可行性与有效性。同时本研究还发现,联合组、后路组术后1个月CCI、ROM与术前相比,差异无统计学意义(P>0.05),而前路组术后1个月CCI、ROM较术前丢失(P<0.05),提示前路手术可造成CCI、ROM丢失,而后路手术、前后路联合手术具有优势。YANG 等[26]采用颈椎前路椎体切除与融合术治疗CSM,发现术后患者颈椎运动范围在屈曲、伸展、左右侧屈、左右旋转方面分别平均丢失9.8%、28.5%、8.9%、9.9%、10.6%、7.8%,与后路手术的3.5%、16.4%、3.2%、6.3%、7.0%、5.7%相比,明显较高,提示前路手术可导致明显的颈椎运动范围丢失,与本研究结论相符。
有研究指出,退变颈椎间盘中炎症反应在CSM发病中起到重要作用,其中IL-1β是白介素家族成员之一,可通过致炎,广泛参与人体组织破坏、水肿等病理过程[27]。TNF-α有炎症介质作用,参与机体炎症反应[28]。研究指出,CSM患者颈椎间盘髓核组织中TNF-α、IL-1β表达高于单纯颈椎骨折或骨折合并脱位患者,并与CSM发生具有相关性[29]。研究发现,颈椎前路手术治疗CSM,可降低TNF-α水平,并伴有临床症状体征的缓解[30]。可见IL-1β、TNF-α等细胞因子调控了椎间盘退变的进展,但现阶段颈椎间盘髓核组织中IL-1β、TNF-α表达与手术疗效的关系尚不明确。本研究创新性探讨发现,椎间盘组织中IL-1β、TNF-α与疗效呈负相关关系(P<0.05),提示检测椎间盘髓核组织中IL-1β、TNF-α表达可预测手术疗效,为临床决策提供参考。值得注意的是,一期前后路联合手术由于手术时间较长,出血量增加,术前应全面评估患者一般情况,明确对手术的耐受性,且行后路术时,不仅应保证减压的范围,亦应注意适度,尤其是向两侧减压时,至侧块、椎板交接位置即可,可避免根性牵拉痛的发生,同时术中需转换体位,应做好头颈部的固定工作,防止对脊髓造成继发损伤。
一期前后路联合手术治疗CSM,可改善患者神经功能,提高患者颈椎功能与稳定性,疗效显著,且检测椎间盘髓核组织中IL-1β、TNF-α表达可预测手术疗效,为临床决策提供参考。
