基于气相色谱的植物油特征脂肪酸高温热氧化特性研究
2019-01-23刘元法李进伟
刘 剑,刘元法,李进伟
(江南大学 食品学院,食品科学与技术国家重点实验室,江苏 无锡214122)
油脂因其能够提供高热值和人体组织发育必需的脂肪酸,在人类饮食中起着至关重要的作用。在食品生产加工过程的许多高温处理过程中,植物油会产生许多工业所需要的颜色、风味和成分的变化,但同时脂质热氧化也是导致营养损失、油质劣化,甚至有毒有害化合物产生的主要原因[1-5]。
植物油在高温下的热氧化过程要比自动氧化复杂得多,现有植物油热氧化机制多是建立在动力学基础上,通常根据反应物(如氧气等)的消耗、特征产物(如氢过氧化物、丙二醛等)的生成,对可能的氧化反应进程进行推断。但植物油氧化反应体系实际上复杂且多变,加成、脱氢、裂解反应相互竞争会改变氧化路径和中间产物[6]。由于油脂体系的复杂性,使得直接研究植物油高温热氧化的进程变得比较困难,而植物油的基本组成——甘油三酯和脂肪酸则在结构体系上相对简单。相较于植物油中甘油三酯组成复杂程度,脂肪酸的组成能够更简单直接地反映植物油组成情况。并且,关于植物油热氧化稳定性,许多研究人员都得出相同的结论:不同种类植物油热氧化稳定性与其脂肪酸组成有直接密切的关系[1,2,6-9]。还有研究人员进一步提出了植物油氧化稳定性和自身脂肪酸组成之间关系的量化模型、预测模型,其中Kerrihard等[1]的研究表明植物油氧化稳定性与其主要脂肪酸组成之间有极强的相关性(R=0.915)。Redondo-Cuevas等[10]的研究结果表明几种主要的饱和脂肪酸、单不饱和脂肪酸、双不饱和脂肪酸、多不饱和脂肪酸对植物油氧化稳定性的贡献率达到67%。因此,植物油的氧化进程、氧化特性与其主要组成的脂肪酸息息相关,组成植物油主要的脂肪酸在高温条件下的氧化模型、氧化特性、稳定性的研究,对揭示复杂的植物油体系热氧化进程有着指导作用。由此可以推测植物油和其组成中的主要脂肪酸在热氧化动力学模型和参数上也可能存在较好的相关性,甚至由脂肪酸体系到复杂植物油体系,在氧化稳定性等特性方面可能存在一定的预测性,但关于植物油基本组成脂肪酸的氧化进程、氧化特性方面的研究报道甚少。
许多相关研究表明常用植物油脂肪酸组成中含量最高的是棕榈酸、油酸、亚油酸、亚麻酸[1,11-12]。因此,本研究着眼于植物油煎炸等高温处理过程,将反应理想化为高温、无催化剂、氧气充足条件下的氧化过程,以组成常用植物油的4种主要脂肪酸棕榈酸、油酸、亚油酸、亚麻酸为研究对象,分析其在不同的高温条件下(120、140、160、180℃)的热氧化过程,建立动力学模型,并对动力学参数进行求解,分析特征脂肪酸氧化特性,为甘油三酯、植物油体系高温热氧化进程的动力学研究提供支持,为揭示植物油与其本身脂肪酸组成之间的关系奠定基础。另一方面,通过对植物油特征脂肪酸热氧化特性的研究,可以对不同种类植物油在实际加工过程中的高温氧化进行预估,对氧化控制提供指导。
1 材料与方法
1.1 试验材料
棕榈酸、油酸、亚油酸、亚麻酸,均购于百灵威官网,为色谱纯。三氟化硼乙醚溶液(分析纯),甲醇溶液(分析纯),正己烷(分析纯、色谱纯),脂肪酸甲酯混标,二十一碳烷酸甲酯(色谱纯),氯化钠,去离子水。
热氧化发生装置(自制);数显恒温油浴锅,氢火焰离子化检测器自动进样气相色谱仪(Shimadzu GC-2010PLUS,日本),离心机,分析天平,数显恒温水浴锅,离心管,滤膜,注射器。
1.2 试验方法
1.2.1 模拟热氧化
将50 g脂肪酸样品放入内径5 cm、高度15 cm的厚壁玻璃试管内,通过试验用氧气瓶提供30 mL/min 的稳定氧气流,吹扫容器中样品表面。厚壁试管置于自动数显恒温油浴锅中持续加热,通过控制反应温度使试样加速氧化,恒温油浴锅温度设置分别为120、140、160、180℃。定时取样,对每种脂肪酸分别间隔0、1、2、3 ……12 h取样,迅速对所取样品进行冰浴冷却。
1.2.2 底物残余量测定
对1.2.1保存的样品及时进行甲酯化操作,方法参照GB/T 17377—2008《动植物油脂 脂肪酸甲酯的气相色谱分析》,随后以二十一碳烷酸甲酯为内标物,利用气相色谱分别测定120、140、160、180℃恒温加热条件下,不同时间点试样热氧化后的底物残余量。
气相色谱条件:TR-FAME 260M154P色谱柱(60 m×0.25 mm,0.25 μm);程序升温为60℃保持3 min,以5℃/min升至175℃,保持 15 min,以2℃/min 升至220℃,保持10 min;载气为高纯氮气;分流比100∶1;进样量1 μL;进样口温度250℃;检测器温度250℃。
2 结果与讨论
2.1 底物残余量分析
采用内标法用气相色谱仪对试样中的脂肪酸残余量进行定量检测,绘制出不同底物不同温度恒温热氧化降解过程。图1为棕榈酸、油酸、亚油酸、亚麻酸在120、140、160、180℃恒温加热条件下的残余量变化曲线。由图1可知,在120、140、160、180℃恒温加热条件下,所有的脂肪酸试样都发生了显著的氧化降解,且随着恒温热处理温度升高,氧化程度不断加深。对于同一种脂肪酸试样,随着恒温热处理的温度升高,底物发生氧化降解反应的进程也存在显著差异,整个反应的平均速率随着温度升高而显著提高;不同温度下反应速率均符合先增后减再缓慢增加的趋势,但在较低温度下出现反应速率减缓的“台阶”过程更加显著。此外,在同一温度下,不同的脂肪酸发生氧化降解的进程和反应速率也存在显著差异,不饱和度越高的脂肪酸起始氧化速率和平均降解速率越快,这是由于脂肪酸碳链不饱和键的热氧化稳定性决定的,即在相对分子质量接近的情况下,随着不饱和度的增加,脂肪酸氧化稳定性降低[13]。利用Origin 7.5软件对不同温度下的4种脂肪酸残余量(cA)随加热时间(t)变化过程进行多项式拟合,结果见表1。由表1可知,多项式拟合结果均为极显著,且相关性均高于0.99。
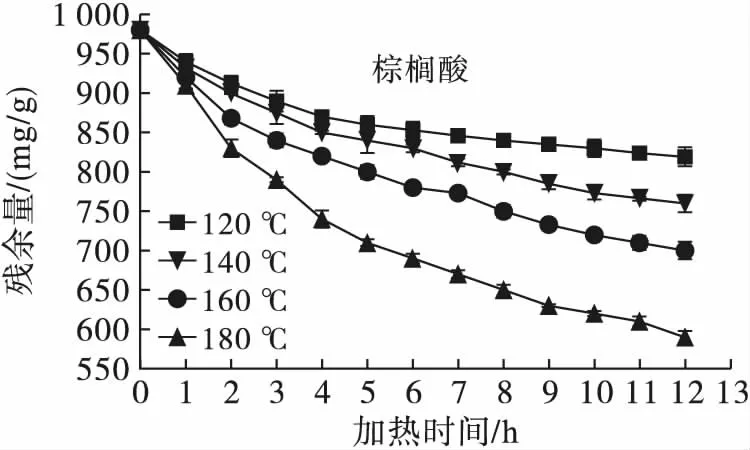
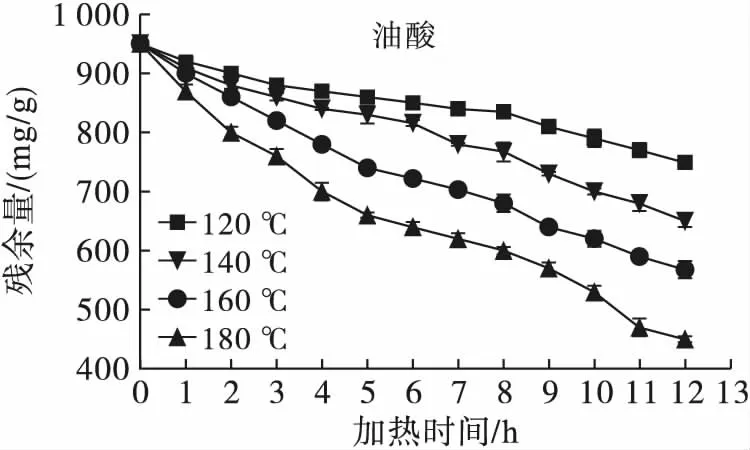
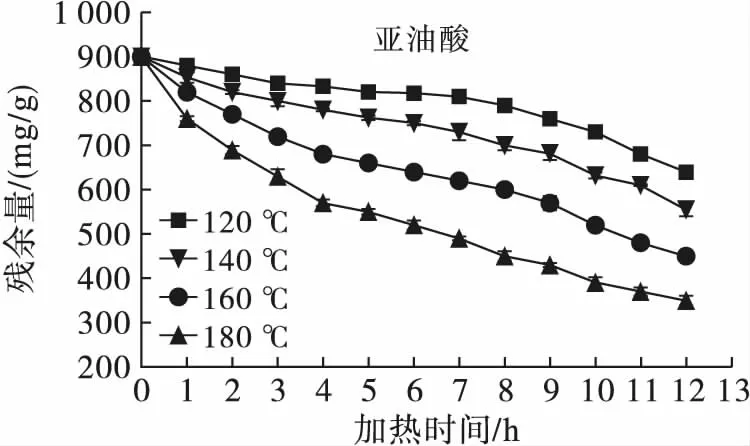

图1 4种脂肪酸在不同温度下的热氧化降解曲线

试样温度/℃回归方程R2棕榈酸120cA=-0.166t3+4.299t2-41.122t+978.6910.999140cA=-0.139t3+3.699t2-42.736t+975.0510.996160cA=-0.215t3+5.435t2-57.555t+973.7520.995180cA=-0.280t3+7.812t2-86.104t+981.5400.998油酸 120cA=-0.194t3+3.417t2-30.009t+948.0230.996140cA=-0.137t3+2.198t2-31.586t+943.0330.994160cA=-0.138t3+3.475t2-53.979t+951.1700.998180cA=-0.437t3+9.341t2-91.816t+951.4810.996亚油酸120cA=-0.322t3+4.466t2-29.577t+901.6930.996140cA=-0.302t3+4.879t2-43.625t+895.3800.997160cA=-0.446t3+8.889t2-80.613t+896.3530.997180 cA=-0.459t3+11.157t2-113.171t+882.1620.994
续表1

试样温度/℃回归方程R2亚麻酸120cA=-0.257t3+4.877t2-44.271t+698.7010.991140cA=-0.296t3+6.042t2-57.721t+696.2100.995160cA=-0.161t3+3.844t2-59.661t+689.7160.997180cA=-0.253t3+7.953t2-101.790t+686.4100.996
2.2 动力学参数计算及热氧化模型建立
利用表1中对不同脂肪酸试样在不同温度下热氧化过程的拟合方程,采用化学动力学的分析方法,对整个氧化反应的反应级数进行确定。高温下脂肪酸氧化的过程可以简化为氧气与脂肪酸发生反应,生成一种氧化产物的过程,其宏观反应速率方程为:
(1)
式中:rA为化学反应速率;k为反应速率常数;cA为脂肪酸试样的瞬时残余量;cB为反应过程中氧气的质量浓度;n、m分别表示反应底物脂肪酸和氧气的反应级数。
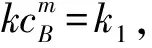
(2)
此外,整个反应的速率可以用任意时刻t及其对应的反应体系中的脂肪酸残余量cA来表示:
(3)
对方程(3)两边取自然对数得:
ln(-dcA/dt)=nlncA+lnk1
(4)
由方程(4)可知,ln(-dcA/dt)与lncA呈现线性关系。结合表1各种脂肪酸在不同温度下的氧化降解过程的多项式拟合方程,并对各自不同条件下的拟合方程进行求导,可分别求出0、1、2……12 h所对应的ln(-dcA/dt)与lncA数值,将所得数据绘图,进行线性拟合,可得到一条直线。4种脂肪酸在不同温度下的化学反应级数n和反应速率常数k1可分别通过该直线的斜率n和截距lnk1求得,计算结果见表2。

表2 棕榈酸、油酸、亚油酸、亚麻酸在不同温度条件下热氧化过程的动力学参数
化学反应速率常数其数值表示相当于参加反应的物质都处于单位浓度(1 mol/L)时的反应速率,受温度、催化剂、反应物表面性质的影响。由表2可知,4种脂肪酸的反应速率常数随不饱和度的增加而增大,且对于同一种脂肪酸其反应速率常数,随温度升高而增大。说明随着不饱和度的增加,整个反应的速率加快,随着温度上升,脂肪酸氧化反应速率加快,且都存在数量级的差距,说明不饱和度和反应温度对脂肪酸热氧化反应速率有显著影响。在植物油的应用过程中应该更加注重高不饱和脂肪酸的影响,需高温处理的过程建议选用饱和脂肪酸含量较高的植物油。对于高不饱和脂肪酸含量高的植物油,则需要严格控制温度,这一点可结合Chen等[14]的研究建议:通过研究棕榈酸的热氧化自由基变化过程,确定了氧化速率突变的温度点为175℃,从而建议高棕榈酸含量的植物油最高加工温度不宜超过175℃,其他种类植物油可以参照此法找到适宜的加工温度。同时,在抗氧化剂的添加上,应该着重添加对不饱和脂肪酸含量高的植物油氧化酸败抑制效果好的抗氧化剂,以及充分利用多种抗氧化剂复配效果的优势[15]。比较相同温度下不同脂肪酸氧化的反应速率常数可知,棕榈酸与油酸的反应速率常数、亚油酸与亚麻酸的反应速率常数差距较大,温度每升高20℃,反应速率常数相差近105倍;而油酸与亚油酸之间反应速率常数的差距较小,温度每升高20℃,反应速率常数相差约102倍。比较同一脂肪酸在不同温度下的反应速率常数变化可知,不饱和度越高,温度对其反应速率的影响越大。由此可见,在对植物油热氧化进行控制时,高不饱和脂肪酸含量越高的植物油,对温度的控制更显重要。
2.3 氧化稳定性评价
对Arrhenius方程k=Aexp(-Ea/RT)的两边取对数得:
lnk=-Ea/RT+lnA
(5)
式中:k为反应速率常数;Ea为活化能;R为理想气体常数;T为温度;A为指前因子。由方程(5)可知,lnk与1/T呈线性相关关系,根据4个不同温度下得到的速率常数,以lnk对1/T进行线性回归分析,结果见图2。

图2 4种脂肪酸热氧化过程中lnk对1/T的线性回归分析
由图2可知,4种脂肪酸高温条件下热氧化过程的lnk对1/T的线性相关性均较好,其中棕榈酸、油酸、亚油酸线性回归分析显示其P值均小于0.01,呈极显著线性关系,亚麻酸热氧化过程中lnk对1/T的线性回归分析P值为0.018 5,呈显著的线性关系。依据方程(5),根据其直线斜率-Ea/R和截距lnA,可计算出4种脂肪酸热氧化降解反应活化能Ea和指前因子A(见表3)。由表3可以看出,棕榈酸、油酸、亚油酸、亚麻酸的氧化活化能Ea依次降低,即发生氧化降解所需要的能量越来越低,因此可以得出热氧化稳定性排序:棕榈酸 > 油酸 > 亚油酸 > 亚麻酸。Nik等[16]和Refaat[17]的研究得出了与此相同的结论,原因就在于4种脂肪酸的相对分子质量差异不大的情况下,不饱和度越高,碳碳共价键对温度越敏感,发生反应所需的最低能量越低。
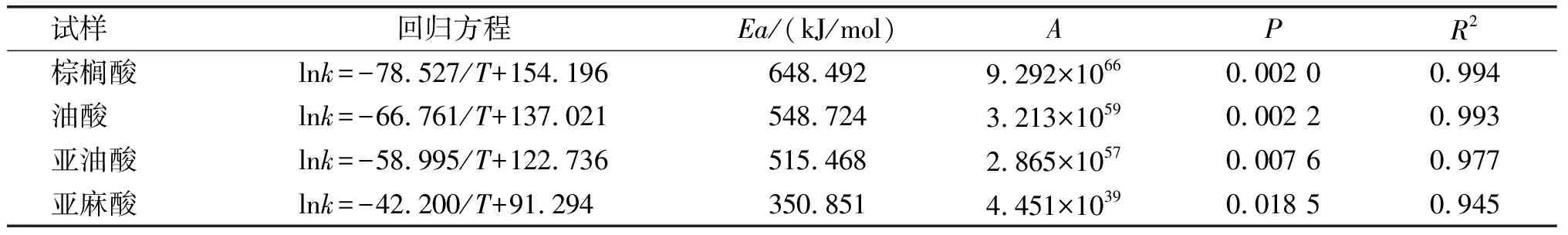
表3 棕榈酸、油酸、亚油酸、亚麻酸高温热氧化模型的氧化活化能(Ea)和指前因子(A)
3 结 论
(1)方法建立:利用自制模拟高温热氧化装置和气相色谱检测方法,结合微分动力学方程,能够很好地求解植物油特征脂肪酸高温热氧化过程的动力学参数和氧化降解模型。鉴于体系之间的相似性和相关性,这种方法可被推荐用于甘油三酯、植物油等体系热氧化反应动力学参数的求解和氧化反应进程模型的建立。
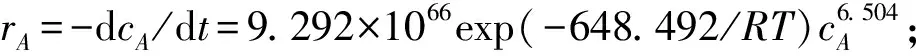
(3)热氧化特性:不同的热氧化模型及相应动力学参数(Ea、n、k),可用于比较不同种类脂肪酸的氧化特性。氧化活化能Ea能够很好地反映不同试样的氧化稳定性,随着不饱和度的升高,4种脂肪酸氧化活化能降低,即氧化稳定性降低;不饱和度越高,脂肪酸热氧化受浓度的影响越小,因此植物油中占一定比例的高不饱和度脂肪酸是决定其氧化稳定性的关键,在热氧化控制中应该着重控制高不饱和度的脂肪酸氧化进程。同时,不饱和度越高,温度对其反应速率的影响越大。由此可见,在对植物油热氧化进行控制时,高不饱和脂肪酸含量越高的植物油,对温度的控制和抗氧化剂的使用更显重要。本研究能够为植物油煎炸等高温处理条件下的氧化控制提供指导,对复杂体系的植物油热氧化过程、氧化降解模型、氧化特性、热氧化稳定性的研究提供支持。结合此研究的结果,以不同植物油为研究对象进行相关研究,将有助于反映植物油热氧化和基本脂肪酸组成之间的关系,进一步揭示植物油体系热氧化的过程及特性。
