免疫透射比浊法自建检测系统钩状效应性能确认方法的建立
2019-01-10李明洋
夏 勇, 薛 灏, 李明洋, 纪 玲
(北京大学深圳医院检验科,广东 深圳 518036)
《医学实验室质量和能力认可准则》(ISO 15189:2012)[1]要求实验室应对非标准方法检验程序进行确认,方法确认应尽可能全面,并通过客观证据,即性能特征形式,来证实满足检验预期用途的特定要求。然而,目前我国针对临床化学自建检测系统精密度、正确度、准确性、分析测量范围和临床可报告范围等性能确认的具体方法尚未达成共识,针对免疫透射比浊法检测项目钩状效应的性能确认方法就更不多见了。本研究通过对3种非配套IgG试剂的比较,探讨免疫透射比浊法自建检测系统钩状效应的性能确认方法。
1 材料和方法
1.1 样本
收集北京大学深圳医院住院患者检测后的剩余血清,置于-20℃冰箱内保存、备用,制备高浓度及低浓度IgG样本。
1.2 仪器与试剂
AU5400全自动生化分析仪及IMMAGE 800特定蛋白分析仪(美国Beckman-Coulter公司)。3种非配套免疫透射比浊法IgG试剂盒[试剂A(上海科华生物工程股份有限公司)、试剂B(北京利德曼生化股份有限公司)、试剂C(德国德赛诊断系统有限公司)]及配套校准品。IMMAGE 800特定蛋白IgG试剂盒及配套校准品。
1.3 方法
1.3.1 仪器参数设置 3种非配套IgG试剂上机参数按各厂家说明书要求进行设置,见表1。

表1 3种非配套IgG试剂的上机参数
1.3.2 不同浓度IgG样本的制备和检测 采用IMMAGE 800特定蛋白分析仪对高浓度及低浓度IgG样本进行检测。3次检测结果的平均值即为高浓度及低浓度样本的理论浓度(H:70.0 g/L、L:5.5 g/L)。采用AU5400全自动生化分析仪检测18个浓度梯度的IgG样本:0(生理盐水)、0.5L、L、0.1H、0.2H、0.3H、0.4H、0.5H、0.6H、0.7H、0.8H、0.9H、H、1.5H、2H、3H、4H、5H。所有样本重复检测3次,记录检测结果、反应A值以及各反应测定点的A值。
1.3.3 Heidel-berger曲线的绘制及安全范围的比较 绘制3种非配套IgG试剂理论浓度和实测浓度的Heidel-berger曲线,比较不同试剂Heidelberger曲线的平衡点及安全范围。
1.3.4 钩状效应的识别和确认 对AU5400全自动生化分析仪钩状效应识别参数Check Point 1~3(CP1~3)、Limit Point 1~2(LP1~2)、Decision Value 1~3(DV1~3)8个参数进行设置。比较不同浓度梯度IgG样本的时间-反应曲线特征,对钩状效应5个监测时间节点进行设定。CP1和CP3分别为反应起始点和终点,CP2是抗原抗体反应速率最快点;LP1为反应起始点,LP2为钩状效应发生时A的峰值点。叠加不同浓度抗原的时间-反应曲线,形成剂量-反应曲线,比较从抗原适量到过量的过程中快速反应期内A值变化速率及峰值上升幅度的差异,设定钩状效应的3个判定值。钩状效应判定公式1要求DV1≤(CP2-CP1)/(CP3-CP1)≤DV2,绘制反应速率比与浓度的变化关系图,以CP2反应完成速率的差异来判断钩状效应是否存在;钩状效应判定公式2要求LP2-LP1≥DV3,绘制A峰值上升幅度与浓度的变化关系图,必要时以LP2 A峰值上升幅度来区分低浓度反应和钩状效应。
1.3.5 识别参数的确认 重新检测18个浓度梯度的IgG样本,对钩状效应识别参数进行确认。
2 结果
2.1 Heidel-berger曲线及相关参数
针对抗原过量的情况,试剂C的综合性能优于试剂A,试剂A的综合性能优于试剂B。见图1、表2。

图1 3种非配套IgG试剂的Heidel-berger曲线
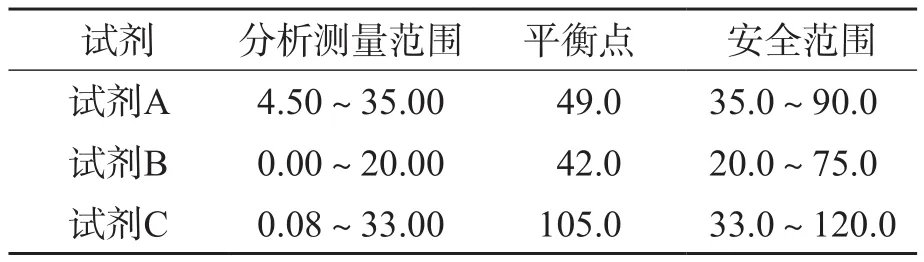
表2 3种非配套IgG试剂Heidel-berger曲线相关参数比较 (g/L)
2.2 剂量-反应曲线特征
试剂A低浓度区A峰值低,在反应曲线中间区段(18~20点)达到反应平衡;随着浓度升高A峰值逐渐上升,A值在反应终点前区段(25~27点)仍随着时间的延长缓慢上升,且浓度越高,表现越明显;当出现钩状效应时,A峰值下降,在反应终点前仍缓慢上升,与低浓度反应曲线交织在一起。试剂B的A峰值较试剂A低,在正常浓度范围内,反应曲线前区段(12~15点)即达到反应平衡;出现钩状效应时的剂量-反应曲线与试剂A相似。试剂C在正常浓度范围内的剂量-反应曲线与试剂B相似,随着浓度的升高A峰值上升,较试剂B更加明显;当出现钩状效应时,IgG浓度达到210 g/L之前A峰值继续上升,即使IgG浓度达到350 g/L,A峰值仍保持在高位;当发生钩状效应时,A值在12~14点到达峰值后迅速下降,出现特征性“钩状效应拐点”。见图2。

图2 3种非配套IgG试剂的剂量-反应曲线
2.3 钩状效应的识别参数和确认结果
3种非配套IgG试剂在10~11点加完试剂2后,A值均迅速上升,试剂A、试剂B、试剂C抗原抗体反应速率最快区间分别为10~12、10~12和10~11点,分别作为各自的CP1、CP2,将27点即CP3设定为反应终点。当发生钩状效应时,试剂A、试剂B A峰值出现在27点,试剂C A峰值出现在13点。试剂A通过公式1的反应速率比0<(A12-A10)/(A27-A10)<0.6即可区分是否存在钩状效应;试剂C与试剂A相似,存在抗原过量的钩状效应(A12-A10)/(A27-A10)>0.87;试剂B从抗原适量到过量的过程中,无论是快速反应期内的A值变化速率还是A峰值上升幅度的差异均未得到有效区分,钩状效应的识别浓度范围尚未超出其安全范围。设定上述钩状效应的识别参数后,重新检测18个浓度梯度的IgG样本,再次确认,得到3种非配套IgG试剂(试剂A、试剂B、试剂C)钩状效应报警的浓度范围分别为49~350、28~70、42~350 g/L。见表3、图3、图4。

表3 3种非配套IgG试剂钩状效应识别参数的比较

图3 3种非配套IgG试剂反应速率比与浓度变化的关系
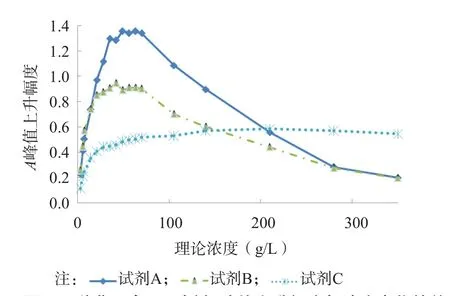
图4 3种非配套IgG试剂A峰值上升幅度与浓度变化的关系
3 讨论
免疫透射比浊法定量检测的原理是当抗原与抗体比例合适时,A值会出现随着抗原浓度的上升而上升的现象。实验室通过分析测量范围确认试验,可发现高浓度区域的线性偏离以及抗原过量等问题。一旦样本中抗原浓度继续升高,超出其安全范围,就会出现钩状效应,导致无任何报警提示的负偏差结果出现。即使在封闭的免疫透射比浊法特定蛋白分析仪上设置钩状效应检查程序,也会出现因抗原过量而导致结果假性偏低的情况发生[2-3]。由此可见,钩状效应是免疫透射比浊法与免疫散射比浊法共同面临的一个问题,钩状效应的确认是检测结果准确的质量保证[4]。
特定蛋白开放检测系统(非标准检验程序)通过分析测量范围确认试验,利用全自动生化分析仪上的“线性检测功能”,可发现高浓度区域线性偏离以及抗原过量问题。通过绘制Heidel-berger曲线,确定不同试剂反应的平衡点(A峰值对应的浓度为抗原过量拐点)、后带限(剂量-反应曲线右侧与分析测量范围上限A值相等的浓度点)及抗原过量的安全范围(分析测量范围上限至后带限之间),可反映各试剂中抗体的含量、亲和力及效价水平,并可有效评价特定蛋白检测试剂盒的综合性能。Heidel-berger曲线结果表明,适当降低分析测量范围上限,可有效扩大其安全浓度范围。如将本研究试剂C的分析测量范围上限从35 g/L下调至33 g/L,其安全范围上限可提升到120 g/L,即可基本满足临床上大多数IgG的病理浓度分布。进一步比较3种非配套IgG试剂的钩状效应剂量-反应曲线特征可发现有“峰降缓升”型和“峰高快降”2种类型。“峰降缓升”型具体表现为:剂量-反应曲线的A峰值明显下降,剂量-反应曲线与低浓度反应曲线交织在一起,但反应终点前A值仍缓慢上升。该型可利用A值在反应终点前的“缓升”与低浓度进行区分,并可利用A值“峰降”与正常高浓度进行区分,本研究中的试剂A、试剂B均为此型。“峰高快降”型具体表现为:剂量-反应曲线到达A峰值时间提前,A峰值保持在高位,A值到达峰值后快速下降,下降持续到终点前,本研究中试剂C为此型[5]。“峰高快降”型需将钩状效应判定公式2中的LP2设定在“钩状效应拐点”上,而非正常反应终点。
本研究通过对比不同试剂钩状效应识别参数发现,并不是所有试剂都能找到合适的报警阈值。试剂B可能因抗体的量或效价不足,当使用当前设置的报警参数时,并不能完全实现有效报警。因极端高浓度样本难以获取,故本研究以增加样本量的方式来建立报警参数,研究结果可能与真实的高浓度样本反应曲线特征存在一定的差异。此外,由于不同厂家的特定蛋白检测试剂盒之间存在一定的批间差,因此不同试剂批次之间可能会存在报警参数差异,故在识别参数建立过程中,可降低报警阈值,以提高敏感性。
本研究通过对3种非配套IgG试剂进行比较,初步探讨了免疫透射比浊法钩状效应性能确认方法,即绘制覆盖病理浓度范围的Heidelberger曲线,确定安全范围及平衡点;观察时间-反应曲线,确定A值到达峰值的时间点,通过抗原抗体快速反应期A值变化的速率,确定钩状效应的监测点;判断钩状效应剂量-反应曲线类型,比较从抗原适量到过量的过程中,快速反应期内A值变化速率、达到峰值时间及上升幅度的差异,确定钩状效应监测的判定值;模拟不同浓度的样本对自建检测系统钩状效应的识别参数进行确认,当涉及试剂批号改变时,需再次对设定参数进行验证。
