Cu2+对材料在海水中腐蚀行为的影响
2019-01-02成涛
,成涛, ,, ,
(1.台山核电合营有限公司,台山 529228; 2.苏州热工研究院电站寿命管理技术中心,苏州 215004)
SEC系统在核电运行系统中称为重要厂用水系统(也称为安全厂用水系统),其功能是在正常运行和事故工况条件下把与安全相关的构筑物、系统和部件传输来的热量通过SEC管道输送到最终热阱——海水。在现有核电站中,SEC管道多为不锈钢管道、碳钢加内衬(衬涂层、衬橡胶、衬塑料、衬水泥砂浆)管道以及对强度要求不高的树脂管道[1]。某些SEC管道在服役过程中添加含铜杀菌剂(为防止微生物腐蚀),或某些铜部件发生腐蚀等,都会造成SEC系统中局部Cu2+富集,并在管道、板式热交换器等构件表面析出Cu单质,Cu单质的析出一方面降低了热交换器的换热效率,另一方面加速了SEC管道的腐蚀,为核电站的安全运行带来潜在隐患。
目前,国内外学者对Cu2+作用下的腐蚀行为研究主要集中在非海水环境中Cu2+对钢[2-7]、铝合金[8-10]和690合金[11]的腐蚀影响上。 SEPULVEDA等[2]通过研究泥浆中溶解Cu2+对碳钢输送管道耐蚀性的影响发现碳钢腐蚀增重随着Cu2+含量的增加而增加,附着在管道表面Cu2+的还原是腐蚀加速的关键因素。QU等[3]采用电化学方法研究了双(环己酮)草酸二腙(BCO)和Cu2+对冷轧钢腐蚀行为的影响,发现Cu2+显著提高了BCO对冷轧钢腐蚀的抑制效率。SOARES等[8]研究了酸性介质中氯化物和Cu2+对易拉罐用铝材腐蚀性能的影响,发现Cl-和Cu2+的协同作用加速了铝罐的腐蚀进程。林震霞等[11]采用慢应变速率试验研究了国产690 合金在含有Cu2+和Cl-混合溶液中的应力腐蚀开裂(SCC)行为,结果表明在同时含有Cu2+和Cl-的介质中,国产690合金的SCC敏感性明显增加。目前,有关核电站二回路设备材料在含Cu2+海水环境以及在含Cu2+及Cu的氧化物介质中腐蚀行为的研究报道较少。因此,本工作以SEC管道常用材料A106B碳钢和304L不锈钢为研究对象,采用浸泡试验和动电位极化曲线法研究了这两种材料在含Cu2+海水中的腐蚀电化学行为,探索了其在含Cu2+海水中的腐蚀电化学规律和腐蚀机理,以期为电站SEC管道服役期间的腐蚀预防和修复提供一定的理论依据和指导。
1 试验
1.1 试样
试验材料是市售A106B碳钢和304L不锈钢,其化学成分见表1,金相组织见图1。由图1可见:A106B碳钢的金相组织为铁素体+珠光体组织;304L不锈钢的金相组织为典型的奥氏体组织,并有一定量的孪晶。
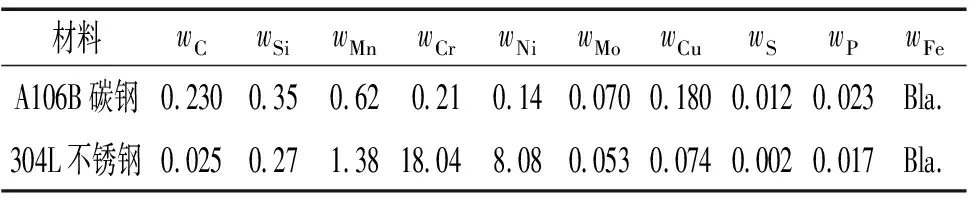
表1 试验材料的化学成分Tab.1 Chemical composition of test materials %

(a) A106B (b) 304L不锈钢图1 试验材料的金相组织Fig.1 Microstructure of the tested materials
浸泡试验用试样尺寸为20 mm×20 mm×3 mm,试验前用砂纸(200~800 号)逐级打磨试样表面,然后用去离子水、丙酮和无水乙醇清洗后吹干,称量并测量尺寸后待用。电化学试验用试样尺寸为10 mm×10 mm×3 mm,背面焊接Cu导线,保留10 mm×10 mm工作面,非工作面用环氧树脂包封,试验前用砂纸(200~800 号)逐级打磨试样表面,然后用去离子水、丙酮和无水乙醇清洗后吹干待用。
1.2 试验方法
1.2.1 浸泡试验
浸泡试验用溶液为含不同量Cu2+的人造海水,人造海水成分如表2所示,Cu2+加入量分别为0,10,50,100,500,1 000 mg/L。试验时间为7 d,试验温度为50 ℃。浸泡试验结束后取出试样并清洗、烘干后称量,计算平均腐蚀速率,同时观察试样的宏观和微观腐蚀形貌。

表2 人造海水的成分Tab.2 Composition of artificial seawater (g·L-1)
1.2.2 电化学试验
动电位极化曲线测试在CS310电化学工作站上完成,采用经典三电极体系,工作电极为试样,参比电极为饱和甘汞电极(SCE),辅助电极为Pt电极。试验溶液同浸泡试验用溶液,试验温度为室温。将工作电极静置于试验溶液中30 min后,以20 mV/min的扫描速率进行动电位极化曲线测试,扫描范围为开路电位(OCP)-0.2 V至阳极电流密度大于500 μA/cm2。
2 结果与讨论
2.1 宏观腐蚀形貌
由图2可见:A106B碳钢试样在含不同量Cu2+的人造海水的腐蚀形貌为均匀腐蚀;在无Cu2+的人造海水中腐蚀后,试样表面平整,加入Cu2+后,试样表面平整度下降,出现很浅的点状小腐蚀坑,随着Cu2+含量的升高,小腐蚀坑逐渐密集,并伴有黄褐色的腐蚀产物附着。

(a) 0 mg/L (b) 10 mg/L

(c) 50 mg/L (d) 100 mg/L
由图3和图4可见:304L不锈钢试样在未添加和添加10 mg/L Cu2+的人造海水中浸泡7 d后,试样表面仍保持金属光泽,肉眼未发现明显的点蚀坑;在含50~1 000 mg/L Cu2+的人造海水溶液中腐蚀7 d后,试样表面均出现点蚀坑,且随着溶液中Cu2+含量的升高,点蚀变得严重;在含500 mg/L Cu2+的人造海水中腐蚀后7 d后,最大点蚀深度约为1 000 μm,在含1 000 mg/L Cu2+的人造海水中腐蚀后7 d后,最大点蚀深度约为1 500 μm。
2.2 腐蚀速率
由图5可见:随着试验溶液中Cu2+含量的升高,碳钢试样的腐蚀速率增大。在无Cu2+的人造海水中,碳钢试样的腐蚀速率为0.163 g/(m2·h),试验溶液中加入10 mg/L Cu2+后,碳钢试样的腐蚀速率为0.200 g/(m2·h),较无Cu2+时的增大23%;当溶液中Cu2+含量分别增至50,100,500,1 000 mg/L时,碳钢试样的腐蚀速率较无Cu2+时的增大97%,1 214%,412%和847%。

(a) 0 mg/L (b) 10 mg/L

(c) 50 mg/L (d) 100 mg/L

(e) 500 mg/L (f) 1 000 mg/L图3 不锈钢试样在含不同量Cu2+的人造海水溶液中腐蚀7 d后的表面腐蚀形貌Fig.3 Surface corrosion morphology of stainless steel samples after corrosion in artificial seawater containing different content of Cu2+ for 7 d
由图6可见:在无Cu2+的人造海水溶液中浸泡后,304L试样的腐蚀速率很低,仅为0.001 2 g/(m2·h),溶液中加入10 mg/L Cu2+后,304L试样的腐蚀速率为0.008 3 g/(m2·h) ,是无Cu2+时的6.9倍;当溶液中Cu2+含量分别增至50,100,500,1 000 mg/L时,304L试样的腐蚀速率分别是未添加Cu2+时的68.4,140,405,592倍。可见,Cu2+的存在极大地提高了304L不锈钢的在海水中的腐蚀速率。
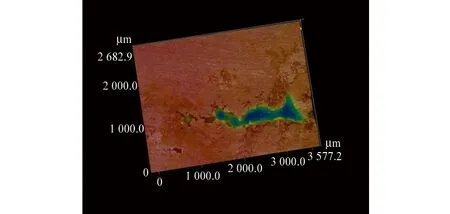
(a) 500 mg/L

(b) 1 000 mg/L图4 不锈钢试样在含500 mg/L和1 000 mg/L Cu2+的人造海水中腐蚀后点蚀坑的三维形貌Fig.4 Three-dimensional morphology of pitting pits of stainless steel samples after corrosion in artificial seawater containing 500 mg/L (a) and 1 000 mg/L (b) Cu2+
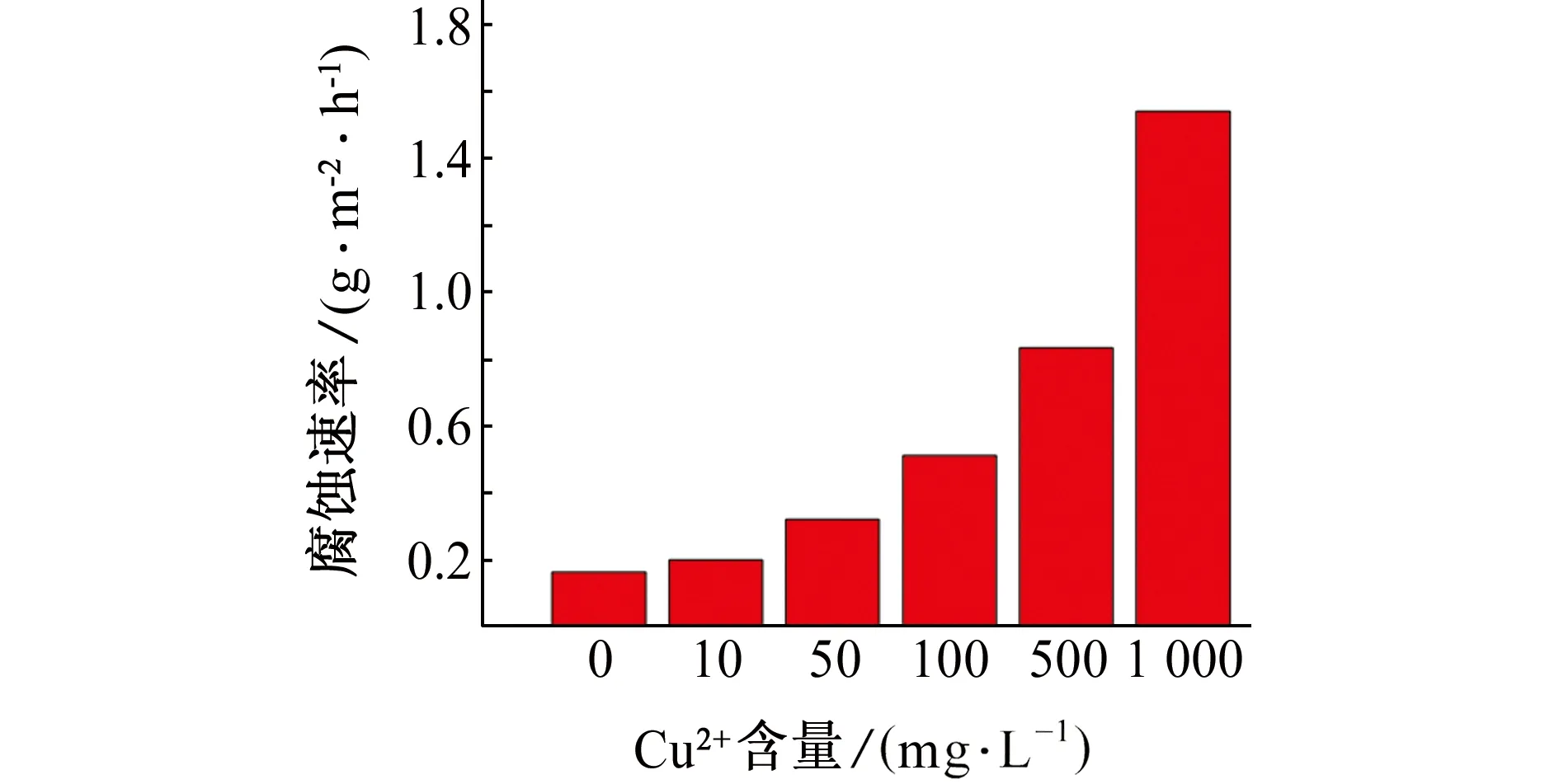
图5 碳钢试样在含不同量Cu2+的人造海水溶液中腐蚀7 d后的腐蚀速率Fig.5 Corrosion rates of carbon steel samples after corrosion in artificial seawater containing different content of Cu2+ for 7 d
2.3 微观腐蚀形貌
由图7可见:碳钢试样在含不同量Cu2+的人造海水溶液中腐蚀7 d后,腐蚀形貌相差不大,试样表面都比较平整,并伴有细小的颗粒状凸起。能谱分析结果(图略)表明,腐蚀后试样表面主要为Fe和少量的O,Cu含量很少,只有极个别区域Cu含量较高,这表明腐蚀析出的Cu及其他腐蚀产物十分疏松,清洗后在基体上基本没有残留附着。
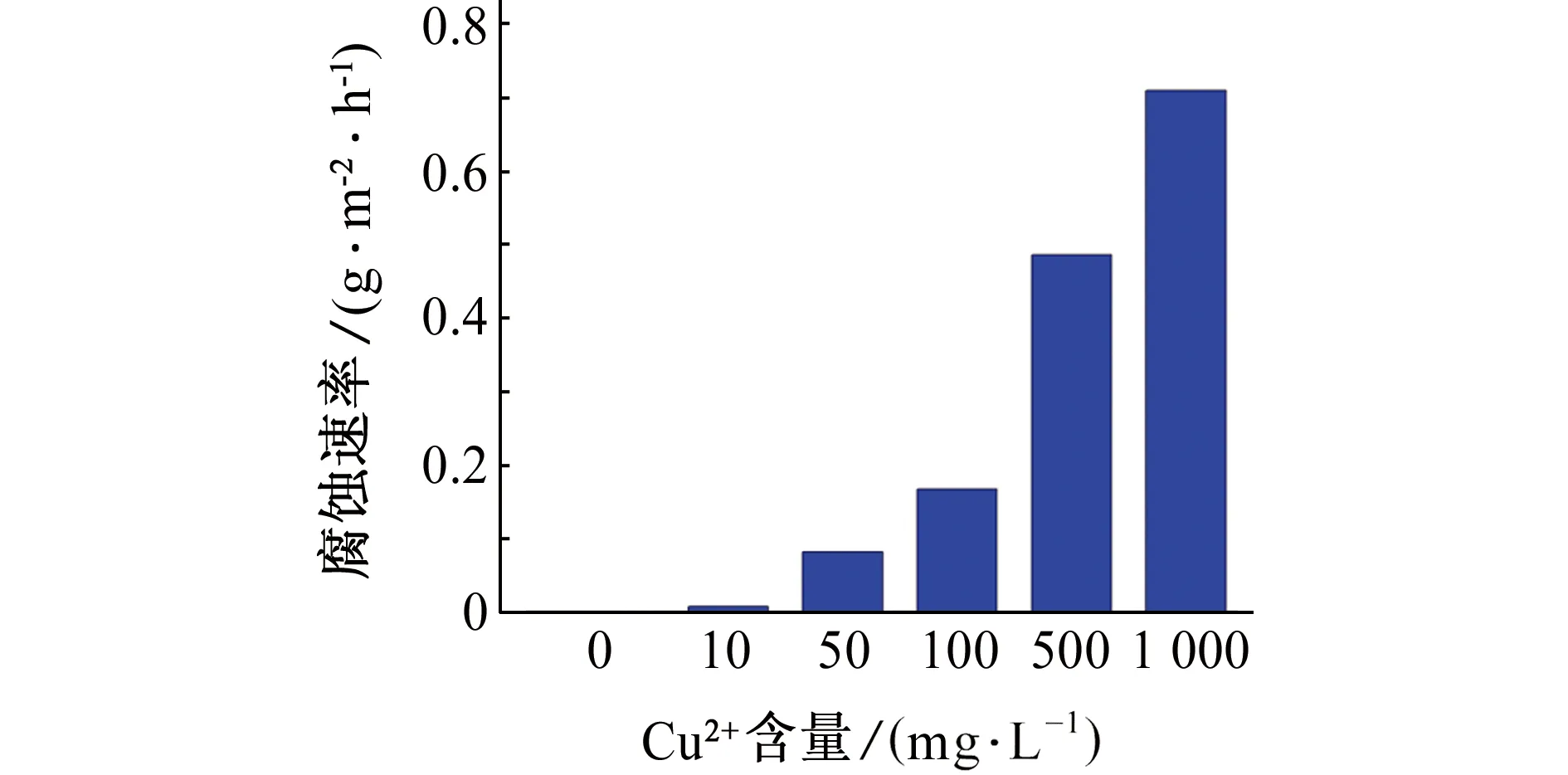
图6 不锈钢试样在含不同量Cu2+的人造海水溶液中腐蚀7 d后的腐蚀速率Fig.6 Corrosion rates of stainless steel samples after corrosion in artificial seawater containing different content of Cu2+ for 7 d

(a) 0 mg/L (b) 10 mg/L

(c) 50 mg/L (d) 100 mg/L

(e) 500 mg/L (f) 1 000 mg/L图7 碳钢试样在含不同量Cu2+的人造海水溶液中腐蚀7 d后的微观腐蚀形貌Fig.7 Micro corrosion morphology of carbon steel samples after corrosion in artificial seawater containing different content of Cu2+ for 7 d
由图8可见:不锈钢试样在含不同量Cu2+的人造海水溶液中腐蚀7 d后,表面均出现点蚀坑,在无Cu2+时点蚀仅开始萌生,钝化膜相对比较完整,点蚀程度很小。随着Cu2+含量升高到10 mg/L,出现少量的几微米到几十微米的小点蚀坑,Cu2+含量继续升高,局部出现比较深的蚀坑,当Cu2+含量为500 mg/L时,蚀坑尺寸达100 μm以上,且在其附近有很多小的点蚀坑分布。可见,随着Cu2+含量升高,点蚀变得严重。

(a) 0 mg/L (b) 10 mg/L
2.4 动电位极化曲线
由图9(a)可见:Cu2+会对碳钢试样在海水中的腐蚀行为产生明显影响。在含10 mg/L Cu2+的人造海水中,碳钢试样的自腐蚀电位略微负移,当Cu2+含量升高至50 mg/L,碳钢试样的自腐蚀电位明显负移。随着Cu2+含量进一步升高,极化曲线明显向右上方移动,即碳钢试样的自腐蚀电位和自腐蚀电流密度均明显提高。同时,随着Cu2+含量升高,阴极控制转变为Cu2+的扩散控制,没有明显的tafel区。

(a) 碳钢

(b) 不锈钢试样图9 试样在含不同量Cu2+的人造海水溶液中的动电位极化曲线Fig.9 Polarization curves of carbon steel samples (a) and stainless steel samples (b) in artificial seawater containing different content of Cu2+

(1)


由图9(b)可见:随着Cu2+含量升高,动电位极化曲线向右上方移动,自腐蚀电位和腐蚀电流密度总体呈增大的趋势,这是由于不锈钢钝化膜的存在,使得阳极溶解反应速率比较低,阳极反应平衡电位没有太大变化,而随着Cu2+含量升高,阴极反应速率加快,阴极平衡电位不断提高,一个阳极反应与两个阴极反应相互耦合,相互极化,导致自腐蚀电位与自电流密度随着Cu2+含量的升高而增大。同时发现,随着Cu2+含量升高,钝化区范围明显缩短,在Cu2+含量低于500 mg/L时,维钝电流密度接近,Cu2+含量继续升高到1 000 mg/L,维钝电流密度显著增大,钝化膜稳定性明显降低,点蚀敏感性提高。
3 结论
(1) A106B碳钢试样在含不同量Cu2+的人造海水溶液中均呈现均匀腐蚀,与无Cu2+时的相比,当溶液中Cu2+含量增至50,100,500,1 000 mg/L 时,腐蚀速率分别增大97%,1 214%、412%和847%;304L不锈钢试样在含不同量Cu2+的人造海水溶液中均呈现点蚀,在无Cu2+人造海水中的试样,肉眼观察不到明显的点蚀,点蚀速率很小,但点蚀已开始萌生,随着Cu2+含量的升高,点蚀速率显著升高,与无Cu2+时的相比,当溶液中Cu2+含量增至50,100,500,1 000 mg/L时,点蚀速率分别增大约68.4,140,405,592倍。
(2) 随着Cu2+含量的升高,碳钢试样的自腐蚀电位负移,Cu2+含量进一步升高到100 mg/L及以上,极化曲线则明显向右上方移动,即自腐蚀电位和自腐蚀电流密度均明显提高。阴极极化反应由以氧的还原反应为主转变为以Cu2+的还原反应为主,阴极控制转变为Cu2+的扩散控制。
(3) 随着Cu2+含量的升高,不锈钢试样的动电位极化曲线向右上方移动,钝化区范围明显缩短,当Cu2+含量低于500 mg/L时,维钝电流密度接近,Cu2+含量继续增大到1 000 mg/L,维钝电流密度也显著增大,钝化膜稳定性明显降低,点蚀敏感性提高。
